升麻中环阿尔廷烷型三萜皂苷及其抗肿瘤活性研究*
2014-12-02陈继永姜永涛张达磊李平林李国强
陈继永,姜永涛,沈 莉,张达磊,李平林,李国强**
(1.中国海洋大学医药学院 海洋药物教育部重点实验室,山东 青岛 266003;2.山东绿叶制药有限公司,山东 烟台 264003;3.烟台大学药学院,山东 烟台 264003)
升麻CimicifugafoetidaL.是毛茛科(Ranunculaceae)升麻属多年生草本植物,是《中国药典》2010年版一部收载的3种升麻药材之一;具有清热解毒,举升阳气的功效,在现代中医上用于治疗风热头痛、咽喉肿痛、子宫脱垂等病症。已有研究表明,环阿尔廷烷型三萜及其糖苷是升麻的主要次级代谢产物,具有抗过敏、抗骨质疏松、保肝、抗病毒、缓解妇女更年期综合症、以及抗肿瘤细胞增殖等广泛的药理活性[1-2]。目前,国内对该物种的研究大都集中于云南和贵州等西南地区;为了进一步阐明升麻药效的物质基础,本研究从中药材的地域特异性出发,首次对目前很少涉及的我国西北地区甘肃产升麻C.foetidaL.进行了较系统的化学和生物活性研究,从其根茎提取物的乙酸乙酯萃取物中共分离鉴定了15个环阿尔廷烷型三萜皂苷(见图1),并对其进行了细胞毒活性评价。
1 仪器与材料
仪器 X-4显微熔点测定仪(温度计未校正);Rudolph Autopol IV旋光仪;Bruker AVANCE 400MHz核磁共振谱仪;Thermo DSQ EI-mass spectrometer质谱仪;日本EYELA中压液相制备系统;柱色谱用硅胶(200~300目,300~400目)和薄层色谱用硅胶均为青岛海洋化工厂产品,ODS-A(50μm,日本 YMC),Sephadex LH-20(Pharmacia公司产品)。常用有机试剂均为国产分析纯。RPMI 1640和DMEM 培养液、青霉素、链霉素、胎牛血清购自Gibco公司,胰酶、MTT、DMSO购自Amresco公司,其它试剂均为国产分析纯。CKX31型倒置显微镜(菲律宾奥林巴士公司),恒温CO2培养箱(美国Thermo公司),5810R型台式高速低温离心机(德国Eppendorf公司),全自动酶标仪(美国Biotek公司)。
材料 升麻根茎于2008年5月采自甘肃省陇南武都地区,烟台大学药学院生药室徐本明副教授鉴定为CimicifugafoetidaL.。植物标本(No.2008018)存放于烟台大学药学院生药标本室。
2 提取与分离
升麻药材(6.0kg)经粉碎后,80%乙醇热回流提取3次;提取液经减压浓缩后得浸膏共450g,分极性萃取得到石油醚萃取物80g、乙酸乙酯萃取物220g和正丁醇萃取物120g。对乙酸乙酯萃取物采用硅胶柱色谱(200~300目),以CHCl3-MeOH(100∶0~50∶50)梯度洗脱,分离获得10个组分(Fr.1~Fr.10)。Fr.2(20g)经反复硅胶柱色谱(CHCl3-MeOH,100∶0~80∶20)分离得到化合物1(58mg)和2(180mg)。以同样方法从Fr.3(10g,CHCl3-MeOH,95∶5)分离得到化合物3(35mg)和4(30mg),从Fr.5(8g,CHCl3-MeOH,90∶10)分离得到化合物 8(40mg)和 9(85mg),从 Fr.7(5g,CHCl3-MeOH(80∶20)分离得到化合物13(15mg)。Fr.4(12g)分别经硅胶柱色谱(CHCl3-MeOH,95∶5)和中压液相制备系统(乙腈-水,50∶50)分离得到化合物5(55mg),6(20mg)和7(48mg);以同样方法从 Fr.6(15g,CHCl3-MeOH,95∶5~80∶20;乙腈-水,45∶55)分离得到化合物10(250mg),11(45mg)和12(28mg)。结合Sephadex LH-20柱色谱(MeOH),从Fr.9(10g,CHCl3-MeOH,80∶20~50∶50)中分离得到化合物14(150mg)和15(85mg)。

图1 化合物1-15的化学结构Fig.1 Chemical Structures of compounds 1-15
3 结构鉴定
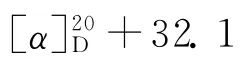
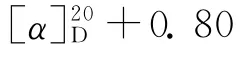
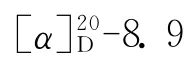
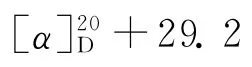
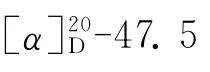
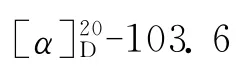

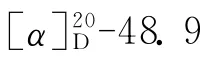
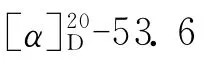
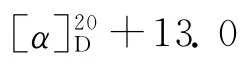
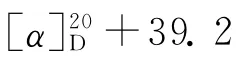


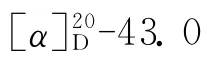
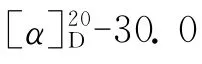
4 细胞毒活性评价
采用MTT法[14]评价化合物1-15对人宫颈癌细胞(HeLa)和人乳腺癌细胞(MCF-7)的细胞毒活性(见表1)。
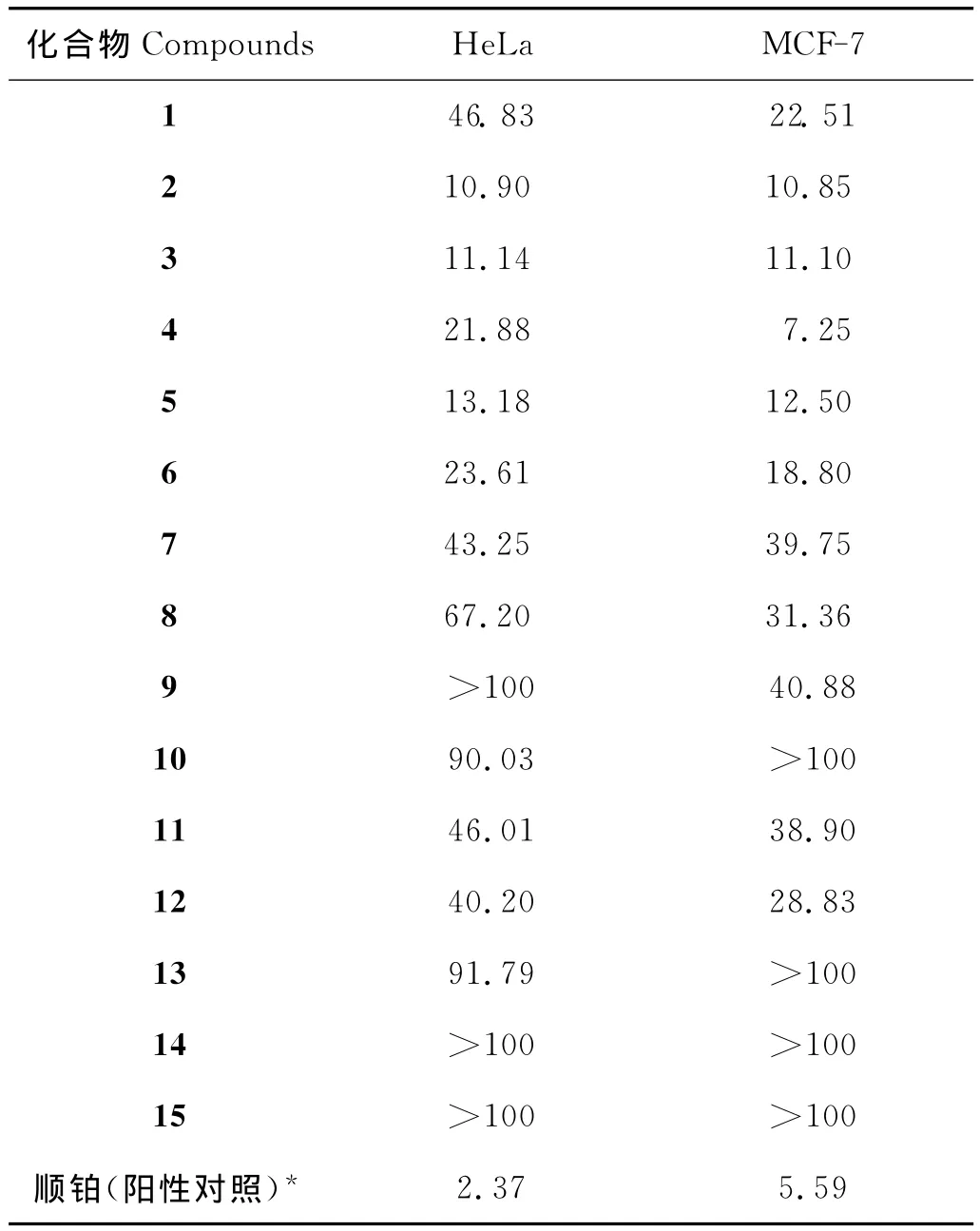
表1 化合物1-15和顺铂对人肿瘤细胞体外毒性(IC50/μmol·L-1)Table 1 Cytotoxicity of compounds 1-15
5 讨论
升麻(Cimicifuga foetidaL.)分布在我国西南(云南、贵州、四川)至西北(陕西、山西、甘肃、青海)的广袤地区,气候和地理环境差别很大,具有潜在的区域特异性。本研究首次对我国西北地区甘肃产升麻进行了较系统的化学和生物活性研究,从中分离得到15个环阿尔廷烷型三萜皂苷,分属cimigenol、asiaticoside、16,23-dione、cimifugenin 和 shengmanol等结构亚型[15];其中化合物6为首次从该属植物中分离得到,化合物3,7和11为首次从该种植物中分离得到。通过细胞毒高通量筛选,发现化合物2~6对两种肿瘤细胞都具有较好的抑制活性,首次发现化合物3~6对HeLa细胞也具有较好的细胞毒活性,表明阿尔廷烷型三萜皂苷中的侧链环氧很可能发挥重要的药效作用。研究结果进一步丰富了我国中药材升麻的化学多样性,同时为其药效的物质基础提供了理论依据。
[1]林玉萍,邱明华 ,李忠荣.升麻属植物的化学成分与生物活性研究 [J].天然产物研究与开发,2002,14(6):58-76.
[2]曹丽,杨卫彬,潘瑞乐,等.兴安升麻总苷抗肿瘤药效研究 [J].中国中医药信息杂志,2008,15(12):31-33.
[3]李从军,李英和,陈顺峰,等.升麻中的三萜类成分 [J].药学学报,1994,29(6):449-453.
[4]Kadota S,Li J X,Tanaka K,et al.Constituents of cimicifuga rhizomaⅡ.Isolation and structures of new cycloartenol triterpenoids and ralated compounds fromCimicifugafoetidaL.[J].Tetrahedron,1995,51(4):1143-1166.
[5]张庆文,叶文才,车镇涛,等.小升麻中的环菠萝烷型三萜及其糖苷成分 [J].药学学报,2001,36(4):287-291.
[6]Ye W C,Zhang J W,Che C T,et al.New cycloartane glycosides fromcimicifugadahurica[J].Planta Medica,1999,65(8):770-772.
[7]卢滨,范云双,万定荣,等.绿升麻中菠萝烷型三萜类成分研究[J].时珍国医国药,2009,20(2):267-270.
[8]Jamroz M K,Jamroz M H,Dobrowolski J Cz,et a1.One new and six known triterpene xylosides fromCimicifugaracemosa:FT-IR,Raman and NMR studies and DFT calculations[J].Spectrochimica Acta Part A,2012,93:10-18.
[9]但春,梁健,周燕,等.升麻中的环菠萝蜜烷三萜成分 [J].中国中药杂志,2009,34(15):1930-1934.
[10]Shao Y,Harris A,Wang M F,et a1.Triterpene glycosides fromCimicifugarcemosa[J].Journal of Natural Products,2000,63(7):905-910.
[11]Kusano A,Shibano M,Kitagawa S,et al.Studies on the constituents ofcimicifugaspecies.XV.two new diglycosides from the aerial parts ofcimicifugasimplexWORMSK [J].Chem Pharm Bull,1994,42(9):1940-1943.
[12]Kusano A,Shibano M,Kitagawa S,et al.Studies on the constituents ofcimicifugaspecies.XXVI.twelve new cyclolanostanol glycosides from the underground parts ofcimicifugasimplexWORMSK.[J].Chem Pharm Bull,1999,47(4):511-516.
[13]Koeda M,Aoki Y,Sakurai N,et al.Studies on the Chinese crude drug“shoma.”Ⅸ.three novel cyclolanostanol xylosides,cimicifugosides H-1,H-2and H-5,from cimicifuga Rhizome [J].Chem Pharm Bull,1995,43(5):771-776.
[14]武文,赵烽,宝丽,等.中华隐孔菌子实体化学成分及细胞毒活性研究 [J].中国药物化学杂志,2011,21(1):47-52.
[15]高璟春,彭勇,杨梦苏,等.毛茛科升麻族植物药用亲缘学初探[J].植物分类学报,2008,46(4):516-536.
