山楂叶总黄酮生物溶蚀性骨架型缓释片的制备
2014-11-04陈思思陈超群陈小慧
张 锴,陈思思,邬 琳,徐 佳,陈超群,陈小慧,杨 群,*
(1.太极集团浙江东方制药有限公司,浙江绍兴 312000;2.绍兴文理学院元培学院,浙江绍兴 312000;3.杭州集和医药咨询有限公司,浙江杭州 310023)
山楂叶为蔷薇科植物山里红Crataegus pinnatifida Bge.var.major N.E.Br.或山楂 Crataegus pinnatifida Bge.的干燥叶[1]。《中国药典》2010年版一部收载了山楂叶提取物,其主要成分为总黄酮。
现代研究表明,山楂叶总黄酮具有扩张冠状动脉、降血脂、降血压、防治动脉粥样硬化、抗氧化、保护心肌、降血糖、抗血小板凝聚、促进消化[2-14]等方面的作用。用于治疗气结血瘀、胸闷憋气、心悸健忘、眩晕耳鸣、冠心病、心绞痛、高脂血、脑动脉供血不足等症。目前已有其中成药制剂(益心酮系列产品)上市,包括片剂、胶囊、滴丸。其中益心酮片已收载于《中国药典》2010年版,需每次服2~3片 (32 mg/片),日服3次,由于心脑血管疾病治疗往往需要长期用药,为减少服药次数,提高病人的顺应性,降低普通制剂血药浓度波动,提高治疗效果,本试验拟设计一种日服1~2次生物溶蚀性骨架型缓释片,并对缓释片的释放机制进行考察。
1 仪器与试药
1.1 仪器 11292型单冲压片机 (上海天凡药机制造厂);ZRC-8ST型智能溶出度测定仪 (天津创新电子设备制造有限公司);UV-2102PCS型紫外可见分光光度计 (尤尼柯 (上海)仪器有限公司);BSA223S型电子天平 (赛多利斯科学仪器(北京)有限公司);DGG-9070B型电热恒温鼓风干燥箱 (上海森信实验仪器有限公司)等。
1.2 试药 山楂叶总黄酮 (药用,太极集团浙江东方制药公司,含量90%);芦丁对照品 (中国食品药品检定研究院,批号100080-20040);硬脂酸镁、微晶纤维素、预胶化淀粉、羟丙甲纤维素(药用,安徽山河药用辅料有限公司);乳糖 (药用,镇江康富生物工程有限公司);硬酯醇、亚硝酸钠、氢氧化钠、无水乙醇等均为分析纯。
2 方法与结果
2.1 建立分析方法
2.1.1 对照品溶液制备 精密称取在120℃干燥至恒重的芦丁对照品25 mg,置50 mL量瓶中,加乙醇适量,超声处理使溶解,放冷,加乙醇稀释至刻度,摇匀。精密量取20 mL,置50 mL量瓶中,加水至刻度,摇匀,即得 (每1 mL中含无水芦丁0.20 mg)。
2.1.2 供试品溶液的制备 取本品20片,精密称定,研细,取约75 mg,精密称定,置50 mL量瓶中,加乙醇适量,超声30 min,放冷,加乙醇稀释至刻度,摇匀,用微孔滤膜 (0.45 μm)滤过,取续滤液,即得。
2.1.3 确定检测波长 精密量取对照品溶液5 mL置25 mL量瓶中,加水至6 mL,加5%亚硝酸钠溶液1 mL,摇匀,放置6 min,加10%硝酸铝溶液1 mL,摇匀,放置6 min,加氢氧化钠试液10 mL,再加水至刻度,摇匀,放置15 min,以相应的试剂为空白,照紫外—可见分光光度法 (药典附录VA),在450~550 nm波长范围内扫描,测定吸光度,确定最大吸收波长。结果:山楂叶总黄酮在508 nm处有最大吸收,故选择508 nm为山楂叶总黄酮的测定波长。
2.1.4 绘制芦丁标准曲线 精密量取对照品溶液1、2、3、4、5、6 mL,分别置25 mL量瓶中,各加水至6 mL,加5%亚硝酸钠溶液l mL,使混匀,放置6 min,加10%硝酸铝溶液l mL,摇匀,放置6 min,加氢氧化钠试液10 mL,再加水至刻度,摇匀,放置15 min,以相应的试剂为空白,照紫外一可见分光光度法 (附录VA),在508 nm波长处测定吸光度,以吸光度 (A)对浓度 (C)进行回归,得回归方程:A=11.549C +0.0418,r=0.99995(n=6),线性范围为0.008~0.048 mg/mL。
2.1.5 稳定性试验 精密量取芦丁对照品溶液5 mL,置25 mL量瓶中,照“2.1.4”项下的方法,自“加水至6 mL”起,放置0、1、2、4、8和24 h,依法测定吸光度,计算吸光度的RSD。计算得吸光度的RSD为0.37%(n=6),表明样品溶液在24 h内稳定。
2.1.6 精密度试验 精密量取芦丁对照品溶液5 mL,置25 mL量瓶中,照“2.1.4”项下的方法,自“加水至6 mL”起,依法测定吸光度6次,计算平均吸光度和RSD。计算得平均吸光度为0.504,RSD为0.29%(n=6),表明精密度良好。
2.1.7 重复性试验 精密称取同一样品6份,各20片,按“2.1.2”项下方法操作,制备供试品溶液。精密量取 5 mL,置 25 mL量瓶中,照“2.1.4”项下的方法,自“加水至6 mL”起,依法测定吸光度,计算供试品溶液总黄酮的平均含量和RSD(n=6)。计算得总黄酮平均含量为0.519 g/g,RSD为0.55%(n=6),表明重现性良好。
2.1.8 回收率试验 精密称取1.5 mg芦丁对照品6份,分别加入处方量辅料,置100 mL量瓶中,照“2.1.2”项下方法制备样品,照“2.1.4”项下方法测定吸光度,计算平均回收率和RSD。结果,平均回收率为100.57%,RSD为0.18%,表明该方法准确可靠,可用于山楂叶总黄酮生物溶蚀性骨架型缓释片中总黄酮的含量测定。
2.2 山楂叶总黄酮缓释片的处方优化 以硬脂醇为生物溶蚀性骨架材料,再辅以其他辅料如填充剂预胶化淀粉、乳糖,黏合剂羟丙基甲基纤维素(HPMC K10),润滑剂硬脂酸镁制作缓释片。处方见表1。

表1 处方Tab.1 Formulation
2.3 缓释片制备 按上述处方称取硬脂醇,放入蒸发皿中于80℃水浴加热至熔融,备用;取处方量的山楂叶总黄酮,加入硬脂醇中混合均匀后,从水浴中取下,放冷至室温;取乳糖、预胶化淀粉置研钵中研细,过80目筛,加入上述混合物中,混合均匀;向上述混合物中加入适量羟丙甲纤维素胶浆 (以80%乙醇适量溶解)混合制软材,至软材握之成团,轻压即散,挤压过16目筛制湿颗粒;将湿颗粒放入干燥箱中,40~50℃干燥30~45 min;取出过16目筛整粒,加硬脂酸镁,总混;用直径10 mm的浅冲压片,控制片剂硬度5.0~6.0 kg、片重300 mg。
2.4 片剂释放度的测定 取制得缓释片6片,分别精密称重,照释放度测定法(《中国药典》2010版二部附录XD第一法),用溶出度测定法 (2010版《中国药典》二部附录X C第二法)的装置,以水900 mL为释放介质,温度为 (37±0.5)℃,转速为每分钟50转,依法操作,经1、2、3、4、5、6、8、10和 12 h时,分别取溶液 5 mL,用0.45 μm微孔滤膜滤过,并即时补充相同温度、相同体积的释放介质,分别精密量取续滤液3 mL,置25 mL量瓶中,照标准曲线绘制项下的方法,自“加水至6 mL”起依法测定吸光度,从标准曲线上读出供试品溶液中芦丁的含量,计算累积释放百分率。见表2。

表2 累积释放百分率 (%)Tab.2 Cumulative release percentage(%)
结果:释药速率随硬酯醇、羟丙甲纤维素用量增加而减慢,随乳糖、预胶化淀粉用量增加而加快,因为硬酯醇用量越大,溶蚀越慢,羟丙甲纤维素用量增加,片剂黏结力增强,溶蚀越慢,乳糖、预胶化淀粉用量增加,释药加快。1~6号处方释药较慢,在12 h内释药不够完全,7号处方释药缓慢而持久,累积释放百分率2 h为23.3%,5 h为55.2%,8 h为78.4%,12 h为92.2%,在12 h内呈现良好的缓释特征。见图2。确定的最佳处方组成为:山楂叶总黄酮100.0 g,硬脂醇26.0 g,羟丙甲纤维素10.0 g,乳糖60.0 g,预胶化淀粉60.0 g,硬脂酸镁4.0 g,制成866片。
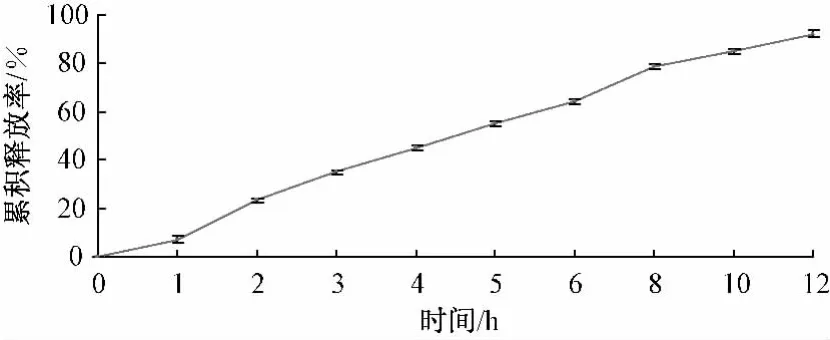
图1 释放度曲线Fig.1 Release curves
2.5 拟合释放动力学方程 将缓释片的体外释放数据分别按零级、一级、Higuchi和Ritger-Peppas释药动力学方程进行拟合。见表3。

表3 缓释片体外释药动力学模型拟合结果Tab.3 Fitting results of sustained-release tablets in vitro release kinetics model
结果:采用的各种模型中,一级动力学模型优于其他模型。对于片状骨架型制剂来讲,Ritger-Peppas方程中释放指数在0.5~1.0之间时,药物释放机制为扩散和溶蚀综合作用的结果。由表1可知本实验的释放指数n值为0.9862,由此可推断山楂叶总黄酮生物溶蚀性骨架型缓释片属于扩散和溶蚀双重释药机制。
2.6 山楂叶总黄酮生物溶蚀性骨架型缓释片的含量测定 取缓释片20片,精密称定,研细,取适量,精密称定,照“2.1.1”项供试品溶液制备项下的方法,制备供试品溶液。精密量取5 mL置25 mL量瓶中,照“2.1.4”项标准曲线绘制项下的方法,自“加水至6 mL”起依法测定吸光度,代入标准曲线计算供试品溶液中芦丁的含量,计算缓释片的总黄酮的含量。结果:本品每片含总黄酮以无水芦丁计(C27H30O16)为103.1 mg。
3 讨论
心血管系统疾病为当今人类死亡率最高的三大主要疾病之一,山楂叶总黄酮制剂在临床上广泛用于心脑血管系统疾病的治疗,主要剂型有普通片剂,胶囊、滴丸。这些普通制剂必须通过一日多次给药才能达到药物治疗浓度,同时药物进入血液循环后血药浓度波动很大。在心血管系统疾病治疗中,由于药物治疗窗较窄,使用普通制剂之后血药浓度很快就会达到峰值,易产生毒副作用,之后血药浓度会快速下降,达到谷值,低于有效浓度,从而不能起到治疗作用,而药物缓释制剂克服了这一缺点。将山楂叶总黄酮制成生物溶蚀性骨架型缓释片,减少服药次数,大大提高了病人的顺应性;血药浓度平稳,有利于降低药物的毒副作用,提高治疗效果;允许病人作为门诊病人接受药物治疗,降低治疗费用。
本试验以硬脂醇为生物溶蚀型骨架材料,再以填充剂预胶化淀粉、乳糖等调节药物释放速度,以释放度为指标优化处方。确定的最佳处方组成为:山楂叶总黄酮100.0 g,硬脂醇26.0 g,羟丙甲纤维素10.0 g,乳糖60.0 g,硬脂酸镁4.0 g,预胶化淀粉60.0 g。体外释放度试验表明,其具有高效、长效的特点,可延缓药物的释放。分别采用零级释放、一级释放、Higuchi模型对体外释放数据进行拟合,结果表明,山楂叶总黄酮生物溶蚀骨架型缓释片释放符合一级动力学方程,制得的缓释片在12 h内呈现良好的缓释特征。
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:30.
[2]史逸达.山楂叶总黄酮药理作用浅析[J].中国中医药咨讯,2012,4(1):437.
[3]鞠晓芸,方泰惠,张文通.山楂叶总黄酮冻干粉对麻醉犬冠脉结扎所致心肌梗死的影响[J].南京中医药大学学报,2005,21(6):381-383.
[4]杨宇杰.山楂叶总黄酮对高脂血症大鼠血管功能损伤的保护作用[J].中草药,2007,38(11):1687.
[5]叶希韵,王耀发.山楂叶总黄酮对血管内皮细胞氧化损伤的保护作用[J].中国现代应用药学杂志,2002,19(4):267-268.
[6]Roddewing C,Hensel H.Reaction of local myocardial blood flow in nonanes the tized dogs and an esthetized cats tooraland parenteral application of a Crataegus fraction(oligo meric procyanidin)[J].Arzneim Forsch,1977,27(7):1407-1410.
[7]喻 斌,李宏轶,张 良,等.山楂叶总黄酮对麻醉犬冠脉结扎所致心肌缺血的保护作用[J].中药新药与临床药理,2008,19(6):461-464.
[8]李 莉,吕 红,庞 红.山楂叶总黄酮抗衰老作用的实验研究[J].时珍国医国药,2007,18(9):2143.
[9]陈 雄.山楂叶总黄酮对大鼠肾缺血/再灌注损伤的保护作用[J].实用儿科杂志,2007,22(5):359-360.
[10]陈芝芸,严茂祥,何蓓晖.大鼠非酒精性脂肪性肝炎(NASH)形成中氧化应激水平变化及山楂叶总黄酮对其影响[J].医学研究杂志,2007,36(12):33-36.
[11]Delporte M L,Funahashi T,Takahashi M,et al.Pre-and posttranslation al negaive effect of 13-adrenoceptor agonistson adiponectin secretion:in vitro and in vivo studie[J].Biochem J,2002,367:677-685.
[12]纪影实,李 红,杨世杰.山楂叶总黄酮对H2O2诱导PC12细胞凋亡的保护作用[J].中国药理学通报.2006,2006,22(6):760.
[13]叶希韵,张 隆,沈 菊,等.山楂叶总黄酮对糖尿病小鼠糖脂代谢的影响[J].中草药,2005,36(11):1683-1687.
[14]焦利萍.山楂叶总黄酮对急性血淤模型大鼠血液流变学指标的影响[J].中国医药与临床,2008,8(1):49-50.
