喷雾干燥法制备盐酸千金藤碱微囊
2014-11-04张壮丽王陆巡赵志鸿王桂芳张小俊
张壮丽,王陆巡,赵 宁,赵志鸿,王桂芳,张小俊
(郑州大学医药科学研究院,河南郑州 450052)
盐酸千金藤碱 (Cepharantine Hydrochloride)是由防己科千金藤属植物地不容块根中提取分离出的单体生物碱—千金藤碱 (Cepharanthine),经成盐制得的一种双苄基异喹啉类生物碱化合物。盐酸千金藤碱具有逆转肿瘤多药耐药性、抗氧化、抗炎、抑菌、镇痛、免疫调节、抗肺纤维化、抗肿瘤、升高白细胞等生物学活性[1-6]。盐酸千金藤碱目前仅注射剂一种剂型,剂型单一、给药途径单一、患者的顺应性较差。药物微囊化后可制备成多种终端剂型,如片剂、胶囊剂等,可增加给药途径,提高患者顺应性,从而提高其药用价值。喷雾干燥技术是药物微囊化的一个有效方法,具有操作简便、可控性好、成囊率高、产品分散等特点,是最具工业化应用价值的微囊化方法[7-9]。本实验采用喷雾干燥法,将盐酸千金藤碱进行微囊化,为盐酸千金藤碱的新剂型开发提供实验依据。
1 仪器与试药
实验型喷雾干燥机DC-1500(上海达程实验设备有限公司);高效液相色谱仪P680A(美国戴安公司);78-1磁力加热搅拌器 (金坛市华峰仪器有限公司);ABS135-S(METTLER TOLEDO);颗粒图像处理仪PIP8.1(欧美克仪器有限公司);超声波发生器CSF-1A(上海超声波仪器厂);DSC-60A型差示扫描量热仪 (日本岛津公司)。
盐酸千金藤碱 (自制,纯度>98.5%);Eudragit S100(德国罗姆公司;上海云卓贸易有限公司赠送);甲醇 (色谱纯,赛默飞世尔科技);蒸馏水;其他试剂为分析纯。
2 方法与结果
2.1 制备方法 取处方量的Eudragit S100溶于100 mL 95%乙醇中制得4%的溶液,将盐酸千金藤碱溶于少量甲醇中,加入上述乙醇溶液中,加入适量甘油和蓖麻油,充分溶解后进行喷雾干燥。
2.2 色谱条件 Agilent TC-C18色谱柱 (250 mm×4.6mm,5 μm),流动相为甲醇-水-氨水(84∶16∶0.2);检测波长283 nm;体积流量0.5 mL/min;柱温为室温。
2.3 溶液的制备 取盐酸千金藤碱对照品适量,精密称定,加甲醇制成约200 μg/mL的对照品溶液。取盐酸千金藤碱微囊约0.1 g,精密称定,于100 mL量瓶中,加甲醇适量超声1 h使其溶解,放至室温,加甲醇定容至刻度,摇匀,过滤,取续滤液作为供试品溶液;以空白微囊按供试品溶液的制备方法制备阴性对照溶液。
2.4 方法学考察[10]
2.4.1 专属性试验 分别吸取“2.3”项下的对照品、供试品和阴性对照品溶液各20 μL进样,按“2.2”项色谱条件试验。供试品溶液色谱图中,有与对照品溶液保留时间相同的吸收峰,阴性对照溶液无此吸收峰。表明该法阴性无干扰,专属性强。
2.4.2 线性关系考察 精密称取盐酸千金藤碱对照品适量,用甲醇配成101 mg/mL贮备液,精密吸取1、5、10、20、30、40、50 μL进样,以峰面积为纵坐标、测定量 (μg)为横坐标,进行线性回归,得回归方程为:Y=23.379X - 113.55,(r=0.9999)。结果表明:在盐酸千金藤碱0.101~5.05 μg间与峰面积有较好的线性关系。
2.4.3 加样回收试验 取已知含量的盐酸千金藤碱微囊,分别加入一定量的盐酸千金藤碱对照品,按“2.3”项下方法制备供试品溶液。测得低、中、高质量浓度的样品回收率分别为99.71%、100.94%、100.92%,RSD 分 别 为 2.23%、1.99%、1.88%(n=3)。
2.4.4 精密度和重复性试验 取同一对照品溶液,重复进样测定6次,计算RSD为0.38%。精密称取6份同一供试品,按“2.3”项下方法制备供试品溶液进行测定,计算RSD为0.22%。表明方法的精密度和重复性良好。
2.4.5 稳定性试验 精密吸取同一供试品溶液,分别于0、2、6、12、24、36、48、72h时进样测定。计算RSD为2.21%(n=6),表明盐酸千金藤碱溶液72 h内稳定。
2.5 包封率及载药量的测定 包封率 (%)=微囊中实际含药量/实际投药总量×100%;载药量(%)=微囊中实际含药量/微囊总重量×100%。按“2.3”项方法处理微囊,计算微囊包封率及载药量。
2.6 制备工艺考察
2.6.1 单因素考察 以包封率为评价指标,对Eudragit S100溶液浓度及其芯材比例进行单因素考察。当Eudragit S100的浓度分别为2%、3%、4%、5%(100mL乙醇中 Eudragit S100的质量浓度),按“2.1”项方法所制得微囊的包封率分别为46.3%、59.8%、72.4%、65.1%。当Eudragit S100的用量为4%时所制得的微囊包封率最高,外观较好,呈干燥粉末状,显微镜下观察有大量微囊,大小较为均匀,故选定Eudragit S100的浓度为4%。选择芯材比1∶3、1∶4、1∶5,分别进行喷雾干燥,得到的微囊进行包封率检测,结果分别为59.47%、73.62%、66.16%,故选择芯材比为1∶4。
2.6.2 正交试验[11-12]在预实验的基础上,选择进风口温度 (A)、进液速度 (B)、喷雾压强 (C)进行考察,各因素均确定为三个水平,以包封率为考察指标,选用L9(34)正交表安排试验。因素水平见表1;结果及方差分析见表2、表3。
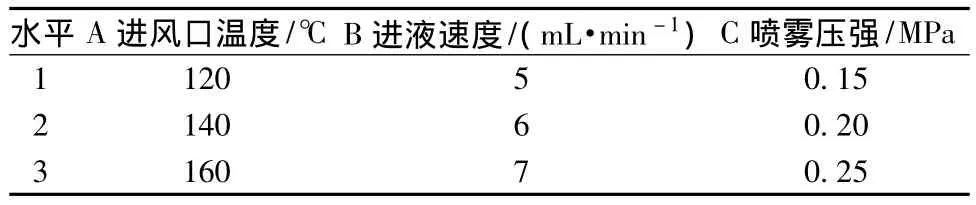
表1 正交试验因素水平Tab.1 Factors and levels
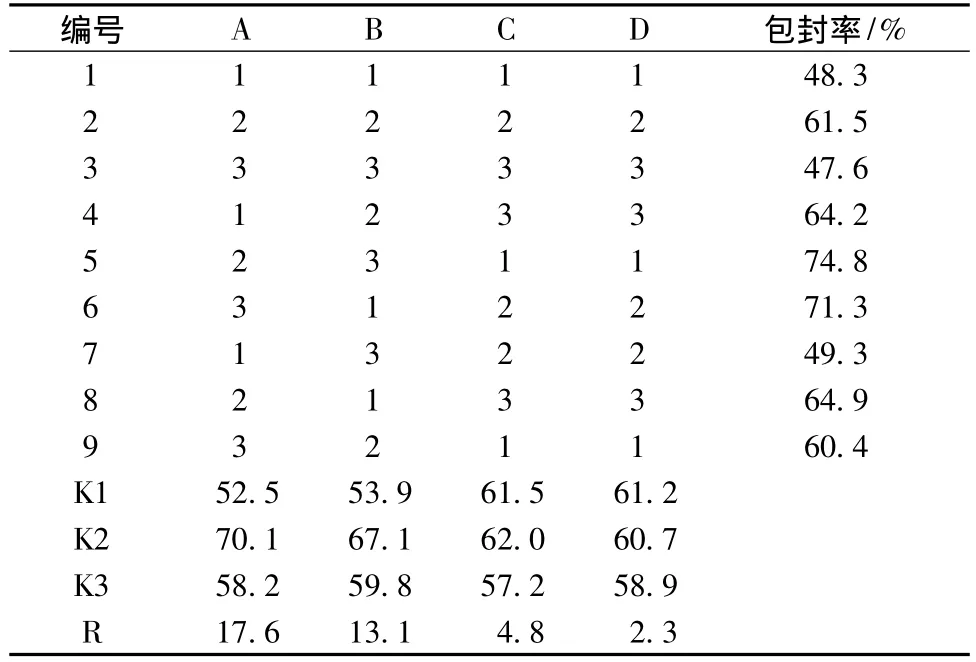
表2 正交试验结果Tab.2 Results of orthogonal design

表3 方差分析Tab.3 Results of variance analysis
方差分析结果显示,各因素影响微囊包封率的顺序是A>B>C,即进风口温度>进样速度>喷雾压强,其中A、B二因素影响显著。最佳工艺条件为A2B2C2,即进风口温度140℃,进样速度6 mL/min,喷雾压强0.2 MPa。
2.7 验证试验 按正交试验结果选定的最优喷雾干燥工艺进行3批验证试验。结果见表4。
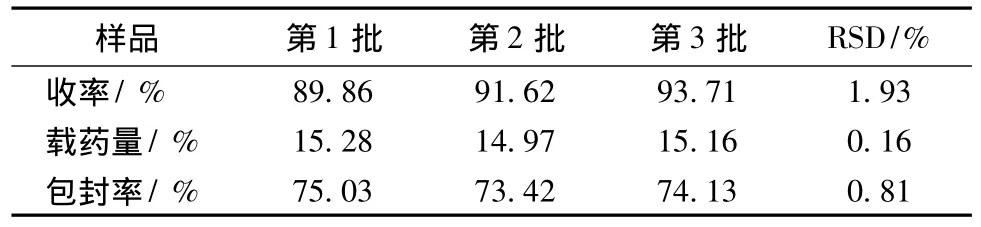
表4 验证试验结果Tab.4 Results of verification test
由验证试验结果可知,3批样品的产率、载药量和包封率重复性较好,表明该处方和工艺可行,重现性良好。
2.8 形态及粒径分布 肉眼观测到的微囊为白色或乳白色粉末,呈疏松状,流动性较好。显微镜下观察,微囊外观圆整、表面光滑,无黏连,测得平均粒径为23.97 μm。见图1。
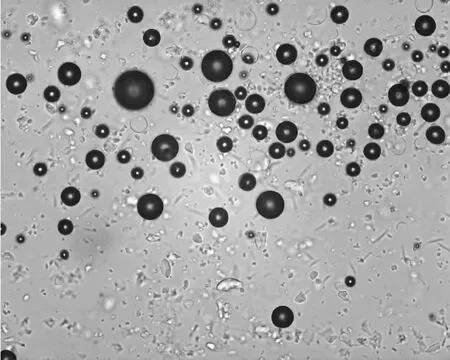
图1 微囊显微镜图片 (400×)Fig.1 Micrograph of microcapsules(400×)
2.9 差示扫描量热 (DSC)分析[13-14]分别取盐酸千金藤碱、空白微囊、盐酸千金藤碱与空白微囊物理混合物、盐酸千金藤碱微囊适量,均以空Al2O3为参比,在加热速率为10℃/min,加热范围为20~250℃,氮气体积流量40 mL/min的条件下,分别测得各样品的DSC曲线,以确定药物在微囊中的分散状态。结果见图2。
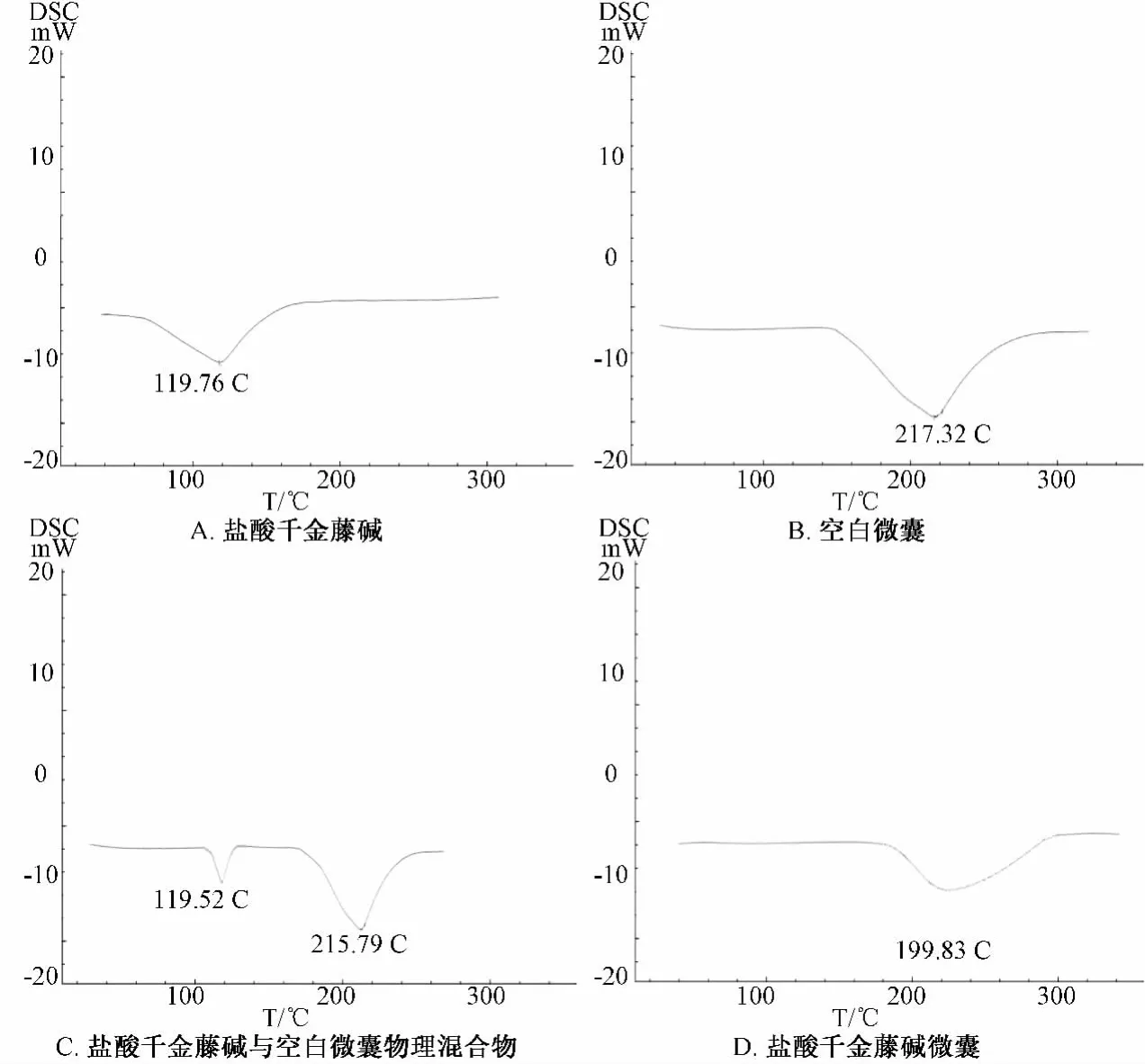
图2 DSC图谱Fig.2 Differential Scanning Calorimetry(DSC)curves
3 讨论
3.1 盐酸千金藤碱味苦,原有剂型单一,给药途径单一,微囊化后不但可以掩味,而且可制备成多种终端剂型,丰富其给药途径,提高患者的顺应性,方便临床使用。
3.2 本实验采用喷雾干燥法制备盐酸千金藤碱微囊,以正交试验法优选制备工艺,以微囊的收率、载药量、包封率为指标,进行验证试验,证实了工艺稳定可行;对所得微囊进行了形态、粒径和DSC考察,结果表明,优化的工艺适合盐酸千金藤碱微囊的制备,为日后盐酸千金藤碱新剂型的开发提供了实验参考。
3.3 喷雾干燥法制备微囊,对工艺参数的考察十分重要。因本实验中采用的喷雾干燥机其出风口温度自动与进风口温度匹配,因此,未考察出风口温度。
3.4 由DSC图谱可看出,盐酸千金藤碱、Eudragit S100自身的特征峰在微囊中均消失,产生了微囊新特征峰,说明盐酸千金藤碱与Eudragit S100不是简单的物理混合,而是以新的相互结合的状态存在,从而形成了微囊。
3.5 制备工艺中加入蓖麻油和甘油可起到良好的增塑作用,有效地减少黏壁和静电吸附现象。
3.6 前期对盐酸千金藤碱的溶解性考察发现,甲醇对盐酸千金藤碱的溶解性好于乙醇,因此,在制备方法中,盐酸千金藤碱先用少量甲醇溶解,再加入Eudragit S100的乙醇溶液中。
3.7 正交试验的预实验发现,包封率和产率基本呈现正相关的关系,载药量范围波动不大,因此,正交试验中采用包封率为主要考察指标。为了更为全面地考察优选工艺的重现性,在验证试验中分别考察了产率、载药量和包封率。
[1]彭有梅,王 宁,王亚峰,等.盐酸千金藤碱逆转K562/ADR细胞多药耐药性及其机制[J].药学学报,2012,47(5):594-599.
[2]马 方,张 艳,王 宁,等.盐酸千金藤碱对急性脂肪肝小鼠脂代谢及过氧化的影响[J].中华中医药杂志,2011,26(6):1429-1432.
[3]王 晓,郑立运,赵志鸿,等.盐酸千金藤碱抗乙型肝炎病毒的体外实验研究[J].时珍国医国药,2010,21(12):3109-3111.
[4]王晓丽,郑立运,张 艳,等.盐酸千金藤碱对急性肝损伤小鼠保护作用的研究[J].中华中医药杂志,2009,24(10):1384-1387.
[5]吴冬梅,崔 英.盐酸千金藤碱对鼻咽癌SUNE-1细胞生长抑制的观察[J].中华肿瘤防治杂志,2009,16(9):649-652.
[6]夏 薇,马 方,江金花,等.盐酸千金藤碱对环磷酰胺所致小鼠白细胞减少的治疗作用[J].郑州大学学报:医学版,2007,42(3):494-496.
[7]房信胜,王建华,穆象山,等.丹参素微囊的喷雾干燥法制备及其体外释药的研究[J].中草药,2009,40(11):1732-1735.
[8]沈 岚,徐德生,冯 怡.喷雾干燥技术制备微囊的研究进展[J].中成药,2005,27(2):207-209.
[9]蔡鑫君,程巧鸳,赵 宁,等.喷雾干燥法制备川芎嗪壳聚糖微球的研究[J].中草药,2008,39(5):679-681.
[10]董娟妮,闫高颖,杨 洋,等.HPLC法同时测定乐脉胶囊中9种成分[J].中成药,2013,35(12):2644-2649.
[11]蒋益萍,张巧艳,张 宏,等.正交试验优选五味子木脂素类成分的提取工艺[J].中成药,2013,35(11):2390-2394.
[12]杨振亚,卢丹逸,马志国.正交试验法优选沙苁蓉提取工艺[J]. 中成药,2014,36(1):177-179.
[13]吕慧侠,周建平,戴影秋,等.海藻酸钙掩味微囊的制备[J].中国药科大学学报,2007,38(2):125-128.
[14]王 玮,金邻豫,白 颖,等.不同方法制备壳聚糖微囊形成机理初探[J].河南大学学报:医学版,2010,29(4):253-257.
