废钒催化剂综合利用的实验研究
2014-10-17郝喜才石海洋
郝喜才,石海洋
(1.开封大学五年制专科部,河南开封 475004;2.开封大学化学工程学院)
钒是稀有金属,在自然界中分散而不集中,富集的钒矿不多,提取和分离比较困难。从废钒催化剂中回收钒,既能避免对环境的污染,又能节约宝贵的资源。目前,废钒催化剂回收钒的方法分为湿法和火法。火法工艺成熟,但能耗高、环境污染严重、回收率低。湿法又可分为碱浸沉淀法和酸浸沉淀法,后者又分直接酸浸法和还原酸浸法。由于废钒催化剂中往往残留有相当数量的硫酸,直接用碱浸取时,碱用量大大增加,另外会有一定量的硅等杂质进入溶液,易形成胶体而难以分离;而直接酸浸法存在着操作复杂、流程长、产品纯度低、回收率低等问题,应用也受到限制,所以研究报道大都用还原酸浸法回收钒。目前国内外大多致力于从废钒催化剂中回收利用钒的研究,而较少提及钾和硅的回收[10]。针对现有工艺的不足,笔者在还原酸浸法的基础上,对浸钒、提钒等环节加以改进,着重对萃取法提钒过程中的工艺参数做了研究,并综合回收了钒、硅、钾,以期实现变废为宝、保护环境的目的。
1 实验
1.1 原料分析
实验所用废钒催化剂来自于开封某化工集团,其主要化学组成(质量分数):V2O5,5%~6%、K2SO4,20%~27%、SiO2,65%~70%、Fe2O3,1.1%。该催化剂的特点:1)废钒催化剂在硫酸生成过程中催化SO2的同时,其活性组分V2O5也部分还原成无催化活性的VOSO4。由于VOSO4易在水中溶解,因此可先用水将其浸出。2)为了提高废钒催化剂中钒的浸出率,须先将水中溶解度很小、呈偏酸性的V2O5在酸性条件下还原成VOSO4。此外,由于本实验还要回收硫酸钾,为避免引入杂质钠离子,所以不采用Na2SO3,而采用K2SO3作为还原剂。3)废钒催化剂中质量分数高达20%~27%的K2SO4,不但不会妨碍湿法冶金,而且易转入溶液。这是因为K2SO4可提高离子的水化程度、降低溶液中水分子活度,从而使被萃物与水结合的能力减弱,即提高了被萃物进入有机相的趋势,有利于萃取。
1.2 实验步骤
1.2.1 水浸
将废钒催化剂磨碎至粒径为375 μm左右,经水浸、过滤,得到的滤液即为水浸液(主要成分为VOSO4等一部分钒盐和水溶性钾盐)备用,滤渣进入还原酸浸工序。
1.2.2 还原酸浸
用质量分数为11%(下同)的H2SO4配制成废钒催化剂质量3.0~3.5倍的浸取液,均分为3份,每份加适量的无水K2SO3。第一份浸取液加入滤渣 (水浸渣),加热至沸腾并持续2 h,静置、冷却、沉淀,吸取上清液去氧化工序。向第一次还原酸浸沉淀渣中加入第二份浸取液,进行同样操作,吸取上清液去氧化工序。向第二次还原酸浸沉淀渣中加入第三份浸取液,进行同样操作,吸取上清液去氧化工序,在第三次还原酸浸沉淀渣中只加入同样量的H2SO4溶液,进行同样操作,吸取上清液备用。合并4次还原酸浸液与水浸液得到浸出液,钒总浸出率可达95.8%以上。反应方程式:
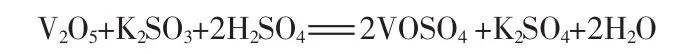
1.2.3 氧化
在浸出液中加入氧化剂KClO3,煮沸到溶液由蓝色转变为黄色。反应方程式:
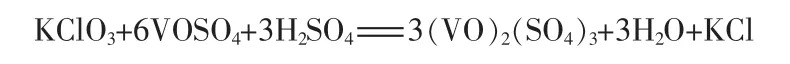
1.2.4 萃取
将氧化液pH调为2.3,用TOA-仲辛醇-煤油溶液作萃取液萃取V5+,V5+进入上层萃取相,其他杂质进入下层萃余相。分析萃取前后钒的含量,计算萃取回收率。经三级萃取,萃取率达99%以上。
用三正辛胺(TOA,R3N)萃取钒时,胺与溶液中的硫酸首先形成胺的硫酸盐,即所谓转型:式中,下角(O)为有机相,未加下角者为水相(下同)。
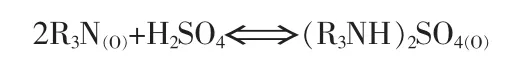
在pH=2.0~2.5时,溶液中钒酸根配合物与胺的硫酸盐萃取时的主要反应式:
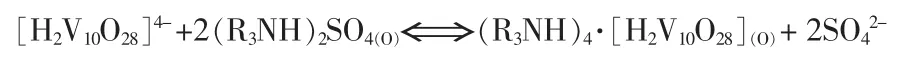
1.2.5 反萃取
将含有五价钒的有机相(萃取液)用NaOH+NaCl作为反萃体系进行反萃取。经过3次反萃,反萃取率可达99.4%。分相后的有机相(上层)作为萃取液可反复循环使用。
此外,反萃取过程中还应加入极少量过硫酸铵,使有机相中夹带的少量四价钒被氧化为五价钒,从而使钒酸铵晶体纯度提高。如果不加硫酸铵,则会降低有机相中钒的反萃率,同时破坏钒酸铵的结构,形成乳浊液,增加分相时间。
1.2.6 钒的回收
将反萃后水相的pH调至8左右,加入氯化铵,使之过量2倍左右,可使多钒酸铵转变成偏钒酸铵,沉淀率达99%以上。再经过滤、焙烧等工序,可得到红棕色的V2O5样品,纯度>99%。反应式:
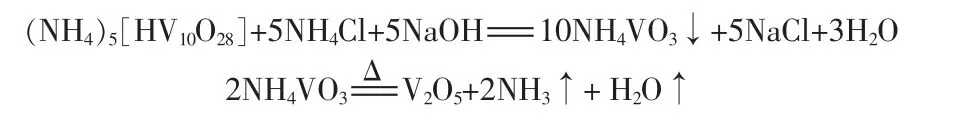
1.2.7 硫酸钾的制备
其他杂质在主要成分为K2SO4的萃余相中浓度很低,因此可以直接蒸发浓缩至一定密度,冷却、静置、过滤、干燥后得到的晶体即为硫酸钾产品。
1.2.8 工业液体硅酸钠的制备
废钒催化剂还原酸浸渣的主要成分为无定型二氧化硅、石英和方石英等,在一定温度下用一定浓度的氢氧化钠溶液浸取一段时间,过滤得到的滤液经适当蒸发,即为工业液体硅酸钠产品。主要反应:
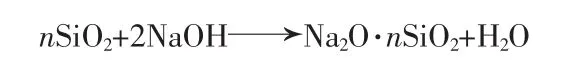
1.2.9 工艺流程(图1)
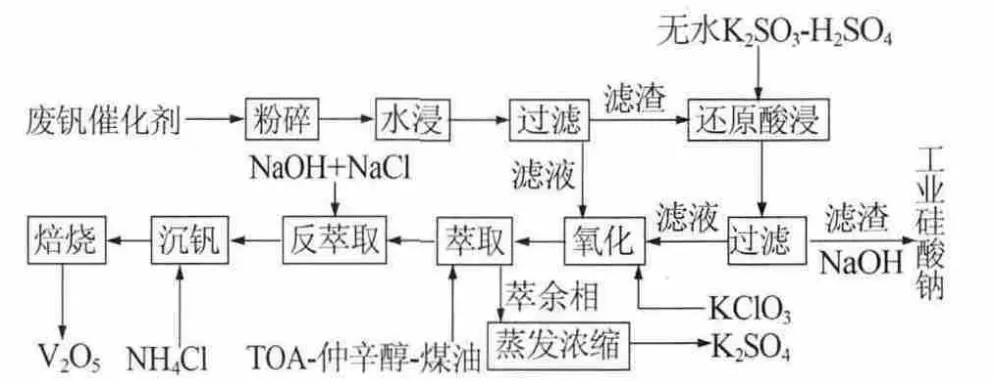
图1 工艺流程示意图
2 结果与讨论
2.1 萃取剂及其浓度对萃取的影响
钒的萃取剂,视钒在溶液中存在的形态不同来选择。三脂肪胺(如TOA)能萃取酸性介质中V5+的络合阴离子,磷类萃取剂能萃取酸性介质中的VO2+,季胺盐能在碱性溶液中萃取V5+;中性的VOCl2可用仲辛醇和三辛基氧化膦(TOPO)萃取[2]。废钒催化剂经水浸和还原酸浸的浸出液被氧化后,钒(V)以钒酸根络合阴离子形式存在,故可用三脂肪胺类萃取剂萃取。
在其他条件不变的情况下,考察了TOA含量(质量分数)对钒萃取率的影响,结果见图2。由图2可以看出,随着TOA含量的增加,钒的萃取率也随之升高。但TOA含量太高时,不仅会造成萃取液黏度增大、相分离困难,同时会令有机相在萃余水相中的损失增加,由此导致钒萃取率下降。因此,实验选择适宜的TOA起始质量分数为9%。
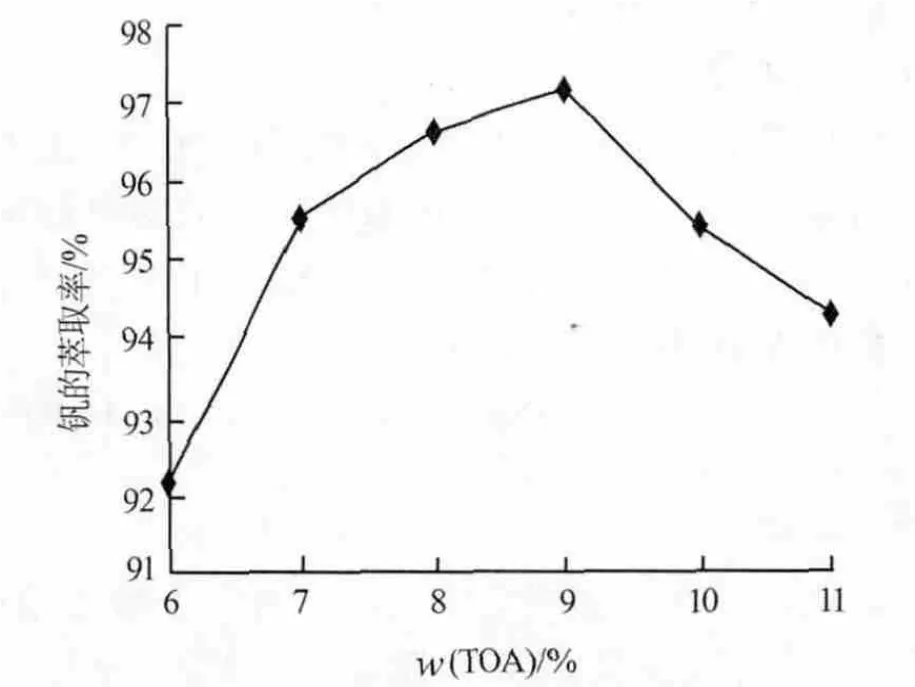
图2 TOA的含量对钒萃取率的影响
2.2 稀释剂对萃取的影响
在萃取液的组成中,加入稀释剂不仅能改变萃取剂浓度,对萃取能力起到有效调节和控制,使之易于被萃取离子和其他杂质分离,而且能改变萃合物在有机相中的溶解度,甚至能促使萃取剂萃取性质的改变。如用胺萃取钒时,稀释剂的极性越小,萃取剂胺的聚合状态越多(为二聚),则分配比越大,萃取能力越强。因此,不同稀释剂(如煤油、四氯化碳、氯仿、苯、低碳醇、高碳醇等)对萃取率的影响效果差别较大。经过比较得知,煤油作稀释剂时的效果较好。
2.3 调节剂对萃取效果的影响
实验通过对多种调节剂的选择对比,结果表明仲辛醇作调节剂时效果较佳。它不仅具有破乳作用,而且气味较正辛醇易于被人接受,价格低廉。在其他条件相同的情况下,考察了仲辛醇加入量(质量分数,%)对钒萃取率的影响,结果见表1。由表1可以看出,在有机相中添加调节剂仲辛醇,不仅能大大改善分相效果,减少有机相的损失,而且能保证萃取过程的顺利进行。综合考虑,实验选择适宜的仲辛醇加入量为3%。
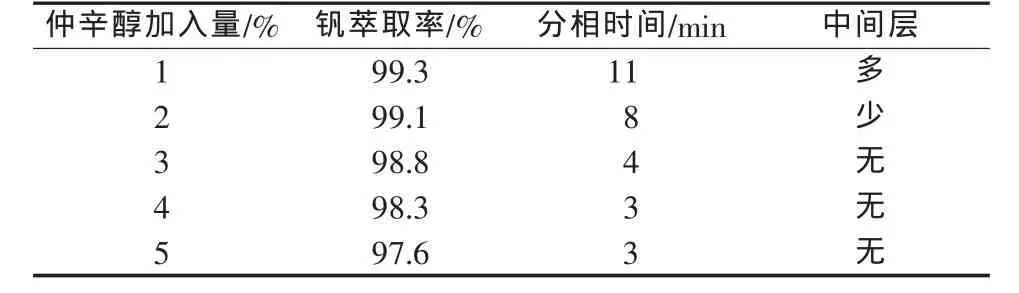
表1 仲辛醇加入量对钒萃取率的影响
2.4 水相pH与萃取时间对萃取的影响
钒在水溶液中,随着其浓度和pH的不同存在复杂的聚集状态,并且这些聚集状态之间处于互相共存的平衡体系。当其中某一种聚集状态的浓度增减时,平衡发生移动,一种聚集状态可能变成另一种聚集状态。一般来说,各含钒络阴离子中钒原子数(n)与含钒络阴离子的价数(z)的量荷比(n/z)越大,络阴离子的半径越大,水化程度就越弱,理论萃取量也就越大。大离子的空腔作用也有利于萃取。为了提高萃取量,应使被萃取的含钒阴离子具有最大的n/z值。调整溶液中的pH使溶液内的钒形成n/z值较大的含钒离子,对于萃取过程来说十分重要。在其他条件不变的情况下,实验考察了水相pH对钒萃取率的影响,结果见图3a。由图3a可见,溶液pH对钒萃取率影响很大,因此萃取过程中酸度要严格控制。综合考虑,实验选择适宜的水相pH在2.3左右。
在室温、水相pH=2.3、9%TOA+3%仲辛醇+88%煤油(均为质量分数)、有机相与水相体积比为1∶3、三级萃取的条件下,考察测定了萃取时间对钒萃取率的影响,结果见图3b。由图3b可见,在2 min以内,随着萃取时间的增加,有机相中钒的萃取率也随之增大。但萃取时间超过2 min时,钒萃取率变化不大,同时萃取设备也要相应增加。综合考虑,实验选择适宜的萃取时间为2.5 min。
2.5 反萃取剂浓度及反萃取时间对反萃取的影响
从三脂肪胺络合物中反萃钒是衡量萃取剂效果的重要性质之一。不少研究者认为:氨水或和氯化铵的溶液是较有效的反萃取剂。但它们的最大缺点是沉出的NH4VO3易粘附器壁,且偏钒酸铵中含有有机相,使萃取剂机械损失增加。考虑到工业生产的可能性,实验在其他条件相同的情况下,考察了反萃取剂组成对反萃效果的影响,结果见表2。
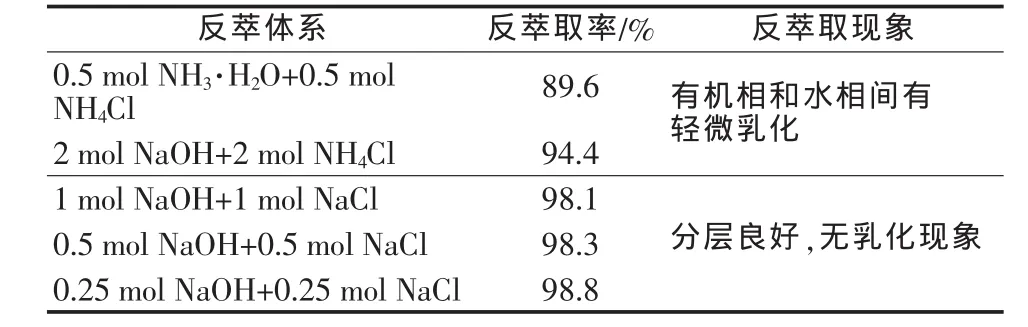
表2 反萃取组成对反萃取的影响(二级反萃) %
根据表2结果及减少反萃取剂消耗、控制水相适宜的酸碱度和沉淀偏钒酸铵所必须的钒浓度等方面考虑,采用0.25 mol NaOH+0.25 mol NaCl作为反萃液比较合适。
此外,实验还考察了反萃取时间(1~6 min)在室温、0.25 mol NaOH+0.25 mol NaCl、有机相与水相体积比为2∶1、pH>8、三级反萃的条件下对反萃取效果的影响。结果表明,反萃取时间越长,不但反萃取率会提高,而且有机相积存量和需求的设备也会相应增加。综合各种因素,实验选择适宜的反萃取时间为3 min,此时反萃取率高达99.4%。
2.6 产品质量
表3~5为按图1工艺流程得到的产品V2O5、K2SO4、工业液体硅酸钠与相应国家标准的对比。由表 3~5可见,实验制得的产品 V2O5、K2SO4、工业液体硅酸钠的主要化学组成均符合相应国家标准。
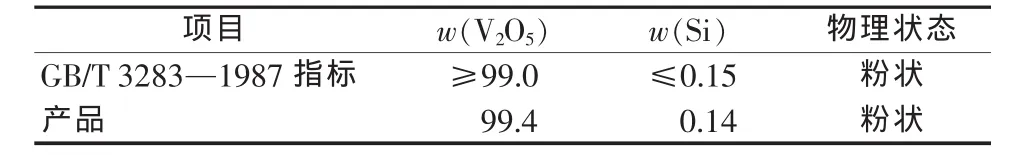
表3 五氧化二钒与GB/T 3283—1987《五氧化二钒》标准对比 %
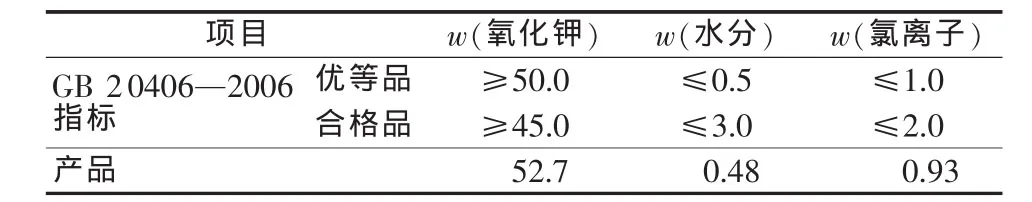
表4 硫酸钾与GB 20406—2006《农业用硫酸钾》标准对比 %

表5 工业液体硅酸钠与GB/T 4209—2008《工业硅酸钠》标准对比 %
3 结论
1)以废钒催化剂为原料,经水浸-还原酸浸-萃取-沉钒等环节制得五氧化二钒、硫酸钾、工业液体硅酸钠的工艺,不仅综合回收利用了钒、钾、硅,而且产品的主要成分含量均达到了相应国家标准的要求,实现了变废为宝的目的,具有显著的环境效益、经济效益和社会效益。
2)从氧化后的废钒催化剂浸出液中萃取多钒酸根络阴离子时,被萃取物量荷比大,加上萃取物离子半径以及盐析作用等多种因素,TOA对钒的选择性很高,钒在萃取相与萃余相中的分配比很大,且不与铁等其他金属杂质发生作用,故无需预先除去铁等其他金属杂质离子,可直接萃取提钒。这样既减少了部分除杂工作、节省原料消耗,又可直接制备高纯产品。
3)废钒催化剂回收工艺条件:将废钒催化剂磨碎至375 μm左右,经水浸和还原酸浸的浸出液经氧化后,在水相pH为2.3时,用9%TOA-3%仲辛醇-88%煤油(均为质量分数)溶液萃取,在浸取时间为2.5 min条件下,经三级萃取,钒的萃取率达99%以上;在pH>8、反萃取剂为0.25 mol NaOH+0.25 mol NaCl、反萃时间为3 min、反萃取级数为3的情况下,钒的反萃取率高达99.4%。
4)该工艺的钒、钾回收率分别达91.5%和93.8%,适合于一般有条件的小型化工厂生产。
[1]刘彬,于少明,张颖,等.废钒催化剂综合回收利用技术的研究[J].无机盐工业,2012,44(11):57-59.
[2]周崇清.钒的萃取[J].湿法冶金,1993(2):30-36.
[3]蒋馥华,张萍.用溶剂萃取法从废钒催化剂制备高纯五氧化二钒[J].硫酸工业,1996(2):32-36.
[4]李尚勇,谢刚,俞小花.从含钒浸出液中萃取钒的研究现状[J].有色金属,2011,63(1):100-104.
[5]戚文彬.表面活性剂与分析化学 上册[M].北京:中国计量出版社,1986:143.
[6]徐光宪,袁承业.稀土的溶剂萃取[M].北京:科学出版社,1987:113.
