水合肼催化还原法制备4-氨基二苯胺
2014-10-09程正载王从月林素素颜晓潮
程正载,龚 凯,王 洋,王从月,林素素,颜晓潮
(1.武汉科技大学化工学院,湖北 武汉 430081;2.湖北省煤转化与新型炭材料重点实验室,湖北 武汉 430081;3.南加州大学化工系,美国 洛杉矶 CA90089;4.温州市环境保护局,浙江 温州 325027)
4-氨基二苯胺俗称RT培司,又称对氨基二苯胺,是一种重要的橡胶和纺织防老剂中间体,主要用于生产对苯二胺类橡胶防老剂4010、4010NA、4020和688等[1]。4-氨基二苯胺常用的合成方法主要有苯胺法、甲酰苯胺法、硝基苯法和二苯胺法[2]。4-氨基二苯胺大多数是由4-硝基二苯胺还原得到,而4-硝基二苯胺通常都由苯胺法或甲酰苯胺法制备;4-氨基二苯胺也可通过硝基苯法合成4-硝基二苯胺与4-亚硝基二苯胺的混合体系,再加氢还原制得。还原硝基化合物的方法主要有活泼金属还原法、硫化物还原法、催化氢化法[3]。由于加氢催化还原三废少,产品质量和收率较高,备受厂家的青睐,是生产4-氨基二苯胺的发展方向之一[2]。加氢还原的主要影响因素为催化剂的选择[4]。文献[5]报道了二苯胺直接合成4-氨基二苯胺法,该法简化了生产工艺流程,同时避免了接触致癌性中间物N-亚硝基二苯胺等亚硝基有机化合物的可能性,产物收率可达93.5%。Ankur A Banerjee等[6-7]以 Raney nickel作为催化剂,当以异丙醇作为供氢体溶剂时,产物收率可达到95%;而以4-甲基-2-戊醇作为供氢体溶剂时,产物收率只3%;此外,他们还以5%palladium-on-carbon代替Raney nickel作为催化剂,以甲酸作为供氢体溶剂,在85℃催化还原4-硝基二苯胺,收率可达100%。朱建良等[8]开发了一种廉价的负载型加氢还原催化剂,即采用Ni/C加氢还原对硝基二苯胺,4-硝基二苯胺的转化率大于99%,产物4-氨基二苯胺收率大于95%。而以水合肼为还原剂,配以Fe(OH)3/C为催化剂还原4-硝基二苯胺的相关文献未见报道,该法相对于其他几种还原方法,原料来源更广泛,产率高,实验操作简单,对环境十分友好。
1 实验部分
1.1 主要仪器和试剂
85-2型恒温磁力搅拌器,常州国华电器有限公司;VERTEX 70型傅里叶变换红外光谱仪,德国BRUKER公司;1100LC-MS液相色谱-质谱仪,美国Agilent公司。
4-硝基二苯胺按文献[9]方法制得;80%水合肼,CP,湖北大学化学试剂厂;无水乙醇,AR,国药集团化学试剂有限公司。
1.2 还原反应催化剂的合成[10-12]
在250mL锥形瓶中加入2.10g FeCl3·6H2O和0.21g AlCl3,再加入15g活性炭(用40%硝酸处理:于70℃活性炭在40%硝酸中加热回流40min,然后在蒸馏水中回流洗涤9次,每次20min,最后用乙醇溶液回流洗涤20min,过滤,烘干),磁力搅拌下加入2.4g NaOH,于60℃水浴恒温2h,冷却后减压抽滤,然后将滤饼放入80℃的真空干燥箱烘干,得到Fe(OH)3负载量约5%(质量分数,下同)的Fe(OH)3/C复合催化剂14.56g。运用同样的方法可制得Fe(OH)3负载量约10%的Fe(OH)3/C催化剂。
1.3 对氨基二苯胺的合成
将0.05mol 4-硝基二苯胺和0.45g Fe(OH)3/C加入到Schlenk柱形瓶中,用真空泵抽真空,通入氮气,置换三次,用注射器向反应瓶中加入20mL无水乙醇,加热至80℃,保持30 min,使对硝基二苯胺充分溶解于乙醇当中。之后再向反应瓶中注入5mL 80%水合肼,为使反应完全,水合肼选择过量。在80℃保温反应1h。
反应结束后,减压蒸除乙醇,冷却静置至瓶底部有灰色结晶生成。测得结晶熔点为71~75℃,初步断定为对氨基二苯胺。
2 结果与讨论
2.1 催化合成反应结果及催化性能分析
实验得到高纯度的4-氨基二苯胺,表明Fe(OH)3/C催化体系对4-硝基二苯胺类化合物具有较好的催化性能,收率最高达到98.6%,目标产物纯度超过95%。该类反应的催化机理是高价态的铁被水合肼还原成低价铁,低价铁进而还原硝基化合物成为相应的胺类化合物,而自身则恢复为高价态Fe(Ⅲ)[13],即Fe(Ⅱ)/Fe(Ⅲ)的“氧化还原循环对”是Fe(OH)3/C催化4-硝基二苯胺反应的真正活性中心。
2.2 4-氨基二苯胺合成结果分析
2.2.1 LC-MS分析
图1为合成产物的LC分析结果,表明所得产物纯度超过95%(质量分数)。

图1 4-氨基二苯胺液相色谱
MS:m/z=184 (M+),167,107,91,80,65,51,39。由图2可看出:m/z=184.0与相邻的质荷比较小的m/z=167.3关系合理,可以认为m/z=184.0的峰为分子离子峰;m/z=167.3的峰为失去—NH2的碎片峰;m/z=166.0的峰为脱去一个—NH2而形成C6H5NHC6H4—碎片离子峰;m/z=107.0的峰为失去一个苯环而形成的碎片离子峰;m/z=92.2的峰为仲胺的—N键断裂而形成的 C6H5NH—碎片离子峰[14];m/z=38.8,51.0,65.1,77.1为芳香碳氢碎片。

图2 4-氨基二苯胺质谱
2.2.2 IR分析
图3为4-氨基二苯胺的红外光谱。

图3 4-氨基二苯胺的红外光谱
由图3可知:3475.3和3441.8cm-1处为伯胺的伸缩振动吸收峰,可以确定该化合物中含有—NH2基团。2359.9cm-1处为芳香族仲胺中N—H键伸缩振动吸收峰,1689.5cm-1处为芳香族仲胺中N—H键弯曲振动吸收峰,可以确定该化合物结构中含有亚胺基(—NH—)。1591.9,1510.4cm-1处为苯环 C ==C 骨架振动吸收峰;3045.3,3021.3cm-1处为弱的芳环==C —H 伸缩振动吸收峰。1203.0,1181.0,1109.6cm-1处为芳香族伯胺C—N键伸缩振动吸收峰。1122.9cm-1处为芳香族仲胺C—N键伸缩振动吸收峰。837.0,687.5,750.8cm-1处有3个芳环=C—H键弯曲振动。
2.3 合成条件对反应的影响
2.3.1 反应温度
反应温度对反应的影响见表1。
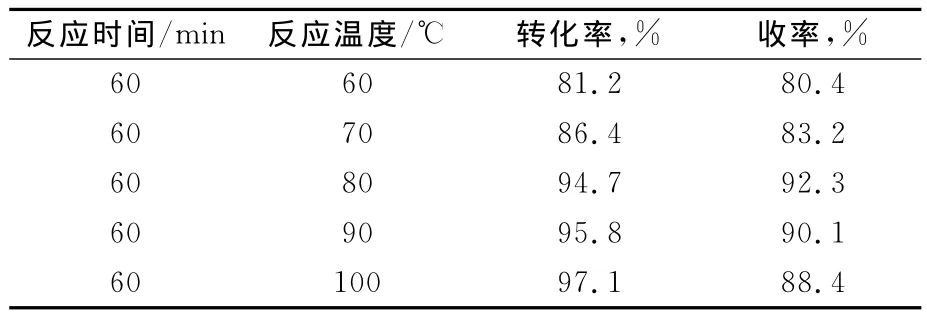
表1 不同温度对反应的影响
由表1可知:随着反应温度升高,转化率提高,较佳的反应温度为70~80℃。实验中发现,当温度高于80℃时,水合肼一经滴入就会马上分解产生大量气泡,一部分初生态氢来不及与硝基反应而逸出,从而影响反应的收率。
2.3.2 催化剂用量和含量
催化剂用量对反应收率(质量分数)的影响结果见表2。
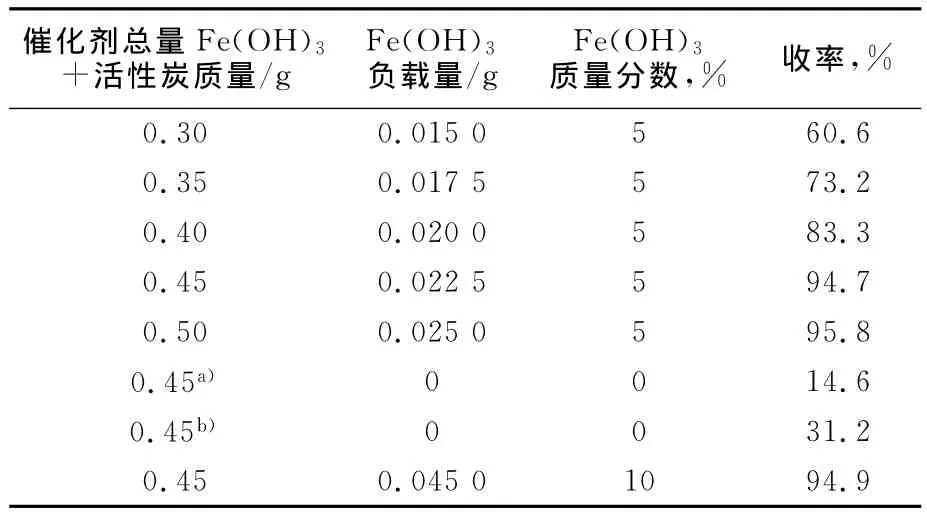
表2 不同催化剂用量和含量对反应的影响
由表2可知:1)未经酸处理并且未负载铁的活性炭的催化活性很低(收率小于15%),而经酸化学处理后的活性炭表面因形成了含氧官能团,可引发水合肼分解,并影响4-硝基二苯胺的吸附而具有一定的催化活性,目标产物收率提高近1倍。这与文献[15]结果相似;2)Fe(OH)3负载量为5%的复合催化体系得到收率相当于未负载Fe(OH)3但经过酸处理的活性炭催化所得到的收率的3倍;进一步提高Fe(OH)3/C催化体系的质量或Fe(OH)3负载量,收率均无明显影响。由此可见,酸化学处理活性炭和Fe(OH)3的组合催化体系效率更高。较低的铁负载量对产物后续的分离纯化更为有利[16],故实验首选硝酸化学处理的活性炭,再负载约5%的Fe(OH)3组成0.45g复合催化剂。
产生以上结果的原因是:复合催化剂中Fe(OH)3起到主催化剂作用,酸处理过的活性炭具有部分催化作用,也有利于2种反应物料在其上的吸附;Fe(OH)3负载量加大,催化剂活性中心数目相应增加,加快催化还原反应的进行。采用多孔性的酸处理过的活性炭来负载少量的高活性的Fe(OH)3,可以增加单位量的高价铁催化活性中心与吸附态的反应物料间的接触机会,催化还原反应效率大大提高。
2.3.3 水合肼用量
水合肼在一定温度和催化剂条件下分解出氢气,进而还原4-硝基二苯胺,得到4-氨基二苯胺。为使反应充分进行,理论上水合肼的用量应该过量。基于使用的催化体系具有很高的催化效率,水合肼用量不必过多。在复合催化剂用量0.45 g、反应温度80℃的条件下,考察水合肼用量对反应的影响,结果见表3。

表3 水合肼用量对反映的影响
由表3可知:当水合肼用量小于5.0mL时,随着水合肼用量的增加,反应收率明显增加,这说明了水合肼过量的必要性。但随着水合肼用量的进一步增加,收率没有太大的变化,这说明此时反应物已经基本还原完全,水合肼的用量对反应已经不会产生决定性的影响。综合考虑,选取水合肼用量5.0mL为最佳反应用量。
3 结 论
a.以水合肼催化还原法制备4-氨基二苯胺,较佳工艺条件为:4-硝基二苯胺用量0.05mol,含Fe(OH)3负载量约5%的Fe(OH)3/C催化剂0.45 g,水合肼5mL,反应温度80℃,反应时间60min,所得产物4-氨基二苯胺的收率可达到98.4%。
b.采用水合肼催化还原法制备4-氨基二苯胺不仅可以避免硫化碱还原带来的比较严重的“三废”污染和可能导致下游产品催化剂中毒的问题,而且还能避免加氢催化对设备要求较高和催化加氢工艺不完善的限制。水合肼催化还原法得到的产物收率较高,清洁环保。
[1]钱伯章,王祖纲.精细化工技术进展与市场分析[M].北京:化学工业出版社,2005:121-122.
[2]郭传顺.甲酰苯胺法催化加氢还原制RT培司工艺研究及条件优化[D].南京:东南大学,2006.
[3]李君,蒋毅,程极源.对苯二胺类防老剂的合成[J].合成化学,2000,8(1):34-38.
[4]张超林.硝基苯法制备对氨基二苯胺的研究进展[J].化工进展,2008,27(2):180-183.
[5]Symon T.Preparation of p-aminodiphenylamines:US,4313002[P].1982-01-26.
[6]Banerjee A A,Mukesh D.Heterogeneous catalytic transfer hydrogenation of 4-nitrodiphenylamine to p-phenylenediamines[J].J Chem Soc Chem Commun,1988(8):1275-1276.
[7]Banerjeea A A,Mukesha D.Heterogeneous catalytic transfer hydrogenation reactions of 4-nitrodiphenylamine[J].Applied Catalysis,1990,59(1):1-12.
[8]朱建良,秦文荣,欧阳平凯.强碱性体系中4-硝基二苯胺催化加氢还原工艺研究[J].南京工业大学学报,2002,24(6):48-51.
[9]郭佃顺,黄汝骐,高蓉华,等.4-硝基二苯胺合成方法的改进[J].化学通报.1995(7):43-44.
[10]Lauwiner M,Rys P,Wissmann J.Reduction of aromatic nitro compounds with hydrazine hydrate in the presence of an iron oxide hydroxide catalyst:Ⅰ.the reduction of monosubstituted nitrobenzenes with hydrazine hydrate in the presence of ferrihydrite[J].Applied Catalysis A:General,1998,172(1):141-148.
[11]Lauwiner M,Roth R,Rys P.Reduction of aromatic nitro compounds with hydrazine hydrate in the presence of an iron oxide/hydroxide Catalyst:Ⅲ.The selective reduction of nitro Groups in aromatic azo compounds[J].Applied Catalysis A:General,1999,177(1):9-14.
[12]孙汉洲,赵芳,邓集平,等.2,2-二(4-羟基-3-氨基)苯基丙烷的合成[J].合成化学,2004,12(5):508-510.
[13]Benz M,Van der Kraan A M,Prins R.Reduction of aromatic nitrocompounds with hydrazine hydrate in the presence of an iron oxide hydroxide catalyst:Ⅱ.activity,X-ray diffraction and Mössbauer study of the iron oxide hydroxide catalyst[J].Applied Catalysis A:General,1998,172(1):149-157.
[14]何永利.4-氨基二苯胺合成工艺研究[D].南京:南京理工大学,2009.
[15]周宏跃,石雷,孙琪.酸处理活性炭催化水合肼还原硝基苯[J].催化学报,2012,33(9):1463-1469.
[16]蔡可迎,周颖梅,岳伟.FeO(OH)/C催化水合肼还原芳香族硝基化合物制备芳胺[J].化学世界,2009(7):418-419.
