阳离子有序相 Ce2Zr2O7.97的石墨还原制备及其结构表征
2014-09-18罗德礼芮筱亭
谢 华,江 阔,罗德礼,芮筱亭
(1.表面物理与化学重点实验室,四川 绵阳 621907;2.南京理工大学 材料科学与工程学院,江苏 南京 210094;3.西南科技大学 核废物与环境安全国防重点学科实验室,四川 绵阳 621010)
烧绿石型 A2Zr2O7+x(A=Ln或 An;0≤x≤1)因具有优异的抗辐照能力和良好的化学稳定性,被认为是高放废物、尤其是长寿命超铀核素的理想候选固化介质材料。Yamamura等[1]和 Otobe 等[2]已 成 功 合 成239Pu2Zr2O7、241Am2Zr2O7,并发现该固化体在自辐照室温条件下放置1年,其结构将从有序的烧绿石向无序的萤石发生转变;随后,Sykora等[3]在An2Zr2O7(An=Am,Cf)固化体中亦观察到相同的相转变,他们采用Kim[4]提出的萤石相晶胞常数估算法计算得到烧绿石Cf2Zr2O7在存放1年后其 Cf3+/Cf4+摩尔比为1∶6,根据Pauling静电价规则,为平衡多余的、占据烧绿石中氧空位的氧离子,Cf3+必须给出电子以实现电荷平衡,由此引起Cf及Zr原子周围配位环境发生改变,导致有序的烧绿石结构将逐渐向亚稳、富氧相Cf2Zr2O7+x(0<x≤1)以及缺氧型萤石结构 Cf0.5Zr0.5O2-y转变。因此,对于烧绿石型锕系核素固化体的结构稳定性及对抗辐照等性能的影响值得重点关注和研究。
由于Ce是三价超铀核素良好的模拟物,Ce2Zr2O7展现出与An2Zr2O7极其相似的物理化学性质。Tsuyoshi等[5]发现将Ce2Zr2O7暴露在空气中,其晶胞常数将从1.075nm逐渐降至1.065nm。因此,采用 Ce2Zr2O7+x体系模拟研究 An2Zr2O7+x(0<x≤1)的结构稳定性具有很好的借鉴价值。目前,已报道的Ce2Zr2O7+x系列化合物有以及 Ce2Zr2O8(P213)[8,10-11]等。通过文献调研不难发现,以上各种材料的制备工艺较为苛刻,均需通过氩氢还原首先制备出纯相的烧绿石相Ce2Zr2O7,之后再将其置于氧气或暴露于空气中氧化得到。在氩氢还原条件下制备纯相Ce2Zr2O7要求还原温度高于1 400℃,还原时间不少于48h,且需反复还原4次以上方能得到,再加之氧化阶段的氧浓度较难控制,从而限制了对Ce2Zr2O7+x材料的研究与开发。
受CeO2催化氧化CO气体的启发[12],本文提出一种sol-喷雾热解与石墨还原相结合的方法制备Ce2Zr2O7+x相,并通过改变还原时间和温度等工艺参数,探索在不同还原条件下Ce2Zr2O7+x的相结构及与氩氢还原法的异同。
1 实验
1.1 实验材料及样品合成
实验选用纯度为99.99%的 Ce(NO3)3·6H2O、Zr(NO3)4·3H2O 粉末为初始原料,准确称量后将其分别配制成浓度为0.1mol/L的标准水溶液,之后按照n(Ce)∶n(Zr)=1∶1取标液混合并搅拌约0.5h,向混合液中加入适量的柠檬酸、聚乙二醇20000和质量浓度为65%~68%的浓硝酸添加剂以获得澄清透明溶胶。还原样品前驱体的制备在sol-喷雾热解装置(图1)中进行,实验采用0.3MPa的压力将澄清溶胶雾化到温度为600℃、φ20mm×50mm的刚玉坩埚内,收集样品在400℃的炉中煅烧2h以去除挥发性物质,待用。还原实验在有石墨参与的还原装置(图2)中进行,称取约200mg煅烧粉末置于该装置中进行石墨还原实验,其还原工艺参数列于表1。

图1 sol-喷雾热解装置示意图Fig.1 Diagrammatic sketch of sol-spray pyrolysis device

图2 石墨还原装置示意图Fig.2 Diagrammatic sketch of graphite reduction device

表1 样品还原工艺参数Table 1 Reduction process parameter of sample
1.2 测试及表征
采用X’pert-PRO型X射线衍射仪(荷兰帕那科公司)对合成粉体进行物相分析(Cu Kα1靶,λ=0.154 06nm,步进0.02°,扫描角度10°~90°)。红外光谱采用KBr压片法,仪器为德国BR公司VER型红外光谱分析仪,波数范围为400~4 000cm-1;样品的结构精修选用 GSAS程序[13],其峰形及本底分别采用Pseudo-Voigt函数和六次多项式进行拟合,最后对各原子位置、原子位置占有率及其温度因子进行修正。
2 结果及讨论
不同还原温度(Tred)、相同还原时间(t=24h)条件下获得的样品XRD谱示于图3。从图3a可知,当还原温度达1 000℃时,样品将形成c-(Ce0.75Zr0.25)O2相 (PDF:28-271)和t-(Zr0.88Ce0.12)O2相 (PDF:82-1398)两 种 固 溶体,但无法获得单相 Ce2Zr2O7+x。参照 CeO2-ZrO2二元体系相图[13]可知,共晶温度Te=(1 050±50)℃是其发生共晶转变的临界温度,当Tred>Te时,其烧结产物为c+t相;当Tred<Te时,具有[ZrO6]结构的t相将转变为[ZrO7]配位的m相。而本实验仍能在缓慢降温过程中将t相保持至室温,这可能归因于以下3方面的原因。首先,sol-喷雾热解法是制备纳米热障涂层材料的常规方法,根据谢乐公式估算可知,本实验获得的t相粒径约为45nm。Garvie[14]的实验结果表明,当t相粒径小于30nm时,其表面能将低于m相,t相能在室温下稳定存在。因此,t相纳米晶的获得可能是本实验中观察到t相的主要原因之一。其次,Ce4+的离子半径较的大,Ce4+掺杂ZrO2将增加ZrO2的晶格常数并减少ZrO2局部的氧-氧排斥力,从而增加t-ZrO2的稳定性。Li等[15]和Cohen等[16]发现向ZrO2中掺杂大离子半径Ce4+或U4+能保持c-ZrO2相至室温是其例证。另外,石墨易与氧气发生反应生成CO和CO2的混合气体,其作用相当于消耗了还原装置中部分氧气而导致氧分压降低,且这种弱的还原环境一直存在于整个实验过程中。Rauh等[17]的研究结果表明,ZrO2易在缺氧环境下形成缺氧型ZrO2-x,其氧空位浓度与氧分压的1/6次方呈反比,氧空位浓度对氧分压非常敏感。而分布在氧化锆体内锆离子周围的空位不仅降低了局部氧-氧间的排斥力,使配位层产生较大的畸变,而且释放了部分层间应力促进了t-ZrO2的稳定。因此,缺氧型t-ZrO2-x相的生成可能也是其在室温下稳定存在的原因之一。

图3 不同还原温度和还原时间条件下各样品的XRD谱Fig.3 XRD spectra of samples under different reduction temperatures and time
继续提高石墨还原温度至1 050℃,之前形成的c+t固溶体将被一种新的单相化合物所取代,该结果完全违背了CeO2-ZrO2二元相图在相同条件下给出的相组成,说明在有石墨参与的烧结环境中,其物相合成机理与空气气氛完全不同。更值得关注的是,获得的还原相拥有与烧绿石相同的有序阳离子结构,其表征阳离子有序的特征衍射峰(111)、(311)、(331)、(511)非常明显。随着还原温度的进一步升高(1 100℃≤Tred≤1 300℃),不同还原温度产物的XRD谱几乎不再发生改变,说明当Tred≥1 050℃时,合成的还原相应具有相同的晶体结构。但仔细观察不难发现,(111)特征峰随还原温度的降低明显展宽,峰展宽可能意味着其结构中存在平行于{112}方向的反相筹界[18],该相界打破了长程有序的Ce/Zr原子排列,即随还原温度的降低,阳离子有序化程度将随之下降。虽然还原产物的物相相同,但其结构中局部阳离子排列与氧的配位环境仍存在细微差别。另外,在1 100℃≤Tred≤1 300℃范围内,不再观察到明显的相变现象,说明还原相中的Ce元素未发生进一步的成分偏移,烧绿石型还原相能在1 050~1 300℃还原温度区域内稳定存在。
还原样品随还原时间变化的XRD谱如图3c所示(Tred=1 050℃)。从图3可知,不同还原时间产物的XRD谱非常相似,说明延长时间不会导致其发生相分离,这与YSZ在1 425℃、含氧静态空气中发生热降解的机制完全不同。还原相稳定存在的原因仍应归因于样品烧结气氛的差异。由于实验结束后石墨仍有大量残余,证明在整个实验过程中,均有石墨与氧气相互作用并主导样品的合成气氛。Sanjuán等[19]发现在空气气氛中升高烧结温度,其作用等同于提高样品的还原气氛,根据CeO2-ZrO2二元相图,各相中Ce含量将随还原气氛的增加(即随烧结温度的提高)而向设计成分靠近。在本实验中,由于弱的还原气氛一直存在,还原产物则被保持至室温而不发生分解。但将最强衍射峰(222)面放大后不难看出,各还原样品的XRD衍射峰仍存在细微差别,其规律为:随还原时间的延长,(222)晶面呈规律性向低角度偏移,还原相的晶格常数值增加。该现象是否为热应力导致的晶格膨胀尚有待进一步研究。

图4 样品的IR谱Fig.4 IR spectra of samples
不同还原条件下制备的样品IR谱如图4所示。可看出,3种还原温度和时间下获得的样品IR谱很相近,说明这些条件下获得的物相相同,与前面XRD谱结果完全吻合。但当Tred从1 300℃降至1 200℃及以下时,407cm-1处的振动峰将发生劈裂(411和419cm-1)。众所周知,IR谱主要反映晶格的对称性和分子中化学键的极性。振动峰发生劈裂应归因于不同还原样品中Ce/Zr原子的氧配位环境不同。
为进一步明确还原相的晶体结构,将Tred=1 050℃、t=24h条件下获得的样品XRD谱与烧绿石相Ce2Zr2O7的标准XRD卡进行了对比分析,结果发现还原样品的衍射角明显向右偏移,晶格常数较烧绿石相的小,这意味着在石墨参与的还原实验中,形成的还原气氛较弱以致无法获得Ce2Zr2O7相。目前,在已报道的Ce2Zr2O7+x系列物相[5,7-12]中的晶体结构均可容纳有序阳离子的亚晶胞。将还原相的IR谱(图4)与 Thomson等[6-7]给出的 Ce2Zr2O8的IR谱对比不难发现,两者的振动频率非常接近,说明在石墨参与的弱的还原条件下,获得的物相可能属于富氧相或Ce2Zr2O8(P213)。进一步对比 Ce2Zr2O8的XRD谱发现,Ce2Zr2O8相中除具有表征阳离子有序的超结构峰外,还存在如(110)、(200)等微弱的特征峰,而从本实验所得还原样品的XRD谱(图1a)中却未能观察到这些谱峰,因此初步推断所获得样品的结构可能属于空间群。将Tred=1 100℃、t=24h下获得的还原样品的XRD谱与Ce2Zr2O7.97的标准谱进行了全谱拟合,其拟合度分别为Rwp=12.62%,Rp=8.9%,拟合效果图如图5所示,精修所得晶胞参数分别为a=1.054 75(6)nm,V=1.173 426nm3,该值与文献[9]的精修结果接近。从35°~40°及42°~45°衍射区放大图也不难看出其计算与实验值完全吻合。因此,本实验在石墨还原条件下生成的物相被确定为空间群为的富氧相Ce2Zr2O7.97。而从精修所得结构数据(表2)可知,该物相结构中包含有4种不同的Ce原子、Zr原子以及11种氧原子。从原子占有率结果不难看出,与烧绿石结构中氧空位(8b/32e)对应的3个氧位(O3、O4、O11)均被氧离子不同程度地填充,其占有率分别为0.206 (5)、0.370(2)、0.506 (3)。以上精修结果说明石墨所形成的还原气氛较弱,无法阻止瞬间形成的氧空位又被快速扩散的氧离子所填充。根据Thomson等对Ce2Zr2O7.97相的晶体结构的解析结果[9]可知,Ce与Zr的氧配位数均超过8,致使Ce2Zr2O7.97相的晶体结构对称性降低。
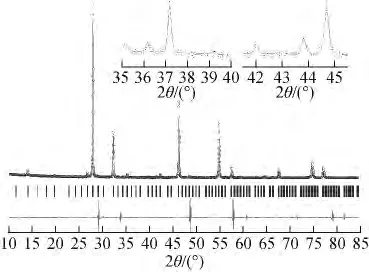
图5 Tred=1 100℃、t=24h还原条件下获得的样品XRD结构精修谱Fig.5 Rietveld XRD spectrum for sample prepared under reduction conditions of Tred=1 100℃ and t=24h

表2 Tred=1 100℃、t=24h还原条件下获得的样品XRD结构精修数据Table 2 Refined structure data for sample prepared under reduction conditions of Tred=1 100 ℃ and t=24h
3 结论
采用石墨还原法在相同还原时间(24h)不同温度范围(1 050℃≤Tred≤1 300℃)内,以及相同还原温度(Tred=1 050℃)不同还原时间(24h≤t≤72h)内均可合成 Ce2Zr2O7.97单相样品,且该还原相在以上条件下均能稳定存在并一直保持至室温而不发生热分解,其稳定机制主要归因于石墨消耗还原装置中的氧所形成的弱的还原气氛,这为An2Zr2O7+x废物固化体的存放环境提供了参考。还原产物Ce2Zr2O7.97具有与烧绿石相Ce2Zr2O7相同的有序阳离子结构,但其氧空位被大部分氧离子所填充,说明实验中还原气氛太弱以致于无法阻止快速扩散的氧离子向晶体内部的氧空位迁移,最终导致Ce2Zr2O7.97相晶体结构对称性低于烧绿石相Ce2Zr2O7。本文提出的采用石墨还原法制备富氧相Ce2Zr2O7.97有望成为一种较传统制备工艺更简单经济的新方法。
[1]YAMAMURA H,NISHINOA H,KAKINUMAA K,et al.Thermal expansion and solubility limits of plutonium-doped lanthanum zirconates[J].Solid State Ionics,2003,158(1-2):359-365.
[2]OTOBE H,AKABORI M,ARAI Y,et al.Oxygen potentials of(Am0.5Np0.5)O2-x[J].Journal of the American Ceramic Society,2009,92(2):174-178.
[3]SYKORA R E,RAISON P E,HAIRE R G.Self-irradiation induced structural changes in the transplutonium pyrochlores An2Zr2O7(An=Am,Cf)[J].Journal of Solid State Chemistry,2005,178(1):578-583.
[4]KIM D J.Effect of Ta2O5,Nb2O5,and HfO2alloying on the transformability of Y2O3-stabilized tetragonal-ZrO2[J].Journal of the American Ceramic Society,1990,73(1):115-120.
[5]TSUYOSHI S,YOSHIO U,KURODA K.Crystal structure of Ce2Zr2O7andβ-Ce2Zr2O7.5[J].Journal of the Ceramic Society of Japan,2004,112(1):440-444.
[6]THOMSON J B,ARMSTRONG A R,BRUCE P G.A new class of pyrochlore solid solution formed by chemical[J].J Am Chem Soc,1996,118(65):11 129-11 133.
[7]THOMSON J B,ROBERT A,BRUCE G.An interstitial pyrochlore formed by chemical intercalation of oxygen[J].Chemical Communications,1996,10(3):1 165-1 166.
[8]OTSUKA Y S,IZU N,OMATA T,et al.Thermodynamic behavior of various phases appearing in the CeZrO4-CeZrO3.5system and the formation of metastable solid solutions[J].Journal of Electrochemical Society,1998,145(4):1 406-1 413.
[9]THOMSON J B,ROBERT A,BRUCE G.An oxygen-rich pyrochlore with fluorite composition[J].Journal of Solid State Chemistry,1999,148(1):56-62.
[10]OTSUKA Y S,IZU N,OMATA T,et al.Oxygen release behavior of CeZrO4powders and appearance of new compoundskandt*[J].Journal of Solid State Chemistry,1998,138(2):47-54.
[11]OMATA T,KISHIMOTO H,OTSUKA Y M,et al.Vibrational spectroscopic and X-ray diffraction studies of cerium zirconium oxides with Ce/Zr composition ratioZ1prepared by reduction and successive oxidation oft0-(Ce0.5Zr0.5)O2phase[J].Journal of Solid State Chemistry,1999,147(1):573-583.
[12]LAACHIR A,PERRICHON V,BADRI A,et al.Reduction of CeO2by hydrogen magnetic susceptibility and Fourier-transform infrared,ultraviolet and X-ray photoelectron spectroscopy measurements[J].Journal of the Chemical Society:Faraday Transactions,1991,87(1):1 601-1 607.
[13]EWI T,MASAHIRO Y,SHIGEYUKI S.Revised phase diagram of the system ZrO2-CeO2below 1 400 ℃ [J].Journal of the American Ceramic Society,1983,66(7):506-510.
[14]GARVIE R C.Occurrence of metastable tetragonal zirconia as a crystalline size effect[J].Journal of Physical Chemistry,1965,69(1-2):1 238-1 243.
[15]LI P,CHEN I W,HAHN E P.Effect of dopants on zireonia stabilization—An X-ray absorption study,Ⅱ:Tetravalent dopants[J].Journal of American Ceramic Society,1994,77(5):1 281-1 288.
[16]COHEN I,SEHANER B E.Ametallographic and X-ray study of the UO2-ZrO2system[J].Journal of Nuclear Materials,1963,9(1):18-52.
[17]RAUH E G,GARG S P.The ZrO2-x(cubic)-ZrO2-x(cubic+tetragonal)phase boundary[J].Journal of the American Ceramic Society,1980,63(1-2):239-240.
[18]TOSHIHIRO M,YOSHIASA A,KANAMARU F,et al.Structure analyses of the pyrochlore-and fluorite-type Zr2Gd2O7and anti-phase domain structure[J].Solid State Ionics,1989,31(1):319-328.
[19]SANJUÁN M L,OLIETE P B,VÁREZ A,et al.The role of Ce reduction in the segregation of metastable phases in the ZrO2-CeO2system[J].Journal of the European Ceramic Society,2012,32(1-2):689-696.
