抗癫疒间肽纳米粒的制备及体外释药性能的研究
2014-08-15王石健王彬辉章文红张晓芬
王石健,王彬辉,章文红,张晓芬,吴 敏
0 引言
抗癫疒间肽(Anti-epilepsy peptide,AEP)是从东亚钳蝎粗毒液中分离的一种具有生物学活性的多肽,分子量为8 300 Da,有良好的抗癫疒间作用,具有作用强、用量小、毒性低等特点[1]。但AEP为水溶性大分子蛋白多肽类药物,很难透过血脑屏障入脑,因此,改变AEP在体内分布,增加其在病灶药物浓度是关键。
聚乙二醇-聚乳酸-聚乙醇酸嵌段共聚物[Polyethyleneglycol-modified poly(d,l-lactide-co-glycolide),PEG-PLGA]是一种新型的两亲性嵌段共聚物,既可有效延缓药物释放,又可显著改善药物在体内的分布,是具有较强靶向作用的载体。PLGA是一种生物相容性好、可生物降解的高分子材料,在体内代谢为H2O和CO2,被FDA批准用于临床[2-3]。但PLGA纳米粒因其疏水性迅速被网状内皮系统清除,而采用PEG 修饰PLGA,使PEG-PLGA成为两亲性嵌段共聚物,可延长所载药物在体循环中的滞留时间,且制备过程中不使用添加剂,避免了由此产生的毒性[4-5]。本实验以PEG-PLGA为载体,采用复乳-溶剂挥发法制备AEP纳米粒。
1 材料
1.1 药品与试剂 PEG-PLGA(Mw=2000-35000,山东济南岱罡生物科技有限公司,批号:12132016);异硫氰酸荧光素标记的抗癫疒间肽(Fluorescein isothiocyanate-Anti-epilepsy Peptide,FITC-AEP,杭州中泰生物技术有限公司标记,批号:CH-1200612),泊洛沙姆188(Poloxamer 188,德国BASF公司,批号:WPAF538B),其他试剂均为分析纯。
1.2 仪器 HJ-6B多头磁力加热搅拌机(金坛市金伟实验仪器厂);Optima超速低温离心机(美国Beckman公司);Marvern measurement粒度测定仪(英国马尔文仪器有限公司);JEM-1200EX透射电子显微镜(日本Jeol公司);Labconco冷冻干燥机(英国LABCONCO公司);荧光检测器(日本Shimadzu公司)。
2 方法与结果
2.1 FITC-AEP-PEG-PLGA-NPs制备 精密称取10 mg FITC-AEP溶于10 mL蒸馏水作为水相,100 mg PEG-PLGA溶于2 mL丙酮-乙醇(丙酮-乙醇体积比为3∶1)作为油相,把水相缓慢加入油相中,冰浴条件下超声60 s(功率500 W,工作1.5 s,间歇2 s),形成W1/O,为初乳。将初乳加入到泊洛沙姆188水相溶液中,冰浴条件下超声形成W1/O/W2的复乳。室温磁力搅拌复乳挥去有机溶剂,即得FITC-AEP-PEG-PLGA-NPs溶液。40 000 r/min低温超速离心60 min(4 ℃),沉淀物用蒸馏水洗涤3次,冻干即得FITC-AEP-PEG-PLGA-NPs。
2.2 FITC-AEP-PEG-PLGA-NPs含量的测定
2.2.1 荧光测定条件 采用荧光分光光度法测定FITC-AEP-PEG-PLGA-NPs含量:激发波长:λex=494 nrn;发射波长:λem=518 nm。
2.2.2 线性关系 精密称取FITC-AEP溶于蒸馏水,置10 mL容量瓶中,用蒸馏水溶解,定容,摇匀,并分别稀释成浓度为0.05、0.25、0.5、1、2、5 μg/mL,按“2.2.1”荧光测定条件测定荧光强度。以药物浓度X为横坐标、荧光强度Y为纵坐标,进行线性回归。得回归方程为Y=101.58 X-0.341,r=0.999 8(n=6)。结果表明,FITC-AEP在0.05~5 μg/mL范围内与荧光强度呈良好线性关系。
2.3 FITC-AEP-PEG-PLGA-NPs包封率及载药量测定 称取一定量FITC-AEP-PEG-PLGA-NPs冻干粉,记Xt;离心前测定荧光值,记Y1,根据回归方程,换算成AEP含量;低温超速离心(3 ℃,35 000 r/min,40 min)后,测定上清液测定荧光值,记Y2,根据回归方程,换算成AEP含量,记X2。按式1、2计算包封率与载药量。
包封率%=(X1-X2)/X1×100%……式1
载药量%=(X1-X2)/Xt×100%……式2
X1:NPs中AEP量;X2:NPs中的游离AEP量;Xt:冻干粉量。
2.4 FITC-AEP-PEG-PLGA-NPs制备工艺优化 在单因素试验的基础上,选择FITC-AEP用量(A)、PEG-PLGA浓度(B)、丙酮-乙醇比例(C)、复乳超声时间(D)为试验因素,各因素选取3个水平,按正交设计表L9(34)安排试验,正交设计因素水平见表1。
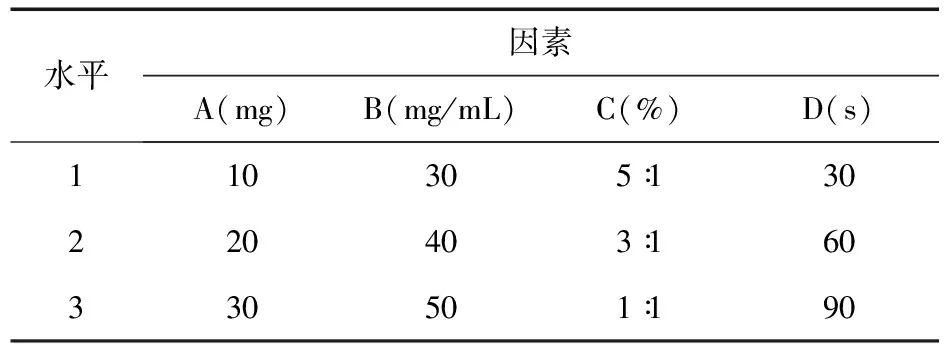
表1 正交试验因素水平表
以粒径、包封率与载药量为考察指标,应用综合加权评分法对正交试验结果进行综合分析,粒径(y1)、包封率(y2)和载药量(y3)分别按30%、35%和35%的系数积分,综合评分(y)=35×(1-y1/168.2)+30×y2/83.5+35×y3/6.87,通过直观分析及方差分析,优选最佳的工艺,结果见表2、表3。
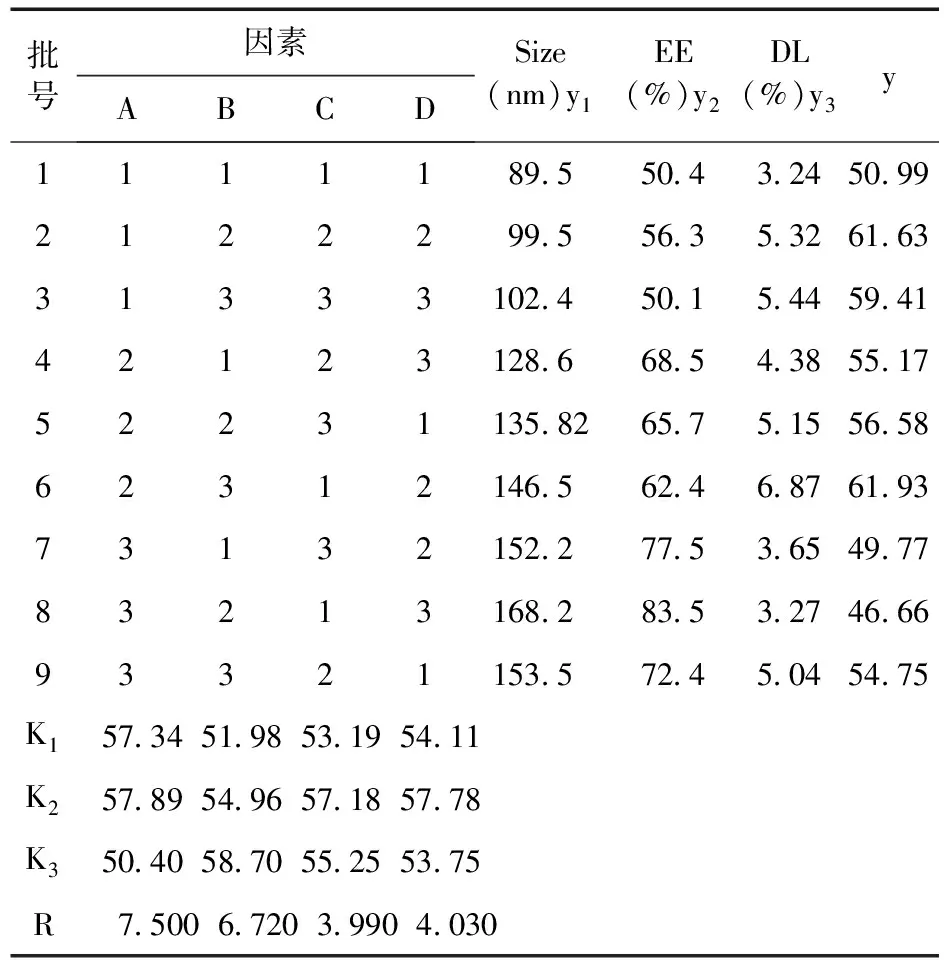
表2 正交试验方案和结果

表3 方差分析表
由表3方差可知,FITC-AEP用量(A)、PEG-PLGA浓度(B)、复乳超声时间(D)对FITC-AEP-PEG-PLGA-NPs的制备工艺有显著性影响。综合各因素K值,确定最佳制备工艺为 A2B3C2D2,即FITC-AEP用量20 mg、PEG-PLGA浓度50 mg/mL、丙酮-乙醇比例3∶1、复乳超声时间60 s。
2.5 FITC-AEP-PEG-PLGA-NPs制备工艺验证 按正交试验优化的工艺制备3批FITC-AEP-PEG-PLGA-NPs,考察工艺稳定性,结果见表4。

表4 制备工艺验证
2.6 FITC-AEP-PEG-PLGA-NPs形态 FITC-AEP-PEG-PLGA-NPs冻干粉加蒸馏水溶解,溶液滴于铜网上,静置15 min后用滤纸吸干,以3.0%磷钨酸溶液于铜网上负染10 min后,透射电子显微镜形态,见图1。由图1可见,FITC-AEP-PEG-PLGA-NPs呈圆形或类圆形,表面光滑圆整。
2.7 FITC-AEP-PEG-PLGA-NPs体外释放 采用动态透析袋法研究FITC-AEP-PEG-PLGA-NPs体外释药特性。精密量取FITC-AEP-PEG-PLGA-NPs冻干粉适量(含AEP 1 mg)溶解于pH 7.4 PBS溶液,置于已处理过的透析袋内,扎紧袋口,将含药透析袋置于250 mL释放介质中,37 ℃恒温水浴振荡(75 r/min),于0.1、0.25、0.5、0.75、1、1.5、2、3、4、6、8、10、12、18、24、48 h取样0.2 mL,立即补加等量同温释放介质。按“2.2.1”荧光测定条件测定,并计算累积释放曲线,见图2。
由图2可知,FITC-AEP-PEG-PLGA-NPs 在pH 7.4 PBS缓冲液中的释药行为呈现突释和缓释两个阶段,前3 h属于突释阶段,药物释放39.7%左右。随后释放趋向平缓,48 h时药物释放85.3%。分别用零级动力学方程、一级动力学方程、Higuchi方程和Weibull方程对其体外释药进行拟合,结果体外释放符合Weibull释放模型,Weibull方程为lnln(1/1-Q)=0.675 4lnt-1.279 3(r=0.991 8)。
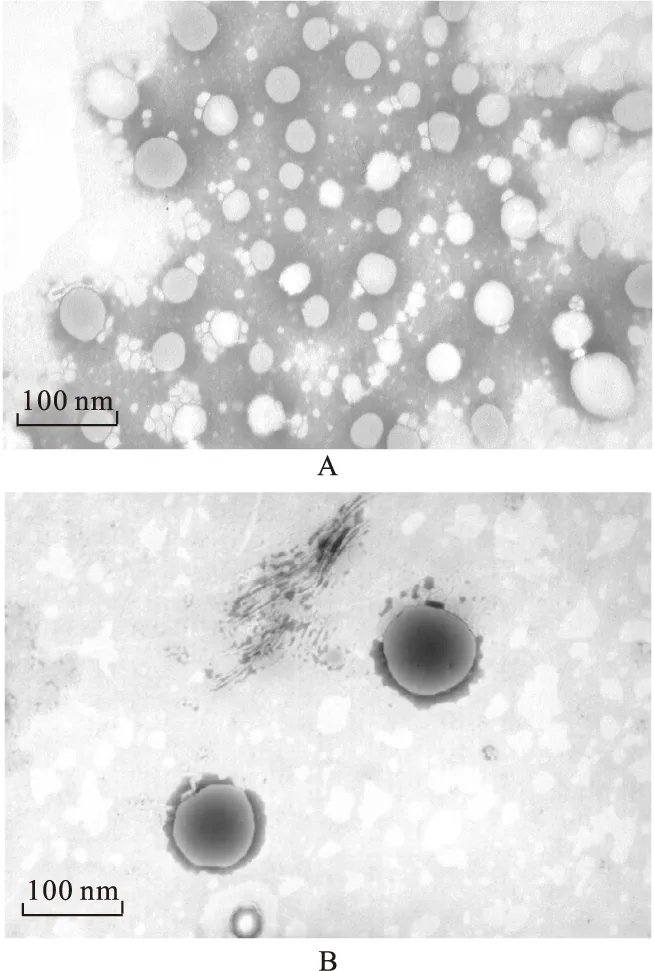
图1 FITC-AEP-PEG-PLGA-NPs透射电镜照片
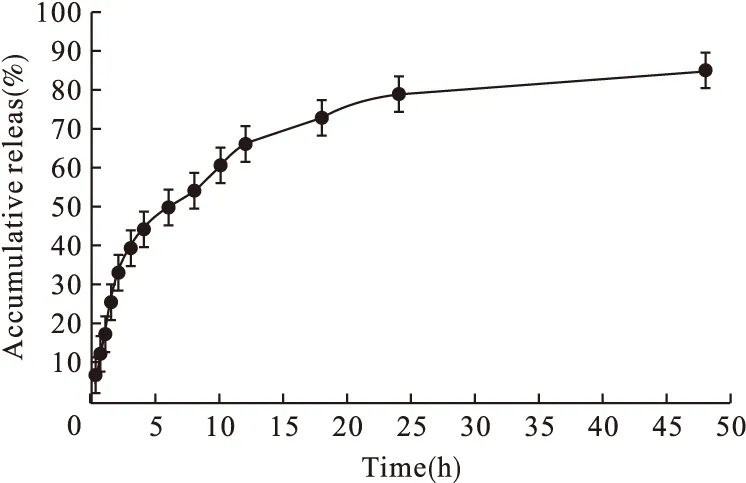
图2 FITC-AEP-PEG-PLGA-NPs体外释药曲线
3 讨论
3.1 癫疒间是一组因大脑病灶神经元过度放电所致的中枢神经系统功能短暂失调的脑部疾病,具有慢性、反复发作的特点,是神经系统的常见病、难治病。AEP从蝎毒粗毒中分离、纯化出来,由61个氨基酸残基组成,药理研究表明其是一种具有抗癫疒间活性的多肽,对各型癫疒间均具有较强的治疗作用,且其与传统抗癫疒间药如苯妥英钠、卡马西平等相比,具有毒性小、作用强的优点,是一种理想的抗癫疒间药[6-7]。但AEP为水溶性大分子多肽,不易透过BBB到达神经中枢发挥抗癫疒间作用。新型的纳米药物载体用于抗癫疒间药物的输送,既可提高抗癫疒间药的效能,还能降低抗癫疒间药的毒副作用。
3.2 嵌段共聚物是单一线性共聚物分子中存在两种或两种以上结构不同的链段单元按照一定序列组成的聚合物。两亲性嵌段共聚物是一种新型的纳米药物载体,具有很高的内核载药容量和独特的体内分布特征,在结构上可以划分出亲水部分和疏水部分。由于这种独特的化学结构,在水溶液中能形成具有球形内核-外壳结构的共聚物胶束。内核可以作为储存药物的容器,降低毒副作用,外壳可对药物起保护作用,提高药物的稳定性,并且达到缓释作用[5-8]。
3.3 本研究在预试验的基础上,结合抗癫疒间肽的水溶性性质,最终确定W1/O/W2复乳-溶剂挥发法。本研究所述复乳法具体为将载体材料PEG-PLGA溶解在有机溶剂中,将药物水溶液分散在其中,形成W1/O型初乳,再在搅拌条件下将初乳分散到含有表面活性剂的水溶液中,形成W1/O/W2型乳液。该法制备的纳米粒包封率为64.46%,粒径为100.2 nm,PDI为0.111。分析其原因,可能是因为:①采用本法制备的纳米粒由于内水相与外水相被油相隔开,可以避免药物向外水相扩散从而包封率提高;②在外水相中加入的poloxamer188有空间位阻作用,可以阻止纳米粒的聚集,增加稳定性。
3.4 由体外释药曲线可知,FITC-AEP-PEG-PLGA-NPs在pH 7.4 PBS缓冲液中的释药行为呈突释和缓释两个阶段:第一阶段3 h时药物释放39.7%,存在一定突释现象,可能由于AEP吸附在纳米粒表面,或者只是以较弱的键连接在纳米粒表面,使得药物从透析袋中释放比较快;第二阶段曲线趋向平缓,48 h时药物释放85.3%,可能由于大部分AEP进入纳米粒内核,随着载体材料逐渐降解,外液逐步扩散到纳米粒内部并携带药物向介质扩散,释放AEP。考虑到PLGA降解速度较慢,同时在释放过程中外液渗入导致内部结构变密,外液渗入受阻,导致AEP释放速度缓慢,呈现缓释现象。
参考文献:
[1] 王宗仁,邵中军,李晶华,等.抗癫疒间肽重组腺伴病毒载体的构建及鉴定[J].中草药,2005,36(12)1844-1846.
[2] Yu L,Ci T,Zhou S,et al.The thermogelling PLGA-PEG-PLGA block copolymer as a sustained release matrix of doxorubicin[J].Biomater Sci,2013,4(10):411-420.
[3] Lü JM,Wang X,Marin-Muller C,et al.Current advances in research and clinical applications of PLGA-based nanotechnology[J].Expert Rev Mol Diagn,2009,9(4):325-341.
[4] Li M,Panagi Z,Avgoustakis K,et al.Physiologically based pharmacokinetic modeling of PLGA nanoparticles with varied mPEG content[J].Int J Nanomedicine,2012,(7):1345-1356.
[5] Betancourt T,Byrne JD,Sunaryo N,et al.PEGylation strategies for active targeting of PLA/PLGA nanoparticles[J].J Biomed Mater Res,2009,91(1):263-276.
[6] Joseph B,George J.Scorpion toxins and its applications[J].Int J Toxi Pharm Res,2012,4(3):57-61.
[7] Wang Z,Wang W,Shao Z,et al.Eukaryotic expression and purification of anti-epilepsy peptide of Buthus martensii Karsch and its protein interactions[J].Mol Cell Biochem,2009,330(1-2):97-104.
[8] Wen JG,Guo TT,Zhu HY,et al.Preparation and optimization of PEG-PLGA loaded with vincristine sulfate and itsinvitrrelease[J].J Bioequiv Availab,2011,3(9):211-214.
