止汗外用凝胶中姜黄素的定性与定量研究
2014-08-14赵庆年刘汉清
刘 嘉,赵庆年,刘汉清
0 引言
止汗外用凝胶是由郁金、石菖蒲、麻黄根等中药组方而成的治疗自汗、盗汗的外用制剂,临床疗效明确。然而,与多数外用中药制剂一样,止汗外用凝胶制备工艺传统,未对主要有效成分建立精确的含量测定方法,因此,其质量控制尚不完善。姜黄素(curcumin)为止汗外用凝胶剂中的主要成分,具有破血行气,通经止痛之功效。药理学研究证实,姜黄素具有抗炎、抗氧化、抗肿瘤等诸多药理作用[1]。而近年来,姜黄素更是被认为在治疗涉及炎症反应的各种创伤性疾病中有广阔的应用前景[2]。本研究应用TLC法定性鉴别止汗外用凝胶中的姜黄素,并采用HPLC法测定制剂中姜黄素的含量,以期为止汗外用凝胶质量标准的完善提供实验依据。
1 仪器与试药
Agilent1100高效液相色谱仪,DAD紫外检测器(美国安捷伦公司);KQ-250B型超声波振荡器(昆山市超声仪器有限公司);HH-S型水浴锅(巩义市英峪予华仪器厂);WD-9403B型紫外仪(北京六一仪器厂);薄层硅胶G板(青岛海洋化工厂)。姜黄素对照品(批号:1215-9708,供含量测定用,中国药品生物制品检定所);郁金对照药材(购自江苏省药材公司,经江苏建康职业学院赵庆年副教授鉴定);止汗外用凝胶(自制,规格:10 g/支,批号:121113、121127、121217)。乙腈、甲醇为色谱纯,水为重蒸水,其余试剂均为分析纯。
2 方法与结果
2.1 姜黄素的TLC鉴别[3]①对照品溶液的配制:取姜黄素对照品0.2 mg,加入甲醇2 mL,溶解即得。②供试液、阴性制剂对照液及阳性药材对照液的配制:取止汗外用凝胶供试品、不含郁金的按制剂制备工艺制备成的阴性制剂供试品各10 g,郁金对照药材1 g,分别加入无水乙醇60 mL,水浴回流至提取液无色时,滤过,滤液分别浓缩至40 mL,滤过,分别制得。③点样、展开:取薄层硅胶G板先以10%的甲酰胺-丙酮溶液展开1次,取出,晾干备用。取上述阴性制剂对照液、供试液、阳性药材对照液及对照品溶液及各10 μL,分别点样于上述处理过的硅胶G板上,以氯仿∶甲醇∶甲酸(96∶4∶0.6)为展开剂,展开,取出,晾干。④结果:在365 nm紫外灯下检视,供试品薄层色谱与姜黄素对照品及阳性药材对照品薄层色谱在相同位置显亮黄色斑点(见图1)。
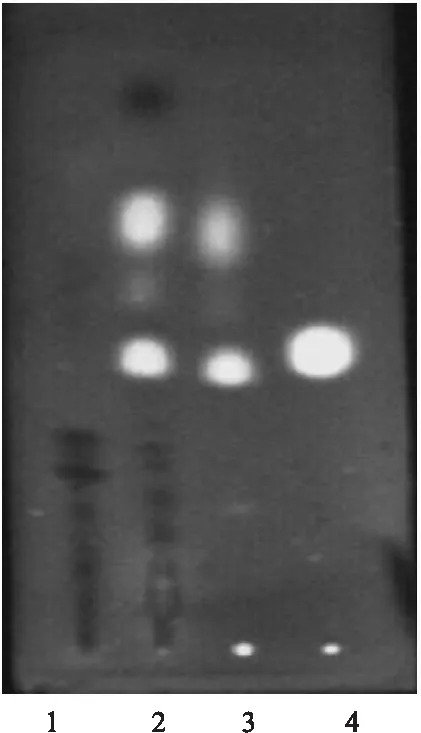
图1 姜黄素的TLC鉴别图谱
2.2 姜黄素的含量测定
2.2.1 色谱条件 Ecosil ODS C18色谱柱(4.6 mm×250 mm,5 μm);流动相:乙腈∶水∶冰醋酸(45∶55∶6);流速:1.0 mL/min;检测波长:254 nm;柱温:室温;进样量:20 μL。
2.2.2 溶液配制 ①对照品溶液:精密称取姜黄素对照品适量,加甲醇配成0.2 mg/min的对照品溶液。②供试液:精密称取样品10 g,用10倍量甲醇浸泡2 h后,超声提取3 h,离心,取出上清液。药渣同前处理2次。合并3次提取液,适当浓缩,以甲醇定容至10 mL,0.45 μm滤膜滤过,即得。③阴性对照液:根据处方及相应工艺制备缺郁金的阴性制剂样品,按供试液的配制方法配制即得。
2.2.3 检测波长选择 取姜黄素对照液以适量的流动相稀释后,在200~400 nm波长范围内扫描,结果其在254 nm处有最大吸收,故确定254 nm为检测波长。
2.2.4 专属性试验 取上述对照品溶液、供试品溶液、阴性对照液各20 μL,按“2.2.1”项下的色谱条件进样、测定。结果显示,姜黄素的色谱峰峰型良好,保留时间约8 min,与其他色谱峰分离良好。在阴性对照液的色谱图中,姜黄素相应的保留时间处无色谱峰,说明阴性供试液无干扰,见图2。
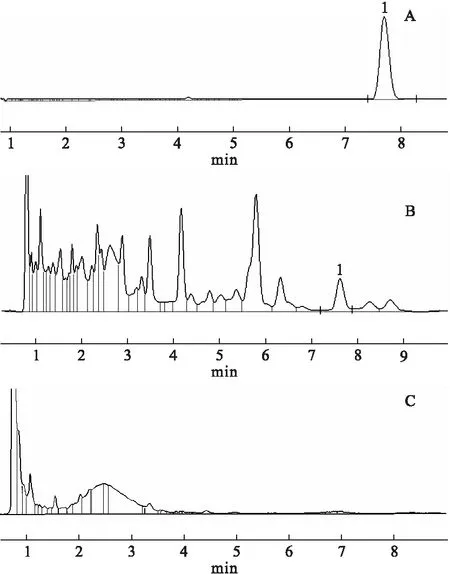
图2 姜黄素的含量测定色谱图
2.2.5 标准曲线 精密称取姜黄素对照品适量,加甲醇配成0.1、0.2、0.5、0.6、0.7、0.8 mg/min的对照品溶液,分别进样20 μL,按“2.2.1”项下的色谱条件测定,以姜黄素的浓度(X)为横坐标,以峰面积(Y)为纵坐标,计算得到线性回归方程:Y=329 786X-106 402,r=0.999 4。结果表明,姜黄素在0.1~0.8 mg/min的浓度范围内与峰面积线性关系良好。
2.2.6 精密度、重复性及稳定性试验 精密吸取浓度为0.2 mg/min的对照品溶液,按“2.2.1”项下的色谱条件,重复进样5次,RSD为0.75%(n=5),表明仪器精密度良好。精密吸取浓度为0.2 mg/min的对照品溶液5份,按“2.2.1”项下色谱条件分别进样测定,RSD为1.42%(n=5),表明方法重复性良好。取同一供试液(批号:121113),按“2.2.1”项下的色谱条件,于1、2、3、4、5 h分别进样测定,结果RSD为1.54%(n=5)。表明5 h内供试液稳定性良好。
2.2.7 加样回收试验 精密称取已知含量的姜黄素样品适量,分别精密加入0.2 mg姜黄素对照品,按上述的方法处理并测定。姜黄素加样回收率=(测得量-原样品含量)/加入量。结果见表1。
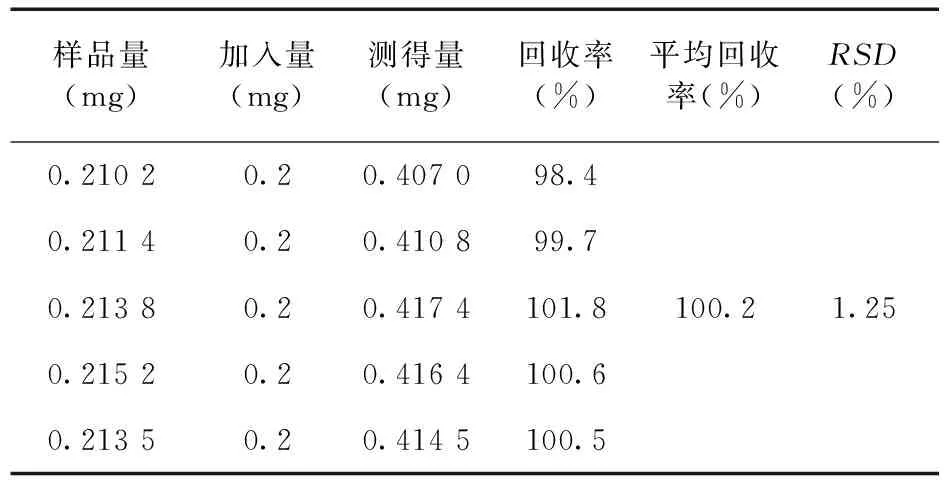
表1 加样回收率试验结果(n=5)
2.2.8 样品测定 取本组3个批号的样品,按“2.2.2”项下方法制备供试液,按“2.2.1”项下色谱条件测定姜黄素的含量,结果见表2。
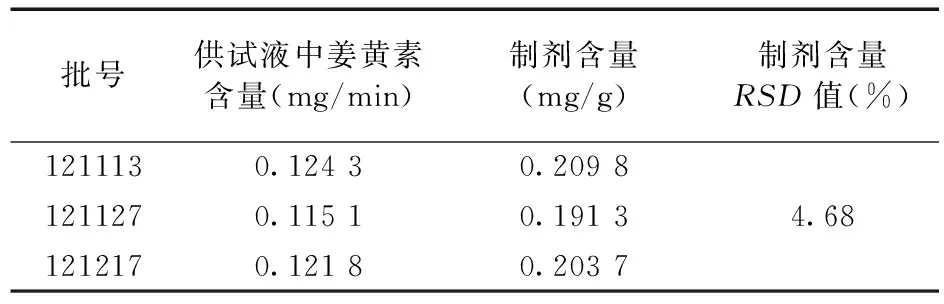
表2 止汗外用凝胶样品中姜黄素的含量测定结果
3 讨论
在TLC定性鉴别中,我们以无水乙醇为提取溶剂,水浴回流法提取止汗外用凝胶供试品中的姜黄素;而在HPLC含量测定时,我们则以甲醇为溶剂,采用超声法提取制剂中的姜黄素。提取溶剂选择不同的原因为:在薄层鉴别中,采用溶解范围更广的无水乙醇能提取出制剂样品中更多的相关成分,使得薄层色谱更易对比识别。而在HPLC测定时,如使用无水乙醇为提取溶剂,则会导致提取的成分过多而干扰姜黄素的测定,故选择甲醇为提取溶剂。另外,根据周燕霞等[4]对郁金中姜黄素的提取方法选择的报道及预实验的结果,我们选择了以10倍量甲醇浸泡2 h,超声3 h共提取3次的操作。该法姜黄素得率较普通回流法高,且时间较短、简单易行,值得借鉴。
本研究的液相条件是在2010版药典的基础上,结合预实验结果摸索而出。在先期选择HPLC的流动相时,分别考察了甲醇-水及乙腈-水系统,结果显示,以甲醇-水为流动相可使样品中姜黄素的色谱峰不能与相邻杂质峰较好分离;而乙腈-水系统则存在一定的拖尾现象,在加入扫尾剂冰醋酸后,样品中的姜黄素峰型良好,并能与杂质峰较好地分离。另外,相关文献报道,姜黄素在中性条件下的稳定性较差[5],而在进行HPLC的稳定性研究时,我们亦发现,在5 h内供试液稳定性良好,而在10 h供试液中姜黄素浓度下降10%左右,这提示在进行姜黄素的定性鉴别及含量测定时,应及时进样、现配现用,以免因稳定性下降而导致的测量结果不准确。
综上所述,TLC法定性鉴别和HPLC法定量测定止汗外用凝胶中姜黄素,方法可行,重现性好,为止汗外用凝胶的质量控制提供了可靠依据。
参考文献:
[1] 李琦,金剑,许颖.姜黄素的药理作用及其临床应用进展[J].现代中西医结合杂志,2012,21(12):1366-1368.
[2] 涂燕华,孙连娜.姜黄素与类风湿性关节炎的相关实验研究进展[J].中国实验方剂学杂志,2012,18(19):310-314.
[3] 国家药典委员会.中华人民共和国药典[M].北京:中国医药科技出版社,2010:247.
[4] 周燕霞,唐明林,李元波,等.郁金中姜黄素提取工艺研究[J].广州化学,2006,31(2):34-38.
[5] 韩刚,崔静静,毕瑞,等.姜黄素、去甲氧基姜黄素和双去甲氧基姜黄素稳定性研究[J].中国中药杂志,2008,33(22):2611-2614.
