茵陈汤加减治疗妊娠期肝内胆汁瘀积症meta分析
2014-08-09洪培伟范雪梅
刘 瑶,洪培伟,范雪梅
(1.成都市新都区中医医院,成都 610500;2.四川大学华西第二医院发育与干细胞研究所,成都 610041;3.成都中医药大学第二附属医院,成都 610041)
妊娠期肝内胆汁瘀积症(Intrahepatic cholestasis of pregnancy,ICP)是一种在妊娠期特有的疾病,多发生于妊娠晚期,以瘙痒、黄疸为其临床主要特征,随妊娠终止而迅速恢复,再次妊娠可复发。本病发病机制尚不明确,发病原因与雌激素急剧增加、遗传因素、环境因素等有关。妊娠期肝内胆汁瘀积症的患病率随国家和种族而不同。妊娠期肝内胆汁瘀积症主要危害胎儿,发生围生期不良结局,如早产、胎儿宫内窘迫、胎死宫内等[1]。目前治疗以缓解瘙痒症状,恢复肝功能,降低血胆汁酸水平,监测胎儿宫内状况,改善妊娠结局为目的。中医学认为,妊娠期肝内胆汁瘀积症属“妊娠瘙痒”“妊娠黄疸”范畴。妊娠后,阴血下注胞宫以养胎,肝血易虚,肝气易郁,易感受湿热之邪。湿热蕴积肝胆,肝失疏泄,胆汁外溢,侵淫肌肤,发为本病,治疗以清热利湿退黄为原则。茵陈汤以茵陈、大黄、栀子组成,组成简单,适宜本病。本研究对茵陈汤加减治疗ICP的临床随机对照试验进行分析评价,了解茵陈汤加减治疗ICP的有效性及安全性,以期为临床决策提供循证依据。
1 资料与方法
1.1 文献纳入标准 实验类型:随机对照实验(RCT)。实验对象:诊断为妊娠期肝内胆汁瘀积的患者。诊断标准:参照《中华妇产科学》诊断标准[2]。干预措施:实验组采用茵陈汤为主方的中草药制剂(制剂型不限),添加或未添加其他干预措施;对照组采用西药治疗。
1.2 文献排除标准 重复报道;疗效指标不可用;动物实验。
1.3 疗效判定指标 1)总有效率、瘙痒、黄疸症状改善情况;2)生化指标:谷丙转氨酶(ALT)、谷草转氨酶(AST)、血清总胆汁酸(TBA)、直接胆红素(DBIL)、总胆红素(TBIL)的变化情况;3)妊娠结局:胎儿窘迫、羊水污染、早产率、新生儿体重、产后出血、剖宫产情况。4)不良反应。
1.4 资料检索 中文检索词:妊娠期肝内胆汁瘀积症、妊娠黄疸、妊娠瘙痒、中医、中西医、中药、中草药、汤药;英文检索词:Intrahepatic cholestasis of pregnancy,cholestasis,intrahepatic,Cholestasis of pregnancy,regnant jaundice,pruritus gravidarum,drugs,Chinese herbal,medicine,Chinese tradition,Chinese traditional medicine,herb medice,phytotherapy。计算机检索Cochrane,荷兰医学文摘数据库(EMBASE)(1984~),(美)联机医学文献分析和检索系统 (MEDLINE)(1950~),PubMed(1966~),中国知网(CNKI)(1979),中国生物医学文献数据库(CBM)(1978),维普网(VIP)(1989~),万方学位论文数据库(1978)。中国ChiCTR,澳大利亚ANZCTR,英国ISRCTN,国际临床试验注册协作网ICTRP,美国ClinicalTrials.gov。最后检索日期:2013年7月。
1.5 文献纳入 阅读所有检索文献的摘要及关键词,对可能符合纳入标准的研究做进一步的全文评价。
1.6 文献方法学质量评价 2名研究者根据Cochrane Handbook指南独立提取文献信息,对试验进行质量评估,如有争议,则与第三位研究者讨论解决(纳入试验具体信息未列出,可联系作者获取)。
1.7 统计分析 采用Cochrane协作网提供的RevMan5.1版本进行数据分析。计数资料(如二分类变量)采用危险比率(OR),计量资料采用加权均数差(WMD)为合并统计量。连续变量的变化以差值的均数和标准差来衡量。对于计算多个研究结果采用异质性检验。如存在异质性,则通过进行亚组分析或随机效应模型进行矫正。
2 结果
2.1 纳入文献情况 研究共发现54篇文献符合纳入标准,所收集文献研究均在国内实施。
2.2 茵陈汤加减疗效的统计分析结果
2.2.1 总有效率
2.2.1.1 茵陈汤加减方VS单纯西药组 有4个试验[3-6]进行了茵陈汤加减方与单纯西药组总有效率的比较。异质性检验显示,组间差异无统计学意义(P=0.87,I2=0%)。分析结果显示,试验组的总有效率显著高于对照组(0R=4.98,95%CI[2.76,9.00],P<0.00 001)。
2.2.1.2 茵陈汤加减方结合西药组VS单纯西药组 有15个试验[7-21]进行了茵陈汤加减方与单纯西药组总有效率的比较。异质性检验显示,组间差异无统计学意义(P=0.82,I2=0%)。分析结果显示,试验组的总有效率显著高于对照组(OR=4.86,95%CI[3.32,7.10],P<0.00 001)。
2.2.2 皮肤瘙痒情况
2.2.2.1 茵陈汤加减方VS单纯西药组 有2个试验[22-23]进行了茵陈汤加减方与单纯西药组皮肤瘙痒好转的比较。异质性检验显示,组间差异无统计学意义(P=0.27,I2=16%)。分析结果显示,试验组的皮肤瘙痒好转率显著高于对照组(0R=3.29,95%CI[1.62,6.71],P=0.001)。
2.2.2.2 茵陈汤加减方结合西药组VS单纯西药组 有14个试验[24-37]进行了茵陈汤加减方与单纯西药组皮肤瘙痒好转的比较。异质性检验显示,组间比较有统计学意义(P<0.0 001,I2=70%)。分析结果显示,试验组的皮肤瘙痒好转率显著高于对照组(0R=7.95,95%CI[3.70,17.09],P<0.00 001)。
2.2.3 黄疸情况
2.2.3.1 茵陈汤加减方VS单纯西药组 陈怡[22]研究结果显示,茵陈汤加减方黄疸消退率高于单纯西药组,两者比较,差异无统计学意义(OR=0.88,95%CI[0.27,2.83],P>0.05)。
2.2.3.2 茵陈汤加减方结合西药组VS单纯西药组 有2个试验[25-36]进行了茵陈汤加减方与单纯西药组黄疸消退率比较。异质性检验显示,组间差异无统计学意义(P=0.24,I2=28%)。分析结果显示,试验组的黄疸消退率显著高于对照组(0R=17.97,95%CI[3.36,96.17],P=0.0 007)。
2.2.4 治疗前后生化指标改善情况 见表1。
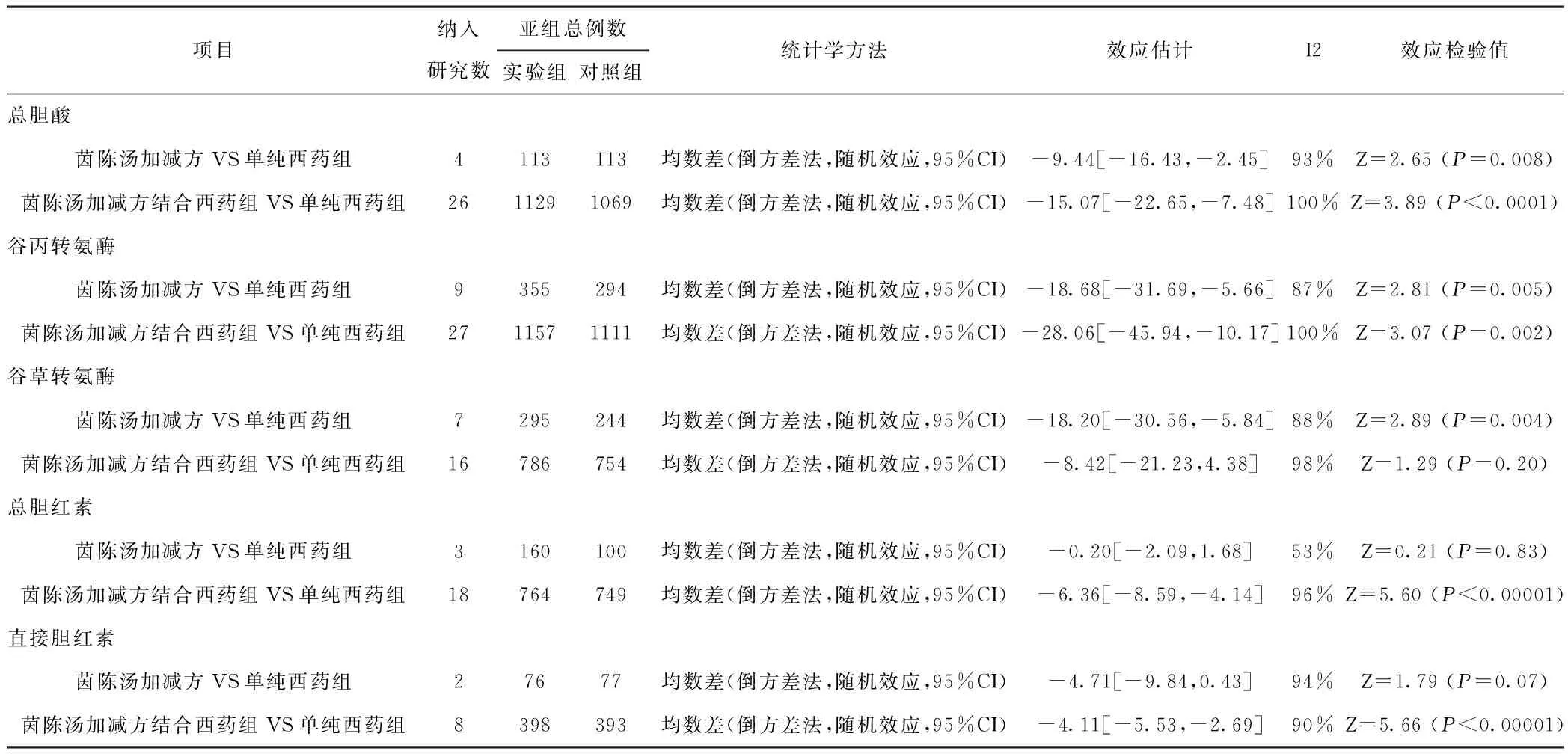
表1 生化指标分析 例
2.2.4.1 总胆汁酸(TBA)水平
2.2.4.1.1 茵陈汤加减方VS单纯西药组 有4个试验[22,38,3,4]进行了茵陈汤加减方与单纯西药组TBA水平的比较。异质性检验显示,组间有统计学意义(P<0.00 001,I2=93%)。分析结果显示,试验组的TBA水平改善显著高于对照组(0R=-9.44,95%CI[-16.43,-2.45],P=0.008)。
2.2.4.1.2 茵陈汤加减方结合西药组VS单纯西药组 有26个试验[7,9,13,14,16,19-21,25,27-29,31-35,39-47]进行了茵陈汤加减方与单纯西药组TBA水平的比较。异质性检验显示,组间有统计学意义(P<0.00 001,I2=100%)。分析结果显示,试验组的TBA水平改善显著高于对照组(0R=-15.07,95%CI[-22.65,-7.48],P<0.0 001)。
2.2.4.2 谷丙转氨酶(ALT)水平
2.2.4.2.1 茵陈汤加减方VS单纯西药组 9个试验[3-6,22,23,38,48,49]进行了茵陈汤加减方与单纯西药组ALT水平的比较。异质性检验显示,组间有统计学意义(P<0.00 001,I2=87%)。分析结果显示,试验组的ALT水平改善显著高于对照组(0R=-18.68,95%CI[-31.69,-5.66],P=0.005)。
2.2.4.2.2 茵陈汤加减方结合西药组VS单纯西药组 有27个试验[7,9,13-16,19-21,25,27-29,31,34,37,39-44,46,47,52,55]进行了茵陈汤加减方与单纯西药组ALT水平的比较。异质性检验显示,组间有统计学意义(P<0.00 001,I2=100%)。分析结果显示,试验组的ALT水平改善显著高于对照组(0R=-28.06,95%CI[-45.94,-10.17],P=0.002)。
2.2.4.3 谷草转氨酶(AST)水平
2.2.4.3.1 茵陈汤加减方VS单纯西药组 7个试验[3-6,22,23,38]进行了茵陈汤加减方与单纯西药组AST水平的比较。异质性检验显示,组间有统计学意义(P<0.00 001,I2=88%)。分析结果显示,试验组的ASL水平改善显著高于对照组(0R=-18.20,95%CI[-30.56,-5.84],P=0.004)。
2.2.4.3.2 茵陈汤加减方结合西药组VS单纯西药组 Meta分析结果显示,2组差异均无统计学意义。
2.2.4.4 总胆红素(TBIL)水平
2.2.4.4.1 茵陈汤加减方VS单纯西药组 Meta分析结果显示,2组差异均无统计学意义。
2.2.4.4.2 茵陈汤加减方结合西药组VS单纯西药组 有18个试验[14,16,19,21,25,28,31,32,37,39-41,45-47,50,52,55]进行了茵陈汤加减方与单纯西药组TBIL水平的比较。异质性检验显示,组间有统计学意义(P<0.00 001,I2=96%)。分析结果显示,试验组的TBIL水平改善显著高于对照组(0R=-6.36,95%CI[-8.59,-4.14],P<0.00 001)。
2.2.4.5 DBIL水平
2.2.4.5.1 茵陈汤加减方VS单纯西药组 Meta分析结果显示,2组差异均无统计学意义。
2.2.4.5.2 茵陈汤加减方结合西药组VS单纯西药组 有8个试验[14,16,21,31,39,40,45,55]进行了茵陈汤加减方与单纯西药组DBIL水平的比较。异质性检验显示,组间有统计学意义(P<0.00 001,I2=90%)。分析结果显示,试验组的DBIL水平改善显著高于对照组(0R=-4.11,95%CI[-5.53,-2.69],P<0.00 001)。
2.2.5 妊娠结局
2.2.5.1 茵陈汤加减方VS单纯西药组 见表2。
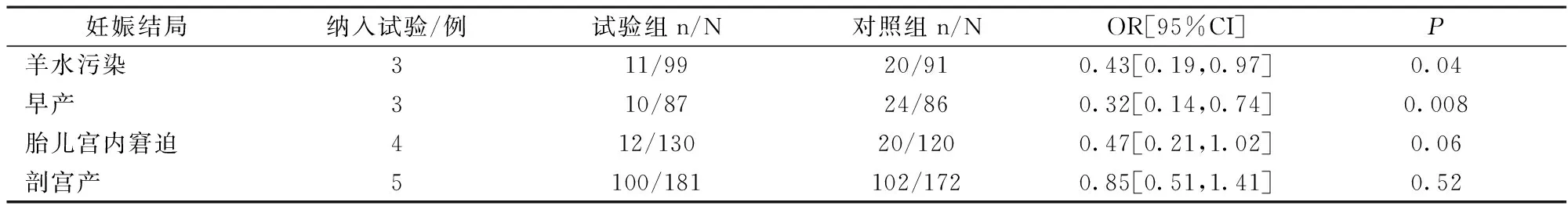
表2 茵陈汤加减方VS单纯西药组妊娠结局
张新[5]研究结果显示,茵陈汤加减方产后出血率低于单纯西药组,两者比较,差异无统计学意义(P>0.05)。有2个[5,48]试验进行了茵陈汤加减方VS单纯西药组的新生儿体质量Meta分析。结果显示,2组差异无统计学意义(OR=39.79,95%CI[-39.36,118.94],P=0.32)。
2.2.5.2 茵陈汤加减方结合西药组VS单纯西药组 见表3。
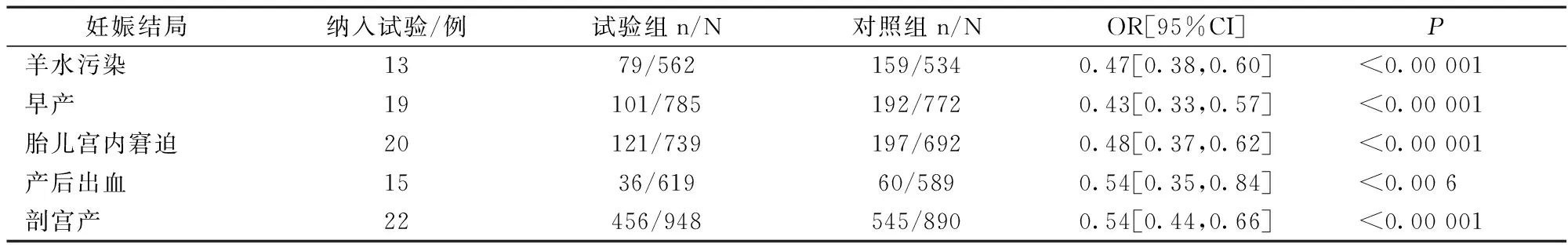
表3 茵陈汤加减方结合西药组VS单纯西药组妊娠结局
有8个[7,16,19,29,32,37,44,55]试验进行了茵陈汤加减方结合西药组VS单纯西药组的新生儿体质量Meta分析。结果显示,异质性检验显示,组间差异无统计学意义(P<0.0 001,I2=43%)。分析结果显示,试验组的新生儿体质量显著高于对照组(0R=271.04,95%CI[233.83,308.24],P<0.00 001)。
2.2.6 不良反应 茵陈汤加减结合西药组VS单纯西药组 有2个试验[25,40]对不良反应进行了观察,1个试验[40]报道了部分不良反应。丁少娜[40]研究报道治疗组出现的主要不良反应为恶心、头痛、面色潮红等,占6.4%(6/94)。茵陈汤加减方VS单纯西药组尚无文献对不良反应进行观察。
3 讨论
3.1 纳入试验的方法学质量讨论 本系统评价所纳入的研究同时存在方法学质量、试验设计问题。本研究仅有7个试验[6,16,22,37,48,49,55]为随机对照试验,其余试验仅提及“随机”,没有详细描述随机方法,同时纳入研究皆无提及分配隐藏。本研究54篇文献中提及盲法的文献仅1篇,且为单盲,其余皆无详细的盲法描述,可能导致实施偏倚和测量偏倚的产生。因临床试验观察及随访时间长,观察对象可能因各种原因中断随访或退出试验。纳入研究中有1篇报告退出、失访的情况,其余均未提及,产生的偏倚可能性较大,影响研究真实性。所纳入试验中有2个试验[25,40]对不良反应进行了观察,1个试验[40]报道了部分不良反应。本研究纳入试验发表年份均在1999~2012年,但纳入研究均系客观的质量评价后获得的,由此产生的选择性偏倚较小。本研究所纳入的研究均方法学质量低下,目前仍缺乏茵陈汤加减方治疗ICP的高质量研究报道,同时存在各试验对照组西药使用的药物、方法、剂量、治疗时间的差异,人群差异(人种、地理环境等差异)以及各试验生化指标检测时间的差异,可能会对结局指标产生影响,导致异质性产生,影响研究结果。
3.2 系统评价分析结果讨论
3.2.1 茵陈汤加减方VS单纯西药组 与单纯西药组相比,茵陈汤加减方治疗后总有效率、皮肤瘙痒好转率,血清TBA、ALT、AST水平改善显著高于对照组,羊水污染、早产、胎儿宫内窘迫发生率明显低于对照组,而在其他黄疸消退率、TBIL、DBIL水平改善、剖宫产率、产后出血、新生儿体质量方面无统计学意义。单纯西药组通过使用药物缓解瘙痒症状,恢复肝功能,降低血胆汁酸水平,达到改善妊娠结局的目的。而中医学以清热利湿退黄为原则治疗本病。茵陈汤中茵陈清利湿热、退黄疸,栀子泻火除烦、清热利湿、凉血解毒,大黄泻热逐瘀、利胆退黄。同时,现代医学研究表明,茵陈能使胆汁流量增加,促进胆酸和胆红素的排泄,有明显的利胆作用;栀子可增加胆汁流通,有明显的利胆和改善胆汁瘀积作用[18]。中医学从整体出发,辨证论治,应用茵陈汤加减方治疗ICP能明显减轻瘙痒,降低早产、羊水污染、胎儿窘迫发生率。
3.2.2 茵陈汤加减方结合西药组VS单纯西药组 与单纯西药组相比,茵陈汤加减方结合西药组治疗后总有效率、皮肤瘙痒好转率、黄疸消退率,血清TBA、ALT、TBIL、DBIL水平改善,新生儿体重显著高于对照组,羊水污染、早产、胎儿宫内窘迫、产后出血发生率、剖宫产率明显低于对照组,而在其他AST水平改善方面无统计学意义。中西医联合疗法将中医整体辨证论治与西医对靶器官的调节相结合共同治疗疾病,更具有优势。
3.3 本系统评价的意义 本研究全面客观收集茵陈汤加减方治疗ICP临床证据而做的评价,相信能对临床决策起一定的帮助作用。但因所纳入临床试验欠规范且方法学质量偏低,尚未得出一个较为概括性的结论。因研究纳入人群均为中国人,该结论存在一定局限性。综上,茵陈汤加减方对皮肤瘙痒改善较单纯的西药组治疗好,早产、羊水污染、胎儿宫内窘迫发生率较单纯西药组低;茵陈汤加减方结合西药组对皮肤瘙痒好转、黄疸消退较单纯的西药组好,羊水污染、早产、胎儿宫内窘迫、产后出血发生率、剖宫产率明显低于单纯西药组。生化指标,如AST、ALT、TBA、DBIL、TBIL,因各试验组间异质性较大,茵陈汤加减方在生化指标上的改善尚有待大规模临床随机对照试验进行验证。目前尚无充分证据证明茵陈汤加减方治疗ICP的有效性和安全性优于单纯西药治疗。故此为全面评估茵陈汤治疗ICP的有效性和安全性,尚需更多严格设计的随机双盲对照试验支持。
[1]Lammert F,Marschall H-U,Glantz A,et al.Intrahepatic cholestasis of pregnancy:molecular pathogenesis,diagnosis and management[J].Hepatol.2000,33:1012-1021.
[2]曹泽毅.中华妇产科学[M].北京:人民卫生出版社,2004:472-473.
[3]黄健.“护肝利胆汤”为主治疗妊娠期肝内胆汁瘀积症29例[J].江苏中医药,2002,23(11):37.
[4]张春敏.自拟止痒退黄汤治疗妊娠胆汁瘀积症临床观察[J].中医药临床杂志,2012,24(12):1169-1170.
[5]张新,王佩娟,张蕾.加味茵陈汤治疗妊娠期肝内胆汁瘀积症的临床观察[J].辽宁中医杂志,2006,33(12):1590-1591.
[6]赵翠英,陈静琴,陈华,等.茵黄合剂治疗妊娠肝内胆汁郁积症的临床研究——附100例疗效观察[J].江苏中医,2000,21(3):8.
[7]曹淑萍,史雪莉,侯秀环.中西医结合治疗妊娠期肝内胆汁瘀积症40例[J].陕西中医学院学报,2006,29(2):31-33.
[8]傅巧琴,方华英,陈慧君,等.中西医结合治疗妊娠期肝内胆汁瘀积症临床观察[J].实用中西医结合临床,2006,6(1):25.
[9]顾雪芳.中西医结合治疗妊娠期肝内胆汁瘀积症28例[J].现代中西医结合杂志,2008,17(23):3593-3594.
[10]黄春蕾.中西医结合治疗妊娠期肝内胆汁瘀积症30例[J].云南中医中药杂志,2009,30(2):17.
[11]金敏霞.中西医结合治疗妊娠期肝内胆汁瘀积症100例[J].浙江中西医结合杂志,2006,16(11):698-699.
[12]刘丽,李世彤.中西医结合治疗妊娠期肝内胆汁瘀积症32例疗效观察[J].云南中医中药杂志,2007,28(9):14.
[13]施燕.茵陈解毒汤治疗妊娠肝内胆汁瘀积症50例[J].中国中医药科技,2010,17(6):555-556.
[14]宋晓晖,徐元萍,马莎,等.中西医结合治疗妊娠期肝内胆汁瘀积症对妊娠结局的影响[J].数理医药学杂志,2012,25(2):164-165.
[15]王慧艳.中西医结合治疗妊娠期肝内胆汁瘀积症43例[J].南京中医药大学学报(自然科学版),2001,17(6):353-354.
[16]夏卫红.抗瘀胆汤治疗妊娠期肝内胆汁瘀积症的临床疗效评价[D].长沙:湖南中医学院,2004.
[17]姚芳.中西医结合治疗妊娠期胆汁瘀积症临床分析[J].浙江中西医结合杂志,2012(9):49-50.
[18]于灵,何江丽.中西医结合治疗妊娠期肝内胆汁瘀积症23例效果分析[J].中外健康文摘,2012,09(29):405-406.
[19]曾琼.健脾利湿中药治疗妊娠期肝内胆汁郁积症18例[J].中西医结合肝病杂志,2009,19(1):50-51.
[20]张友伍.中西医结合治疗妊娠期肝内胆汁瘀积症疗效观察[J].医学理论与实践,2008,21(10):1198-1200.
[21]郑虹,周洁,赵宇,等.中西医结合治疗妊娠期肝内胆汁瘀积症[J].浙江中西医结合杂志,2004,14(10):609-610.
[22]陈怡,陈凤英.中药治疗妊娠肝内胆汁瘀积症的临床疗效与机制[J].中国中药杂志,2009(11):117-119.
[23]夏玉兰.胆郁合剂治疗妊娠期肝内胆汁瘀积症疗效分析[J].实用中医药杂志,2012,28(8):632-633.
[24]卞桂萍.中西医结合治疗妊娠期肝内胆汁瘀积症的疗效分析[J].东南大学学报:医学版,2006,25(2):101-103.
[25]陈晓燕,莫洁芳.中药结合地塞米松治疗妊娠肝内胆汁瘀积症[J].四川医学,2005,26(6):659-660.
[26]黄雪莉.中西医结合治疗妊娠肝内胆汁瘀积症60例[J].江西中医药,2008,39(7):47.
[27]蓝九红.中西医结合治疗妊娠期肝内胆汁瘀积症36例[J].浙江中医杂志,2008,43(12):713.
[28]马忠芳.中西医结合治疗妊娠肝内胆汁瘀积症35例[J].中国民族民间医药,2010,19(19):113-114.
[29]倪飞英.中西医结合治疗妊娠期肝内胆汁瘀积症(附133例临床病例分析)[J].中国计划生育和妇产科,2009,1(1):60-62.
[30]宋涛,刘赛欧.中西医结合治疗妊娠期肝内胆汁瘀积症60例[J].贵阳中医学院学报,2001,24(2):25.
[31]孙晓芳,计霞萍.中西医结合治疗妊娠期肝内胆汁瘀积症85例[J].中国妇幼保健,2009,24(36):5262-5263.
[32]王芳,赵汝珠,李妍芹,等.茵陈黄疸冲剂治疗妊娠期肝内胆汁瘀积症临床观察[J].中国中医急症,2007,16(5):543-544.
[33]吴惠平.中西医结合治疗妊娠期肝内胆汁瘀积症疗效观察[J].现代中西医结合杂志,2007,16(4):434-435.
[34]颜云华.中西医结合治疗妊娠肝内胆汁瘀积症50例疗效观察[J].齐齐哈尔医学院学报,2006,27(18):2207.
[35]张群英.中西医结合治疗妊娠期肝内胆汁瘀积症34例——附单用西药治疗27例对照[J].浙江中医杂志,2001,36(9):383.
[36]赵淑英.中西医结合治疗妊娠肝内胆汁瘀积症临床疗效分析[J].山西临床医药,2001,10(12):941-942.
[37]朱妮娜,黄顺彬.中西医结合治疗妊娠期肝内胆汁瘀积症疗效分析[J].四川中医,2008,26(8):69.
[38]高晓燕.妊娠期肝内胆汁瘀积症中西药治疗比较[J].黑龙江中医药,2006,56(1):42.
[39]艾国华,张晓红.中西医结合治疗190例妊娠期肝内胆汁瘀积综合征的临床观察[J].亚太传统医药,2012,8(4):84-85.
[40]丁少娜.腺苷蛋氨酸联合中药治疗妊娠期肝内胆汁瘀积症疗效分析[J].中国基层医药,2010,17(4):490-491.
[41]邱玉叶.自拟方治疗妊娠期肝内胆汁瘀积症120例临床报告[J].浙江中医药大学学报,2011,35(1):45-46.
[42]沈慈慧,陶冶.中西医结合治疗妊娠期肝内胆汁瘀积症30例[J].浙江中医杂志,2009,44(5):347-348.
[43]孙丽珍.疏肝利胆中药治疗妊娠肝内胆汁瘀积症临床观察[J].中国中医急症,2008,17(1):43,45.
[44]王晓燕,石玉萍.中西医结合治疗妊娠期肝内胆汁瘀积症100例临床分析[J].卫生职业教育,2010,28(16):137-138.
[45]张莉,许吟.茵栀黄注射液在妊娠期肝内胆汁瘀积症治疗中的辅助应用[J].贵阳中医学院学报,2003,25(2):30-31.
[46]赵瑞芳.中西医结合治疗妊娠期肝内胆汁瘀积症临床分析[J].现代中西医结合杂志,2011,20(35):4497-4498.
[47]周加林,施卫兵.自拟茵蒲合剂治疗妊娠期肝内胆汁瘀积症30例[J].中医药临床杂志,2012,24(7):660-661.
[48]黄金阳,刘淮.中西两种药物治疗妊娠期肝内胆汁瘀积症的疗效分析[J].中国中西医结合杂志,2004,24(4):309-311.
[49]胡娅莉,万铭.妊娠期肝内胆汁瘀积症治疗方法的研究[J].江苏中医,1999,20(8):31.
[50]程华.腺苷蛋氨酸联合中药治疗妊娠期肝内胆汁瘀积症的临床疗效观察[J].健康必读(中旬刊),2012,11(10):266-267.
[51]范惠文,宋一楠.中西药联合治疗妊娠期肝内胆汁瘀积症50例临床观察[J].新疆中医药,2012,30(2):42-43.
[52]王建定,赖启明.中西医结合治疗妊娠期肝内胆汁瘀积症35例[J].浙江中西医结合杂志,2011,21(2):102-103.
[53]金方,李艳芳,金克勤.思美泰结合中药茵白汤治疗妊娠肝内胆汁瘀积症[J].浙江中医药大学学报,2010,34(2):187-188.
[54]沈岚,赵剑虹.中西医结合治疗妊娠期肝内胆汁瘀积症[J].浙江中西医结合杂志,2005,15(5):287-288.
[55]赵秀芳.中西药联合治疗妊娠肝内胆汁瘀积症[J].国际医药卫生导报(学术版),2005,11(22):38-40.
