XELOX方案与SOX方案治疗Ⅳ期胃癌患者的疗效与安全性比较
2014-08-08卢战辉
卢战辉
XELOX方案与SOX方案治疗Ⅳ期胃癌患者的疗效与安全性比较
卢战辉
目的 对比分析XELOX方案与SOX方案治疗Ⅳ期胃癌患者的疗效与安全性。方法 根据化疗方案将125例Ⅳ期胃癌患者分为观察组(71例)与对照组(54例)。观察组采用XELOX方案(卡培他滨联合奥沙利铂)治疗,对照组采用SOX方案(替吉奥联合奥沙利铂)治疗。化疗2个周期后对所有患者进行疗效与不良反应评价。结果 ①2组患者近期疗效相比差异无统计学意义(P>0.05)。②2组患者腹泻、恶心呕吐、肾脏毒性、周围神经炎、口腔黏膜炎、脱发等不良反应分级相比差异无统计学意义(P>0.05),观察组肝脏毒性分级显著低于对照组(P<0.05)。③2组患者中位无进展生存期、1年生存率相比差异无统计学意义(P>0.05)。结论 XELOX方案与SOX方案治疗Ⅳ期胃癌患者的近期疗效与远期疗效均相当,但是前者的肝脏毒性较轻,是临床治疗Ⅳ期胃癌的理想化疗方案。
卡培他滨;替吉奥;奥沙利铂;胃癌
(ThePracticalJournalofCancer,2014,29:1607~1609)
胃癌是目前全球第4大常见恶性肿瘤,尽管手术是唯一有可能治愈胃癌的方法,但是对不可切除以及术后复发的晚期胃癌来说,化疗是其主要的治疗手段[1-2]。传统曾用单药如氟尿嘧啶、丝裂霉素C、依托泊苷、阿霉素、表柔比星等治疗晚期胃癌,但是疗效不佳,有效率低,于是联合方案逐步应用于临床,但是不同方案的性能不一[3]。本研究旨在对比分析XELOX方案与SOX方案治疗Ⅳ期胃癌患者的疗效与安全性,现报告如下。
1 资料与方法
1.1 一般资料
选取2010年7月-2012年9月我院收治的125例患者。纳入标准:①经病理诊断确诊为胃癌;②临床分期为Ⅳ期;③预计生存时间≥3个月;④有客观可测量的肿瘤病灶;⑤最近6个月内未接受化疗;⑥签署知情同意书,服从本研究安排。排除标准:①合并肝、肾、心、骨髓等重要脏器功能不全的患者;②病情在1个化疗周期后迅速进展,或化疗过程中出现严重不良反应,或合并严重非肿瘤因素,导致化疗被迫放弃的患者。根据化疗方案将上述患者分为观察组与对照组。观察组71例,男性49例,女性22例;年龄52~74岁,平均(63.8±5.4)岁;病理类型:低分化腺癌39例,中低分化腺癌16例,高中分化腺癌10例,黏液腺癌6例;胃癌手术治疗史45例;合并肝脏转移24例,恶性腹水21例,腹膜转移11例,卵巢转移9例,肺转移4例。对照组54例,男性37例,女性17例;年龄50~71岁,平均(62.1±5.0)岁;病理类型低分化腺癌30例,中低分化腺癌12例,高中分化腺癌9例,黏液腺癌3例;胃癌手术治疗史34例;合并肝脏转移19例,恶性腹水16例,腹膜转移8例,卵巢转移6例,肺转移3例。2组患者一般资料相比差异无统计学意义(P>0.05)。
1.2 研究方法
观察组患者接受XELOX方案治疗,具体措施为奥沙利铂130 mg/m2,第1天静脉滴注>2 h;卡培他滨1 000 mg/(m2·d),口服,2次/天,早餐、晚餐后服用,d1~d14;间隔7 d,21 d为1个化疗周期。对照组患者接受SOX方案治疗,具体措施为奥沙利铂130 mg/m2,第1天静脉滴注>2 h;替吉奥80 mg/(m2·d),服用方法与卡培他滨一致;间隔7 d,21 d为1个化疗周期。不良反应处理:①合并骨髓抑制时,给予重组人粒细胞集落刺激因子,或促红细胞生成素,或白介素-2对症处理。②合并恶心呕吐时,给予昂达司琼止吐以及质子泵抑制剂抑酸。③合并手足综合征时,给予维生素B6、维生素B1对症处理。所有患者均接受2个周期的化疗,化疗结束后对所有患者进行疗效与不良反应评价。
1.3 近期疗效评价标准
采用《实体瘤的疗效评价标准》1.1 版进行疗效评价,该标准将患者疗效分为完全缓解(CR)、部分缓解(PR)、疾病进展(SD)、疾病稳定(PD)。
1.4 不良反应分级标准
根据抗肿瘤药物不良反应分级标准(WHO标准)对腹泻、恶心呕吐、肾脏毒性、肝脏毒性、周围神经炎、口腔黏膜炎、脱发等不良反应进行分级,分为0级~Ⅳ级。
1.5 统计学分析
采用SPSS 19.0统计软件进行数据分析,计数资料以百分率(%)表示。组间近期疗效、不良反应分级比较采用秩和检验,无进展生存期Kaplan-Meier法进行分析,生存率比较用Log-Rank检验,P<0.05为差异有统计学意义。
2 结果
2.1 2组患者近期疗效的比较
2组患者近期疗效分别为60.6%、61.1%,差异无统计学意义(P>0.05),见表1。
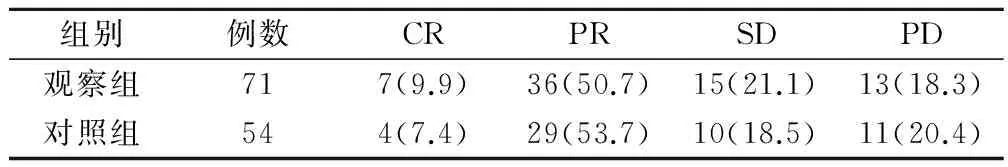
表1 2组患者近期疗效的比较(例,%)
2.2 2组患者不良反应分级的比较
2组患者腹泻、恶心呕吐、肾脏毒性、周围神经炎、口腔黏膜炎、脱发等不良反应分级相比,差异无统计学意义(P>0.05),但观察组肝脏毒性分级显著低于对照组(P<0.05)。见表2。
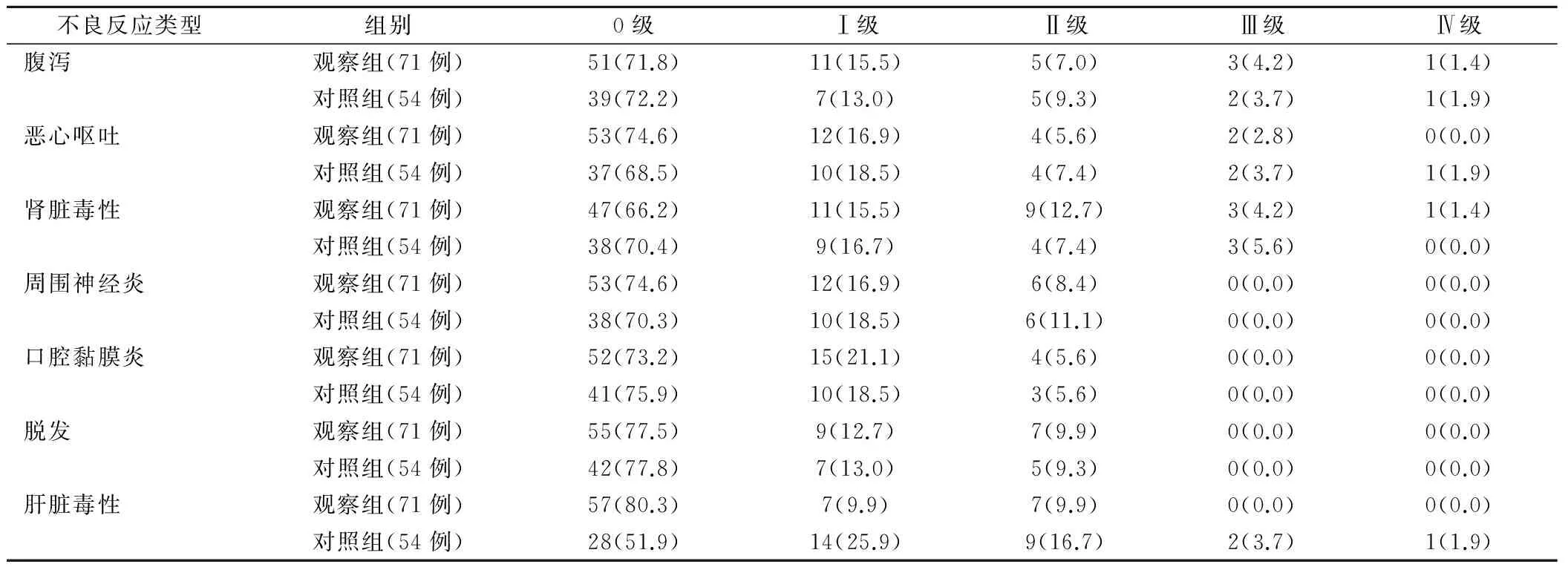
表2 2组患者不良反应分级的比较(例,%)
2.3 2组患者远期疗效的比较
观察组、对照组中位无进展生存期分别为6.3个月、7.1个月,1年生存率分别为46.5%(33/71)、44.4%(24/54)。2组患者中位无进展生存期、1年生存率相比,差异无统计学意义(P>0.05)。
3 讨论
晚期胃癌的联合化疗方案在20世纪70~80年代,主要有FAM、ELF、FAMTX等方案,但有效率均较低,尤其是FAM、ELF方案,其有效率不到10%[4]。在20世纪80~90年代,含铂类化疗方案如EAP、FLEP、CF、PELF、ECF方案等应用于临床,尽管治疗有效率有所提高,但仍不甚满意。进入21世纪,新一代化疗药物如紫杉醇、多西紫杉醇、伊立替康、奥沙利铂、卡培他滨、替吉奥等在临床上用于晚期胃癌的化疗,基于新一代化疗药物的联合方案亦逐步在临床上推广,这大大改善了晚期胃癌的疗效[5-6]。
XELOX方案由卡培他滨、奥沙利铂组成,该方案传统用于治疗进展期大肠癌,后来研究发现该方案对晚期胃癌亦有一定的疗效。Park 等[7]报道XELOX方案治疗37例晚期胃癌患者,结果可见总有效率为63%;中位无进展生存期、中位总生存期分别为5.8个月、11.9个月;主要血液学不良反应是贫血,发生率高达70%(26/37),Ⅲ~Ⅳ级中性粒细胞减少发生率为11%(4/37),其中1例患者出现中性粒细胞减少性发热,其他常见的非血液学不良反应有神经病变、呕吐、手足综合征、腹泻,其发生率分别为70%、50%、39%、33%,以Ⅰ~Ⅱ级常见,Ⅲ~Ⅳ级罕见。Luo 等[8]报道XELOX方案治疗50例晚期胃癌患者,结果可见总有效率为42%;中位进展期、中位总生存期分别为5.8个月、11.1个月;主要血液学不良反应是中性粒细胞减少,发生率为56%(28/50),Ⅲ~Ⅳ级中性粒细胞减少为12%(6/50),其中2例患者出现中性粒细胞减少性发热,其他非血液学不良反应有呕吐、手足综合征、腹泻、感觉神经毒性,其发生率分别为34%、26%、24%、22%。由上述研究可知,XELOX方案是疗效确切、耐受性好的晚期胃癌一线化疗方案。
随着替吉奥应用于临床,基于替吉奥的联合化疗方案亦用于晚期胃癌的治疗,其中以SOX方案较为常用,该方案是由替吉奥、奥沙利铂组成。Oh 等[9]报道SOX方案治疗41例晚期胃癌患者,其中22例患者部分缓解,15例患者疾病稳定,1例患者疾病进展;中位进展期、中位总生存期分别为4.6个月、7.8个月;主要不良反应是Ⅱ级贫血、Ⅰ~Ⅱ级中性粒细胞减少、Ⅰ级血小板减少,其他非血液学不良反应有Ⅲ级呕吐、Ⅲ级腹泻。由此可知,SOX方案治疗晚期胃癌的疗效与安全性亦获得肯定。
在本研究中,观察组采用XELOX方案治疗,对照组采用SOX方案治疗。在治疗效果方面,2组患者近期疗效、中位无进展生存期、1年生存率相比差异无统计学意义(P>0.05),即2个方案治疗Ⅳ期胃癌疗效相当。在治疗安全性方面,2组患者腹泻、恶心呕吐、肾脏毒性、周围神经炎、口腔黏膜炎、脱发等不良反应分级相比,差异无统计学意义(P>0.05),观察组肝脏毒性分级显著低于对照组(P<0.05),这说明XELOX方案治疗Ⅳ期胃癌可以取得更好的安全性。综上所述,XELOX方案治疗Ⅳ期胃癌值得临床推广应用。
[1] 王会忠.不同化疗方案在晚期胃癌治疗中的临床效果比较〔J〕.实用癌症杂志,2014,29(2):183-184,187.
[2] 张信强,徐 燕,陈明祥.替吉奥胶囊单药联合放疗治疗晚期胃癌的临床观察〔J〕.临床肿瘤学杂志,2013,18(7):628-630.
[3] 高丹丹,刘 磊,白玉贤.晚期胃癌化疗及分子靶向治疗研究进展〔J〕.中国肿瘤临床,2012,28(23):1978-1981.
[4] 庄庆昕.晚期胃癌化疗策略进展〔J〕.临床肿瘤学杂志,2011,16(8):760-764.
[5] 程晓春,陈 俊,郭 建,等.多西紫杉醇联合卡培他滨或氟尿嘧啶治疗晚期胃癌的对比研究〔J〕.中国药业,2013,22(9):67-68.
[6] 阮新建,张书霞,贾得前,等.奥沙利铂联合替吉奥治疗晚期胃癌的临床观察〔J〕.实用癌症杂志,2014,29(1):51-52.
[7] Park YH,Lee JL,Ryoo BY,et al.Capecitabine in combination with Oxaliplatin (XELOX) as a first-line therapy for advanced gastric cancer〔J〕.Cancer Chemother Pharmacol,2008,61(4):623-629.
[8] Luo HY,Xu RH,Wang F,et al.Phase Ⅱ trial of XELOX as first-line treatment for patients with advanced gastric cancer〔J〕.Chemotherapy,2010,56(2):94-100.
[9] Oh SY,Kwon HC,Jeong SH,et al.A phase Ⅱ study of S-1 and oxaliplatin (SOx) combination chemotherapy as a first-line therapy for patients with advanced gastric cancer〔J〕.Invest New Drugs,2012,30(1):350-356.
(编辑:甘 艳)
Comparison of the Efficacy and Safety of XELOX and SOX for Stage Ⅳ Gastric Cancer
LUZhanhui.
GeneralHospitalofJinshuiDistrict,Zhengzhou,450014
Objective To compare the efficacy and safety of XELOX and SOX in the treatment of stage Ⅳ gastric cancer.Methods 125 cases of stage Ⅳ gastric cancer were divided into the observation group(71 cases) and the control group(54 cases) according to their therapeutic regimen,and the observation group
XELOX(Capecitabine plus Oxaliplatin),while the control group was given SOX(Gimeracil and Oteracil Porassium plus Oxaliplatin).The efficacy and adverse reactions were evaluated after 2 cycles of chemotherapy.Results There was no significant difference in short-term efficacy between the 2 groups(P>0.05).There were no significant differences in diarrhea,nausea and vomiting,kidney toxicity,peripheral neuritis,oral mucositis and alopecia between the 2 groups(P>0.05),while the degree of hepatotoxicity in the observation group was significantly lower than that of the control group(P<0.05).There were no significant differences in median progression-free survival time and 1-year survival rate between the 2 groups(P>0.05).Conclusion The XELOX and SOX have similar short-term and long-term efficacy in the treatment of stage Ⅳ gastric cancer,but the XELOX has lower degree of hepatotoxicity,which is an ideal chemotherapy for stage Ⅳ gastric cancer.
Capecitabine;Gimeracil and Oteracil Porassium;Oxaliplatin;Gastric cancer
450014 河南省郑州市金水区总医院
10.3969/j.issn.1001-5930.2014.12.031
R735.2
A
1001-5930(2014)12-1607-03
2014-06-10
2014-11-06)
