半纤维素热解反应的微观反应机理研究
2014-08-07曹小玲熊家佳邓胜祥张航罗海银唐世斌
曹小玲,熊家佳,邓胜祥, 张航,罗海银,唐世斌
(1.长沙理工大学 能源与动力工程学院, 长沙 410004;2.中南大学 能源科学与工程学院, 长沙 410083)
引言
生物质能作为一种清洁的可再生能源,逐步引起了全世界的广泛关注。生物质热解是一种高效转化生物质能[1-5]的新技术,它是生物质气化和生物质燃烧的起始过程。目前,对于生物质热解机理的研究仍处于摸索阶段。半纤维素由于结构复杂且多变,热解过程发生大量的脱水、化学键的合成与断裂、小分子化合物聚合等反应,不易掌握其整个热解过程,所以相关的研究与报道也相对较少,对其理化性质以及热解反应机理缺乏深入的研究。[6-9]对半纤维素热解反应的微观机理进行深入研究不仅有助于了解生物质的热解过程,为生物质的热解技术提供理论基础,而且对生物质能的利用以及富含半纤维素的工业废弃物的利用在造纸行业领域具有重要的工程价值。[10]
研究发现,半纤维素的典型模化物木聚糖热解反应后会得到一种非常重要的产物2-糠醛,而且几乎所有的关于木聚糖热解反应的研究中都能发现2-糠醛的存在。[11]本文以2-糠醛为切入点来研究半纤维素的热解反应机理。
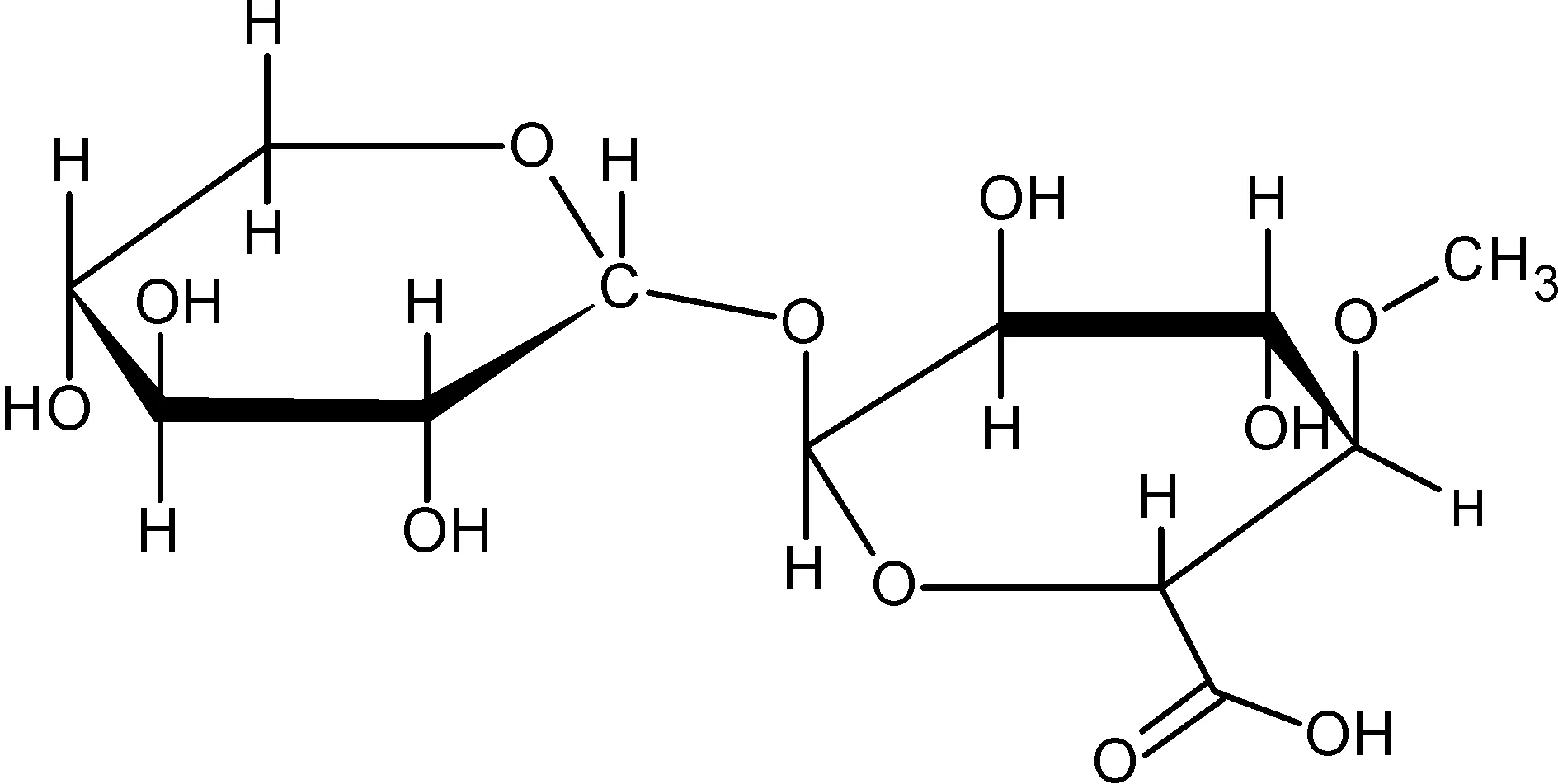
图1 4-O-甲基-D-葡萄糖醛酸-D-木糖
1 反应路径设计
半纤维素的二聚体模型物分子4-O-甲基-D-葡萄糖醛酸-D-木糖,如图1所示。其中的D-木糖作为半纤维素主链的代表,4-O-甲基-D-葡萄糖醛酸作为支链的代表。将热解反应分为两个阶段[12-15]来研究,其中第一阶段为二聚体4-O-甲基-D-葡萄糖醛酸-D-木糖的解聚,第二阶段为解聚后的两个单体分别反应生成半纤维素热解反应的典型产物2-糠醛。
1.1 第一阶段二聚体模型化合物的解聚反应
4-O-甲基-D-葡萄糖醛酸-D-木糖的解聚如图2所示。4-O-甲基-D-葡萄糖醛酸-D-木糖分子和水分子在一定的温度条件下被激发,此时二聚体从中间断裂,断裂的部分分别连接上水分子的羟基和氢原子,形成D-木糖分子和4-O-甲基-D-葡萄糖醛酸分子,这样整个二聚体的解聚就完成了,即第一阶段的热解反应完成。这个阶段表示两个糖基单元的分离,代表半纤维素分子的支链从主链上脱离,是半纤维素的热解最开始的阶段。

图2 二聚体4-O-甲基-D-葡萄糖醛酸-D-木糖的解聚
1.2 第二阶段单体1反应生成2-糠醛
在较低温度时,木聚糖的热解反应主要发生在其支链上,即糖基单元4-O-甲基-D-葡萄糖醛酸分解过程,如图3所示。甲氧基脱离,羧基发生脱酰基反应,这两部分形成CH3OH分子和CO2分子。剩下来的杂环发生开环反应,脱去水分子再形成一个新的杂环分子,从六元环变成五元环。五元环再脱去水分子,形成2-糠醛分子。这是热解反应第二阶段低温时支链上发生的反应,称为第二阶段反应1。

图3 4-O-甲基-D-葡萄糖醛酸反应生成2-糠醛
1.3 第二阶段单体2反应生成2-糠醛
随着热解温度的升高,热解反应深入进行,木聚糖的主链发生解聚反应分解为很多糖基单元。糖基单元D-木糖单体发生分解,通过一系列反应得到各种小分子化合物,其中包括木聚糖热裂解的典型产物2-糠醛。如图4所示,杂环发生开环反应,形成新的杂环,从六元环变成五元环。新形成的五元环的支链上发生脱水反应形成甲醛基。剩下的部分再脱去两分子水形成剩下2-糠醛分子。这是热解反应第二阶段温度升高时主链上发生的反应,称为第二阶段反应2。

图4 D-木糖反应生成2-糠醛
2 计算方法
密度泛函理论[16](DFT)在考虑电子相关效应的同时,不仅可进行大分子体系的计算,而且计算结果准确、可靠。对于比较轻的元素,比如C、H、O和N等,B3LYP/6-31G(d,p)基组就很合适。
为了进一步研究半纤维素的热解反应机理和其反应路径,采用Gaussian09程序中的密度泛函理论中的B3LYP /6-31G( d,p)方法,对半纤维素的模型化合物二聚体4-O-甲基-D-葡萄糖醛酸-D-木糖在设计反应路径中的各反应物、产物、中间体及过渡态进行了几何构型的全优化,并对热力学量考虑了振动零点能(ZPE)校正,然后进行频率计算,得出各个构想的单点能。采用TS方法来寻找过渡态,过渡态有惟一的虚频振动频率。计算反应各驻点的振动频率,分析每一个过渡态的真实性。在做频率计算时,加入关键词temperature=(300K,500K,700K,900K,1100K)等,分别控制热解反应的不同温度条件,最后用内禀反应坐标IRC方法来验证所设计的热解反应过程的正确性,正确衔接过渡态结构和反应物、中间体、产物,验证前面设计的反应路径,从而得到半纤维素热解反应机理模型。
3 计算结果及分析
3.1 第一阶段二聚体模型化合物的解聚反应动力学分析
按照过渡状态理论,反应物与位能面的鞍点(即过渡态)均处于基态时,它们的最低位能差就是活化能。根据此原理,在对反应物、产物及过渡态分别进行几何构形的优化后,再对它们做频率计算,得到了经过零点能校正后的总能量E。

表1 第一阶段热解反应在不同温度下的焓变ΔH(单位:kJ/mol)
由表1可以看出,热解反应的第一阶段是反应物R1和R2反应先产生过渡态TS1,然后TS1反应生成产物P1及P2。R1和R2反应生成过渡态TS1这一步是吸热反应,700K时吸收的热量最少,此时的焓变为69kJ/mol。TS1反应生成P1和P2这一步是放热反应,300K时放出的热量最少,此时的焓变为-110kJ/mol。整个反应即热解反应第一阶段是放热反应。
对比5个温度下的反应焓变ΔH发现,如表2所示,随着温度的升高,反应的放热越来越多,到700K左右热解反应达到峰值,温度再升高,反应的放热反倒减少。700K时反应放热最多,表示此时反应更容易进行,反应速率是最大的。
这个反应路径在不同温度下的反应自由能变ΔG均小于0,表明第一阶段的热解反应可以自发进行。随着温度的升高,反应自由能变ΔG呈现波动的趋势,结合焓变ΔH分析可知,300K时温度较低,整个反应是放热反应,温度越低反应越容易发生,同时产物的转化率也越高。随着温度的升高,500K时产物的转化率最低。700K时反应放热最多,表示此时反应更容易进行,反应速率是最大的,同时此时的ΔG也较500K时小,产物的转化率较500K时高。根据勒夏特列原理,再往后温度继续升高,放热反应会向逆反应的方向进行,即反应的正反应越难进行,产物的转化率降低。

表2 第一阶段反应路径的动力学变值(单位:kJ/mol)
综合上述分析可以发现,700K应该是第一阶段的热解反应发生的最佳温度。

图5 第一阶段反应的势能剖面图
图5为第一阶段热解反应的势能剖面图。从图中可以看出,反应物R1和R2反应先产生过渡态TS1,然后TS1反应生成产物P1及P2。
3.2 第二阶段单体1反应生成2-糠醛动力学分析
由表3和图3可以看出,在热解反应第二阶段的反应1是反应物R3反应先产生过渡态TS21,然后TS21反应生成中间体IM21和产物P3及P4。R3反应生成TS21是吸热反应,不同温度下焓变相同,都是190kJ/mol,说明温度对这一步的反应影响不大。TS21反应生成中间体IM21和产物P3及P4是放热反应,随着温度的变化,焓变值略有不同,低温和高温时放热较多,500K时放热最少,此时的焓变为-227kJ/mol。接着中间体IM21反应生成过渡态TS22,这一步也是吸热反应,1100K时吸收的热量最少,此时的焓变为230kJ/mol。过渡态TS22反应生成中间体IM22和产物P5,这一步是放热反应。中间体IM22反应生成过渡态TS23,最后TS23反应生成产物P5和P6。IM22反应生成TS23是吸热反应,TS23反应生成P5和P6是放热反应。整个反应即热解反应第二阶段反应1是放热反应。
表4给出了热解反应第二阶段反应1在不同温度下的动力学数据。5个温度下的反应焓变ΔH均小于0,表示这个反应是放热反应。随着温度的升高,反应放出的热量呈现波动的情况,到500K左右放出的热量最少。

表3 第二阶段热解反应1在不同温度下的焓变ΔH(单位:kJ/mol)
热解反应第二阶段反应1在不同温度下的反应自由能变ΔG均小于0,表示反应1可以自发进行。随着温度逐渐升高,反应自由能变ΔG逐渐变大,说明温度的升高不利于反应1正反应的进行。温度的继续升高,产物的转化率也逐渐降低。300K时反应物的转化率最高,1100K时反应物的转化率最低。
综合上述分析可以发现,500K左右时第二阶段反应1的反应速率最大。

表4 第二阶段反应1在不同温度下的动力学变值(单位:kJ/mol)
图6为第二阶段反应1的势能剖面图。从图中可以看出,反应物R3先反应产生过渡态TS21,然后TS21形成三个自由基(产物P3、P4和中间体IM21)。中间体再次反应,IM21反应生成过渡态TS22,然后TS22形成自由基(产物P5和中间体IM22)。中间体IM22生成过渡态TS23,然后生成产物P6和P5。

图6 第二阶段反应1的势能剖面图
3.3 第二阶段单体2反应生成2-糠醛动力学分析
由表5和图4可以看出,热解反应第二阶段的反应2是反应物R4先产生过渡态TS31,然后TS31反应生成中间体IM31。R4反应生成TS31是吸热反应,不同温度下焓变相同,都是170kJ/mol,说明温度对这一步的反应影响不大。TS31反应生成中间体IM31是放热反应,随着温度的变化,焓变值略有不同,300K时放热最多,此时的焓变为-160kJ/mol。接着中间体IM31反应生成过渡态TS32,这一步也是吸热反应,300K时吸收的热量最多,此时的焓变为150kJ/mol。然后过渡态TS32反应生成中间体IM32和产物P5,这一步是放热反应,随着温度的变化,反应放出的热量呈现波动,700K时放热最少,此时的焓变是-89kJ/mol,900K时放热最多,此时的焓变是-101KJ/mol。再接着是中间体IM32反应生成过渡态TS33,最后TS33反应生成产物P6和P5。IM32反应生成TS33是吸热反应,TS33反应生成P5和P6是放热反应。整个反应即热解反应第二阶段反应2是吸热反应。

表5 第二阶段热解反应2在不同温度下的焓变ΔH(单位:kJ/mol)
表6 中给出了热解反应第二阶段反应2在不同温度下的动力学数据。5个温度下的反应焓变ΔH均大于0,表示这个反应是吸热反应。随着温度的升高,反应吸收的热量越来越多,到700K左右达到峰值,温度再升高,反应吸收的热量反而减少。700K时反应吸收的热量最多,表示此时的反应最容易进行,反应速率是最大的。
热解反应第二阶段反应2在不同温度下的反应自由能变ΔG均小于0,表明反应2可以自发进行。随着温度的升高,反应自由能变ΔG逐渐变大,表明温度的升高不利于反应2正反应的进行。随着温度的继续升高,产物的转化率逐渐降低。300K时反应物的转化率最高,1100K时反应物的转化率最低。
综合上述分析可以发现,700K左右时第二阶段反应2的反应速率最大。

表6 第二阶段反应2在不同温度下的动力学变值(单位:kJ/mol)
图7为第二阶段反应2的势能剖面图。从图中可以看出,反应物R4先反应产生过渡态TS31,然后TS31形成自由基(中间体IM31)。中间体再次反应,IM31反应生成过渡态TS32,然后TS32形成自由基(产物P5和中间体IM32)。中间体IM32生成过渡态TS33,然后生成产物P6和P5。

图7 第二阶段反应2的势能剖面图
4 结论
在半纤维素热解反应过程中,利用其模型物二聚体4-O-甲基-D-葡萄糖醛酸-D-木糖来代替天然的半纤维素作为研究对象,将热解反应分为两个阶段来研究,第一阶段为二聚体4-O-甲基-D-葡萄糖醛酸-D-木糖的解聚,第二阶段为解聚后的两个单体分别反应生成半纤维素热解反应的典型产物2-糠醛。
从各条反应路径计算得到的热力学数值上分析得出以下结论:随着温度的升高,反应放出的热量越来越多,到700K左右热解反应达到峰值,温度再升高,反应的放热反倒减少。但随着温度的继续升高,产物的转化率也逐渐降低。300K时反应物的转化率最高,1100K时反应物的转化率最低。综合分析每个反应的动力学变值可以发现,700K左右是第一阶段的热解反应即二聚体解聚发生的最佳温度,500K左右为第二阶段反应1即支链分解反应的最大反应速率,700K左右为第二阶段反应2即主链分解反应的最大反应速率。
参考文献:
[1]宋卫东,方彤,王乾坤,等.2009年《世界能源展望》要点综述[J].能源技术经济,2010,22(1):18-22.
[2]中国可再生能源学会,中国科学院广州能源研究所.中国新能源与可再生能源年鉴2010[K].西安:中国可再生能源学会,2010.
[3]Ahmed I I,Gupta A K.Kinetics of woodchips char gasification with steam and carbon dioxide[J].Applied Energy, 2011, 88(5): 1613-1619.
[4]Umeki K,Yoshikawa K,Namioka T.Analysis of an updraft biomass gasifier with high temperature steam using a numerical model[J].Applied Energy, 2012, 90(1): 38-45.
[5]郭艳,王垚,魏飞,等.生物质快速裂解液化技术的研究进展[J].化工进展,2001,(8):13-17.
[6]武书彬,彭云云.TG-FTIR联用研究半纤维素的热裂解特性[J].化工进展,2009,28(8):1478-1484.
[7]彭云云.蔗渣半纤维素的化学结构及其热裂解特性研究[D].广州:华南理工大学,2006.
[8]刘朝,李豪杰,黄金保.木聚糖热解过程的分子动力学模拟[J].功能高分子学报,2010,23(9):291-296.
[9]谭洪.生物质热裂解机理试验研究[D].杭州:浙江大学,2005.
[10]王凤娟,黄峰,杨桂花,等.半纤维素对浆纸质量的影响[J].造纸科学与技术,2010,29(1):28-32.
[11]张智,刘朝,李豪杰,等.木聚糖单体热解机理的理论研究[J].化学学报,2011,69(9):2099-2107.
[12]董优雅.油菜籽粕生物质热解过程及产物特性研究[D].北京:北京化工大学,2011.
[13]刘军利.木质纤维类生物质定向热解行为研究[D].南京:中国林业科学研究院,2011.
[14]杨卿.麦草及其三种主要组分的热解规律[D].广州:华南理工大学,2010.
[15]胡亿明.木质生物质各组分热解过程和热力学特性研究[D].南京:中国林业科学研究院,2013.
[16]Bicout D,Field M.Quantum Mechanical Simulation Method for Studing Biological System(Les Houches Workship)[M].Berlin:Springer-Verlag,1995:1-21.
