葡萄糖基双子表面活性剂的制备与表征
2014-08-03闫顺杰杜斌斌杜山山杨宗锋丁交通牛瑞婷曹丹妮辛志荣
闫顺杰,杜斌斌,杜山山,杨宗锋,丁交通,牛瑞婷,曹丹妮,辛志荣
(烟台大学化学化工学院,山东 烟台 264005)
双子表面活性剂是一代新型的表面活性剂,其独特的二聚或多聚结构赋予了其更多的优良特性.相对于传统意义上的表面活性剂而言,双子表面活性剂具有更高的表面吸附性、较低的Krafft点、结构可控性以及良好的钙皂分散性能和复配效应,且在水溶液中易聚集成胶团[1-5],表现出pH响应性、胶束-囊泡可转化性等一些特殊的自组装行为[6-8].双子表面活性剂在三次采油[9]、药物运输[10]、基因工程[11-12]、新材料制备[13]等领域有着广泛的应用前景,这引起了人们的浓厚兴趣和极大关注.
糖基双子表面活性剂是一类以天然可再生的糖类作为原料的非离子表面活性剂[14].由于采用具有多元醇结构的糖类作为其亲水头基,糖基双子表面活性剂除了表现出表面活性高[15-16]、对皮肤和眼睛等组织器官温和无刺激作用、生物相容性好等特点外,还有着优良的生态学、毒理学性质和生物安全特性[17-19].在糖基双子表面活性剂的制备过程中,往往要对糖基体的非选择性基团进行相关的保护和脱保护处理[20-22],从而会造成合成路线繁杂,纯化困难以及产率较低;若采用选择性高的酶来催化制备糖基双子表面活性剂[23-25],也会面临着酶的种类单一,产物难以分离、成本较高等一系列问题.本研究直接以未保护的葡萄糖和烷基伯胺作为起始材料,首先在温和条件下合成了单头基的还原性葡萄糖醇中间体,再以乙二醇二缩水甘油醚为联接试剂制备了具有二聚结构的糖基双子表面活性剂.随后对产物的化学结构、表面张力以及起泡稳泡性能进行了表征,并在热力学稳定角度对糖基双子表面活性剂的吸附作用和胶束化作用进行阐释.
1 实验部分
1.1 试剂与仪器
葡萄糖,分析纯,Aladdin;正辛胺,分析纯,Aladdin;十二胺,分析纯,Aladdin;十六胺,GC,Aladdin;硼氢化钠,分析纯,上海展云化工有限公司;甲醇钠,分析纯,天津市光复精细化工研究所;乙二醇二缩水甘油醚,分析纯,东京化成工业株式会社.实验中其余试剂均为分析纯,未近一步纯化.
JC2000D1接触角测量仪,上海中晨数字技术设备有限公司;FTS135型FTIR傅里叶红外光谱仪,美国BioRad公司;Unity-400型核磁共振仪,美国Varian公司.
1.2 葡萄糖基双子表面活性剂的合成
将50 mmol葡萄糖和50 mmol 正辛胺加入到盛有100 mL甲醇的250 mL三颈瓶中,室温下搅拌24 h后,冰水浴冷却,然后加入54 mmol NaBH4,继续搅拌,直至没有气泡生成.向反应液中滴加浓盐酸(1 mol/L),调节pH值至1~2,此时体系有沉淀生成.反应液冰水浴中静置后抽滤,滤饼用少量的冰水和冰乙醇洗涤3次,真空干燥得到N-辛烷基葡萄糖醇盐酸盐.N-辛烷基葡萄糖醇盐酸盐在稍过量的甲醇/甲醇钠溶液中室温搅拌一天后升温回流.冷却,有白色沉淀析出,抽滤得到粗产物[19].粗产物在甲醇中重结晶3次,得到白色粉末状的单头基N-辛烷基葡萄糖醇表面活性剂(a).称取10 mmol N-辛烷基葡萄糖醇(a)、5 mmol乙二醇二缩水甘油醚置于盛有80 mL甲醇的100 mL三颈瓶中,在70 ℃水浴中搅拌反应24 h.减压蒸馏去除溶剂,真空干燥后得到N-辛烷基葡萄糖醇双子表面活性剂(A).合成路线见图1.
用类似的方法制备出单头基表面活性剂N-十二烷基葡萄糖醇(b),N-十六烷基葡萄糖醇(c),以及N-十二烷基葡萄糖醇双子表面活性剂(B)和N-十六烷基葡萄糖醇双子表面活性剂(C).
1.3 表面活性剂的表征
1.3.1 红外谱图分析 产物用KBr压片制样,利用FTS135型的傅里叶红外光谱仪(FTIR)进行测试,扫描范围400~4 000 cm-1,分辨率2 cm-1,扫描次数32次.
1.3.2 核磁谱图分析 以氘代甲醇为溶剂,TMS为内标物,采用Varian公司的Unity-400型核磁共振仪对产物(a),(b),(c),(A),(B),(C)进行测试.
1.3.3 表面张力测试 在室温(20 ℃)下,采用悬滴法测表面张力.配制一系列浓度梯度的不同表面活性剂溶液,利用JC2000D1接触角测量仪测定表面张力,每个浓度下的表面活性剂溶液的表面张力测3次,取平均值.
1.3.4 起泡性测试 根据GB/T7462—1994,采用改进的Ross-Miles法,对浓度为2.5 g/L的N-烷基葡萄糖醇双子表面活性剂的水溶液进行起泡性与稳泡性的测定.取10 mL表面活性剂溶液加入50 mL的具塞试管量筒中,剧烈晃动,以30 s时的泡沫高度表征其起泡能力,以300 s时的泡沫高度与30 s时的泡沫高度比值表征泡沫的稳定性.
2 结果与讨论
2.1 表面活性剂的红外谱图分析
2.1.1 单头基表面活性剂红外谱图分析 由图2可以看出,3 425 cm-1处为羟基O—H的分子内氢键的伸缩振动吸收峰,3 230 cm-1为分子间氢键O—H伸缩振动吸收峰,2 922 cm-1为甲基上的C—H对称伸缩振动的吸收峰,2 850 cm-1为亚甲基上的C—H对称伸缩振动的吸收峰,1 465 cm-1和1 434 cm-1处为亚甲基和甲基上的C—H弯曲振动吸收峰,1 250 cm-1为C—N键的伸缩振动吸收峰,1 050 cm-1和1 085 cm-1分别为伯醇和仲醇C—O的伸缩振动吸收峰,725 cm-1为长链—CH2—的面内摇摆振动吸收峰.
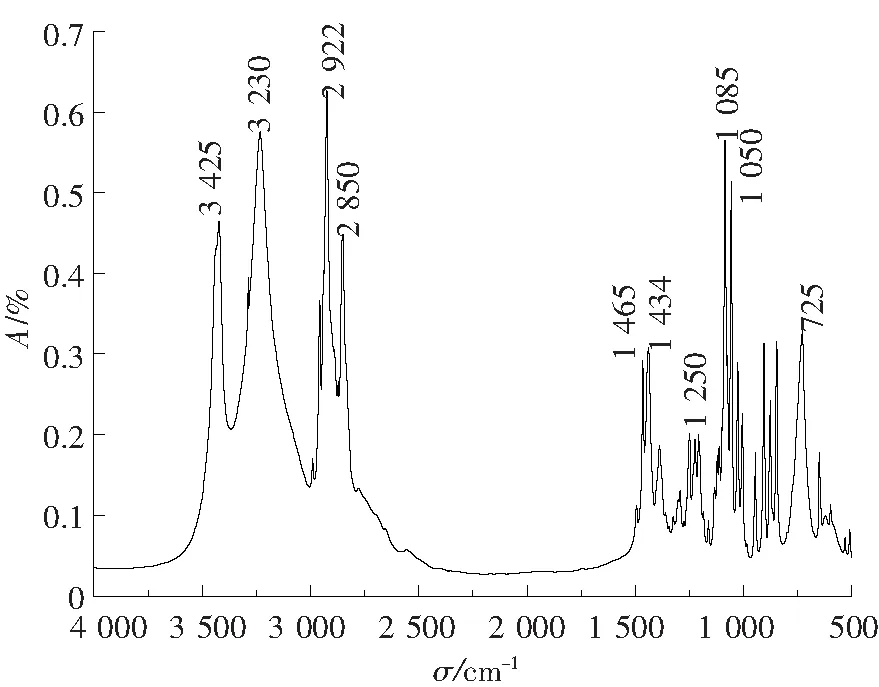
图2 N-辛烷基葡萄糖醇表面活性剂(a)的红外谱图
由于合成的N-烷基葡萄糖醇表面活性剂的结构相似,只是烷基链长度有所差别,所以产物N-辛烷基葡萄糖醇(a)、N-十二烷基葡萄糖醇(b)、N-十六烷基葡萄糖醇(c)的红外谱图类似.
2.1.2 双子表面活性剂红外谱图分析 由图3可以看出,3 420 cm-1处为羟基O—H的分子内氢键的伸缩振动吸收峰,3 230 cm-1为羟基分子间氢键伸缩振动吸收峰,2 925 cm-1为甲基上的C—H伸缩振动吸收峰,2 850 cm-1为亚甲基上的C—H伸缩振动吸收峰,1 460 cm-1和1 434 cm-1处为亚甲基和甲基上的C—H弯曲振动吸收峰,1 250 cm-1为C—N键的伸缩振动吸收峰,1 050 cm-1和1 085 cm-1分别为伯醇和仲醇C—O的伸缩振动吸收峰,723 cm-1为长链—CH2—的面内摇摆振动吸收峰.
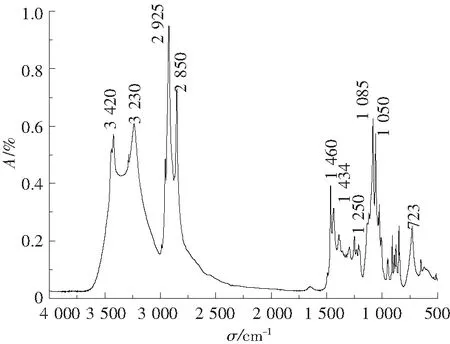
图3 N-辛烷基葡萄糖醇双子表面活性剂(A)的红外谱图
产物(B),(C)与(A)只是烷基链长度不同,其余结构相同,所以产物的红外谱图类似.
2.2 表面活性剂的核磁共振氢谱分析
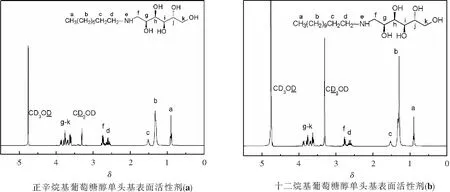
2.2.1 单头基表面活性剂核磁谱图分析 N-辛烷基葡萄糖醇(a)的化学位移(δ): 0.89(t, 3H, CH3),1.32(s, 10H, CH3(CH2)5),1.52(m, 2H, N-CH2CH2(CH2)5),2.52~2.67(m, 2H, N-CH2CH2(CH2)5),2.67~2.79(m, 2H, N-CH2CH2(OH)-),3.60~3.88(m, 6H, CH-OH 和-CH2-OH),4.75(s, 6H, OH和NH).其中,3.30和4.75为溶剂CD3OD的化学位移.
N-十二烷基葡萄糖醇表面活性剂(b)的化学位移(δ): 0.90(t, 3H,-CH3),1.30(s, 18H,-CH2),1.53(m, 2H, N-CH2CH2(CH2)9),2.55~2.70(m, 2H, N-CH2CH2(CH2)9),2.70~2.81(m, 2H, N-CH2CH2(OH)-),3.58~3.90(m, 6H, CH-OH 和-CH2-OH),4.77(s, 6H, OH和NH).
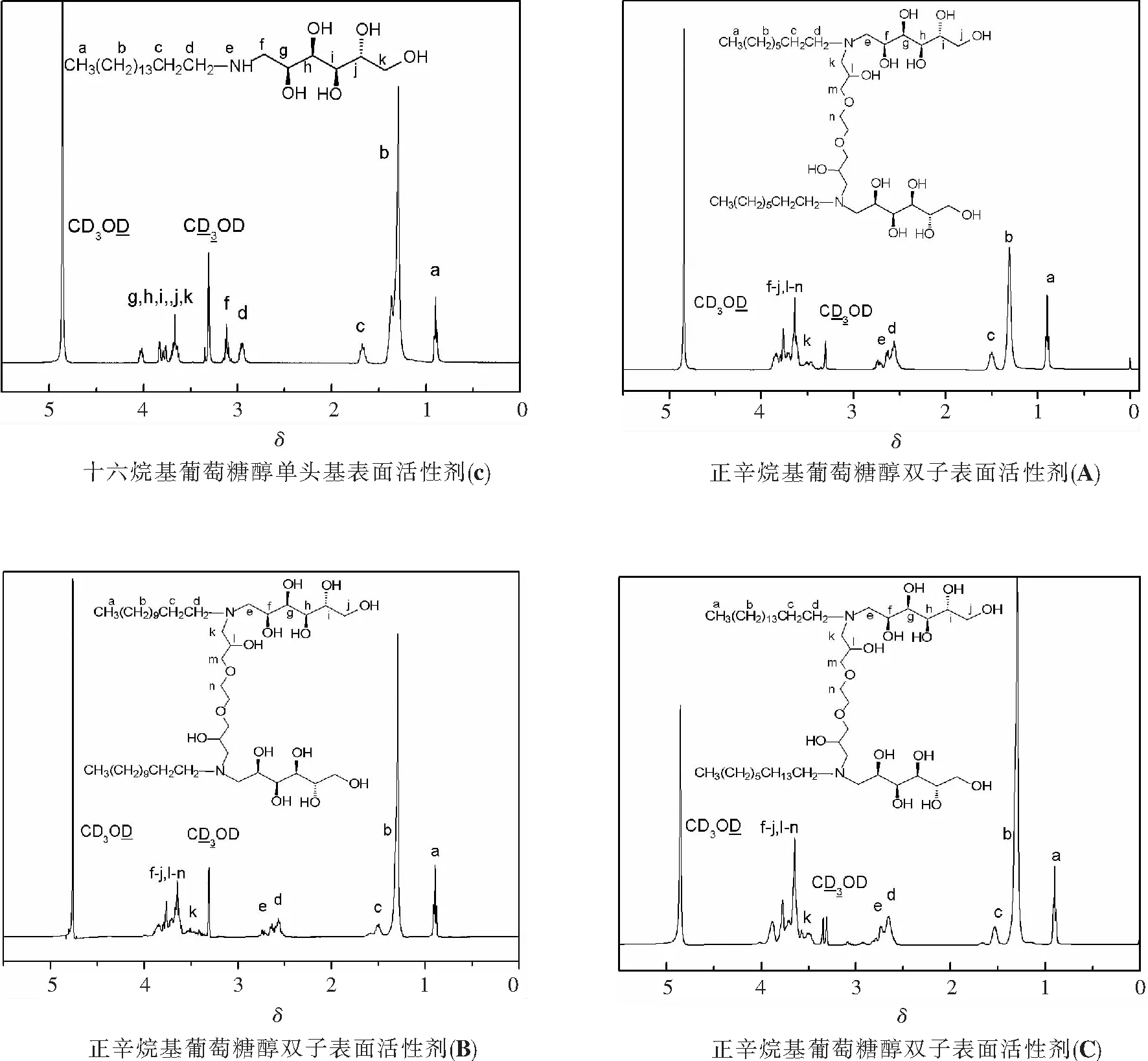
N-十六烷基葡萄糖醇表面活性剂(c)的化学位移(δ): 0.90(t, 3H,-CH3),1.29(s, 26H,-CH2),1.67(m, 2H, N-CH2CH2(CH2)13),2.92~3.01(m, 2H, N-CH2CH2(CH2)13),3.07~3.15(m, 2H, N-CH2CH2(OH)-),3.61~4.04(m, 6H, CH-OH 和-CH2-OH),4.85(s, 6H, OH和NH).
2.2.2 双子表面活性剂核磁谱图分析 N-辛烷基葡萄糖醇双子表面活性剂(A)的化学位移(δ): 0.88(t, 6H, CH3),1.32(s, 20H, CH3(CH2)5),1.50(s, 4H, N-CH2CH2(CH2)5),2.51~2.75(m, 8H, N-CH2CH2(CH2)5和N-CH2(CH2(OH))2),3.43~3.57(m, 4H, N-CH2CH(OH) CH2),3.61~3.87(m, 22H, CH-OH,-CH2-OH和CH2OCH2).其中,3.30和4.85为溶剂CD3OD的化学位移.
N-十二烷基葡萄糖醇双子表面活性剂(B)的化学位移(δ): 0.89(t, 6H,-CH3),1.29(s, 36H, CH3(CH2)9),1.52(s, 4H, N-CH2CH2(CH2)9),2.55~2.76(m, 8H, N-CH2CH2(CH2)9和N-CH2(CH2(OH))2),3.36~3.56(m, 4H, N-CH2CH(OH)CH2),3.58~3.90(m, 22H, CH-OH,-CH2-OH和CH2OCH2),4.77(m, 12H, OH和NH).
N-十六烷基葡萄糖醇双子表面活性剂(C)的化学位移(δ): 0.89(t, 6H,-CH3),1.29(s, 52H, CH3(CH2)13),1.53(s, 4H, N-CH2CH2(CH2)13),2.56~2.85(m, 8H, N-CH2CH2(CH2)13和N-CH2(CH2(OH))2),3.44~3.59(m, 4H, N-CH2CH(OH)CH2),3.60~4.06(m, 22H, CH-OH, -CH2-OH和CH2OCH2),4.85(m, 12H, OH和NH).
2.3 表面活性
2.3.1 单头基表面活性剂表面活性分析 图4为不同碳链长度的N-烷基葡萄糖醇单头基表面活性剂的表面张力浓度曲线.由图4可以看出,在较低浓度范围内,随着表面活性剂浓度的增加,体系的表面张力γ随之降低.当表面活性剂浓度超过其临界胶束浓度(CMC)后,体系的表面张力变化不明显.这是因为当表面活性剂形成胶束结构后,体系中的表面活性剂单体的浓度会维持在一个恒定的水平,表面张力也不会有明显变化.3种表面活性剂溶液的最低表面张力γmin随着表面活性剂烷基链长度的增长而变大,其中N-正辛烷基葡萄糖醇(a)的γmin为55.4 mN/m,而N-十六烷基葡萄糖醇(c)的γmin仅为65.6 mN/m.

图4 N-烷基葡萄糖醇表面活性剂的表面张力浓度曲线
表1是对单头基表面活性剂表面张力浓度曲线的测量结果.其中的表面活性剂在临界胶束浓度(CMC)时的溶液表面吸附量ΓCMC、每个吸附分子所占有的截面积ACMC、胶束化自由能ΔG°mic以及吸附自由能ΔG°ads分别依据公式(1)~(4)求得[26-27].公式中R值为8.314 J·mol-1K-1,NA为阿伏伽德罗常数,π是表面压(数值为纯水的γ0与表面活性剂饱和的γ之差),Cπ为表面压下表面活性剂溶液的摩尔浓度.
(1)

(2)

(3)
(4)
由表1数据看出,3种单头基表面活性剂(a)、(b)、(c)的CMC大小顺序为CMCa>CMCb>CMCc,其中N-十六烷基葡萄糖醇(c)的CMC值最小,说明在3种产物中N-十六烷基葡萄糖醇(c)更倾向于在液体相中聚集成胶束,而不是倾向于吸附在溶液表面;这也与表面活性剂(c)具有最小吸附量ΓCMC的计算结果一致.从整个体系的能量角度来看,产物(c)的胶束化自由能、ΔG°mic以及吸附自由能ΔG°ads分别小于产物(a)、(b),易于形成胶束和表面吸附.这是由于溶液中的水分子对拥有较长烷基尾链的表面活性剂有很强的排斥作用,从而产生较强的界面能.此时,表面活性剂分子将更多以聚集成胶束或者吸附在气液界面的方式来逃离水相,以降低整个体系的能量[4].相对于表面活性剂(a)和(b)而言,(c)的分子吸附量最小但是分子占据的截面积最大,可能是因为其拥有尾链(碳原子数为16)过长,柔性烷基链更多地以铺展或者盘旋扭曲的形态吸附在溶液表面(图5),从而造成ACMC的数值较大但吸附量ΓCMC较小[28].

表1 表面张力浓度曲线测量结果
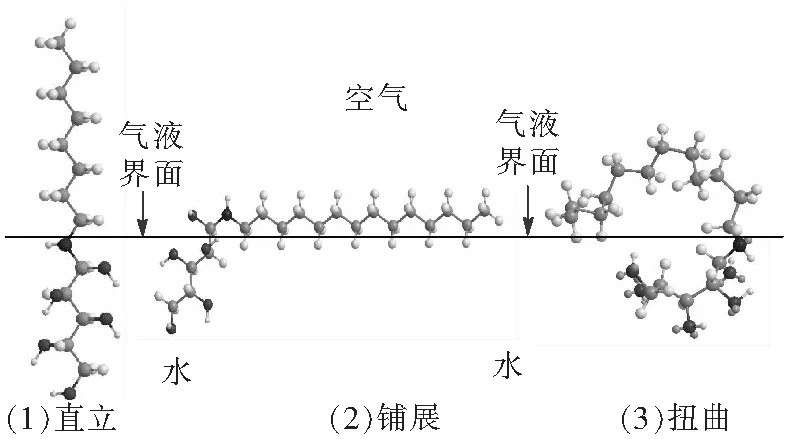
图5 表面活性剂分子在溶液表面的吸附形态
2.3.2 双子表面活性剂表面活性分析 图6为不同碳链长度的N-烷基葡萄糖醇双子表面活性剂的表面张力浓度曲线.由图6可以看出,葡萄糖基双子表面活性剂溶液的表面张力随浓度的增加急剧下降,当浓度达到CMC时,表面张力维持在一个基本不变的较低水平.葡萄糖基双子表面活性剂(A)、(B)、(C)的CMC值分别为0.26、0.07,0.45 mmol/L,能够保持在一个很低的范围内,说明葡萄糖基双子表面活性剂更易形成胶束,具有更高的表面活性.

图6 N-烷基葡萄糖醇双子表面活性剂水溶液的表面张力浓度曲线
表2是对双子表面活性剂表面张力浓度曲线的分析结果.表中C20表示溶液表面张力下降20 mN/m时需要的表面活性剂浓度,以此用来衡量表面活性剂降低表面张力的效率.以CMC/C20的比值来衡量表面活性剂在溶液表面吸附和在体相中胶束化两种趋势的相对大小,比值越大则意味着表面活性剂更倾向于吸附在溶液表面.由表2中数据可以看出,产物(A)、(B)的C20值明显小于产物(C),表现出良好的降低表面张力的效率.产物(A)的CMC/C20值略大,表明(A)易于吸附在气-液界面.但(A)的吸附量略小于(B)、(C),可能是因为分子排列疏松,不够紧密.
比较表1和表2发现,具有线性结构的单头基表面活性剂在水中的溶解性并不高,而二聚结构的表面活性剂较相应的单头基表面活性剂的溶解度大1个数量级左右,其CMC值比前者也有明显的降低.产物(A)、(B)比产物(a)、(b)的CMC值要低1~2个数量级.单头基表面活性剂溶液的最低表面张力γmin分别为55.4、61.7、65.6 mN/m,而双子表面活性剂可以将溶液的表面张力降低到33.0、33.2、38.6 mN/m.这表明,双子表面活性剂较传统的单头基表面活性而言,具有更高的表面张力降低能力.双子表面活性剂的胶束化自由能ΔG°mic以及吸附自由能ΔG°ads值低于单头基表面活性剂数值,表现为热力学支持过程[21].双子表面活性剂(C)的ACMC值比单头基表面活性剂(c)明显降低.出现这种情况,是因为单头基的N-烷基葡萄糖醇表面活性剂分子通过乙二醇二缩水甘油醚的联接后形成了二聚结构,从而通过化学键的作用,有效地拉紧了表面活性剂分子间的距离.双子表面活性剂头基联接紧密,有效降低了头基在水溶液中的吸附和聚集过程中的静电排斥和水化阻力;同时,联接链也拉近了疏水尾链的距离,从而增强了表面活性剂分子在自组织过程中的协同效应[29].乙二醇二缩水甘油醚作为柔性的联接链,可以弯向烷烃尾链,额外增加疏水部分的疏水效果.这就使葡萄糖基双子表面活性剂具有优异的表面活性和特殊的自组装行为.

表2 双子表面活性剂表面张力浓度曲线测量结果
2.4 起泡性
由图7可以看出,葡萄糖基双子表面活性剂(A)、(B)、(C)在30 s时泡沫高度分别为35、27、21 mL(起泡测试前的表面活性剂溶液用量为10 mL),表现出了良好的起泡能力.这是因为从能量的角度来看,体系的能量随着液体表面积的增加而增大.低的表面张力可以减少生成泡沫时做的功,有利于一定总表面积的泡沫形成[26],而糖基双子表面活性剂溶液具有低的表面张力,所以能够表现出较好的起泡能力.
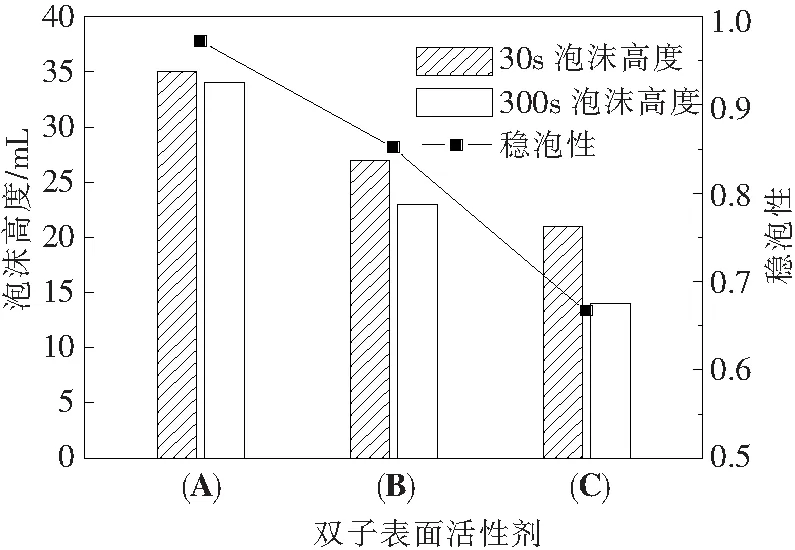
图7 N-烷基葡萄糖醇双子表面活性剂的起泡性和稳定性
产物(A)、(B)在300 s时泡沫高度分别为34、23 mL,泡沫比值分别为0.97和0.85.比值越高,说明表面活性剂的泡沫体积衰减的速率较慢,泡沫可以长时间的存在,从而体现出较好的稳定性.同时,泡沫稳定与否,和表面膜的强度有关.葡萄糖基双子表面活性剂的多羟基结构可使分子间形成大量氢键,相互作用增加,导致膜强度增加,从而使泡沫具有较好的稳定性[30-31].产物(C)虽然起泡性较好,但是泡沫的稳定性(0.66)差,不能长时间存在.这可能是因为产物(C)分子质量较大,在同一质量浓度(2.5 g/L)下溶液中的表面活性剂分子数略少,表面吸附分子排列的不够紧密、相互作用较弱,从而导致了溶液的表观粘度较小,表面膜的强度下降,最终影响泡沫的稳定性.
3 结 论
制备的烷基链长度为八碳、十二碳、十六碳的N-烷基葡萄糖醇双子表面活性剂(A)、(B)、(C)分别将水溶液的表面张力降低到33.0、33.2、38.6 mN/m.其临界胶束浓度分别为0.26、0.07、0.45 mmol/L,相对于传统表面活性剂要低1~2个数量级.这说明二聚结构的双子表面活性剂可以在联接链的作用下,有效地降低分子间的距离,表现出比传统线性表面活性剂更高的降低表面张力的能力和效率.葡萄糖醇双子表面活性剂(A)、(B)、(C)具有较好的起泡性.其中,(A)和(B)的泡沫可以长时间存在,稳定性好.
参考文献:
[1]赵剑曦. 新一代表面活性剂:Gemini[J].化学进展, 1999, 1(4): 348-357.
[2]Sakai K, Sakai H, Abe M. Recent advances in gemini surfactants: Oleic acid-based gemini surfactants and polymerizable gemini surfactants[J]. Journal of Oleo Science, 2011, 60(4):159-163.
[3]Sekhon B S. Gemini (dimeric) surfactants [J]. Resonance, 2004: 42-49.
[4]赵剑曦. Gemini表面活性剂的研究与发展方向[J].研发前沿, 2008: 14-19.
[5]Kuliszewska E. Gemini surfactants: New class of surface actives agents [J]. Przemysl Chemiczny, 2009, 88(11): 1229-1233.
[6]Siddiqui U S, Aslam J, Ansari W H, et al. Micellization and aggregation behavior of a series of cationic gemini surfactants (m-s-m type) on their interaction with a biodegradable sugar-based surfactant (octyl-beta-D-glucopyranoside) [J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2013, 421:164-172.
[7]Luc W, Marco S, Gooitzen D, et al. Transfection mediated by pH-sensitive sugar-based gemini surfactants; potential for in vivo gene therapy applications [J]. Journal of Molecular Medicine, 2006, 84: 774-784.
[8]Markus J, Jan B F N E. Novel sugar-based gemini surfactants: Aggregation properties in aqueous solution[J]. Journal of Physical Organic Chemistry, 2004, 17: 934-944.
[9]Guo Yongjun, Liu Jianxin, Zhang Xinming, et al. Solution property investigation of combination flooding systems consisting of gemini-non-ionic mixed surfactant and hydrophobically associating polyacrylamide for enhanced oil recovery [J]. Energy & Fuels, 2012, 26(4): 2116-2123.
[10]Kumar M, Jinturkar K, Yadav M R, et al. Gemini amphiphiles: A novel class of nonviral gene delivery vectors[J]. Critical Reviews in Therapeutic Drug Carrier Systems, 2010, 27(3): 237-278.
[11]Mohammed S W, Michel D, El-Aneed A, et al. Development of lyophilized gemini surfactant-based gene delivery systems: Influence of lyophilization on the structure, activity and stability of the Lipoplexes [J]. Journal of Pharmacy and Pharmaceutical Sciences, 2012, 15(4): 548-567.
[12]Munoz U M, Misra SK, Barran B A L, et al. How does the spacer length of cationic gemini lipids influence the lipoplex formation with plasmid DNA?: Physicochemical and biochemical characterizations and their relevance in gene therapy [J]. Biomacromolecules, 2012, 13(12): 3926-3937.
[13]Chunping Song, Dongqing Wu, Fan Zhang, et al. Gemini surfactant assisted synthesis of two-dimensional metal nanoparticles/graphene composites [J]. Chemical Communications, 2012, 48(15): 2119-2121.
[14]闫顺杰,杨宗峰,杜斌斌,等. 糖基双子表面活性剂的研究进展 [J]. 日用化学工业, 2013, 43(3): 217-223.
[15]Warwel S, Bruse F, Schler H. Glucamine-based gemini surfactants I: Gemini surfactants from long chainN-alkyl glucamines andα,ω-diepoxides [J]. Journal of Surfactants and Detergents, 2004, 7(2): 181-186.
[16]Warwel S, Bruse F, Schler H. Glucamine-based gemini surfactants II: Gemini surfactants from long chainN-alkyl glucamines and epoxy resins [J]. Journal of Surfactants and Detergents, 2004, 7(2): 187-193.
[17]Sakai K, Tamura M, Umezawa S, et al. Adsorption characteristics of sugar-based monomeric and gemini surfactants at the silica/aqueous solution interface [J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2008, 328(1-3):100-106.
[18]Tyagi P, Tyagi R. Synthesis, structural properties and applications of gemini surfactants: A review [J]. Tenside Surfactants Detergents, 2009, 46(6):373-382.
[19]Urszula L, Kazimiera A W, Irena M, et al. Novel glucose-derived gemini surfactants with a 1,1′-ethylenebisurea spacer: Preparation, thermotropic behavior, and biological properties [J]. Journal of Surfactants and Detergents, 2006, 9(2): 115-124.
[20]Mariano J L C, JoséK, Alicia F C. Structure-properties relationship of dimeric surfactants from butyl glucosides [J]. Molecules, 2000, 5: 608-609.
[21]Mariano J L C, JoséK, Alicia F C. Ecologically safe alkyl glucoside-based gemini surfactants [J]. Arkivoc, 2005, 7: 253-267.
[22]Mariano J L C, Alicia F C, JoséK. Synthesis and interfacial properties of sugar-based surfactants composed of Homo-and Heterodimers [J]. Journal of Surfactants and Detergents, 2006, 9(3): 279-286.
[23]Piera E, Infante M R, Clapes P. Chemo-enzymatic synthesis of arginine-based gemini surfactants [J]. Biotechnology and Bioengineering, 2000(3): 323-331.
[24]Chunli Gao, Michael J W, Evgeny N V. Enzymatic synthesis of dimeric and trimeric sugar-fatty acid esters [J]. Enzyme and Microbial Technology, 1999, 25: 264-270.
[25]Chunli Gao, Anna M F, Michael J, et al. Regioselective synthesis of dimeric (gemini) and trimeric sugar-based surfactants [J]. Journal of Surfactants and Detergents, 1999, 2(3): 293-302.
[26]赵国玺,朱步瑶. 表面活性剂作用原理[M].北京:中国轻工业出版社, 2003: 225-300.
[27]Fu Han, Gaoyong Zhang. New family of gemini surfactants with glucosamide-based trisiloxane [J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2004,237: 79-85.
[28]Menger F M, Keiper J S. Gemini surfactants [J]. Angewandte Chemie International Edition, 2000, 39(11): 1906-1920.
[29]游毅,邓永淑,李二军,等. Gemini表面活性剂烷烃尾链在吸附和聚集过程中的疏水协同效应 [J]. 物理化学学报, 2010,26(8):2200-2204.
[30]Peter S P, Marcus P, Per C, et al. Surface properties of surfactants derived from natural products. Part 2: Structure/property relationships-foaming, dispersion, and wetting [J]. Journal of Surfactants and Detergents, 2004, 7(2):161-167.
[31]赵剑曦.Gemini高效稳泡剂[J]. 精细与专用化学品, 2011, 19(6): 11-14.
附录A: 核磁共振谱图