玻璃体腔穿刺注射雷珠单抗与激光光凝治疗糖尿病性黄斑水肿的疗效与安全性的Meta分析
2014-07-14易湘龙
高 雯, 易湘龙
(新疆医科大学第一附属医院眼科, 乌鲁木齐 830054)
糖尿病性视网膜病变(diabetic retinopathy,DR)是指糖尿病患者因高血糖致全身各组织器官的微血管发生病变、毛细血管的周细胞坏死,随后内皮细胞亦变薄,内屏障功能受损,血管内的液体成分由管内渗出到组织中,造成视网膜病变和功能障碍。糖尿病可致眼部各组织发生病变,而视网膜病变则是导致糖尿病眼病不可逆盲的最严重的并发症。其中糖尿病黄斑水肿(diabetic macular edema,DME)则是糖尿病患者视力下降的首要原因[1]。
目前国内外采取多种方式治疗这一致盲的主要疾病。虽然激光治疗是目前糖尿病性黄斑水肿的标准治疗方法,但是此方法只能帮助减缓视力进一步丧失和稳定现有视力,却不能恢复已经丧失的视力[2]。此外,对于糖尿病性黄斑水肿的治疗方法还包括糖皮质激素、蛋白激酶C抑制剂、肿瘤坏死因子α等药物治疗。近年来,随着各种药物研究的进展和激光光凝术的改革,对于DME的治疗方式趋于多样化,血管内皮生长因子(vascular endothelial growth factor,VEGF)抑制剂药物的使用也越来越受到重视[2]。对于以往主导治疗的激光光凝术,抗VEGF类的药物优势也愈加明显[3]。国内外对于DME的激光和药物治疗进行了大量的临床试验,本研究通过对比激光光凝,尤其是格栅样光凝治疗与玻璃体腔内注射雷珠单抗(lucentis)治疗DME的疗效及其安全性进行Meta分析,以对比2种方案对于不同程度的糖尿病黄斑水肿的优势及劣势,为指导临床治疗提供依据。
1 资料与方法
1.1研究的入选标准研究的类型:(1)RCT无论是否采用盲法;(2)发表日期1997年1月1日-2014年1月31日;(3)随访至少6个月。患者的纳入标准:经过内分泌科明确诊断为糖尿病,并且经过眼底荧光造影(FFA)或者光学相干断层扫描(OCT)确诊为黄斑水肿的患者。排除标准:(1)其他原因引起的黄斑水肿者;(2)激光治疗组采用黄斑区局灶性激光光凝者;(3)数据不全、无法提供原始数据及重复发表的研究。3项中符合1项者即排除。干预的措施:单独行玻璃体腔穿刺注射雷珠单抗(lucentis)加假激光治疗或者单独行视网膜激光光凝(主要是格栅样光凝)加假玻璃体腔注射治疗;排除6个月内行2种或2种以上治疗方式的病例。
1.2结果指标的测定(1)视力的变化:所有视力均转换成术前最佳矫正视力(best corrected visual acuity,BCVA),视力提高的标准为提高美国糖尿病视网膜病变早期治疗研究组(early treatment diabetic retinopathy study, ETDRS)提供的视力表提高3行或者3行以上;视力不变的标准为ETDRS视力不变或者在3行内;视力下降的标准为EDTRS视力降低3行或者3行以上。(2)黄斑水肿的变化:测量黄斑中心凹厚度(CMT),观察临床眼底检查、FFA或者OCT检查。(3)手术后的并发症:结膜出血、眼痛、眼充血、眼压升高、高血压、恶心、充血性心脏衰竭等。
1.3检索策略(1) Pubmed(1966年-2014年1月):检索地址为:http://www.ncbi.nlm.nih.gov/pubmed/advanced。检索策略:①“diabetic macular edema”OR“diabetic macularoedema”AND“treatment”;②“diabetic macular edema”OR“diabetic macular oedema”AND“lucentis”OR“Ranibizumab”;③“diabetic macular edema”OR“diabetic macular oedema” AND“photocoagulation”OR“laser”。(2) Embase(1966年-2014年1月):检索地址http://embase.com。检索策略同(1)。(3) Cochrane对照试验登记中心(Cochrane Central Register of Controlled Trials,CCRCT)(2014年1月):检索网址:http://gateway.ovid.com。检索策略同(1)。(4) 中国生物医学文献数据库(CBM)(2014年):检索地址http://202.116.108.3/cbmbin。检索策略:①“糖尿病性黄斑水肿”AND“治疗”;②“糖尿病性黄斑水肿”AND“雷珠单抗”OR“lucentis”OR“Ranibizumab”;③“糖尿病性黄斑水肿”AND“激光”。(5)中国期刊网全文数据库(CNKI)(2014年):检索网址:http://202.205.11.135。检索策略同(4)。(6)中国科技期刊全文数据库(VIP)(2014年):检索网址:http://202.116.140.1。检索策略同(4)。
1.4论文筛选将上述数据搜索的摘要结果以文本形式导入Endnote X7软件中,限定作者、发表时间及论文题目为条件,去除重复的数据进行初步筛选,选出可入选的文章,通过网络及图书馆检索获得全文,再根据通读全文,将符合纳入标准的文章入选,将不符合纳入条件的排除。
1.5资料的收集分析对符合纳入条件的全文,提取数据用Excel2007制表,主要提取内容如下:(1)研究对象:研究的眼数、年龄、性别、纳入标准。(2)干预方法:玻璃体腔内穿刺注药术、视网膜激光光凝术。(3)视力:视力检查的方法、术前平均视力、术后平均视力、术前最佳矫正视力。(4)黄斑水肿:术前黄斑中心凹视网膜厚度、术后黄斑中心凹视网膜厚度。(5)其他:研究设计的方法学、随访时间、术后并发症、对照组设计类型。采用Review Manager 5.2软件进行统计学分析。
1.5.1 异质性检验 在进行Meta分析之前,对需要合并的数据进行异质性分析,以每篇文章的样本含量多少作为权重,计算出加权均数及加权方差后,拟定各研究总体的效应值相同,即服从χ2分布。以P=0.05为显著水平,决定进行合并的模型。若异质性检验结果P>0.05,可认为组间异质性较小,用固定效应模型;若P<0.05,则可认为组间异质性较大,采用随机效应模型[4]。
1.5.2 效应尺度的计算 对于计数资料选择优势比(odds ratio,OR)反映效应尺度,对于计量资科采用平均差异(mean difference,MD)反映效应尺度。根据异质性检验的结果决定合并的效应模型,再进行效应尺度的合并,判断治疗差异有无统计学意义,同时计算合并的OR或MD的95%可信区间。
2 结果
2.1检索结果初检出282篇文献,去除重复文献192篇,通过阅读题目和摘要排除不符文献173篇,初筛出文献19篇。阅读19篇文献的全文,排除1篇横断面研究、4篇玻璃体腔穿刺注药并同时行激光治疗的文献、7篇玻璃体注药后再延期行激光治疗的RCT文献、1篇原研究延期观察的文献、1篇安慰剂对照的RCT文献,最终纳入5篇RCT文献[2,5-8]。其中,玻璃体腔注射雷珠单抗组305例305只眼,激光光凝组289例289只眼。5篇文献均为随机对照试验,见表1、2。
2.2结果分析
2.2.1 视力变化的分析 5组试验中均报道了治疗前后视力及黄斑中心凹厚度的改变,但因喻娟[7]研究中样本量较小,阳性率较大,不能明确显示完全随机对照,故评定为质量等级较低,不加入合并分析。其余4组数据[2,5-6,8]中,不存在组间异质性(I2=24%,P=0.27>0.05),采用固定效应模型进行分析。随访6个月时,视网膜激光光凝组与玻璃体腔穿刺注射雷珠单抗组比较,视力的改变差异具有统计学意义[95%CI(0.22,0.47),z=5.84(P<0.000 1)](图1),即玻璃体腔穿刺注射雷珠单抗对于视力的提高比视网膜激光光凝更加明显。
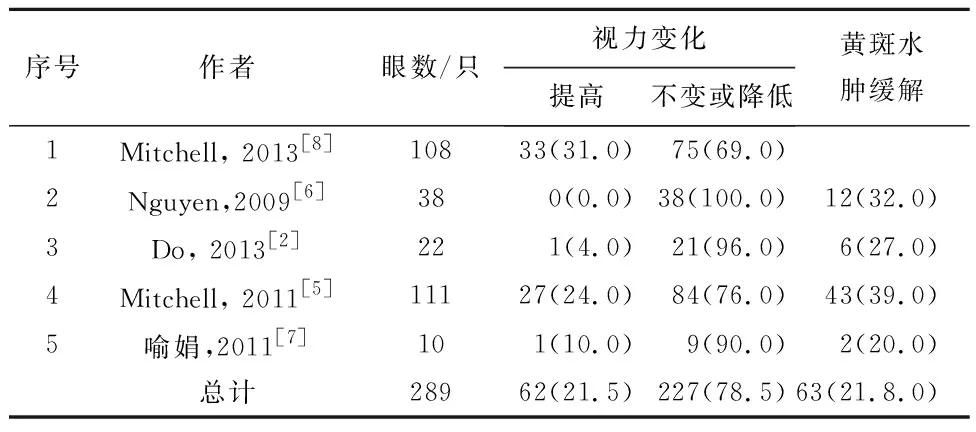
表1 视网膜激光光凝治疗糖尿病黄斑水肿的视力及黄斑水肿变化情况/例(%)
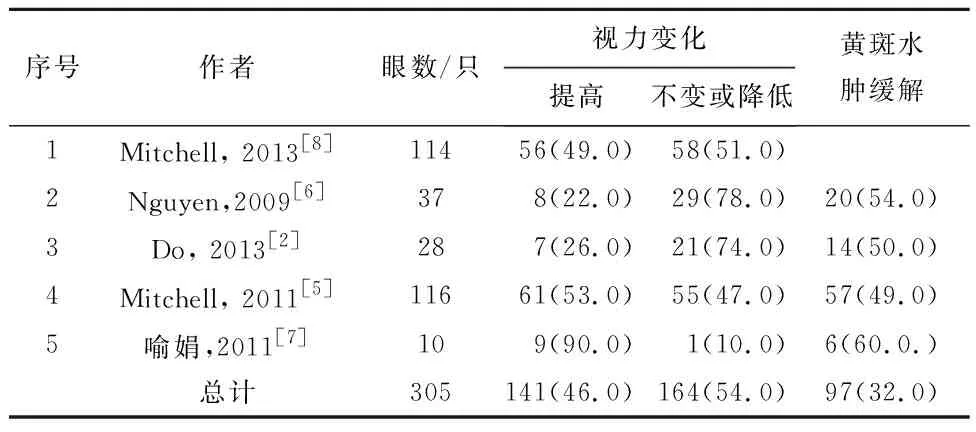
表2 玻璃体腔穿刺注射雷珠单抗治疗糖尿病黄斑水肿的视力及黄斑水肿变化情况列表/例(%)
2.2.2 黄斑中心凹厚度变化的分析 5组数据中,Mitchell等[8]的研究中未对治疗前后的CMT进行具体描述,故在分析治疗对于CMT的影响时剔除此项研究。喻娟[7]研究中仍由于样本量较小,产生的偏倚较大,对此不进行合并分析。另外3组研究[2,5-6],对治疗前后CMT进行了很好地比较,组间不存在异质性(I2=0%,P=0.52>0.05),采用固定效应模型进行分析。根据分析结果可以看出,随访6个月期间,玻璃体腔穿刺注射雷珠单抗组与视网膜激光光凝组比较,黄斑中心凹厚度的改变比较差异具有统计学意义[95%CI(0.36,0.84),z=2.77(P=0.006)](图2),即玻璃体腔穿刺注射雷珠单抗对于黄斑中心水肿的减轻较视网膜激光光凝更加明显。
2.2.3 术后并发症的分析 Mitchell等[8]以及Do等[2]研究中,未针对并发症进行具体描述。Nguyen等[6]报道,在玻璃体腔穿刺注射雷珠单抗治疗组中出现1例玻璃体腔出血反应,在视网膜激光光凝组中出现4例玻璃体腔出血反应及1例黄斑区水肿加重并玻璃体腔轻度出血。
Mitchell等[5]研究中,玻璃体腔穿刺注射雷珠单抗组115例中出现的不良反应:6例(5.2%)血栓栓塞事件,2例(1.7%)心绞痛,2例(1.7%)肺栓塞,1例(0.9%)脑血管意外,1例(0.9%)心肌梗死,9例(7.8%)高血压,1例(0.9%)非球内出血,1例(0.9%)鼻出血,1例(0.9%)蛋白尿。视网膜激光光凝组110例中出现的不良反应:1例(0.9%)血栓栓塞事件,1例(0.9%)肺栓塞,9例(7.8%)高血压,1例(0.9%)非球内出血,1例(0.9%)鼻出血。喻娟[7]研究中,玻璃体腔穿刺注射雷珠单抗组术后发生结膜下出血2例,其余并发症如注药引起的白内障、感染性眼内炎、视网膜脱离等均未出现。
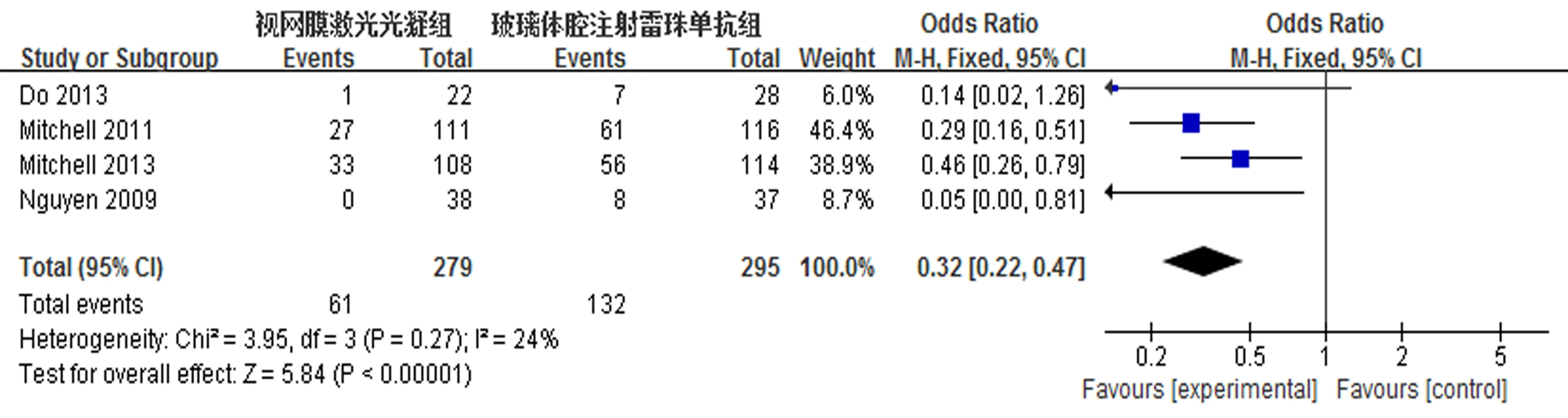
图1 视网膜激光光凝与玻璃体腔穿刺注射雷珠单抗后BCVA比较的meta分析
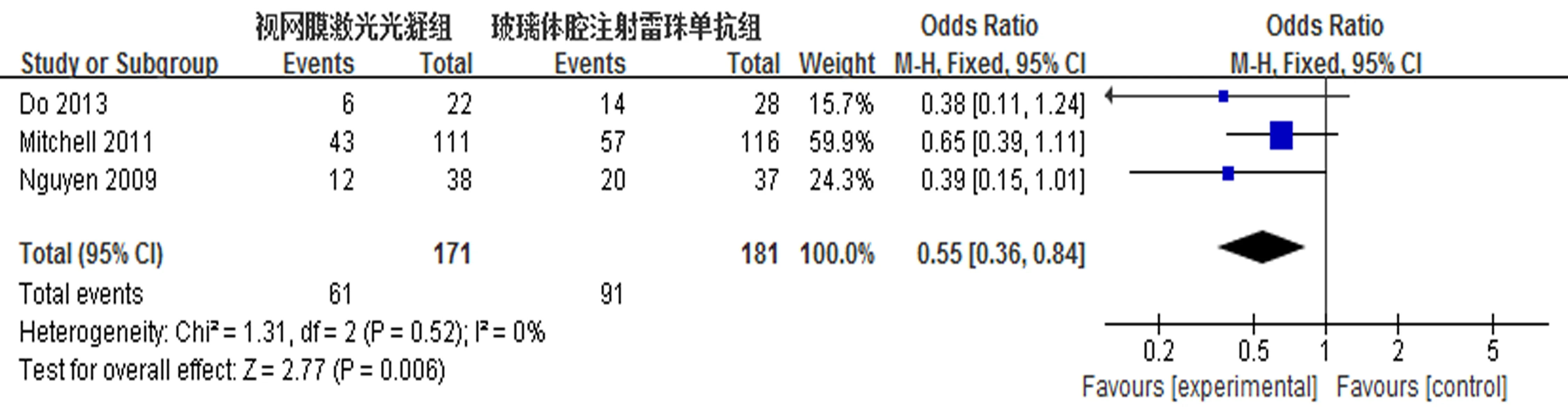
图2 视网膜激光光凝与玻璃体腔穿刺注射雷珠单抗后CMT比较的meta分析
3 讨论
糖尿病性视网膜病变(DR )是导致失明的全球人口主要原因之一[9]。研究表明,有10%~25%的糖尿病患者存在黄斑水肿[10],对于并发有严重的糖尿病视网膜病变的人群中,糖尿病黄斑水肿的患者比例更高[11]。血管渗漏、血管生成和神经元变性是DR的主要特征[12]。目前有效的干预措施,包括DR治疗系统性风险因素,如升高血糖、血压和血脂异常[13]。眼部治疗包括血管内皮生长因子A ( VEGF-A )抑制剂、激光光凝和手术治疗[14]。齐慧君等[15]通过对纳入研究的分析,认为激光光凝术对于糖尿病性黄斑水肿的治疗仍具有非常显著的疗效,但是也因激光治疗本身的限制性,激光斑随时间延长进一步使视网膜萎缩灶扩大,激光治疗对于视力改变不能增加,反而会有下降的可能。目前抗VEGF治疗已经成为一线治疗糖尿病性黄斑水肿( DME)导致的视力下降的主要方法[16]。为了客观评价单纯注射雷珠单抗和激光治疗的疗效及安全性,本研究选择了国内外公认的数据库进行检索,结果随访6个月,玻璃体腔穿刺注射雷珠单抗和视网膜激光光凝治疗糖尿病性黄斑水肿相比较,BCVA提高的字母数以及CMT差异均有统计学意义。
本研究存在的局限性:(1)纳入研究的数量及观察的眼数均较少;(2)纳入时忽略患者本身晶状体情况,及其对术后高眼压的评估;(3)纳入研究中的混杂因素较多,如糖尿病黄斑水肿类型、糖尿病的病程、激光光凝参数、注药间隔、研究之前患者的治疗情况等。(4)纳入研究中均未对分配隐藏做出明确解释,未对随机方法进行阐述,研究中患者的失访或退出,造成不完整数据偏倚的高度可能。(5)纳入研究的漏斗图形分布趋势不明显,不能确定是否有发表性偏倚。
本研究通过严格的纳入及排除标准,筛检出5篇随机对照试验,对目前最常用于治疗糖尿病性黄斑水肿的视网膜激光光凝术及玻璃体腔穿刺注射雷珠单抗的疗效及安全性进行Meta分析。研究结果表明,随访6个月的时间,玻璃体腔穿刺注射雷珠单抗组(共305只眼)的术后视力的提高及黄斑水肿的缓解均明显高于视网膜激光光凝组(共289只眼),而两组术后并发症无明显差异。
糖尿病性黄斑水肿的治疗方法较多,激光光凝术一直作为最有效的治疗方案用于临床治疗,但是近年来随着对于药物的不断研究,新兴的多种药物中,抗VEGF的雷珠单抗的疗效逐渐被认可,根据目前已行的临床试验中得出,在6个月随访期间,雷珠单抗的疗效显著,但是因为随访时间较短,研究例数较少,对于雷珠单抗及激光光凝的疗效及安全性仍需大量的临床试验进一步证明,对于即将进行的临床试验中,应延长随访时限进一步观察。此外,对于雷珠单抗的剂量、注射的时间和激光光凝术间隔时间都需要进一步试验来证明。
参考文献:
[1] 杨晓璐,邹海东,许迅,等.糖尿病黄斑水肿患病率调查及相关因素分析[J].上海交通大学学报:医学版,2012,32:160-167.
[2] Do DV,Nguyen QD,Boyer D,et al.One-year outcomes of the DA VlNCl study of VEGF Trap-Eye in eyes with diabetic macular edema[J].Ophthalmology,2013,119:1658-1665.
[4] Martin DF, Maguire MG, Fine SL, et al. Ranibizumab and bevacizumab for treatment of neovascular age-related macular degeneration[J].Ophthalmology, 2012,118(10):1706-1712.
[5] Mitchell P, Bandello F, Schmidt-Erfurth U. et al. The RESTORE study:ranibizumab monotherapy or combined with laser versus laser monotherapy for diabetic macular edema[J].Ophthalmology,2011,117:615-625.
[6] Nguyen QD, Shah SM, Khwaja AA, et al. READ-2 Study Group:Two-year outcomes of the ranibizumab for edema of the mAcula in diabetes (READ2) study[J].Ophthalmology,2009,111:2146-2151.
[7] 喻娟. 玻璃体腔注射Lucentis治疗糖尿病性黄斑水肿的临床观察[D].湖南省长沙市:中南大学,2011:1-69.
[8] Mitchell P,Bressler N,Tolley K,et a1.Patient-reported visual function outcomes improve after Ranibizumab treatment in patients with vision impairment due to diabetic macular edema[J].Ophthalmology,2013,121(10):1339-1347.
[9] Virtej A, Loes S, Iden O, et al.Vascular endothelial growth factors andomize in normal human dental pulp: a study of gene and protein expression[J]. Eur J Oral Sci,2013,121(2):92-100.
[10] Sander B,Best J ,Johansen S,et al.Fluorescei n transport through the blood-Cueous and blood-retinal barriers In diabetic macular edema[J].Curr Eye Res,2003,27(4):247-252 .
[11] Gallego-Pinazo R,Suelves-Cogollos AM,Dolz-Marcor,,et a1.Macular laser photocoagulation guided by spectral domain optical coherence tomography versus fluorescein angiography for diabetic macular edema[J].Clin Ophthalmol,2011,5:613-617.
[12] Yang W,Lu J,Weng J,et al.China National Diabetes and Metabolic Disorders Study Group.Prevalence of diabetes among men and women in China[J].N Eng J Med,2010,362:1090-1091.
[13] Funatsu H,Yamashita H,Ikeda T, et al. Angiotensin II and vascular endothelial growt h factor in the vitreous fluid of patients with diabetic macular edema and at her reti nal disorders[J]. Am J Ophthalmol ,2002 ,133(4):537-543.
[14] Early Treatment Diabetic Retinopathy Study Research Group.Photocoagulation for diabetic macular edema,early treatment diabetic retinopathy study report number 1[J].Arch Ophthalmol,1985,103:1796-1806.
[15] 齐慧君,黎晓新.不同分期糖尿病视网膜病变激光治疗预后分析[J].中国实用眼科杂志,2004,22(10):801-803.
[16] Lim JW, Lee HK, Shin MC. Comparison of intravitreal bevacizumab alone or combined with triamcinolone versus triamcinolone in diabetic macular edema: A randomized clinical trial[J]. Ophthalmologica,2012,227(2):100-106.
