碎裂QRS波群可以评价左心室致密化不全性心肌病患者的预后
2014-07-11翟正芹唐闽宁晓辉陈柯萍华伟沙晶张澍
翟正芹 唐闽 宁晓辉 陈柯萍 华伟 沙晶 张澍
• 论著 •
碎裂QRS波群可以评价左心室致密化不全性心肌病患者的预后
翟正芹 唐闽 宁晓辉 陈柯萍 华伟 沙晶 张澍
目的 碎裂QRS波群(fQRS)与多种心脏疾病患者的预后相关。然而,还未有fQRS与左心室致密化不全性心肌病(LVNC)患者预后相关的研究。在不同研究中,LVNC患者的预后有很大差异,且缺乏简单可行的用于评价预后的指标。本研究旨在评估fQRS用于评价LVNC患者预后的价值。方法 回顾性分析64例LVNC患者。窄碎裂QRS波群(f-nQRS):在至少2个相邻心电图导联的R波或S波上出现1个或多个切迹,且QRS波群时限<120 ms;宽碎裂QRS波群(f-wQRS):在至少2个相邻心电图导联的R波或S波上出现2个以上切迹,且QRS波群时限>120 ms。结果 64例患者中,分别有24例(38%)患者的心电图呈现f-nQRS,7例(11%)呈现f-wQRS。在随访期间,13例患者死亡,7例患者接受了心脏移植手术。Kaplan-Meier分析表明:f-nQRS组患者的生存率显著低于非f-nQRS组患者的生存率(P=0.005)。同样,f-wQRS组患者的生存率也明显低于非f-wQRS组患者的生存率(P=0.02)。多因素分析表明:f-nQRS是预测LVNC患者全因死亡率的1个独立指标(HR:5.33;P=0.045)。结论 f-nQRS对于评价LVNC患者的预后具有重要价值,且可能提供1个有效方法用于对患者进行危险度分层。
冠状动脉;急性心肌梗塞;PCI;心室颤动
[ Abstract ] Objective Fragmented QRS complexes (fQRS) were proven to be associated with the prognosis of several heart diseases. However, no data is available regarding fQRS in left ventricular noncompaction cardiomyopathy (LVNC), in which the outcome varies greatly and a simple yet practicable prognostic predictor is needed. The purpose of this study was to determine the prognostic value of fQRS in LVNC patients. Methods Sixty-four LVNC patients were evaluated. Fragmented narrow QRS (f-nQRS) included single or multiple notches in the R or S wave in at least 2 contiguous electrocardiogram (ECG) leads and QRS duration <120 ms, fragmented wide QRS (f-wQRS) included more than 2 notches and QRS duration>120 ms. Results f-nQRS and f-wQRS was present in 24 (38%) and 7 (11%) patients respectively. During follow-up, 13 patients died and 7 patients underwent heart transplantation. Kaplan-Meier analysis revealed that compared with the non-f-nQRS group, the f-nQRS group associated with a significantly lower survival (P=0.005). The f-wQRS group also demonstrated a substantially lower survival as compared with the non-f-wQRS group (P=0.02). Multivariate analysis indicated fnQRS was an independent predictor of all-cause mortality (HR: 5.33; P=0.045). Conclusions In LVNC patients, the presence of f-nQRS has significant prognostic value and may provide a valid method of risk stratification.
[ Key words ] coronary artery; PCI; ventricular fibrillation; Acute Myocardial Infarction. ST-Elevation Myocardial Infarction
左心室致密化不全性疾病(LVNC)是一种较为罕见的心脏病[1-6]。LVNC患者以左心室肌小梁异常粗大、小梁间隙深陷,增厚心肌可分为2个不同层次(薄的致密化层和厚的未致密化层)为特征[1]。在不同研究中,LVNC患者的预后有很大差异,LVNC患者在随访期间的死亡率为2%~47%[6-8]。
碎裂QRS波群(fQRS)是近年来引起广泛关注的无创性心电诊断指标,它定义为在12导联静息心电图呈现不同类型RSR'波且出现切迹的QRS波群[9-18]。现已证实:fQRS不仅可作为评价冠状动脉疾病(CAD)[11-15]、扩张性心肌病(DCM)[13]及Brugada综合征的一项预测指标,还可作为致心律失常型右室心肌病的一项标志物(AVRC)[18]。然而,还未有分析fQRS与LVNC患者预后相关性的研究。本研究旨在调查LVNC患者心电图呈现fQRS的频率,评估fQRS对于评价LVNC患者预后的重要性。
1 方法
1.1 研究人群 本研究回顾性分析自2001年7月至2009年6月在阜外医院被诊断为LVNC的患者。对所有患者的病史、临床表现和检查结果进行评估。排除合并其他已知的先天性和获得性心脏病的患者。
1.2 诊断标准 通过二维和多普勒超声心动图检查对患者进行诊断。利用二维超声心动图检查测量左室舒张末期直径(LVEDD),利用二维双平面改良Simpson方法测量左室射血分数(LVEF)。分析标准如下:①心肌呈现典型的2层结构即:外层为薄的致密化层(心外膜),内层为厚的未致密化层(心内膜)(在收缩末期,未致密化的心内膜层与致密化的心内膜层厚度的最大比值>2,具有特征性);②主要异常心肌节段的部位[未致密化心肌主要(>80%)位于左室心尖部及下壁和侧壁的左室中段];③彩色多普勒超声心动图检查结果显示深陷的小梁隐窝充满来自左室腔的血液[19]。利用上述标准能够对LVNC、DCM、瓣膜性心脏病及高血压性心脏病进行有效鉴别[20]。根据心肌致密化不全累及的部位,将LVNC按照心尖部、前壁、侧壁或后壁进行分类。
1.3 心电图分析 根据波群的时限,fQRS可细分为窄的碎裂QRS(f-nQRS)(QRS波群时限<120 ms)和宽的碎裂QRS(f-wQRS)(QRS波群时限>120 ms)。在至少两个相邻标准心电图导联的R波或S波上出现切迹或出现额外的R波 ,伴或不伴Q波的QRS波群被称为f-nQRS[11]。在上述定义中须排除典型的束支阻滞(BBB)及不完全性右束支阻滞图形。任何时限>120 ms的QRS波群,包括BBB、室内传导阻滞及起搏的QRS波群,被称为宽QRS波群(wQRS)。将在至少两个相邻心电图导联的R波或S波的升支或降支出现2个以上切迹的wQRS称为f-wQRS[14]。f-nQRS组为心电图呈现窄碎裂QRS波群的患者,非f-nQRS组包括心电图无窄碎裂QRS波群表现且QRS波群时限<120 ms的患者。f-wQRS组为心电图呈f-wQRS表现的患者,非f-wQRS组包括心电图无f-wQRS表现且QRS波群时限>120 ms的患者。
1.4 随访 通过电话、信件或电子邮件对所有患者存活与否进行随访。如死亡,需明确死因。主要研究终点为随访期间因各种原因死亡或接受心脏移植手术。1.5 数据分析 以均值±标准差的方式对持续性变量进行数据描述。利用频率计数或百分比对分类变量进行总结。用单变量一般线性模型进行组间的基线人口统计学数据及临床数据的比较。利用χ2检验或Fisher检验评估组间差异。利用Kaplan-Meier生存曲线及单变量和多变量Cox比例风险回归分析对随访获得的患者存活数据进行评估分析。相对风险比用95%置信区间(CIs)的HRs表示。P<0.05被认为存在统计学差异。对双侧进行数据检验。利用SPSS软件(版本为17.0;SPSS,芝加哥,IL)对数据进行分析。
2 结果
2.1 临床资料 对64例患者(其中49例男性患者,平均年龄为44岁)进行队列分析。图1为左心室致密化不全性心肌病的典型超声心动图表现。最常受累的节段为心尖部(80%)和侧壁(78%)。40例(63%)患者出现LVNC患者最常见的临床表现:呼吸困难,22%患者出现心悸,15%患者出现晕厥或先兆晕厥。3例患者出现血栓栓塞性事件。
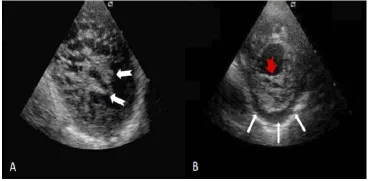
图1 典型LVNC的超声心动图表现A. 一例患者的短轴位(舒张末期)超声心动图显示:明显粗大的肌小梁向外突出,小梁隐窝深陷并与左室腔相通(箭头所指)。B. 另1例患者的短轴位(舒张末期)超声心动图显示:未致密化心肌呈海绵状;薄的心外膜层(白色箭头所指)及极厚的心内膜层(红色箭头所指)
对49例患者进行心脏核磁共振检查,以进一步明确LVNC的诊断。其中21例患者心肌强化延迟,提示心肌纤维化或心肌瘢痕。室间隔区域是心肌强化延迟最常见的部位,21例患者中有10例(47%)心肌强化延迟的部位在室间隔,其次是左室侧壁(38%)、左室前壁(33%)及心尖部(24%)。 典型的心肌强化延迟部位呈带状或补片状,位于心内膜下。χ2检验表明心肌强化延迟与心电图呈现fQRS波群形态之间无显著联系。对50例患者进行24 h动态心电图检查。对12例疑似CAD的患者进行冠脉造影检查,其结果显示冠状动脉无明显异常。9例患者接受植入器械手术,其中5例(2例f-nQRS患者,3例非f-nQRS患者)植入ICD,4例(2例f-wQRS患者,2例非f-wQRS患者)接受了心脏再同步化治疗(CRT 2例, CRT-D 2例)。在随访期间,有2例患者(1例f-nQRS患者和1例非fQRS患者)接受了抗心动过速起搏治疗,2例(1例f-nQRS患者,1例非f-nQRS患者)接受了抗心动过速起搏和ICD电击治疗。
在平均为32±24个月的随访期间,13例患者死亡,7例患者(5例为男性,平均年龄为26岁)接受了心脏移植手术。图2示心电图呈典型的f-nQRS和f-wQRS表现。24例患者(38%)呈f-nQRS表现,21例患者(33%)无f-nQRS表现。19例患者(29%)呈wQRS表现,7例患者(11%)呈f-wQRS表现。随访结束时,心电图呈窄QRS波群和宽QRS波群形态的患者生存率分别为71%和63%。对全因死亡率进行的Kaplan-Meier生存分析表明:不论QRS波群时限如何,与无碎裂QRS波群患者相比,出现碎裂QRS波群的患者生存率更低(对数秩检验 P=0.000)。
2.1.1 f-nQRS组与非f-nQRS组间比较 表1示:f-nQRS组与非f-nQRS组在人口统计学数据和临床表现上无显著差异。然而,两组的LVEF(35±12% vs. 49± 14%,P=0.001)及LVEDD(63±7 vs. 55±13 mm,P=0.036)存在显著差异。f-nQRS组全因死亡率24%(11例)高于非f-nQRS组4%(2例)。Kaplan-Meier生存分析显示:与非f-nQRS组相比,f-nQRS组存活时间明显缩短。(P=0.005,对数秩检验;图3)。
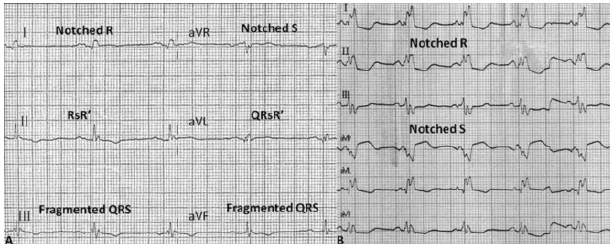
图2 LVNC患者心电图上的碎裂QRS波群A. 下壁和侧壁导联上呈现不同形态的窄碎裂QRS波群 ;B. 宽碎裂QRS波群

表1 f-nQRS组、非f-nQRS组、f-wQRS组及非f-wQRS组的人口统计学数据、临床表现及超声心动图特征的比较
单变量Cox回归分析结果(表2)表明:LVNC患者的生存率与f-nQRS(P=0.015)、LVEF(P=0.011)、LVEDD(P=0.028)及LVEDV(P=0.041)显著相关。然而,LVNC患者的生存率与年龄、性别、房颤或室性心动过速并无明显关联。最终分析结果表明:f-nQRS是预测LVNC患者的全因死亡率或心脏移植的一项独立指标。(HR=5.33; 95%CI:0.98~28.07;P=0.045)
2.1.2 f-wQRS组与非f-wQRS组间比较 两组间的LVEF有显著差别(35%±11% vs. 46%±11%;P=0.026),但LVEDD并无不同(63±13 mm vs. 62 ±11 mm,P=0.796)。非f-wQRS组患者的平均年龄显著高于f-wQRS组(58±6 vs. 41±15;P=0.003)。Kaplan-Meier生存分析显示:f-wQRS组患者的存活时间明显缩短(P=0.02,对数秩检验;图3)。 Cox比例风险回归模型表明:年龄与f-wQRS是死亡率的单变量预测指标,但在多变量回归模型中,这两者均不是死亡率的预测指标(表3)。

图3 全因死亡率Kaplan-Meier分析利用Kaplan-Meier方法分别对f-nQRS组、非f-nQRS组(A)及f-wQRS组、非f-wQRS组(B)的生存曲线进行评估,利用对数秩检验分别对全因死亡率进行评估。该研究调查了fQRS波群对于LVNC患者的预后评估价值。共研究和随访了64例LVNC患者。多变量Cox回归分析表明:f-nQRS波群是预测LVNC患者全因死亡率的独立指标(风险比为5.33;P=0.045)。研究结果显示:对于LVNC患者,f-nQRS具有重要的预后评估价值,且可提供1个用于对LVNC患者进行危险度分层的有效方法。

表2 对窄QRS波群患者全因死亡率的单变量和多变量预测指标进行Cox回归分析的结果
3 讨论
该研究首次将fQRS波群与LVNC患者的预后相关联。fQRS波群(不论是f-nQRS还是f-wQRS)都与LVNC患者在平均为32个月的随访期间显著降低的生存率有关。f-nQRS是预测LVNC患者的全因死亡率或心脏移植的独立指标。
3.1 fQRS波群的产生机制 在常规12导联心电图上出现fQRS波群,已经被认为是心肌除极异常的一项标志。其形成机制已被阐明即:由心肌瘢痕及/或心肌缺血引起左右心室不均匀激活及心肌传导延迟[11-13]。对已知患有CAD的患者进行的心肌SPECT成像检查及钆延迟增强CMIR检查发现fQRS波群出现的部位存在心肌瘢痕[11,12]。
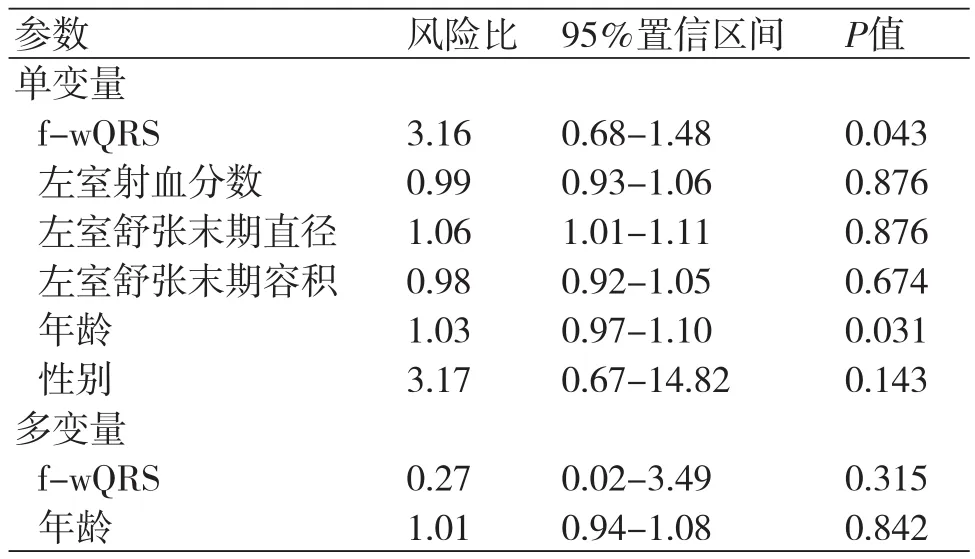
表3 对宽QRS波群患者全因死亡率的单变量和多变量预测指标进行Cox回归分析的结果
3.2 LVNC与fQRS波群形成的关系 已在病理解剖学和病理生理学的角度对LVNC患者的心内膜下心肌缺血及心肌纤维化进行了描述和分析。Jenni等研究人员[19]已经报道了LVNC患者心肌的组织学检查结果。他们发现:在增厚的心内膜层及突出的肌小梁中存在心肌缺血和间质纤维化病灶。其他一些报告指出LVNC患者的心肌存在纤维化病灶,突出的肌小梁中存在坏死的心肌细胞[6,21-23]。利用CMIR[21]、SPECT[22]及铊-201心肌灌注显像[2]的研究表明:LVNC患者心内膜下心肌灌注缺损区与未致密化心肌分布区相一致。因此,LVCN患者的心电图上出现fQRS可能是心内膜下心肌缺血和纤维化的后果,后两者引起局部心肌传导延迟及围绕阻滞区的心肌曲线性激活。
3.3 fQRS波群与全因死亡率增加的关系 该研究并未阐明在心电图上出现fQRS波群的LVNC患者全因死亡率增加的原因。与心肌缺血或纤维化相关的心力衰竭可能是原因之一。
f-nQRS组的LVEF显著低于非f-nQRS组(P=0.001),f-wQRS组的LVEF也显著低于非f-wQRS组(P=0.026)。fQRS与局灶性心肌缺血或心肌瘢痕存在区域相关性,而心肌缺血或瘢痕可能是引起心室功能不全的关键性因素。现已证明在静息心电图上出现fQRS波群与非缺血性心肌病患者显著的心室内非同步化有关[24]。左心室非同步化对患者的血流动力学有不利影响,可能会加重其心力衰竭。Jenni等研究人员[19]证实:左心室壁的未致密化节段及正常节段在心室收缩期增厚不良以及心室壁运动异常(运动减低),导致左心室射血分数下降。与LVNC幸存者相比,已死亡的患者之前发生显著左心功能不全的频率更高[6]。Stanton等[25]研究人员发现:LVNC患者的心功能不全加重会增加死亡风险。我们认为:对于LVNC患者,在静息心电图上出现的fQRS波群是其心功能异常的一项标志,且预示其出现不良结局的风险增加。
4 结论
LVNC患者在标准导联心电图上出现的fQRS波群与其存活期缩短有关。f-nQRS是LVNC患者的全因死亡率或心脏移植的独立预测指标;且可能会提供一项有效方法用于对LVNC患者进行危险度分层。
[1] Chin TK,Perloff JK,Williams RG,et al. Isolated noncompaction of left ventricular myocardium[J]. A study of eight cases. Circulation 1990,82:507-13.
[2] Ichida F,Hamamichi Y,Miyawaki T,et al. Clinical features of isolated noncompaction of the ventricular myocardium:long-term clinical course,hemodynamic properties, and genetic background[J]. J Am Coll Cardiol,1999,34:233-40.
[3] Jenni R,Oechslin EN,van der Loo B. Isolated ventricular noncompaction of the myocardium in adults[J]. Heart 2007,93:11-5.
[4] Elliott P,Andersson B,Arbustini E,et al. Classification of the cardiomyopathies:a position statement from the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases[J]. Eur Heart J 2008,29:270-6.
[5] Kohli SK,Pantazis AA,Shah JS,et al. Diagnosis of left-ventricular noncompaction in patients with left-ventricular systolic dysfunction: time for a reappraisal of diagnostic criteria?[J]. Eur Heart J 2008,29:89-95.
[6] Oechslin EN,Attenhofer Jost CH,Rojas JR,et al. Long-term followup of 34 adults with isolated left ventricular noncompaction:a distinct cardiomyopathy with poor prognosis[J]. J Am Coll Cardiol 2000,36:493-500.
[7] Aras D,Tufekcioglu O,Ergun K,et al. Clinical features of isolated ventricular noncompaction in adults long-term clinical course, echocardiographic properties,and predictors of left ventricular failure[J]. J Card Fail 2006,12:726-33.
[8] Murphy RT, Thaman R, Blanes JG,et al. Natural history and familial characteristics of isolated left ventricular non-compaction[J]. Eur Heart J 2005,26:187-92.
[9] Das MK,Zipes DP. Fragmented QRS: a predictor of mortality and sudden cardiac death[J]. Heart Rhythm 2009,6(suppl 3):S8-14.
[10] Das MK,El Masry H. Fragmented QRS and other depolarization abnormalities as a predictor of mortality and sudden cardiac death[J]. Curr Opin Cardiol 2010,25:59-64.
[11] Das MK,Khan B,Jacob S,et al. Significance of a fragmented QRS complex versus aQwave in patients with coronary artery disease[J]. Circulation 2006,113:2495-501.
[12] Das MK,Saha C,El Masry H,et al. Fragmented QRS on a 12-lead ECG:a predictor of mortality and cardiac events in patients with coronary artery disease[J]. Heart Rhythm 2007,4:1385-92.
[13] Das MK,Maskoun W,Shen C,et al. Fragmented QRS on twelvelead electrocardiogram predicts arrhythmic events in patients with ischemicand nonischemic cardiomyopathy[J]. Heart Rhythm 2010,7:74-80.
[14] Das MK, Suradi H, Maskoun W,et al. Fragmented wide QRS on a 12-lead ECG: a sign of myocardial scar and poor prognosis[J]. Circ Arrhythm Electrophysiol 2008,1:258-68.
[15] Pietrasik G,Goldenberg I,Zdzienicka J,et al. Prognostic significance of fragmented QRS complex for predicting the risk of recurrent cardiac events in patients with Q-wave myocardial infarction[J]. Am J Cardiol 2007;100:583-6.
[16] Das MK, Michael MA, Suradi H,et al. Usefulness of fragmented QRS on a 12-lead electrocardiogram in acute coronary syndrome for predicting mortality[J]. Am J Cardiol 2009,104:1631-7.
[17] Morita H,Kusano KF,Miura D,et al. Fragmented QRS as a marker of conduction abnormality and a predictor of prognosis of Brugada syndrome[J]. Circulation 2008,118:1697-704.
[18] Peters S,Trummel M,Koehler B. QRS fragmentation in standard ECG as a diagnostic marker of arrhythmogenic right ventricular dysplasia-cardiomyopathy[J]. Heart Rhythm 2008,5:1417-21.
[19] Jenni R,Oechslin E,Schneider J,et al. Echocardiographic and pathoanatomical characteristics of isolated left ventricular non-compaction: a step towards classification as a distinct cardiomyopathy[J]. Heart 2001,86:666-71.
[20] Frischknecht BS,Attenhofer Jost CH,Oechslin EN,et al. Validation of noncompaction criteria in dilated cardiomyopathy, and valvular and hypertensive heart disease[J]. J Am Soc Echocardiogr 2005,18:865-72.
[21] Hamamichi Y, Ichida F, Hashimoto I,et al. Isolated noncompaction of the ventricular myocardium: ultrafast computed tomography and magnetic resonance imaging[J]. Int J Cardiovasc Imaging 2001,17:305-14.
[22] Finsterer J,Stollberger C,Feichtinger H. Histological appearance of left ventricular hypertrabeculation/noncompaction[J]. Cardiology 2002,98:162-4.
[23] Dursun M,Agayev A,Nisli K,et al. MR imaging features of ventricular noncompaction: emphasis on distribution and pattern of fibrosis[J]. Eur J Radiol 2010;74:147-51.
[24] Tigen K,Karaahmet T,Gurel E,et al. The utility of fragmented QRS complexes to predict significant intraventricular dyssynchrony in nonischemic dilated cardiomyopathy patients with a narrow QRS interval[J]. Can J Cardiol 2009;25:517-22.
[25] Stanton C, Bruce C, Connolly H,et al. Isolated left ventricular noncompaction syndrome[J]. Am J Cardiol 2009;104:1135-8.
The Correlation Factor Analysis of Fibrillation Ventricular of Acute Myocardial Infarction under the Treatment of PCI
ZHAI Zheng-qin*, TANG Min, NING Xiao-hui, CHEN Ke-ping, HUA Wei, SHA Jing, ZHANG Shu. *Chinese Academic of Medical Sciences ,beijing,100037.
R542.2
A
2095-4220(2014)04-0193-05
2014-08-14)
(本文编辑:李俊峡)
国家自然科学基金(2015-GZ28)
100037 中国医学科学院 北京协和医学院 国家心血管病中心 心血管疾病国家重点实验室 阜外心血管病医院 心律失常中心
唐闽,E-mail:doctortangmin@hotmail.com
