调节不同pH值的免疫吸附洗脱液的细菌内毒素测定
2014-07-07岩林苹曹燕丽吴晶晶任海祥
岩林苹,曹燕丽,吴晶晶,王 婷,苏 华,任海祥
(南京军区南京总医院制剂科,江苏 南京 210002)
调节不同pH值的免疫吸附洗脱液的细菌内毒素测定
岩林苹,曹燕丽,吴晶晶,王 婷,苏 华,任海祥
(南京军区南京总医院制剂科,江苏 南京 210002)
目的 选择不同浓度的氢氧化钠碱性调节剂或直接稀释法对免疫吸附洗脱液的 pH值进行调节比较,建立免疫吸附洗脱液的细菌内毒素检查方法。方法 根据《中国药典》2010年版第二部附录收载的细菌内毒素检查方法,采用鲎试剂法对免疫吸附洗脱液进行干扰试验。结果 稀释32倍的免疫吸附洗脱液对细菌内毒素与鲎试剂的反应无干扰,选择灵敏度为0.015 EU·mL-1的鲎试剂进行细菌内毒素检查。结论 选择直接稀释法调节供试品的 pH值更优于低浓度氢氧化钠碱性调节剂调节供试品的pH值对其进行细菌内毒素的检查。
免疫吸附洗脱液;细菌内毒素;pH值;氢氧化钠碱性调节剂
免疫吸附洗脱液是南京军区南京总医院自制制剂,其临床上用于免疫性疾病,肾移植,中毒,肾小球疾病等。由于此药的pH值过低,考虑到pH值过大或过小均可抑制鲎试剂与细菌内毒素的反应,其原因可能是pH值过大或过小均可破坏极微量的内毒素,因此为了保证免疫吸附洗脱液的用药安全,控制药品的生产质量,我们对如何调节本品的pH值进行了方法探讨。
1 试验仪器与试药
1.1 仪器 ET-96细菌内毒素凝胶法测定仪(天津天大天发科技有限公司);ZH-2自动漩涡混合器(天津药典标准仪器厂);试验所用玻璃仪器均经过250℃干烤2 h。
1.2 试药 细菌内毒素工作标准品(CSE)(规格:120 EU·mL-1批号:150601-200859,中国食品药品检定研究院);鲎试剂(TAL)(规格:每支0.1 mL,灵敏度:0.062 5 EU·mL-1,广东湛江安度斯生物有限公司,批号:1201110;广东湛江博康海洋生物有限公司,批号:1207193);鲎试剂(TAL)(规格:每支0.1 mL,灵敏度:0.015 EU·mL-1,广东湛江安度斯生物有限公司,批号:1201103;广东湛江博康海洋生物有限公司,批号:1203050);细菌内毒素检查用水(BET)(规格:每支5 mL,广东湛江博康海洋有限公司,批号:1201180);无水氢氧化钠(规格:500 g,分析纯,上海实意化学试剂有限公司,批号:090610);免疫吸附洗脱液(规格:每袋500 mL,南京军区南京总医院自制药品,批号:120911、120916、120924)。
2 方法和结果
2.1 鲎试剂灵敏度复核实验 按照《中国药典》2010年版二部附录XIE规定的细菌内毒素检查法规定[1],进行鲎试剂的标示灵敏度复核,结果见表1。所用的鲎试剂灵敏度均符合规定,可用于细菌内毒素的检查。
2.2 细菌内毒素限值(L)的确定 根据免疫吸附洗脱液说明书得知本品最大用量为80 mL/(60 kg ·h)。根据公式:细菌内毒素限值(L)=K/M。K为人用每公斤体重每小时最大可接受的内毒素剂量,本注射剂为 K=5 EU·kg-1·h-1,其中 M为人用每公斤每小时的最大供试品量本品为80 mL/(60 kg·h),则 L=3.75 EU·mL-1。考虑到临床联合用药的安全性和细菌内毒素的累加性,在上述计算限制的基础上将限值提高7.5倍,由此确定免疫吸附洗脱液的细菌内毒素限值为 0.5 EU·mL-1[2]。
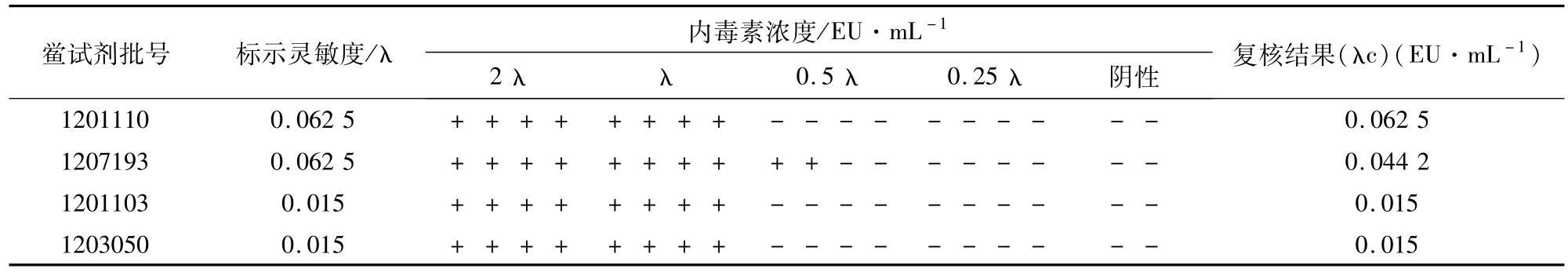
表1 鲎试剂灵敏度复核
2.3 凝胶半定量法测定 将 3批免疫吸附洗脱液,用细菌内毒素检查用水在去除内毒素的容器中配制成两种不同浓度(0.1、0.05 mol·L-1)的氢氧化钠碱性调节剂,分别对原液、稀释后的2、4、8倍供试品溶液进行 pH值调节至大约为6.5左右[3](调节过程:分别取供试品每个梯度溶液1 mL于试管中,滴一滴酚酞指示剂,用刻度移液管缓缓加入氢氧化钠碱性调节剂,溶液变色时分别记下氢氧化钠碱性调节剂的用量;再另取去除热原的试管,直接按前一步骤记录的氢氧化钠碱性调节剂的用量分别加入供试品的每个梯度中)。采用两个厂家 λ为0.062 5 EU·mL-1的鲎试剂,按《中国药典》2010年版二部附录XIE规定的细菌内毒素凝胶半定量检查法进行检测[4]。
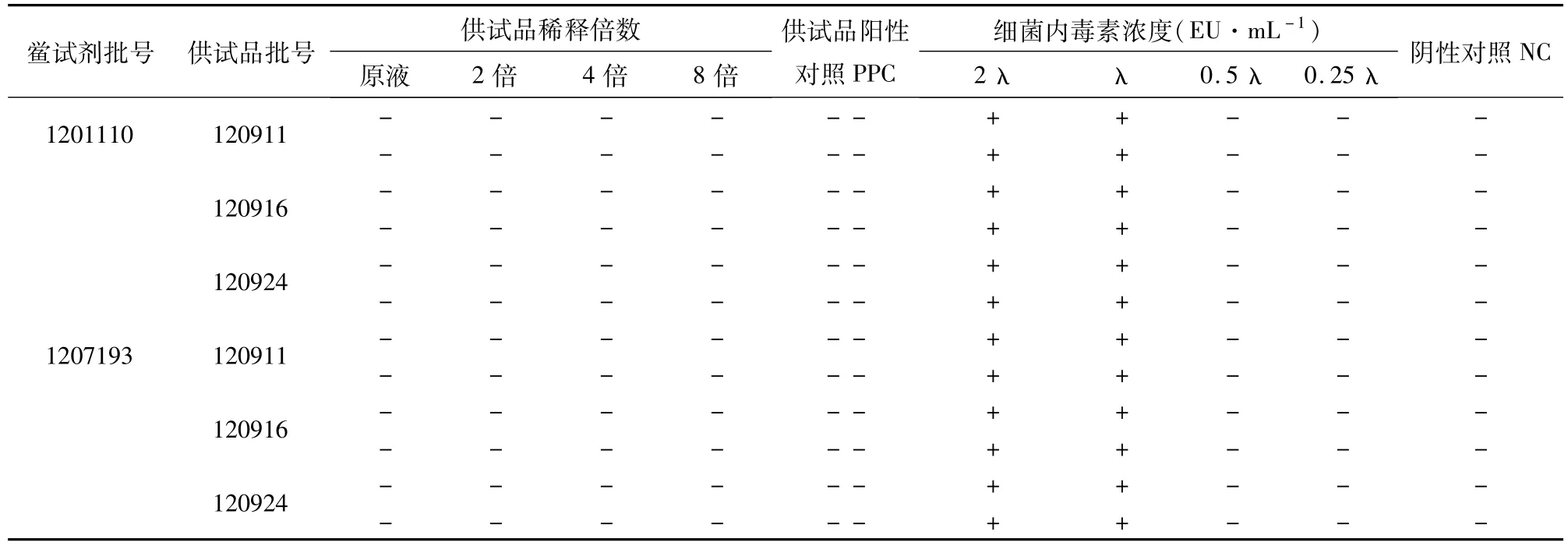
表 2 细菌内毒素凝胶半定量法检测结果 (0.1 mol·L-1NaOH)
由表 2可知,(0.1 mol·L-1)氢氧化钠碱性调节剂对3批免疫吸附洗脱液进行 pH值调节,结果虽能有效调节pH值,但供试品阳性对照(PPC)管均为阴性,表明内毒素失去活性,可能因为氢氧化钠碱性调节剂浓度过高,破坏内毒素,使其失活,此方法不可行。因此选择低浓度(0.05 mol·L-1)氢氧化钠碱性调节剂调节供试品pH值,再进行半定量检测。
表3结果表明,(0.05 mol·L-1)氢氧化钠碱性调节剂对3批免疫吸附洗脱液进行 pH值调节,既能有效调节供试品 pH值,又可保留内毒素活性,通过计算[公式CE=antilg(∑X/2)],系列溶液内毒素浓度的几何平行值(CE)均在规定范围内,方法可行。
2.4 选择高灵敏度的鲎试剂,采用直接稀释法对免疫吸附洗脱液进行细菌内毒素验证[5-7]
2.4.1 干扰预试验 取3批免疫吸附洗脱液用BET水分别稀释为2、4、8、16、32倍稀释液,将此系列浓度溶液记为供试品阴性对照(NPC)。另制备同样系列浓度的供试液,并使2、4、8、16、32倍稀释液的供试品中均含有 2 λ浓度的细菌内毒素,将此系列溶液记为供试品阳性对照(PPC)。取2个厂家灵敏度为 0.015 EU·mL-1的鲎试剂,分别与上述PPC和 NPC进行反应,每一浓度重复两管,并设阳性对照(PC)和阴性对照(NC),对其进行干扰预试 验,结果见表4。
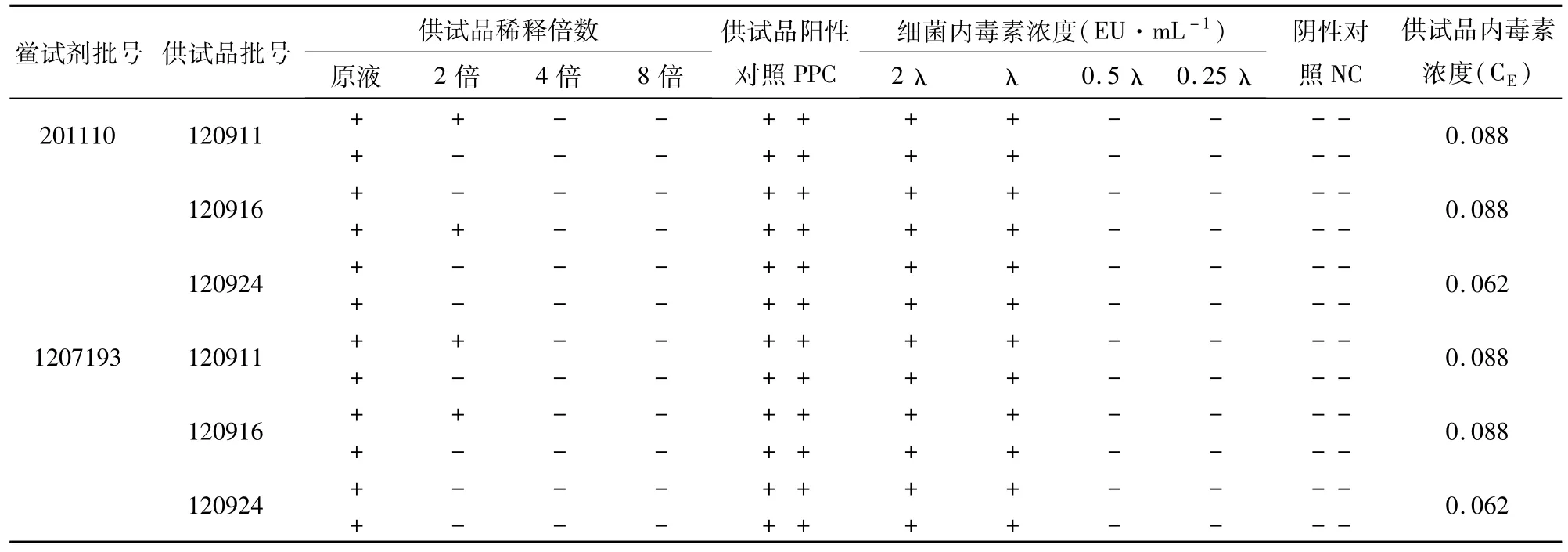
表3 细菌内毒素凝胶半定量法检测结果(0.05 mol·L-1NaOH)
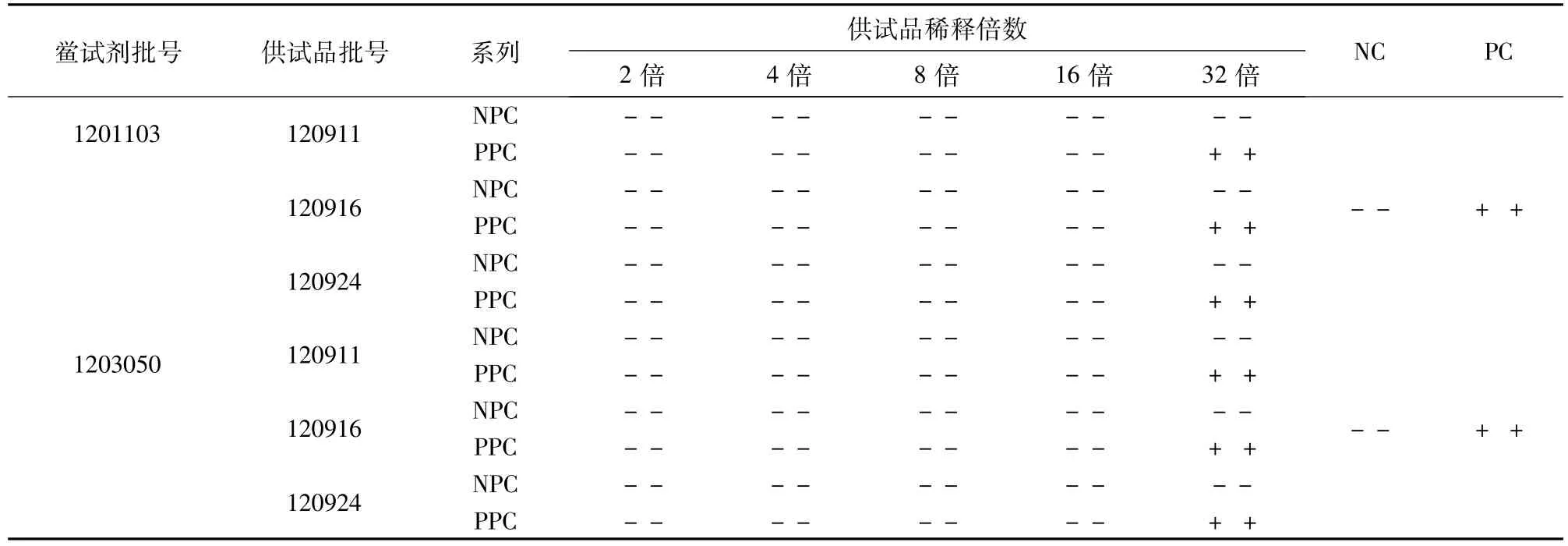
表4 免疫吸附洗脱液干扰预试验
从表4预试验结果表明,供试品在32倍以上的稀释倍数时,和 BET相容性较好,没有干扰,将其初步判断为供试品无干扰浓度。
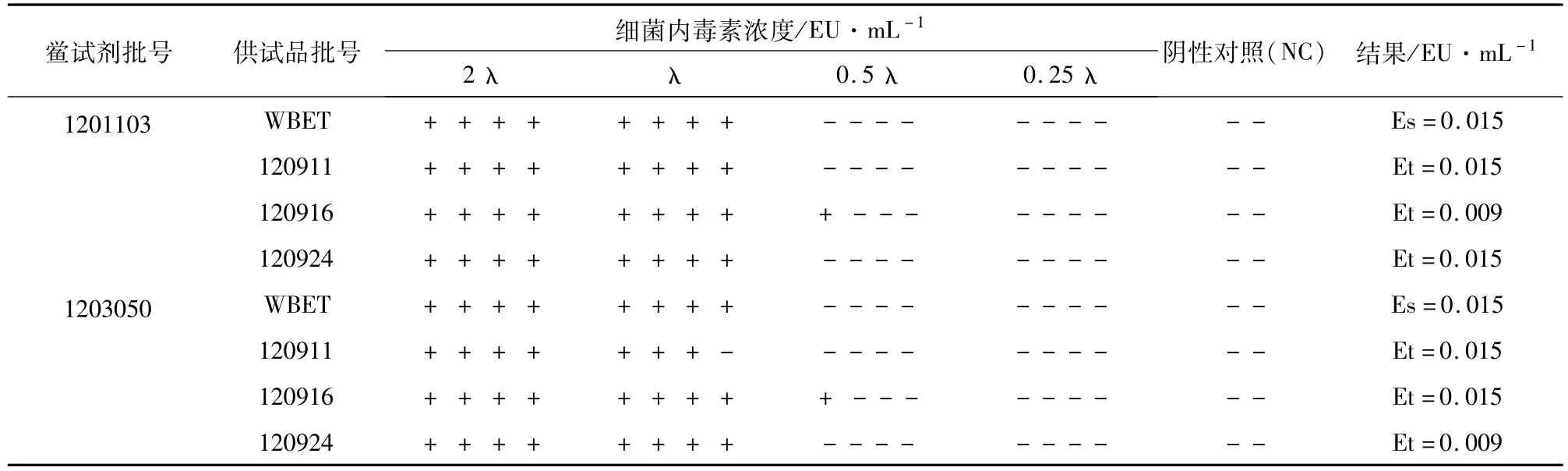
表5 免疫吸附洗脱液的干扰试验
2.4.2 正式干扰试验 为了最终确认是否存在抑制因素的影响,进行正式干扰试验。取3批免疫吸附洗脱液用 BET水分别稀释为32倍,用32倍稀释液和BET水分别将CSE稀释制得 0.03(2 λ)、0.015(λ)、0.007 5(0.5 λ)、0.003 75(0.25 λ)EU· mL-1系列内毒素浓度溶液,与2个厂家灵敏度为0.015 EU·mL-1的鲎试剂反应,每一浓度平行做 4管。另取0.1 mL BET水或供试品 32倍稀释液加入0.1 mL BET水复溶的TAL安瓿中,各平行做两管,作为阴性对照(NC)。按 2010年版中国药典细菌内毒素检查供试品干扰试验进行试验,结果见表5。
表5表明,上述3批供试品对两个厂家鲎试剂的 Et均在 0.5~2.0 Es之间,因此供试品在 32倍稀释时对鲎试剂试验均无干扰,可进行细菌内毒素检查。
2.4.3 供试品细菌内毒素凝胶法检查 取上述 3批供试品分别稀释32倍,使用两批不同厂家灵敏度为0.015 EU·mL-1的TAL,按2010年版中国药典细菌内毒素检查法检查,并同时设立阴性对照(NC)和阳性对照(PC),结果见表6。结果符合规定。

表6 免疫吸附洗脱液的细菌内毒素凝胶法检查
3 讨论
免疫吸附洗脱液的酸性较大,细菌内毒素检测时干扰严重。目前认为强碱物质本身不存在内毒素,可使用于酸度调节[8],本试验用自制的 0.1、0.05 mol·L-1的氢氧化钠碱性调节剂,分别调节本品 pH值约至6.5,即可排除干扰。
根据2010年版《中国药典》规定,细菌内毒检查法中鲎试剂的反应混合液(TAL+供试品)的 pH值应在6~8范围内,本品的 pH值为 2.4左右,稀释成2、4、8倍后,相应的 pH值3.3、4.2、4.8左右,仍不在范围内,采用(0.1 mol·L-1)和(0.05 mol· L-1)两个浓度的无热原的氢氧化钠碱性调节剂将供试品的pH值调节至 6.5左右,进行细菌内毒素凝胶半定量检查试验,表 2、表 3结果表明,用于调节供试品溶液pH值的氢氧化钠碱性调节剂浓度越小,就会使内毒素失去活性的几率越小。
考虑到氢氧化钠碱性调节剂虽无热原,但仍属于外添加物质,于是在不添加氢氧化钠碱性调节剂的情况下,对3批供试品进行向下稀释,现用BET水在容许范围内对供试品进行稀释,目前市售的普通鲎试剂 λ通常在 0.5~0.062 5 EU·mL-1之间,但鲎试剂 λ为0.062 5 EU·mL-1时,最大稀释倍数为16倍的供试品 pH值为5.2左右,不在药典规定的 pH范围内(6~8),因此选择两家高灵敏度的鲎试剂(0.015 EU·mL-1),对供试品进行相对应的进一步稀释,得2、4、8、16、32倍的溶液,测得32倍稀释液的pH值为 5.8左右,比较接近药典规定的pH值范围。而 BET水和鲎试剂本身对供试品 pH值具有一定的缓冲作用,干扰预试验的结果显示供试品在32倍稀释时与 BET相容性较好,没有干扰,可以进行正式的干扰试验。
本试验结果表明,选用低浓度的氢氧化钠碱性调节剂对供试品进行 pH值调节,方法可行,可节约成本,目前普遍采用该法。但每次试验均需临时配制,配制出的溶液 pH值都会不同,且每次均需测试酸碱调节剂用量,相当繁琐,更重要的是不能保证配制过程没有污染。而选用高灵敏度鲎试剂,直接稀释法可简化流程,排除干扰,且干扰试验是成立的,所以认为此方法是可行并成立的。
[1] 国家药典委员会.中国药典:二部[S].北京:中国医药科技出版社,2010:附录100.
[2] 王银娟,陆 崟,岩林苹,等.复方磷酸盐注射液细菌内毒素检查方法的研究[J].中国医药导报,2011,8(32):49-50.
[3] 陆 崟,汪 玥,王银娟,等.免疫吸附洗脱液细菌内毒素检查方法的研究[J].中国研究生学报,2012,25(10):1032-1034.
[4] 蔡庆祥,陈维成.凝胶半定量法检测参附注射液细菌内毒素含量[J].海峡药学,2007,19(1):47.
[5] 何 进,史国兵,高 军,等.枸橼酸钠注射液细菌内毒素检查方法的考察[J].解放军药学学报,2011,27(3):254-255.
[6] 武玉虹,刘丽梅,姚红谊.注射用辅酶 I的细菌内毒素检查[J].安徽医药,2013,17(6):950-952.
[7] 朱 勤.复合磷酸氢钾注射液的细菌内毒素检查法[J].安徽医药,2012,16(8):1190-1192.
[8] 国 明,胡文红,郝玲玲,等.注射用氨力农细菌内毒素检查方法学研究[J].齐鲁药事,2007,26(8):473-475.
Bacterial endotoxin test with immune adsorption eluent by adjusting pH value
YAN Lin-ping,CAO Yan-li,WU Jing-jing,et al
(Department of Preparation,Nanjing General Hospital of Nanjing Military Command,Nanjing,Jiangsu 210002,China)
Objective To establish a method for testing bacterial endotoxin with immune adsorption eluent by adjusting pH value with sodium hydroxide at different concentration as an alkalinity regulator or by direct dilution method.Methods The interference experiments with tachypleus amebocyte lysate(TAL)method on the immune adsorption eluents were performed according to the bacterial endotoxin test in Chinese Pharmacopoeia 2010(Section 2).Results The immune adsorption eluent did not interfere with the bacterial endotoxins test when it was diluted 32 times.Tachypleus amebocyte lysate was used with the sensitivity of 0.015 EU·mL-1.Conclusions It is better to adjust pH value by direct dilution method for testing bacterial endotoxin of immune adsorption eluent than with sodium hydroxide as an alkalinity regulator.
immune adsorption eluent;bacterial endotoxins;pH;sodium hydroxide alkalinity regulator
10.3969/j.issn.1009-6469.2014.05.012
2013-08-14,
2014-01-06)
任海祥,男,副主任药师,研究方向:医院制剂,E-mail:suhuash@sina.com.cn
