手助腹腔镜与开放手术活体供肾切取术的临床研究
2014-07-07成柯刘炼王强李晨星赵于军张盛明英姿
成柯 刘炼 王强 李晨星 赵于军 张盛 明英姿
肾移植是目前治疗终末期肾病的最佳方法。随着等待移植患者数量的增加,供肾短缺已严重阻碍肾移植的发展,亲属活体肾移植在目前及将来的一段时间内仍将是肾移植的一个重要组成部分。随着腹腔镜活体供肾切取术(laparoscopic living donor nephrectomy,LDN)的应用,供者术后恢复更快,同时避免了术后遗留巨大的手术疤痕[1]。但目前我国多数医院顾虑LDN 对供者风险以及较长的学习曲线,多数仍采取传统的开放手术活体供肾切取术(open donor nephrectomy,ODN)。我们认为,手助腹腔镜活体供肾切取术(hand-assisted laparoscopic living donor nephrectomy,HLDN)能很好地均衡腹腔镜取肾及开放取肾的优点及风险。因此,回顾性分析并比较中南大学湘雅三医院移植中心开展HLDN和ODN 两种术式的临床资料,结果报道如下。
1 资料与方法
1.1 研究对象与分组
2004 年1 月至2013 年11 月期间,我中心共完成341 例亲属活体肾移植,均为自愿捐献,供、受者关系以父母捐献给子女为主。受者平均年龄(35 ±15)岁,其中男性211 例(61. 88%),女性130 例(38.12%),原发病为:原发性肾小球肾炎(301 例,88.27%),糖尿病肾病(14 例,4.11%),高血压肾病(13 例,3.81%)。严格按照我国《人体器官移植条例》[2]进行伦理审核、上报,获得批准后进行临床操作。所有供者的选择标准参照荷兰阿姆斯特丹“活体肾移植国际论坛”发布的指南中供者选择的原则、美国和欧洲潜在供者选择和评估指南及我国制定的活体肾移植指南[3-4],均无高血压、心脏病、糖尿病、肺结核、急慢性肾炎、遗传性疾病及肿瘤病史,无精神心理疾病及家族史。供、受者ABO 和Rh 血型相同或相合,群体反应性抗体均阴性,淋巴细胞毒交叉配合试验<10%。
使用双血浆法99mTc-DTPA 血浆清除率测定供者肾小球滤过率(glomerular filtration rate,GFR)。早期以ODN 为主,在双侧肾脏GFR 大致相等的情况下,优先选择左肾;左肾GFR 明显高于右侧时,选择右肾。HLDN 组全部选择左肾为手术侧,若同时合并多种影响手术操作因素(多于2 支复杂血管、既往腹部手术史、CT 血管成像示肾血管畸形)情况时,行ODN。根据供者手术方式的不同,将供者分为HLDN 组(103 例)和ODN 组(238 例),两组供者一般资料和术前血清肌酐水平见表1。
表1 HLDN 组与ODN 组供者术前一般资料比较()

表1 HLDN 组与ODN 组供者术前一般资料比较()
注:HLDN. 手助腹腔镜活体供肾切取术;ODN. 开放手术活体供肾切取术
两组供者均常规麻醉诱导后实施手术。术后予芬太尼20 μg/kg、昂丹司琼8 mg 静脉自控镇痛,供者可根据疼痛程度每隔8 小时自主决定是否静脉使用非甾体抗炎药(氟比洛芬酯50 mg/次)。受者术后常规采用环孢素(或他克莫司)+ 吗替麦考酚酯+泼尼松三联免疫抑制方案抗排斥反应治疗。
1.2 手术方法(均以左肾为例)
1.2.1 HLDN 组手术方法
麻醉成功后,供者右侧卧位,术区常规消毒铺巾。在腹正中线脐上2 cm 处做一长约6 cm 直切口,逐层切开进腹,放置手助器。分别于脐下2 cm及左肾下极平面左侧腹直肌外缘处置直径10 ~12 mm穿刺套管,左手通过手助器进行腹腔内操作,右手操作超声刀。用超声刀切开左侧侧腹膜至腹膜后间隙,显露左肾。游离肾下极,在腰大肌前分离左输尿管和左生殖腺静脉,沿输尿管及生殖腺静脉向肾门方向游离。逐步游离左肾静脉至足够长度,依次结扎左生殖腺静脉、腰静脉和左肾上腺中央静脉。于左肾静脉后上方游离左肾动脉,充分游离至腹主动脉开口平面。游离左肾,于输尿管远端距左肾下极10 cm 处上钛夹后离断,见有清亮尿液溢出后分别用2 枚Hem-o-lok 及钛夹阻断左肾动脉及左肾静脉远肾端后,依次用分离剪离断,用自制肾袋从手助器中将左肾完整取出。创面彻底止血,检查结肠系膜有无破损,酌情放置腹腔引流管,逐层缝合切口。
1.2.2 ODN 组手术方法
麻醉成功后,供者右侧卧位,升高腰桥,术区常规消毒铺巾。取左肋缘下2 cm 腹直肌左侧至第12左肋尖做一长10 ~15 cm 的弧形切口,依次切开皮肤、皮下组织、背阔肌、腹外斜肌、下后锯肌、腹内斜肌、腹横肌至腹膜后间隙。打开左肾周筋膜,沿左肾表面游离左肾上极。在腰大肌前分离输尿管,沿输尿管向上游离至肾盂,游离左肾下极。分离左肾静脉,分别以1 号丝线结扎左生殖腺静脉、腰静脉分支及左肾上腺中央静脉。游离左肾动脉至腹主动脉平面。于左肾下极约10 cm 处提起输尿管予以离断,以4 号、7 号丝线双重结扎输尿管远端残端。血管阻断钳分别阻断左肾动脉、左肾静脉,摘取供肾。以4 号丝线结扎肾蒂残端,以7 号丝线先缝扎再结扎肾动脉残端,以5-0 prolene 线连续缝合肾静脉残端。确切止血、放置腹膜后引流管1 根,逐层关闭切口。
1.3 观察指标
(1)供者观察指标:比较HLDN 组和ODN 组供者手术时长、切口长度、供肾热缺血时间、肾动脉长度、肾静脉长度、术中失血量、围手术期芬太尼用量、术后非甾体抗炎药(non-steroidal anti-inflammatory drugs,NSAIDs)用量和术后恢复劳动天数。术后48 h 使用视觉模拟评分(visual analogue scale,VAS)法评估两组供者疼痛程度,评分范围0 ~10 分,0 分表示无痛,10 分代表难以忍受的最剧烈的疼痛。术后随访供者恢复情况,并于术后7 d、1 个月复查肾功能。
(2)受者观察指标:测定受者术前、术后7 d、术后1 个月血清肌酐水平,并观察其发生移植物功能延迟恢复(delayed graft function,DGF)情况。
1.4 统计学方法
采用SPSS 17.0 统计软件进行数据处理。连续变量采用均数±标准差)表示,采用t 检验进行比较。分类变量用百分比来表示,采用Fisher 确切概率法进行比较。P <0. 05 为差异有统计学意义。
2 结 果
2.1 HLDN 组和ODN 组供者术中情况
HLDN 组供者切口长度为(6.0 ±0.4)cm ,小于ODN 组切口长度(13.5 ±1.0)cm,差异有统计学意义(t =73.56,P <0.05)。ODN 组供者术中失血量为(151 ± 24)mL,多于HLDN 组供者(45 ±12)mL,差异有统计学意义(t =42.56,P <0.05)。两组供者手术时长、供肾热缺血时间、肾动脉长度以及肾静脉长度相比,差异均无统计学意义(t=1.39,1.70,0.00 和1.85,P 均>0.05)。详见表2。
2.2 HLDN 组和ODN 组供者术后情况
103 例HLDN 组供者中有102 例(99.03%)顺利完成手术,1 例(0.97%)主动中转开放(术中发现脾大、肾蒂及肾上极被脾遮挡显露困难),中转开腹后手术及术后恢复顺利,无其他并发症发生。所有供者术中均无脏器损伤,术后均无切口感染和切口疝,术后2 ~3 d 拔除引流管。术后发生肺部感染1 例(0.97%,103)。
238 例ODN 组供者均成功完成手术,术中均无脏器损伤,术后3 ~5 d 拔除引流管;术后7 d 内切口感染1 例(0.42%)、脂肪液化2 例(0.84%);2 例(0.84%)术后24 h 内引流管血性液体增多,行原腰部切口探查示肾上腺处小静脉出血,予重新缝扎止血后恢复顺利。
表2 HLDN 组与ODN 组供者术中资料比较
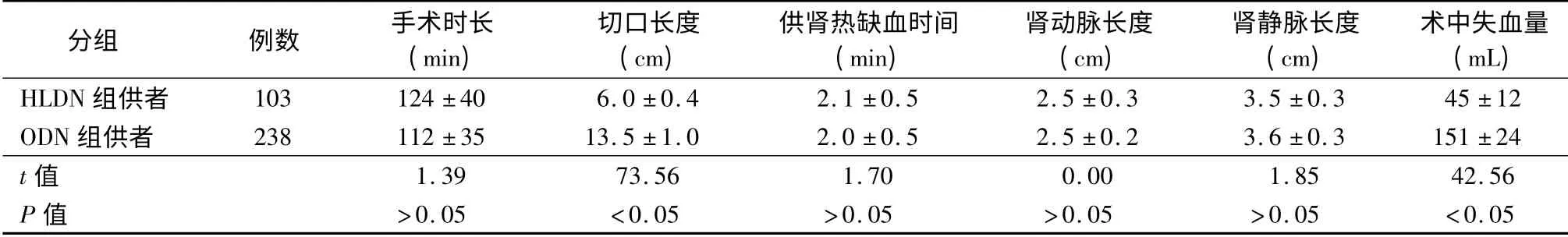
表2 HLDN 组与ODN 组供者术中资料比较
注:HLDN. 手助腹腔镜活体供肾切取术;ODN. 开放手术活体供肾切取术
分组 例数 手术时长(min)切口长度(cm)供肾热缺血时间(min)肾动脉长度(cm)肾静脉长度(cm)术中失血量(mL)HLDN 组供者 103 124 ±40 6.0 ±0.4 2.1 ±0.5 2.5 ±0.3 3.5 ±0.3 45±12 ODN 组供者 238 112 ±35 13.5 ±1.0 2.0 ±0.5 2.5 ±0.2 3.6 ±0.3 151 ±24 t 值1.39 73.56 1.70 0.00 1.85 42.56 P 值>0.05 <0.05 >0.05 >0.05 >0.05 <0.05
HLDN 组供者术后48 h VAS 为(2.3 ±0.6)分,低于ODN 组(3.9 ±0.9)分,差异有统计学意义(t=16.52,P <0.05)。HLDN 组供者围手术期芬太尼用量、术后NSAIDs 用量分别为(1. 7 ± 0. 2)mg 和(22 ±33)mg,均低于ODN 组用量[(1.9 ±0.2)mg和(47 ±42)mg],差异均有统计学意义(t=8.48 和5.37,P 均<0.05)。HLDN 组和ODN 组供者术后恢复劳动天数分别为(23 ±10)d 和(44 ±15)d,差异有统计学意义(t =13.00,P <0.05)。两组供者术后7 d、1 个月血清肌酐水平相比差异均无统计学意义(t=1.76 和0.00,P 均>0.05)。详见表3。
2.3 HLDN 组和ODN 组受者术后情况
HLDN 组和ODN 组受者术前血清肌酐水平分别为(1 110 ±302)μmol/L 和(1 095 ±321)μmol/L,差异无统计学意义(t =0.40,P >0.05)。HLDN 组受者术后7,30 d 血清肌酐水平分别为(106 ±106)μmol/L和(109 ±84)μmol/L,ODN 组受者术后7,30 d 血清肌酐水平分别为(118 ±115)μmol/L 和(120 ±99)μmol/L,两组受者术后同一时间点比较,血清肌酐水平差异均无统计学意义(t =0. 90 和0.98,P 均>0.05)。
术后HLDN 组和ODN 组各有1 例(0.97%和0.42%)受者发生DGF,两组受者发生DGF 比例差异无统计学意义(P =0.513)。给予血液透析等综合治疗,术后2 周内移植肾功能均恢复正常,无移植肾失功。
1 例(0.42%,238)ODN 组受者术后3 个月死于重症肺部感染合并急性排斥反应,死亡时移植肾已失功,1 例(0.42%)发生术后尿漏,1 例(0.42%,238)因术后1 个月移植肾动脉狭窄并栓塞切除移植肾。HLDN 组术后6 个月内无移植物丢失。术后6 个月,HLDN 组和ODN 组受者移植肾存活率分别为100.00%和99.16%。
3 讨 论
有研究表明,亲属活体肾移植的远期效果好于尸体肾移植[5]。在欧美和日本,活体肾移植数量已经超过尸体肾移植[6]。但对健康个体实施非治疗性的侵袭性手术,仍然有悖于医疗中的无害原则。因此,术前必须对供者进行严格的评估、筛选和伦理审查[7]。医疗操作中对手术安全性的保证,术后对供者提供最好护理,使其尽快恢复变得越来越重要。
手助腹腔镜的应用,减轻了活体肾移植供者术后疼痛,减少并发症,显示出极大的优越性。与传统腹腔镜相比,HLDN 有如下优点:(1)增加了手部的精细操作与触觉,可以随时通过触感判断移植肾灌注情况,以调整术中液体管理,从而更好地保护供肾;(2)以手代替器械直接游离、牵拉组织,减少了肾血管、输尿管及腹腔脏器的损伤,通过循生殖腺静脉解剖肾静脉,减少了肾静脉的损伤,同时更有利于腰静脉显露及处理;(3)利用超声刀及丝线结扎处理各支腰静脉及肾上腺静脉,减少了肾静脉损伤及出血,且一旦出现出血等特殊情况,能迅速用手控制,确保术野清晰,增加了手术的安全性。
表3 HLDN 组与ODN 组供者术后资料比较
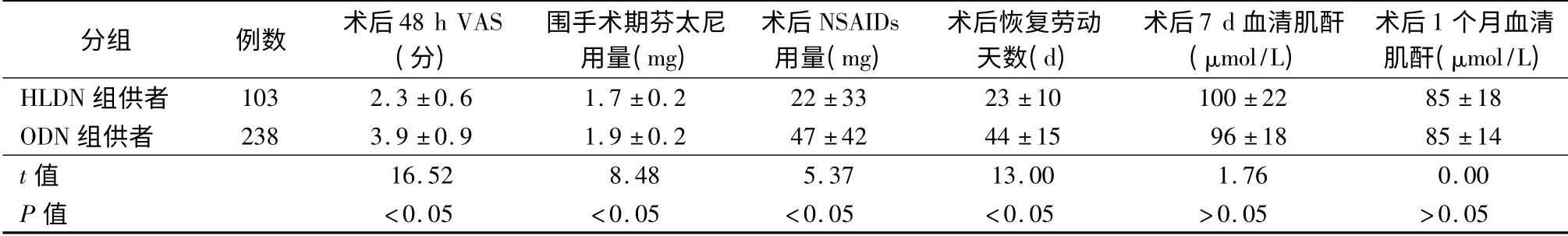
表3 HLDN 组与ODN 组供者术后资料比较
注:HLDN. 手助腹腔镜活体供肾切取术;ODN. 开放手术活体供肾切取术;VAS. 视觉模拟评分;NSAIDs. 非甾体抗炎药
分组 例数 术后48 h VAS(分)围手术期芬太尼用量(mg)术后NSAIDs用量(mg)术后恢复劳动天数(d)术后7 d 血清肌酐(μmol/L)术后1 个月血清肌酐(μmol/L)103 2.3 ±0.6 1.7 ±0.2 22 ±33 23 ±10 100 ±22 85 ±18 ODN 组供者 238 3.9 ±0.9 1.9 ±0.2 47 ±42 44 ±15 96 ±18 85 ±14 t 值HLDN 组供者16.52 8.48 5.37 13.00 1.76 0.00 P 值<0.05 <0.05 <0.05 <0.05 >0.05 >0.05
虽然有观点认为手助腹腔镜是纯腹腔镜的过渡阶段,但笔者认为在其他破坏性手术(如病变器官切除)中可能如此,就活体亲属供肾切取而言,除了安全考虑外,还必须有足够大小的切口以利于快速、无损伤取出供肾,而HLDN 正好兼顾了上述优点。有文献报道HLDN 也有其弊端,主要集中在伤口并发症及肠道并发症发生率增加[8],但是我们目前尚未观察到。在本研究中,HLDN 组供者切口长度、术中失血量、术后48 h VAS、恢复劳动天数、围手术期芬太尼用量以及术后NSAIDs 用量,均少于ODN 组。
一般来说,活体肾移植供者术后严重并发症的发生率很少超过2%,严重的心理后遗症也非常少见[9]。供者外科手术引起的并发症主要包括肺不张(7.4%)、切口感染(4.3%)、气胸(1.5%)、出血(0.9%)、肺炎(0.9%)、切口血肿(0.6%)、尿路感染(0.3%)及手术死亡(0.03%)等,长期风险主要涉及供肾切取手术对供者肾功能及血压的影响,主要表现为高血压及微量蛋白尿的出现,以及慢性肾病的发生[10]。在本研究中,ODN 组供者术后切口感染1 例(0.42%),切口脂肪液化2 例(0.84%),术后出血通过外科止血2 例(0.84%),无其他手术相关并发症。HLDN 组供者均无术中脏器损伤,其中 主 动 中 转1 例(0. 97%),肺 部 感 染1 例(0.97%),无术后切口感染及其他严重并发症,各种并发症累计发生低于同类报道,充分显示了该术式的安全性。
2004 年,荷兰阿姆斯特丹活体肾移植国际论坛的研究报告中指出,活体肾移植供者术后肾功能与对照者(健康兄弟姐妹)相比差异无统计学意义,二者高血压及蛋白尿发生率相似,该研究表明健康活体供肾不会增加肾功能衰竭的风险[11]。但本研究不足之处在于缺乏进一步对HLDN 组供者肾功能更长期的随访观察。有研究表明,HLDN 与ODN 两种术式,受者移植物功能的恢复无明显差异[12],与本研究结果一致。本研究HLDN 组与ODN 组供者术后7 d、1 个月血清肌酐水平差异均无统计学意义,提示两组供者肾功能恢复具有可比性。
HLDN 能很好地平衡腹腔镜取肾及开放手术取肾的优点及风险,易于掌握,可成为亲属活体供肾切取术式的一种可靠选择。
1 Rajab A,Mahoney JE,Henry ML,et al. Hand-assisted laparoscopic versus open nephrectomies in living donors[J]. Can J Surg,2005,48(2):123-130.
2 中华人民共和国国务院. 人体器官移植条例[J/CD]. 中华移植杂志:电子版,2007,1(1):61-63.
3 Ethics Committee of the Transplantation Society. The consensus statement of the Amsterdam Forum on the Care of the Live Kidney Donor[J]. Transplantation,2004,78(4):491 -492.
4 Kälble T,Lucan M,Nicita G,et al. EAU guidelines on renal transplantation[J]. Eur Urol,2005,47(2):156 -166.
5 Knight RJ,Burrows L,Bodian C. The influence of acute rejection on long-term renal allograft survival:a comparison of living and cadaveric donor transplantation[J]. Transplantation,2001,72(1):69-76.
6 Cecka JM. The UNOS renal transplant registry[J]. Clin Transpl,2001:1-18.
7 Taghavi R,Mahdavi R,Toufani H. The psychological effects of kidney donation on living kidney donors (related andunrelated)[J].Transplant Proc,2001,33(5):2636-2637.
8 Halgrimson WR, Campsen J, Mandell MS, et al. Donor complications following laparoscopic compared to hand-assisted living donornephrectomy:an analysis of the literature[J]. J Transplant,2010:825689.
9 Ingelfinger JR. Risks and benefits to the living donor[J]. N Engl J Med,2005,353(5):447-449.
10 Levey AS,Danovitch G,Hou S. Living donor kidney transplantation in the United States—looking back,looking forward[J]. Am J Kidney Dis,2011,58(3):343-348.
11 Delmonico F;Council of the Transplantation Society. A report of the Amsterdam Forum on the care of the live kidney donor:data and medical guidelines[J]. Transplantation,2005,79(Suppl 6):S53-S66.
12 Kim BS,Yoo ES,Kim TH,et al. Renal function recovery in donors and recipients after live donor nephrectomy:hand-assisted laparoscopic vs. open procedures[J]. Korean J Urol,2010,51(4):245-249.
