共沉淀法制备Cu/ZnO催化剂用于1,4-丁二醇合成吡咯
2014-06-11胡云峰潘志强刘万成孙铎王瑞浦
胡云峰,潘志强,刘万成,孙铎,王瑞浦
(东北石油大学化学化工学院,黑龙江 大庆 163318)
吡咯是一种不可或缺的有机化工中间体。又称氮杂茂,为五元杂环化合物,由于其生物活性及共振结构的存在和芳香特性,在医药、农药、食品烟草、精细化工和导电高分子材料等行业有广泛的应用。如合成具有生物活性的海洋溴吡咯生物碱[1]、杀虫剂溴虫腈[2]、香气物质吡咯亮氨酸异辛酯[3],以及具有高性能的导电高分子材料聚吡咯[4]等。
吡咯最早是从煤焦油成分分析中得到的[5],目前国内外生产吡咯比较成熟的工艺,大多数是采用吡咯烷在贵金属催化剂上脱氢制得的[6]。该工艺合成的吡咯有较高的选择性和转化率,但是采用的贵金属较为昂贵,不经济,并且吡咯烷一般需由四氢呋喃氨化、1,4-丁二醇氨化等合成[7-8]。另外,关于由呋喃直接合成吡咯的相关报道也较多[9],该工艺采用的催化剂的主要成分是硅铝。但是含有酸性位的硅铝作为催化剂的主要成分时,呋喃容易发生环聚合,并且未见有以呋喃为主要原料的工业化生产报道。因此,进一步研究一种较为适宜的工艺路线和催化剂进行吡咯的生产尤为重要。
目前,铜系催化剂在醇类脱氢的化工领域有广泛的应用[10],如甲醇脱氢制甲醛、甲酸甲酯,乙醇脱氢氨化合成乙腈,仲丁醇脱氢制甲乙酮,环己醇脱氢制环己酮等。在这些反应中,铜主要以Cu2O、Cu0为反应的活性中心,都表现出了良好的脱氢性能。以ZnO[11-12]为载体制备的Cu/ZnO催化剂用于醇类脱氢反应中,ZnO起到了很好的分散和稳定铜粒子的作用,提高了铜的催化性能。基于本实验室关于Cu/ZnO催化剂在乙醇脱氢氨化合成乙腈[13]与仲丁醇脱氢制甲乙酮的[14]反应研究,采用已筛选出适宜的Cu/ZnO催化剂制备条件,利用共沉淀法下合成Cu/ZnO催化剂,以1,4-丁二醇为原料脱氢氨化合成吡咯,研究了该反应可能的反应机理,以及催化剂中Cu/Zn摩尔比对该反应脱氢活性的影响,筛选出最佳的Cu/Zn摩尔比,并且还比较了Cu0比表面积对于1,4-丁二醇催化脱氢活性的影响。
1 实验部分
1.1 催化剂制备
分别配制一定量的浓度为1 mol/L Cu(NO3)2溶液和浓度为1 mol/L Zn(NO3)2溶液,然后将两种溶液均匀混合,最后配制一定量的浓度为2 mol/L Na2CO3溶液作为沉淀剂。保持在70℃水浴、pH值为中性条件下进行并流共沉淀,得到的乳浊液继续在70℃的水浴中陈化4 h,然后用蒸馏水进行多次洗涤,直至沉淀物的上清液电导率为20 μS/cm,进行最后一次的过滤,将得到的沉淀物转入干燥箱内,在150℃的条件下干燥4 h,再转入马弗炉中,在500℃的条件下焙烧4 h,焙烧后的黑色粉末经压片、研磨、过筛得到20~40目(0.85~0.425 mm)的成品,即所制的催化剂。
1.2 催化剂表征
XRD图谱是采用3C型X射线衍射仪(日本理学)对样品进行分析的,管电压为40 kV,管电流为30 mA,扫描范围5°~60°,扫描速度为2°/min,扫描类型为连续扫描。
H2-TPR图谱测试是采用常规的程序升温还原装置与气相色谱Shimadz GC-8A联用完成的,取0.01 g测试的催化剂样品,先用氮气在300℃下吹扫60 min,净化催化剂表面上气相杂质进行催化剂预处理,然后降温至50℃,改通5%H2-N2混合气以10℃/min的升温速率从50℃升至300℃,以气相色谱Shimadz GC-8A记录TPR曲线。
N2O吸附分解测定Cu0比表面积,取0.01 g催化剂样品,预处理同TPR测试一样,经还原后,在80℃下注入N2O(每次0.08 mL)气体进行定量脉冲,直至吸附峰达到饱和(即出现连续的3个以上的相同峰)为止,进行Cu0比表面积计算,计算方法同姜广申等[14]在Cu0比表面积计算的方法一致。
1.3 催化剂活性测试及产物分析
催化剂活性测试是在自制的连续固定床反应器中进行的。称取4 g催化剂样品置于不锈钢管式反应器中央,上下两段均用惰性石英砂填充。控温系统是通过PID表与热电偶控制的,热电偶触点置于催化剂反应床层中央位置。反应前催化剂须在300℃、0.2 MPa的氢气氛围下还原4 h,然后在常压、280℃下反应8 h。原料氨和1,4-丁二醇(按氨和1,4-丁二醇的摩尔比为1.1∶1)预先混合均匀,通过P230恒流泵(大连依利特分析仪器有限公司)通入反应器中。反应产物经气液分离器冷却后收集液体样品,并经尾气吸收装置后用皂泡计测定产气量。
液相产物、气体产物通过Nexus-670 FTIRShimadz和GCMS2010进行定性分析。并采用装有PEG-20M毛细管柱的Shimadz GC-14C氢焰气相色谱进行定量分析,条件为:COL 100℃,INJ 180℃,DET 250℃,升温速率10℃/min,从100℃升温至230℃,保持17 min。1,4-丁二醇的转化率及吡咯的选择性的计算见式(1)、式(2)。


图1 主要产物(吡咯)及主要副产物(γ-丁内酯)的气质定性分析
2 结果与讨论
2.1 产物的气质和红外(FT-IR)分析结果
催化反应的产物混合物进行的气质定量和定性分析结果如图1。
利用NIST数据库,在m/z为20~100扫描,从图1中15.507 min、17.852 min和26.115 min的保留时间的组分质谱分析结果上分别为吡咯(m/z:28、39、40、41、67),γ-丁内酯(m/z:28、42、56、86)和原料1,4-丁二醇(m/z:31、42、44、57、71)。
对产物进行分离后,其主产物红外图谱的结果在 3401 cm−1、2961 cm−1、1676 cm−1、1525 cm−1、1279 cm−1、730 cm−1、554 cm−1处存在吡咯的特征吸收峰,这与相关文献一致[15],进一步确认了吡咯的生成。
通过产物的分析结果,并结合Yarlagadda等[16]在合成五、六杂环化合物上的研究,给出1,4丁二醇与氨反应合成吡咯的反应机理见图2。从图2中可以看出1,4-丁二醇要先经过脱氢生成醛,然后与氨反应,最后再脱水合成吡咯。因此,要求此过程的催化剂既要具备脱氢的活性中心,又具备脱水作用,从而保证1,4-丁二醇高效的脱氢脱水合成目的产物吡咯。
2.2 不同Cu/Zn摩尔比的Cu/ZnO催化剂的评价结果

图2 1,4-丁二醇合成吡咯的机理
1,4-丁二醇在Cu/ZnO催化剂上的吡咯的选择性和1,4-丁二醇的转化率随不同Cu/Zn摩尔比的变化情况如图3。由图3可见,吡咯的选择性随Cu/ZnO催化剂中Cu含量的增大先增大后减小,在Cu/Zn摩尔比为1∶1时最大。从图3中,还可以看出在ZnO存在的催化剂均高于纯Cu催化剂的转化率,这是由于ZnO提高了Cu0的催化活性。
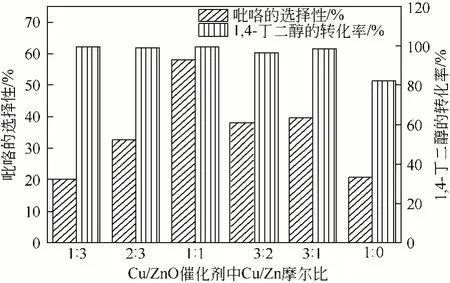
图3 不同Cu/Zn摩尔比的Cu/ZnO催化剂的反应性能
2.3 不同Cu/Zn摩尔比的Cu/ZnO催化剂的TPR结果
图4可见,焙烧后的各种Cu/ZnO催化剂的TPR还原峰都为单峰,并且ZnO的还原温度在600℃左右[14],说明在300℃反应条件下,只有CuO被还原了。Zn的加入,降低了CuO催化剂还原温度,相关文献[17-18]表明,在低温下还原的是较小的或者是高分散在催化剂载体表面的CuO微粒,而在高温下还原的是较大的CuO微粒。这较好的暗示了ZnO具有分散铜的作用,从一定程度上提高催化剂的催化性能。
2.4 不同Cu/Zn摩尔比的Cu/ZnO催化剂处理过程的XRD结果

图4 焙烧后不同Cu/ZnO催化剂的TPR分析图
从图5不同Cu/ZnO催化剂前体XRD图可知,纯CuO催化剂的前体物种全为Cu2(OH)2CO3(2θ=14.78°、17.50°、23.97°、31.16°、32.14°、35.54°);随着Zn物种的引入及含量的增加,Cu/ZnO催化剂中逐渐出现了CuZn(OH)2CO3(2θ=29.64°、31.74°、35.49°、38.52°)和(CuZn)5(OH)6(CO3)2(2θ=12.95°、23.97°、32.50°、33.97°、35.93°、57.14°)以及 Zn5(OH)6(CO3)2(2θ=12.86°、35.85°);直到为纯的Z n O催化剂时的前体物种全部为Zn5(OH)6(CO3)2(2θ=12.86°、28.04°、31.07°、35.85°),说明Cu2+和Zn2+发生了同晶取代。在不同Cu/Zn摩尔比的Cu/ZnO催化剂前体XRD图中还能看到Cu2(OH)2CO3或者Zn5(OH)6(CO3)2的存在,可以说明Cu/ZnO催化剂的两种组分达到了充分取代。并且在Cu/Zn摩尔比为1∶1时,(CuZn)5(OH)6(CO3)2(d:2θ=12.95°、23.97°、32.50°、33.97°、35.93°、57.14°),同晶取代程度达到最大,这与刘志坚等[11]在采用共沉淀法制备Cu/ZnO催化剂的研究较为一致。在采用共沉淀制备Cu/ZnO催化剂过程中,Cu(NO)3、Zn(NO)3和Na2CO3反应主要以Cu2(OH)2CO3、Zn5(OH)6(CO3)2两种沉淀形式存在,而Cu2+和Zn2+在结构上相似,发生相互渗透,发生同晶取代,生成了锌孔雀石微晶 CuZn(OH)2CO3和绿铜锌矿片晶(CuZn)5(CO3)2(OH)6[19]。这两种结构,在催化剂合成后,ZnO能够较好的分散和稳定铜微晶结构。同时,由图6和图7可以看出,不同Cu/Zn摩尔比的催化剂还原前后的Cu和Zn物种的存在形式,进一步说明了起催化活性中心的是Cu0物种,而Zn以ZnO物种的形式存在。与前面催化性能的比较可知,Cu/Zn摩尔比为1∶1时,催化效果最佳,说明Cu、Zn两种物种的同晶取代程度与催化性能有密切关系。
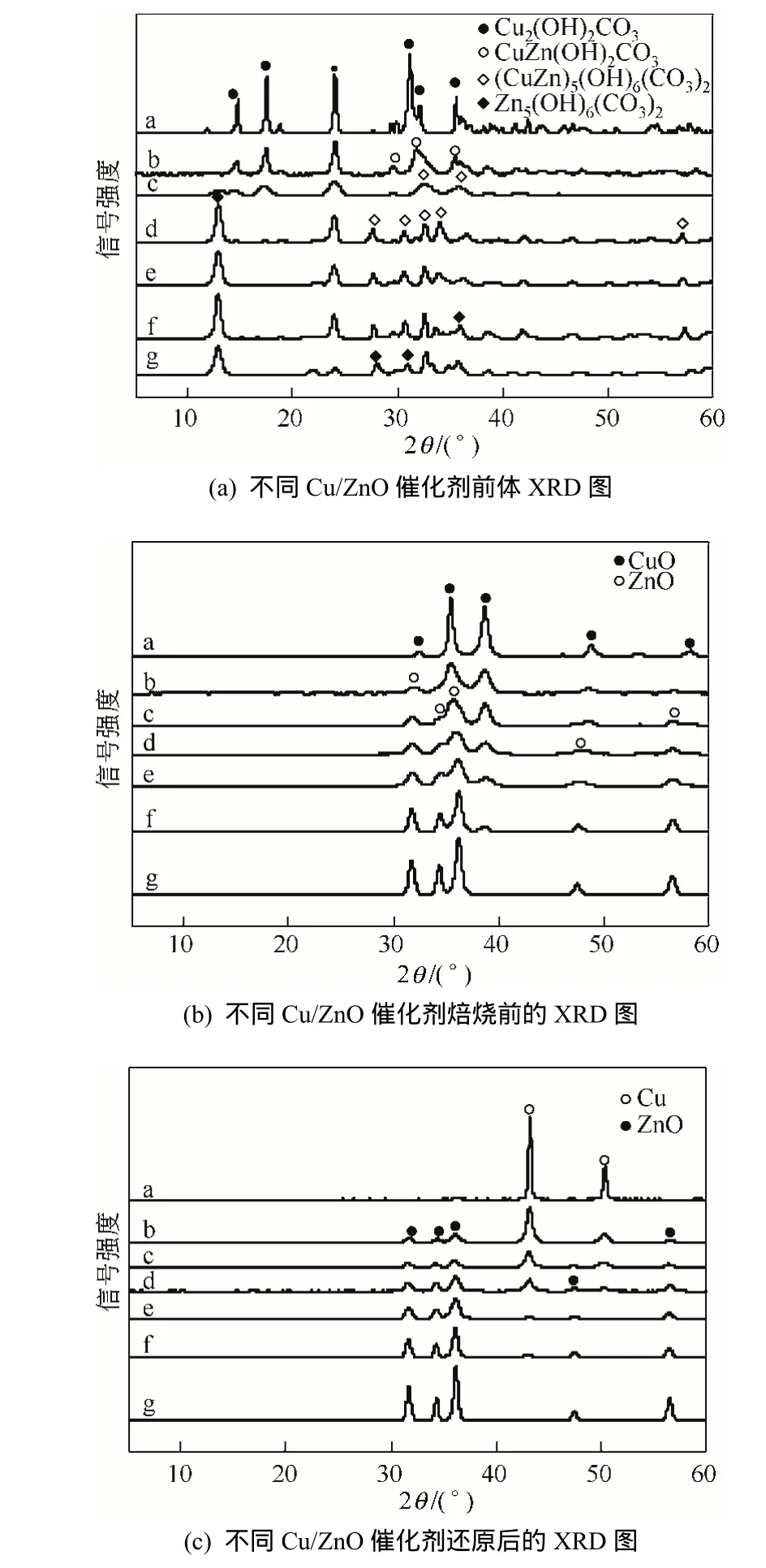
图5 不同Cu/ZnO催化剂处理过程中的XRD图
2.5 不同Cu/Zn摩尔比的Cu/ZnO催化剂的比表面积与催化活性的分析
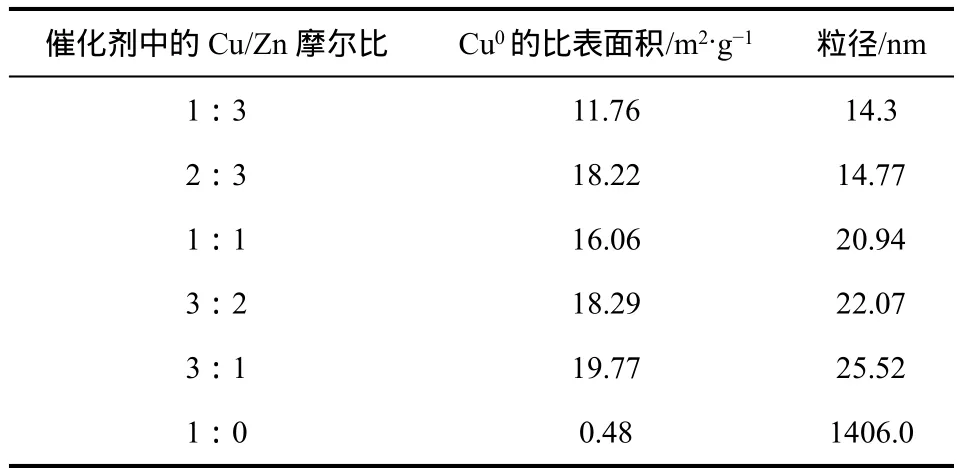
表1 不同比例Cu/ZnO催化剂还原后的Cu0比表面积与 粒径
采用N2O分解测定了不同比例的Cu/ZnO催化剂还原后的Cu0比表面积与粒径如表1中,由表1可以看出,ZnO的引入,铜的比表面积增加了2个数量级,虽然催化剂粒径与催化剂中铜的比例呈线性相关,但是Cu0比表面积与催化剂中铜的比例不呈线性相关,与前面的吡咯选择性相比较,也不呈线性相关。尽管Sodesawa等[20]在异丙醇在Cu/Al2O3催化剂上反应研究中,铜基催化剂的Cu0比表面积与反应产物的选择性呈线性关系,但是也有Nakamura等[21]在Cu/ZnO催化剂上的甲醇合成反应研究中,铜基催化剂的Cu0比表面积与铜的不同晶面有关[21],铜的不同晶面的催化活性可能不同,经本实验研究发现,Cu0比表面积也与铜的不同晶面有关。因此Cu/ZnO催化剂要发挥最佳的催化性能,不仅需要一个适宜的比表面积并且需要较为合适的铜晶面,才能使得ZnO较好的分散Cu颗粒,从而提高催化剂中的反应活性中心密度,提高反应活性。
2.6 反应条件的影响
本实验研究发现,反应条件(氨醇摩尔比、反应温度、空速)对反应结果存在一定的影响。所以选用Cu/Zn摩尔比为1∶1的Cu/ZnO催化剂作为1,4-丁二醇与氨反应合成吡咯反应的催化剂。选用条件为:常压、反应温度280℃、1,4-丁二醇的重时空速为0.46 h−1、氨醇摩尔比为1.1∶1。在考察单一反应条件因素对反应结果的影响时,均保证其他相应的反应条件不变。
2.6.1 反应温度的影响
1,4-丁二醇与氨反应合成吡咯为吸热反应,从热力学和动力学角度上分析,升高温度都有助于反应向吡咯反应方向进行,即提高吡咯的选择性及收率。从图6可知,随反应温度的从230℃升到300℃, 1,4-丁二醇的转化率基本保持在99%左右,吡咯的选择性为23.53%~58%。这与吸热反应的一般规律一致。在反应温度超过300℃的条件没有考察,是由于温度过高,容易导致Cu催化剂失活。因此,在该温度考察条件的范围内,280℃较适宜该反应进行。
2.6.2 反应重时空速的影响

图6 反应温度对反应结果的影响
从图7可知,随反应重时空速从1.84 h−1降低到0.368 h−1, 1,4丁二醇的转化率和吡咯的选择性分别为71.32%~100%和47.92%~59.25%,这是由于降低反应空速,增加了原料与催化剂的接触时间,进而提高了1,4-丁二醇的转化率和吡咯的选择性。进一步提高空速,吡咯的选择性和1,4-丁二醇的转化率变化不大。因此在该重时空速考察范围内,较适宜的重时空速为0.46 h−1。
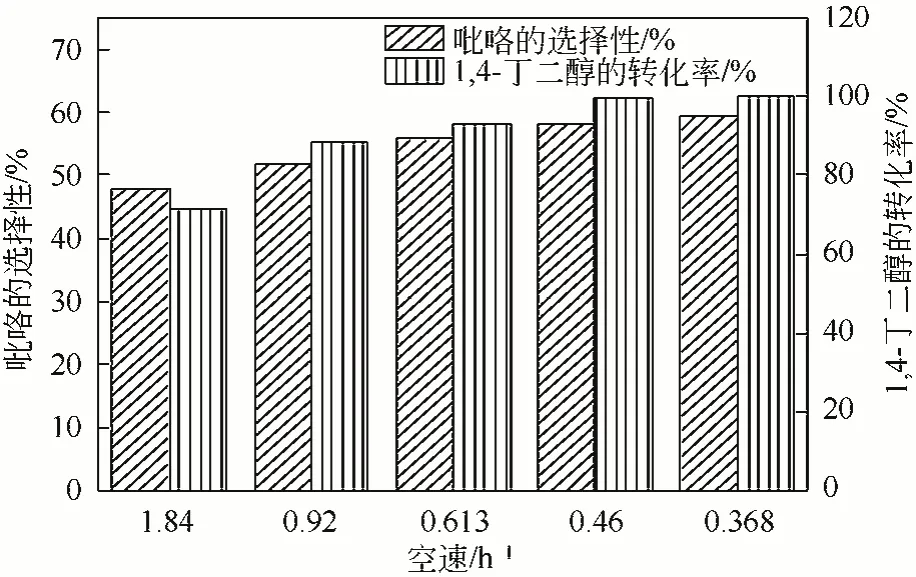
图7 反应重时空速对反应结果的影响
2.6.3 氨醇摩尔比的影响
从图8可知,氨醇摩尔比对吡咯的选择性影响较大。在氨醇摩尔比小于1.1∶1时,醇过量,使1,4-丁二醇不能完全转化成吡咯,易于发生分子内反应生成副产物γ-丁内酯;而氨醇摩尔比大于1.1∶1时,氨过量,吡咯的选择性也下降,这可能是由于氨过量,线时空速增大,使得原料在催化剂上的停留时间短导致的。因此在该氨醇摩尔比的考察范围内,较适宜的氨醇摩尔比为1.1∶1。
3 结论
(1)采用共沉淀法制备的Cu/ZnO催化剂成功的应用于1,4-丁二醇合成吡咯的反应当中。以Cu/Zn摩尔比为1∶1的Cu/ZnO催化剂的吡咯合成反应的适宜条件是:氨醇摩尔比为1.1∶1,反应温度为280℃,空速为0.46 h−1。在该条件下,1,4-丁二醇的转化率为100%,吡咯的选择性可达到了58%。

图8 氨醇摩尔比对反应结果的影响
(2)ZnO具有较好的稳定和分散Cu微晶的能力是由于在催化剂制备过程中Cu2+、Zn2+发生了同晶取代生成了CuZn(OH)2CO3、(CuZn)5(OH)6(CO3)2两种前体,在催化剂成型后,经还原后得到了具有高度分散Cu0的Cu/ZnO催化剂。
(3)以共沉淀法制备的Cu/ZnO催化剂的Cu0比表面积与催化剂的选择性不呈线性关系,与铜的不同晶面有关系。
[1]刘家峰,郭松坡,姜标.海洋溴吡咯生物碱的研究进展[J].有机化学,2005,25(7):788-799.
[2]陆阳,陶京朝,张志荣,等.新型吡咯类杀虫剂溴虫腈合成研究[J].化工中间体,2007(6):13-15,31.
[3]姬小明,张晓藴,赵铭钦,等.新型香料N-(2,5二甲基吡咯)亮氨酸异辛酯的合成及加香应用研究[J].香精香料化妆品,2011(4):6-10.
[4]胡小平,刘志虎,游丹,等.聚吡咯的制备、改性及应用进展[J].化工新型材料,2012,40(7):110-113.
[5]诸平,张文根,敬云.吡咯的研究史探析[J].渭南师专学报:自然科学版,1998,13(5):11-15.
[6]Joachim Wulff-D öring,Michael Hesse,Peter Wahl.Preparation of pyroles:US,006162928A[P].2000-12-19.
[7]赵珊珊,徐卫华,赵继全.四氢呋喃催化氨化合成吡咯烷[J].石油学报,2012,28:127-132.
[8]温晓燕,气相催化合成四氢吡咯的研究进展[J].应用化工,2007,36(9):913-915.
[9]朱照琪.气固相催化反应合成吡咯[D].北京:北京化工大学,2004.
[10]胡云峰,李俊飞,道日吉巴图,等.Cu系催化剂在醇类脱氢反应中的应用研究进展[J].炼油与化工,2011,22(6):1-6.
[11]刘志坚,廖建军,谭经品.甲醇合成催化剂Cu-ZnO的共沉淀机理研究[J].石油化工,1998,27(7):479-483.
[12]王振旅,马红超,朱万春,等.在纳米Cu-ZnO上仲丁醇的催化脱氢[J].高等学校化学学报,2002,23(11):2163-2165.
[13]曹金鹏,胡云峰,徐鹏,等.Cu负载型催化剂用于乙醇氨化合成乙腈[J].化工进展,2011,30(5):1013-1018.
[14]姜广申,胡云峰,蔡俊,等.仲丁醇脱氢制甲乙酮的Cu-ZnO催化剂[J].化工进展,2013,32(2):352-358.
[15]耿丽娜.聚吡咯的制备、表征及气敏性研究[J].河北师范大学学报,2010,34(6):686-630.
[16]Yarlagadda V Subba Rao,Shivanand J Kulkarni,Machiraju Subrahmanyam,et al.Modified ZSM-5 catalysts for the synthesis of five-and six-membered heterocyclics[J].J.Org.Chem.,1994,59(14):3998-4000.
[17]Chary K V R,Sagar G V,Srikanth C S,et al.Characterization and catalytic functionalities of copper oxide catalysts supported on zirconia[J].J.Phys.Chem.B,2007,111(3):543-550.
[18]Sagar G V,Rao P V R,Srikanth C S,et al.Characterization and catalytic functionalities of copper oxide catalysts supported on zirconia[J].J.Phys.Chem.B,2006,110(28):13881-13888.
[19]Spencer M S.The role of zinc oxide in Cu/ZnO catalysts for methanol synthesis and the water–gas shift reaction[J].Topics in Catalysis,1999,8(3-4):259–266.
[20]Pepe F,Angeletti C,Rossi S,Jacono Lo M.Catalytic behavior and surface chemistry ofcopper/alumina catalysts forlsopropanol decomposition[J].J.Catal.,1985,91:69-77.
[21]Nakamura I,Fujitani T,Uchijima T,et al.A model catalyst for methanol synthesis:Zn-deposited and Zn-free Cu surfaces[J].J.Vac.Sci.Technol.A,1996,14(3):1464-1468.
