HPLC测定复方头孢克洛胶囊含量、含量均匀度及溶出度的研究
2014-06-07张琼杨利红苏蕊
张琼 杨利红 苏蕊
复方头孢克洛胶囊处方源于德国药物目录(Pharm Ndex)收载的MUCO Panoral-250,马丁代尔药典(Martndale)也收载了头孢克洛的多组分制剂(Multiingrendient Preparation),Ger( 德 国 ):MUCO Panoral,具有抗感染、止咳祛痰等功效[1-3]。本实验建立以乙腈-0.025 mol/L磷酸二氢钾溶液(用磷酸调节pH值至3.0)(22:78)为流动相HPLC方法,同时测定复方制剂中头孢克洛和溴己新的含量、含量均匀度及溶出度,其专属性强、灵敏度高、操作简便,可更有效地控制药品质量[4-6]。
1 材料
1.1 仪器 岛津2010A HCT液相色谱仪(紫外检测器,工作站),Satorius CP2115天平。
1.2 试药与试液 头孢克洛(批号:130481-200904)、盐酸溴己新(批号:100427-200301),上述对照品均来自中国药品生物制品检定所。乙腈:色谱级,其他试剂均为分析纯,实验用水为超纯水(Milli-Q Plus超纯水系统)制备。
2 方法
2.1 色谱条件 色谱柱:Waters Shield RP C18(4.6 mm×250 mm,5 μm)色谱柱;流动相:乙腈-0.025 mol/L磷酸二氢钾溶液(用磷酸调节pH值至3.0)(22:78);流速1.0 mL/min,柱温30 ℃,检测波长249 nm;进样量:20 μL。理论板数:以溴己新计为11 215;分离度:头孢克洛与溴己新的分离度为36.14。该色谱条件下的色谱图见图1。
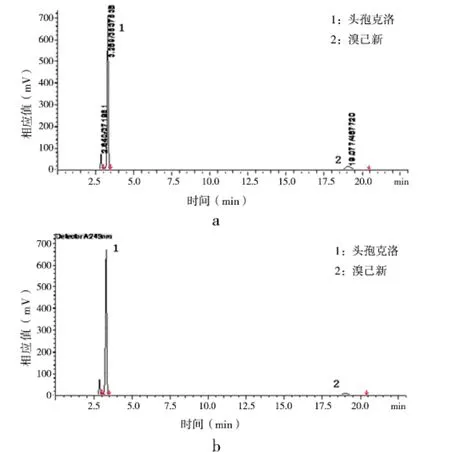
图1 复方头孢克洛胶囊HPLC色谱图
2.2 试验方法 取本品20粒,精密称取其内容物(约相当于头孢克洛50 mg),置100 mL量瓶中,加甲醇30 mL溶解,超声15 min助溶,冷却至室温,加流动相稀释至刻度,摇匀,滤过,取续滤液作为供试品溶液;取盐酸溴己新对照品约32 mg,置100 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀;精密量取上述溶液5 mL,置100 mL量瓶中,加入精密称取的头孢克洛对照品约50 mg,加流动相溶解稀释至刻度,摇匀,作为对照品溶液。精密量取供试品溶液和对照品溶液各20 μL分别注入液相色谱仪,记录色谱图,按外标法以峰面积计算,即得。
3 方法学考察
3.1 含量均匀度的测定
3.1.1 含量均匀度线性试验 精密称取盐酸溴己新对照品22.95 mg置10 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀;精密量取上述溶液2 mL,置50 mL量瓶中,加入精密称取的头孢克洛对照品124.41 mg加流动相溶解并稀释至刻度,摇匀,作为对照品储备液;精密量取对照品储备液3、4、5、6、7、9 mL置25 mL量瓶中,加流动相稀释至刻度,摇匀,制成系列浓度的溶液,按照上述色谱条件依法测定,以浓度与其峰面积进行线性回归,结果头孢克洛和盐酸溴己新回归方程分别为:Y=19 702X+46 386,r=1.0000;Y=28 912X+1334.2,r=1.0000。线性范围分别为280.97~842.90 μg/mL和11.00~33.01μg/mL。
3.1.2 精密度试验 精密量取含量测定项下的对照品溶液20 μL,按照上述色谱条件,连续进样5次,计算头孢克洛和盐酸溴己新峰面积的RSD分别为0.11%和0.24%。试验结果表明本方法的精密度良好。
3.1.3 重复性试验 取批号为13020401的复方头孢克洛胶囊内容物各6份,分别按照“2.2”项下方法进行重复性试验。结果头孢克洛和溴己新含量(标示量%,n=6)分别为101.3%和99.6%,RSD分别为0.09%和0.91%。
3.1.4 加样回收试验 精密称取盐酸溴己新对照品16、20 mg和24 mg分别置25 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀;精密量取上述溶液2 mL,置10 mL量瓶中,分别加入精密称取的头孢克洛40、50 mg和60 mg,加流动相溶解并稀释至刻度,摇匀,作为储备液(低、中、高浓度溶液各平行制备3份);另取已测知头孢克洛和溴己新含量的批号为13020401的复方头孢克洛胶囊内容物约16 mg(n=9),分别置50 mL量瓶中,精密加入各浓度水平的储备液2.5 mL,加流动相溶解并稀释至刻度,摇匀,按上述色谱条件进行加样回收试验。结果复方头孢克洛胶囊中头孢克洛低、中、高3种浓度的平均回收率(n=3)分别为99.8%(RSD=0.25%)、100.1%(RSD=0.35%)和100.3%(RSD=0.86%),溴己新低、中、高3种浓度的平均回收率(n=3)101.2%(RSD=0.47%)、100.9%(RSD=0.68%)和100.4%(RSD=0.98%)。
3.1.5 溶液的稳定性考察 取含量测定下的供试品溶液,按上述色谱条件,在0、2、4、8、12、25 h依法测定头孢克洛和溴己新的峰面积,结果RSD(n=6)分别为0.60%和0.53%,表明溶液中头孢克洛和溴己新在25 h内稳定。
3.1.6 含量均匀度考察 应用本文建立的HPLC含量测定方法,进行两个批号分别为13020401和131108的复方头孢克洛胶囊中溴己新含量均匀度检查。取供试品1粒,置100 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,滤过;精密量取续滤液5 mL置25 mL量瓶中,加流动相稀释至刻度,摇匀,作为供试品溶液,按照含量测定项下的方法测定,同时按复方头孢克洛胶囊现行标准,以氯仿为溶剂,采用紫外分光光度法在252 nm波长处测定溴己新的含量均匀度[7-8]。两种方法测定的结果有明显差异,见表1。

表1 溴己新含量均匀度测定结果
3.2 溶出度测定
3.2.1 溶出实验 本实验结合《中国药典》2010年版二部中头孢克洛胶囊[9],盐酸溴己新片与复方头孢克洛胶囊现行标准YBH04602003中溶出度的方法[8],照《中国药典》2010年版二部附录XC第一法,以水900 mL为溶剂,转速为100 r/min,依法操作,测定了两批复方头孢克洛胶囊的溶出曲线,经5、15、30、45、60 min时取溶出液10 mL,用有机膜滤过[9],至少弃去初滤液5 mL,取续滤液作为供试品溶液;另取头孢克洛与盐酸溴己新对照品各适量,制成相应浓度对照品溶液,照2.1色谱条件,精密量取供试品溶液和对照品溶液各50 μL分别注入液相色谱仪,记录色谱图,按外标法以峰面积计算,计算头孢克洛和溴己新不同时间的溶出量。溶出实验结果表明,30 min,6粒胶囊中头孢克洛平均溶出量达到90%以上,溴己新平均溶出量达到70%以上,6粒胶囊中头孢克洛与溴己新的溶出曲线见图2~3。
3.2.2 溶出度线性关系试验 取盐酸溴己新对照品20.70 mg置10 mL量瓶中,加乙醇5 mL溶解,加水稀释至刻度,摇匀;精密量取上述溶液2 mL置25 mL量瓶中,加入精密称取头孢克洛对照品125.50 mg,加水溶解并稀释至刻度,摇匀,作为对照品储备液。精密量取对照品储备液3、4、5、8 mL和10 mL置100 mL量瓶中,加溶出介质稀释至刻度,摇匀,制成系列浓度的溶液,按照2.1色谱条件,精密量取50 μL注入液相色谱仪,记录色谱图,以浓度与其峰面积进行线性回归,结果头孢克洛和盐酸溴己新回归方程分别为:Y=18 166X+3 737 535,r=0.9991;Y=63 769X-30 211,r=0.9991。线性范围分别为141.71~472.38 μg/mL和4.83~14.53 μg/mL。
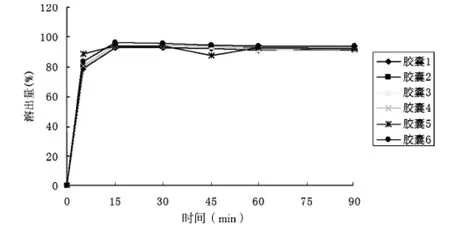
图2 头孢克洛溶出曲线图
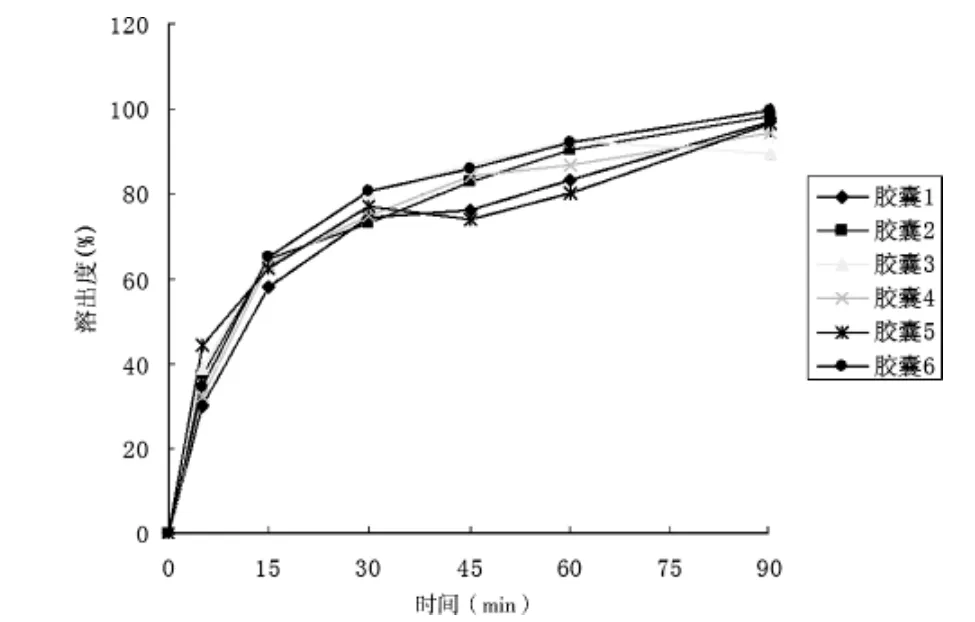
图3 溴己新溶出曲线图
3.2.3 加样回收试验 精密称取盐酸溴己新对照品16 mg、20 mg和24 mg分别置20 mL量瓶中,加适量乙醇(每2 mg加乙醇1 mL)溶解,加水稀释至刻度,摇匀;精密量取上述溶液2 mL,置25 mL量瓶中,分别加入精密称取的头孢克洛50、62和74 mg,加水溶解并稀释至刻度,摇匀,作为储备液(低、中、高浓度溶液各平行制备3份);另取已测知头孢克洛和溴己新含量的批号为13020401的复方头孢克洛胶囊内容物约16 mg(n=9),分别置100 mL量瓶中,精密加入各浓度水平的储备液5 mL,加水溶解并稀释至刻度,摇匀,按2.1色谱条件,精密量取50 μL注入液相色谱仪,进行加样回收试验。结果复方头孢克洛胶囊中头孢克洛低、中、高3种浓度的平均回收率(n=3)分别为99.6%(RSD=0.22%)、100.0%(RSD=0.50%)和100.2%(RSD=0.64%),溴己新低、中、高3种浓度的平均回收率(n=3)100.8%(RSD=0.72%)、101.3%(RSD=0.88%)和99.9%(RSD=0.47%)。
3.2.4 溶液的稳定性考察 取30 min溶出液作为供试品溶液,按上述色谱条件,在0、2、4、8、12 h依法测定头孢克洛和溴己新的峰面积,结果RSD(n=5)分别为0.34%和0.55%,表明溶液中头孢克洛和溴己新在12 h内稳定。
3.2.5 滤膜的吸附作用 取30 min溶出液,分别将原液,无机膜过滤弃去1、2、5 mL初滤液后的溶出液与有机膜过滤弃去1、2、5 mL初滤液后溶出液,精密量取50 μL注入液相色谱仪,记录色谱图,结果表明有机膜过滤弃去5 mL初滤液的溶出液中,头孢克洛与溴己新测定值均与原液测定值的平均偏差小于0.02%,可消除滤膜对头孢克洛与溴己新的吸附影响。
4 讨论
国内现行标准均采用0.005 mol/L四丁基氢氧化铵溶液(用磷酸调节pH值至3.2)-甲醇(62:38)为流动相测定含量,该种试剂对色谱柱损伤大、系统平衡时间长,本文选用磷酸盐溶液为流动相,大幅减少对色谱柱的损伤,头孢克洛与溴己新不仅可同时检出,且分离良好[10-12]。
本文采用HPLC法检测溴己新的均匀度,成功避免了原标准中有毒挥发性试剂-氯仿的使用,具有专属性强、灵敏度高、操作简便、结果准确可靠的特点,同时保护了检验人员的健康。
本文方法可同时测定头孢克洛和溴己新的溶出度,较原标准中仅能检测头孢克洛单一组分的溶出量,可进一步提高该产品质量控制。
[1]何其伟,何其庄,鞠萍,等.复方头孢克洛胶囊处方的优选[J].上海师范大学学报(自然科学版),2002,31(1):74-77.
[2]李新.县级医疗机构中抗生素合理应用的情况分析[J].中国医学创新,2011,8(25):132-133.
[3]金晓威,郑小平,张丽珍,等.静脉药物配置中心常见差错分析及防范[J].中国医学创新,2011,8(34):111-112.
[4]蔡育红,钟慧敏.复方头孢克洛片分剂量的稳定性试验[J].广东药学院学报,2013,29(3):237-239.
[5]贲春梅.南通市老年康复医院门诊处方抗感染药物不合理应用420例分析[J].中国医学创新,2010,7(22):78-79.
[6]吴巧稚,王霆,杨冬玲,等.复方头孢克洛溴己新及其同类药研究进展[J].中国药师,2010,13(5):728-730.
[7]攻丽萍,杨娜,谢元超.HPLC测定复方头孢克洛颗粒的含量[J].中国药品标准,2010,11(6):440-442.
[8]国家食品药品监督管理总局.YBH04602003药品标准:复方头孢克洛胶囊[S].2013.
[9]国家药典委员会.中国药典[M].第2版.北京:中国医药科技出版社,2010:188-190,799-800.
[10]刘卫东,王建成,付庆霞.金刚藤分散片中薯蓣皂苷元HPLC法测定研究[J].中国医学创新,2012,9(2):3-5.
[11]莫碧芳,黄天国,欧静.医院重症病房抗生素合理应用调查及药敏分析[J].中国医学创新,2011,8(8):128-130.
[12]伍良勇,莫兰芳.HPLC法测定麦角隐亭咖啡因片的溶出度和含量均匀度[J].中国药品标准,2009,10(1):55-57.
