紫外分光光度法测定酪氨酸手性固定相键合量
2014-05-14曹月林彭奇均
曹月林,彭奇均
(江南大学化学与材料工程学院,江苏无锡 214122)
配体交换色谱是最为简便有效的拆分DL-氨基酸方法,其中手性固定相起着至关重要的作用。氨基酸作为廉价易得的手性配体,常用于配体交换手性固定相的合成。自 Dovankov与 Gübitz[1]建立发展配体交换色谱以来,不同氨基酸配体交换手性固定相时有报道,如 L-脯氨酸固定相[2-4]、L-苯丙氨酸固定相[5-6]、L-羟脯氨酸固定相[7-8]。氨基酸配体在固定相中的含量影响固定相的分离效果,与配体结合能力较强的待分离物应选择配体键合量少的固定相,与配体结合能力弱的待分离物应选择配体键合量高的固定相[9]。氨基酸亦可用于分离其他手性化合物的固定相合成[10]。
在前人的研究中,配体键合量的测定均采用元素分析法[3-10],但元素分析仪器要求高,普通实验室受仪器制约。可代替元素分析法使用的键合量测定方法仍未检索到。
氨基酸中含有氮元素,氮含量的测定方法较多,如凯氏定氮法[11]、紫外分光光度法[12]等。凯氏定氮法操作繁琐,需要特定的消解瓶,耗时,耗电,释放SO2有害气体;紫外分光光度法操作简单,普通紫外分光光度计和比色管即可,方便快捷。本文建立了紫外分光光度法测定酪氨酸手性固定相键合量的新方法,测定了酪氨酸手性固定相键合量,并与元素分析法进行比较,该方法准确可靠,为氨基酸手性固定相键合量的测定提供了一种新的参考方法。
1 实验部分
1.1 试剂与仪器
KH-560键合硅胶(38 μm)、酪氨酸手性固定相(38 μm)均为自制;过硫酸钾、硝酸钾、氢氧化钠、氯化镁、氯化钙、碳酸钠、硅酸钠均为分析纯。
TU-1901紫外分光光度计;VARIOEL III元素分析仪;MLS-3750高压蒸汽灭菌器;AL204电子分析天平。
1.2 实验原理
氨基酸手性固定相的基质是硅胶,其化学组成为SiO2,不溶于水,但可与强碱反应[13]。手性固定相以氢氧化钠溶液溶解,氨基酸配体游离到溶液中,120~124℃,配体中的有机氮被碱性过硫酸钾消化为硝酸盐[12],见图1。
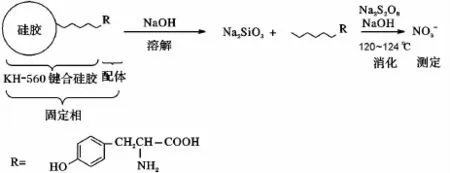
图1 键合量测定示意图Fig.1 Scheme of ligand content determination process
1.3 溶液配制
1.3.1 硝酸根标准溶液 按中华人民共和国环境保护标准 HJ 636—2012规定方法配制10 μg/mL(以氮计)硝酸根标准溶液。
1.3.2 样品待测液的制备 准确称取酪氨酸手性固定相0.1 g于10 mL比色管中,加入2 mL 0.6~1.0 mol/L NaOH溶液,55~75℃水浴至固定相全部溶解,冷却,稀释至刻度。
1.3.3 消化液的制备 取1.0~2.0 mL样品待测液于25 mL比色管中,按中华人民共和国环境保护标准 HJ 636—2012规定方法进行消化,稀释至25 mL。
1.4 硝酸根标准曲线的绘制
按中华人民共和国环境保护标准 HJ 636—2012规定方法进行绘制,见图2。

图2 硝酸根标准曲线Fig.2 Standard curve of nitrate ion
1.5 实验方法
取消化液 5 mL于 25 mL比色管中,加入3 mL 1 mol/L氯化镁(氯化钙),摇匀,加水稀释至10 mL,静置 60 min。取上清液于带孔径 <0.45 μm的针式过滤头的一次性注射器中,将滤液过滤至10 mm比色皿中。以水为参比,测定275,220 nm下吸光度[12],校正吸光度 A=A220-2A275。同时设置KH-560键合硅胶为空白。按下式计算:
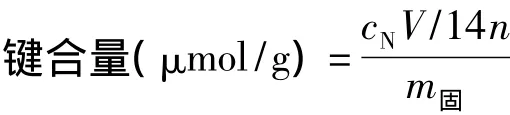
式中 cN——扣除空白后的A带入线性方程计算硝态氮浓度,μg/mL;
V——溶液稀释体积,mL;
n——氨基酸分子中氮原子个数;
m固——固定相样品质量,g。
2 结果与讨论
2.1 固定相溶解条件的确定
取0.1 g酪氨酸手性固定相于10 mL不同浓度的氢氧化钠溶液中,不同水浴温度下溶解,至完全溶解的时间见表1。

表1 不同氢氧化钠浓度和溶解温度下固定相溶解时间Table 1 Dissolved times of CSP in sodium hydroxide with different concentrations at different temperatures
由表1可知,同一温度下,氢氧化钠浓度不影响溶解时间,随温度升高,溶解时间缩短,95℃需2.5 min,75 ℃需4.5 min,55 ℃需16 min。95 ℃时水浴温度高,不易控制,75℃水浴条件相对温和且固定相可快速溶解。
取10 mL不同浓度的氢氧化钠溶液,准确加入0.1 g固定相,75℃水浴溶解,待溶解后继续加入,至不再溶解,加至2 g,冷却,过滤,烘干称重,计算溶解度,结果见表2。
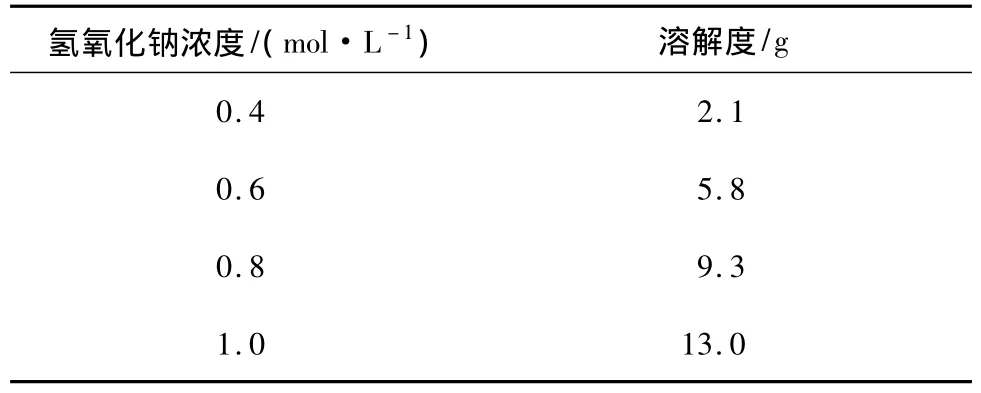
表2 不同浓度氢氧化钠溶液中固定相溶解度Table 2 Solubility of CSP in sodium hydroxide with different concentrations
由表2可知,固定相溶解度与氢氧化钠浓度呈正相关,氢氧化钠浓度在0.4~1.0 mol/L,浓度每增加0.2 mol/L,溶解度增加约3.7 g,固定相溶解的实质是基质中的二氧化硅与氢氧化钠的反应,氢氧化钠总量决定了固定相溶解量。实际溶解过程中,取0.1 g固定相,加入2 mL 浓度0.6 ~1.0 mol/L 氢氧化钠溶液,即固液比为1∶20(m∶V),可保证固定相全部溶解。确定溶解条件为:氢氧化钠浓度0.6~1.0 mol/L,75 ℃,固液比1∶20(m∶V)。
2.2 测定条件的确定
2.2.1 干扰物的确定 过硫酸钾将有机氮转化为硝态氮,有机碳被转化为碳酸根[14],同时体系中含有硅酸根。硝态氮在 220,275 nm双波长下测定[12],结果见图 3。
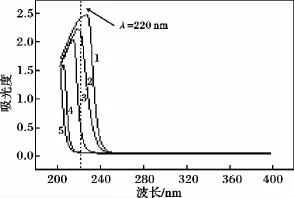
图3 紫外光谱Fig.3 UV spectrograms
由图3可知,硅酸根、碳酸根在220 nm处产生干扰,使测定结果偏大。测定时应除去硅酸根和碳酸根。硅酸根和碳酸根的镁盐、钙盐是难溶或微溶于水的沉淀[13],沉淀法可有效除去硅酸根和碳酸根。沉淀剂应在220 nm和275 nm处无吸收。由紫外光谱可知,氯化镁和氯化钙是良好的沉淀剂。
2.2.2 过滤介质的影响 取适量固定相消化液于25 mL比色管中,加入沉淀剂,分别以滤纸和针式滤头(0.8,0.45,0.22 μm)过滤,测定 220,275 nm 吸光度,结果见表3。

表3 过滤介质的影响Table 3 Influence of filter media
由表3可知,滤纸和0.8 μm针式过滤头孔径过大,无法除去细小沉淀颗粒,使A220、A275大于沉淀前。针式过滤头孔径小于0.45 μm,275 nm处基本无吸收,A220趋于稳定。过滤时应取孔径<0.45 μm的针式过滤头过滤。
2.2.3 静置时间的影响 取5 mL消化液,加入5 mL 1 mol/L的沉淀剂,结果见图4。
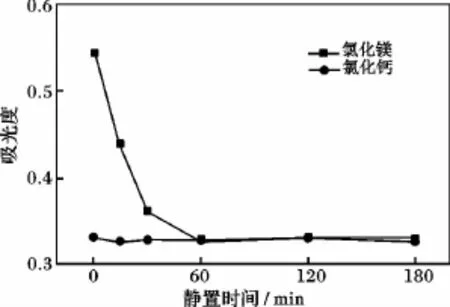
图4 静置时间的影响Fig.4 Influence of quiescence time
由图4可知,氯化镁作为沉淀剂,需静置至少60 min。硅酸镁难溶于水[13],直接以沉淀形式析出。碳酸镁微溶于水[13],在水中其水解成难溶的氢氧化镁[15]:
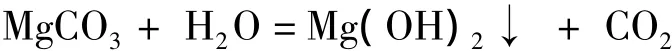
静置过程不仅使沉淀沉降便于过滤,同时使碳酸镁水解成氢氧化镁,测定结果更加准确。氯化钙作为沉淀剂,无需静置,硅酸钙、碳酸钙均难溶于水[13],以沉淀形式析出。但实际操作中,不静置直接过滤,滤头堵塞,过滤困难,静置60 min使沉淀沉降是必要的。
2.2.4 沉淀剂加入量的影响 在前述确定的条件基础上,取5 mL消化液,加入1~5 mL浓度1 mol/L的沉淀剂,结果见图5。
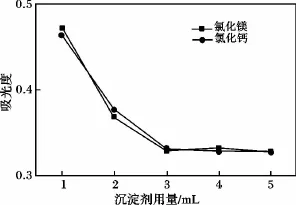
图5 沉淀剂用量的影响Fig.5 Influence of precipitating agent dosage
由图5可知,氯化镁和氯化钙用量小于3 mL,干扰物排除不完全,校正吸光度偏大;≥3 mL后,硅酸根、碳酸根被完全沉淀,校正吸光度趋于稳定。同时,实验中发现,由于消化液中存在由过硫酸钾转化的硫酸根[12],氯化钙加入量过多,生成微溶的硫酸钙,沉淀量增加,易堵塞滤头,难以过滤。以氯化钙为沉淀剂,加入量以3 mL为宜。
2.3 酪氨酸固定相样品键合量测定
2.3.1 方法精密度及加标回收率 取样品待测液1.0 ~2.0 mL,按实验方法进行测定,结果见表4。

表4 精密度实验结果Table 4 Reproducibility of determination of ligand content
由表 4可知,固定相溶液取样量在 1.0~2.0 mL,多次测定结果的相对标准偏差(RSD)均<2%,证明本方法的精密度较高。
分别取同一酪氨酸固定相样品待测液1 mL于25 mL比色管中,加入0~3 mL 10 μg/mL NO3-标准溶液,测定本底量和加标测出量,以硝态氮含量计,计算加标回收率,结果见表5。

表5 加标回收率Table 5 Results of recovery
由表5可知,加标回收率在98.0% ~104%,说明该方法可靠,测定准确度较高。
2.4 对比实验
分别采用紫外分光光度法和元素分析法测定酪氨酸固定相键合量。元素分析法在CHNS模式(炉1:1 150℃,炉2:850℃)下进行,按下式计算键合量(μmol/g),结果见表 6。
式中 N键合硅胶——KH-560键合硅胶氮百分含量,%;
N固——固定相样品氮百分含量,%;
n——氨基酸分子中氮原子个数。

表6 两种方法测定结果比较Table 6 Comparison of the measurement results of the two methods
由表6可知,两种方法均能准确测定酪氨酸手性固定相键合量,元素分析法与紫外分光光度法相对误差3.7%,结果相近。紫外分光光度法可作为元素分析法的替代和补充方法使用。
3 结论
(1)建立了一种紫外分光光度法测定氨基酸手性固定相键合量的新方法。以此方法测得自制酪氨酸手性固定相配体含量为161 μmol/g,RSD<2%,加标回收率在98.0% ~104%,与元素分析法相对误差3.7%,说明该方法准确可靠。该方法降低了仪器要求,具有较高的广泛性与普遍性。
(2)该方法的实质是测定氨基酸配体中的氮元素,亦可用于测定其他氨基酸配体的手性固定相键合量,具有一定的通用性。该方法提供了元素分析法之外新的参考方法,具有重要的实用价值。
[1]Martin G Schmid,Gerald Gübitz.Chiral separation by ligand-exchange[J].Macedonian Journal of Chemistry and Chemical Engineering,2011,30(2):127-137.
[2]Sugden K,Hunter C,Lloyd-Jones G.Ligand-exchange chromatography:I.Resolution of L-and D-proline on a copper(II)-proline complex bound to microparticulate silica gel[J].Journal of Chromatography,1980,192:228-231.
[3]马桂娟.L-脯氨酸聚合物键合手性配体交换色谱固定相Ⅰ的制备及应用[J].吉林农业,2011(12):68-70.
[4]Shi Hongyu,Zhang Haizhu.Modification of chiral stationary phases with L-proline as a selector for ligand-exchange chromatography via introducing hydrophobic groups[J].Chem Res Chinese Universities,2009,25(6):822-826.
[5]章文军,梁莉,李慧.L-苯丙氨酸手性固定相的制备[J].精细化工,2012,29(3):272-275.
[6]Sun Yang,Xu Fei,Gong Bolin.Preparation of L-phenylalanine chiral ligand-exchange chromatographic stationary phase by atom transfer radical polymerization and resolution of racemates[J].Chinese Journal of Chromatography,2011,29(9):918-922.
[7]马桂娟,龚波林,阎超.L-异亮氨酸聚合物手性配体交换固定相的制备及对DL-氨基酸的拆分[J].分析化学,2008,36(3):275-279.
[8]祝馨怡,张玉华,孙伟,等.L-羟基脯氨酸键合手性配体交换色谱固定相的制备及手性拆分[J].分析科学学报,2003,19(2):124-126.
[9]祝馨怡,韩小茜,齐邦峰,等.硅胶键合手性配体交换色谱固定相键合量对 α-氨基酸拆分的影响[J].色谱,2002,20(3):223-226.
[10]谢生明,彭雅,张美,等.氨基酸聚合物作为高效液相色谱手性固定相的研究[J].分析试验室,2013,32(2):1-5.
[11]中华人民共和国国家质量监督检验检疫总局.GB/T 5511—2008谷物和豆类 氮含量测定和粗蛋白质含量计算 凯氏法[S].北京:中国标准出版社,2008.
[12]中华人民共和国环境保护部.HJ 636—2012水质 总氮的测定碱性过硫酸钾消解紫外分光光度法[S].北京:中国环境科学出版社,2012.
[13]大连理工大学无机化学教研室.无机化学[M].5版.北京:高等教育出版社,2006.
[14]董振芳,刘峰,姚乔尔.过硫酸钾氧化法测定水中总有机碳[J].黄渤海海洋,2002,20(2):113-117.
[15]周昌勇.MgCO3转化为 Mg(OH)2的问题探究[J].化学教育,2012(10):73-76.
