观察改良TIPS在治疗门静脉高压消化道出血中的应用
2014-05-09李常青李洪璐郭江魏建赵东蔡亮刁振赢杜宏柳罗燕
李常青 李洪璐 郭江 魏建 赵东 蔡亮 刁振赢 杜宏柳 罗燕
•综合介入•
观察改良TIPS在治疗门静脉高压消化道出血中的应用
李常青 李洪璐 郭江 魏建 赵东 蔡亮 刁振赢 杜宏柳 罗燕
目的 观察改良TIPS在胃食管出血应用中的技术可行性及临床效果。方法 收集接受改良TIPS治疗的肝硬化门静脉消化道出血的患者56例。操作技术改良是在线阵血管探头引导下穿刺右颈内静脉,引入导丝并将Rups-100穿刺系统送至肝右静脉,自肝静脉向门静脉穿刺成功后,引入加强硬度导丝至肠系膜上静脉,撤出Rups-100穿刺系统,直接将8 mm×40 mm球囊经12F鞘沿加硬导丝快速通过肝静脉-肝实质-门静脉,扩张球囊并保留球囊上肝静脉和门静脉切迹图像。支架技术改良是先释放1枚8 mm×60 mm的裸支架,根据球囊切迹,再释放1枚8 mm×40 mm的覆膜支架,覆膜部分覆盖实质全程而不阻挡同侧门静脉入肝血流,其余部分伸入肝静脉内,常规用弹簧栓子和明胶海绵栓塞胃冠状静脉。测量分流前后门静脉压力变化。结果 56例均获得技术性成功,成功率为100%。分流道建立前后门静脉压力分别为(31.20±3.98)mmHg和(17.36±3.48)mmHg,平均下降幅度为(13.839±2.585)mmHg(t=40.062,P<0.001)。随访1~3年。1、2、3年分流道通畅率分别为89.3%、75.0%、67.8%;再出血率分别为7.1%、12.5%、16.1%;肝性脑病发生率为12.5%。有1例术后第2天出现腹腔感染,抗感染治疗7天后好转;有7例于术后1~3年内因分流道完全闭塞而复发再出血,分别给予了介入开通和覆膜支架植入。所有病例均未出现其他严重并发症。5例在随访期间分别死于肝衰竭、肝癌和多器官衰竭。结论 通过对支架的改良,采用模拟Viatorr支架方法能够提高TIPS分流道的中远期通畅率,降低再出血率;简化TIPS操作步骤可减少与技术操作相关的并发症。
肝硬化; 门静脉高压; 改良TIPS; 支架
TIPS作为一项微创技术已经在治疗肝硬化门静脉高压消化道出血中得以较广泛的应用,疗效确切。然而,裸支架较高的分流道狭窄和闭塞率阻碍了该项技术的发展。 Viatorr支架的问世和应用,使TIPS进入了一个新时代,但Viatorr支架至今尚未进入我国市场。为了提高TIPS的治疗效果,改善其预后,笔者采用模拟Viatorr支架及简化TIPS操作方法(改良TIPS)治疗肝硬化门静脉高压消化道出血和顽固性腹腔积液患者56例,取得了满意的临床效果,报道如下。
对象与方法
一、临床资料
2009年6月—2012年6月接受模拟Viatorr支架方法治疗肝硬化消化道出血的患者56例,其中乙肝后肝硬化47例,丙肝后肝硬化6例,酒精性肝硬化2例,病因不明者1例。内镜下治疗后复发再出血者53例,外科脾切除+断流术后复发再出血者3例,同时合并顽固性腹腔积液者9例、脐疝者3例。患者在TIPS前均进行了CT三期扫描。
二、治疗方法
1.操作技术改良:术前常规分析CT三期扫描,了解肝静脉与门静脉的空间关系,确定穿刺深度与角度,并重新塑型穿刺针。在线阵探头引导下,取右颈内静脉为穿刺入路,将超滑导丝引入下腔静脉,沿导丝将Rups-100穿刺系统送至肝静脉开口附近,在导向器的作用下把导丝引入肝右静脉,沿导丝将Rups-100穿刺系统送至肝右静脉约1~2 cm处,快速完成自肝静脉向门静脉的穿刺,拔出针芯1~2 s后可见褐色血液涌出,手推造影证实为靶血管,将导丝引入门静脉主干,沿导丝将5F造影导管送至门静脉主干,造影、测压,更换加硬导丝,保留12F血管鞘于肝静脉内,沿加硬导丝快速将8 mm×40 mm球囊通过肝静脉壁—肝实质—门静脉壁(摒弃Rups-100穿刺系统强行开通分流道),扩张球囊并保存肝静脉和门静脉壁的切迹图像图1、2。
2.支架技术改良:先释放8 mm×60 mm裸支架(Astron,Biotronik GmbH Co.)一枚,保留1~2 cm伸向门静脉分叉部,然后参照球囊切迹释放8 mm×40 mm覆膜支架(Fluency Plus Vascular Stent Graft,BARD Co.)1枚,力求覆盖肝实质全程而不阻挡同侧门静脉入肝血流,造影、测压,常规用不同型号的弹簧栓子栓塞胃冠状静脉和胃短静脉。术后口服阿司匹林(50 mg/d)常规抗凝。
三、统计学分析
采用SPSS16.0软件包建立数据库并进行统计学分析。计量资料进行正态分布检验,正态分布资料采用x±s表示,计数资料采用频数和百分比表示,比较采用χ2检验,P<0.05为差异有统计学意义。
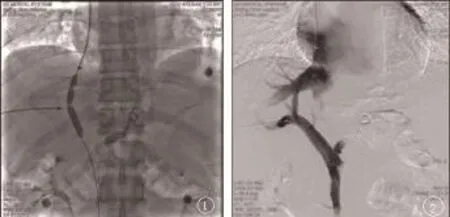
图1 、2 模拟Viatorr支架方法:球囊扩张分流道后保留肝静脉-门静脉切迹(箭示),为覆膜支架释放定位,在肝右静脉与门静脉右支之间建立分流道,分流道开通后,门静脉右支充盈良好,弹簧栓子栓塞后胃冠状静脉消失(箭示)
结 果
1.临床效果 :56例患者均获得一次性治疗成功,技术成功率为100%(图3、4)。分流道建立前后门静脉压力分别为(31.20±3.98 )mmHg和(17.36±3.48)mmHg,平均下降了(13.839±2.585)mmHg,下降幅度为40.77%(t=40.062,P<0.001)。随访1~3年。1、2、3年分流道通畅率分别为89.3%、75.0%、67.8%;再出血率7.1%、12.5%、16.1%;肝性脑病发生率为12.5%。
2.并发症:有1例术后第2天出现严重的腹腔感染,经过7天抗感染治疗好转;7例术后彩色多普勒提示分流道闭塞复发再出血,先后进行了介入开通并植入覆膜支架(图5、6)。患者术中、术后均未出现其他严重并发症。
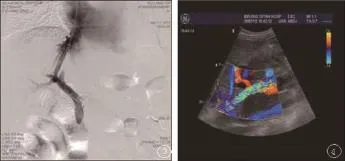
图3 、4 模拟Viatorr支架建立分流道及12个月后彩色多普勒显示分流道通畅,门静脉充盈良好(红色血流信号)
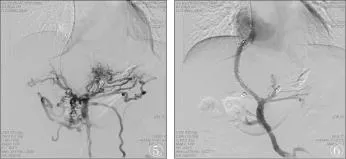
图5 、6 分流道于TIPS后21个月闭塞,造影可见门静脉属支显影,而分流道不显影。重新用覆膜支架修正后分流道通畅
讨 论
自1989年Richter等[1]首次将TIPS技术应用于临床以来,TIPS作为治疗肝硬化门静脉高压消化道出血和顽固性腹腔积液的一种微创手段取得了满意的临床效果。然而,裸支架分流道较高的狭窄率和闭塞率成为阻碍该技术发展的主要障碍。Jalan等[2]认为裸支架展开后门静脉血与肝组织的直接接触,毛细胆管损伤后胆汁向分流道内的直接渗漏,激发了炎性反应,引起假性内膜过度增生,是导致分流道狭窄闭塞的主要原因。Ducoin等[3]在胆汁染色的TIPS标本中发现了巨噬细胞和炎性细胞浸润,也进一步证实了以上观点。
自2004年美国FDA批准 Viatorr支架专用于TIPS以来,分流道通畅率明显提高,Viatorr支架既有4 cm的PTFE覆膜,可以覆盖肝实质全程,又保留了2 cm的裸区,释放后不阻挡同侧门静脉入肝血流[4];PTFE膜是一种高分子复合材料,具有很高的抗拉强度和很好的变应性[5],覆盖双层PTFE膜的Viatorr支架,具有抗血小板聚集、防止血栓形成等特点[6],只是目前这种支架尚未进入我国市场。为了最大程度上实现Viatorr支架的效果,我们将8 mm×60 mm的裸支架与8 mm×40 mm的PTFE覆膜支架(Fluency)叠加,来模拟Viatorr支架。临床观察结果显示模拟Viatorr支架(图2~4),其1、2、3年分流道通畅率分别为89.3%、75.0%、67.8%;与欧洲多中心研究结果(92%、84%、74%)相接近[7]。再出血率分别为7.1%、12.5%、16.1%。模拟Viatorr支架在提高分流道通畅率的同时,伸入门静脉内的部分支架无PTFE膜覆盖,不阻挡同侧门静脉血入肝;分流道建立后门静脉压力下降了40.77%,在很大程度上满足了肝脏血流动力学的需要。徐克等[8]认为:无论分流道是建立在门静脉左支还是右支均不应过度分流,必须保留有效的门静脉灌注压,下降50%的幅度为宜,分流后肝脏才能获得富含营养物质的门静脉血液灌注,对维持肝脏功能具有一定的意义。临床观察中也发现“Viatorr”支架的不足之处,一旦覆膜部分在肝静脉内形成“盖帽”,再次修正分流道时较裸支架困难,因此,模拟Viatorr支架的精确定位以及覆膜部分留置于肝静脉内的长度需要在释放前加以测量,针对不同患者分流道内肝实质的长短不同,选用不同型号的覆膜支架,真正做到模拟Viatorr支架的个体化,可能会取得更好的效果。
线阵探头引导下颈内静脉穿刺,即使存在血管变异也可以一次性穿刺成功;自肝静脉向门静脉穿刺成功后,摒弃将Rups-100穿刺系统强行开通分流道的传统操作方法,直接将球囊快速沿加硬导丝通过肝实质,可避免因Rups-100穿刺系统强行开通过分流道时造成的机械性损伤,减少了技术相关并发症的发生。
模拟Viatorr方法单次医疗费用较裸支架有所增加,但其较高的远期通畅率意味着比裸支架再次干预率低[9],总体“疗效费用比”符合医学经济学。当然,优质价廉的Viatorr支架如果能够在我国临床中得以应用,尤其是TIPS能够在曲张血管破裂出血前早期实施[10],可能才是提高TIPS中远期疗效的关键。
1 Richter GM, Noeldge G, Palmaz JC, et al. The transjugular intrahepatic portosystemic stent-shunt(TIPSS): experience of results of a pilot study[J]. Cardiovasc Intervent Radiol, 1990,13(3):200-207.
2 Jalan R, Elton RA, Redhead DN, et al. Analysis of prognosis variables in the prediction of mortality, shunt failure, variceal rebleeding and encephalopathy following the transjugular intrahepatic portosystemic stent shunt for varicealhaemorrhage[J]. J Hepatol, 1995,23(2):123-128.
3 Ducoin H, EI-Khoury J, Rousseau H, et al. Histopathologic analysis of transjugular intrahepatic portosystemic shunts[J]. Hepatology, 1997,25(5):1064-1069.
4 Vignali C, Bargellini I, Grosso M, et al. TIPS with expanded polytetrafuroethylene covered stent: results of an Italian multicenter study[J]. AJR Am J Roentgenol, 2005,185(2):472-480.
5 张营营, 张其林, 周传志, 等. PTFE膜材料的单向拉伸性能[J]. 建筑材料学报, 2010,13(4):535-539.
6 赵剑波, 李彦豪, 陈勇, 等.经颈静脉门腔分流术中Fluency覆膜支架应用的临床观察[J].中华放射学杂志, 2009,43(4):418-421.
7 Cejna M, Peck-Radosavljevic M, Thurnher SA, et al. Creation of transjugular intrahepatic portosystemic shunts with stent-graft:initial experiences with a polytetrafluoroethylene-covered nitinol endoprosthesis[J]. Radiology, 2001,221(2):437-446.
8 徐克, 邹英华, 欧阳墉.官腔内支架治疗学.北京: 科学出版社, 2004: 417-436.
9 Bureau C, Garcia-Pagan JC, Otal P, et al. Improved clinical outcomes using polytetrafluoroethylene coated stents for TIPS: results of a randomized study[J]. Gastroenterology, 2004,26(2):469-475.
10 García-Pagán JC, Caca K, Bureau C, et al. Early use of TIPS in patients with cirrhosis and bleeding[J]. N Engl J Med, 2010, 362(25):2370-2379.
Observation of modifed TIPS in treatment of gastroesophageal bleeding in portal hgpertension
Li Changqing, Li Honglu, Guo Jiang, Wei Jian, Zhao Dong, Cai Liang, Diao Zhenying, Du Hongliu, Luo Yan. Department of Interventions, Beijing Ditan Hospital, Capital Medical University, Beijing 100015, China
Li Changqing, Email: changqing0402@163.com
Objective To observe feasibility and effcacy of the modifed TIPS in treatment of gastroesophageal bleeding. Methods A total of 56 patients with gastro-esophageal bleeding underwent modified TIPS. Puncture the right internal jugular vein under the guidance of ultrasound, push the Rups-100 to the right hepatic vein along the guide wire, after successful puncture through hepatic vein to portal vein, a stiff wire was exchanged and a balloon (8 mm×40 mm) was sent and infated across the liver parenchymal. A bare stent (8 mm×60 mm) was released through the track, and a stent-graft (8 mm×40 mm) was released within the bare stent according to the markers on the balloon. The stent-graft must cover the liver parenchymal track. Gastric coronary veins were emblazed with coils routinely. The portal pressure were measured before and after the shunt established. Results Of all 56 cases were technically successful (100%). The portal pressure fell to (17.36±3.48)mmHg from (31.20±3.98)mmHg. All patients were followed up from 1 to 3 years. The decrease of portal vein pressure pre- and post-TIPS was statistically significant (t=40.062, P<0.001). During the period of 1—3 years follow-up, the shunts patency rate was 89.3%, 75.0%, 67.8% and the rate of rebleeding was 7.1%, 12.5%, 16.1% respectively; the rate of encephalopathy was 12.5%.One case accepted antibiotics treatment because of sepsis; 7 cases underwent re-TIPS due to the shunt occlusion. No other procedure related complications occured. Five cases died of hepatic failure, hepatocellular carcinoma and multiple organ failure. Conclusions The modifed TIPS with bare stent combined with stent-graft can effectively improve the patency rate of shunt, decrease the rate of rebleeding, and reduce complications related to technique through simplifying the procedure.
Liver cirrhosis; Portal hypertension; Modifed TIPS; Stents
2013-11-08)
(本文编辑:翟仁友)
10.3877/cma.j.issn.2095-5782.2014.02.008
100015 首都医科大学附属北京地坛医院介入科
李常青,Email:changqing0402@163.com
