经胆道支架置入放射性粒子条治疗恶性胆道梗阻
2014-05-09黄兢姚杨维竹江娜郑曲彬黄宁谢杭
黄兢姚 杨维竹 江娜 郑曲彬 黄宁 谢杭
•非血管介入•
经胆道支架置入放射性粒子条治疗恶性胆道梗阻
黄兢姚 杨维竹 江娜 郑曲彬 黄宁 谢杭
目的 探讨经胆道支架置入放射性粒子条治疗恶性胆道梗阻的疗效。方法 38例恶性胆道梗阻的患者,应用125I粒子,每个125I粒子长4.5 mm、直径0.8 mm,送入导管制备粒子条。先行经皮肝穿刺胆道引流(PTCD)术;导丝经皮通过梗阻段,先行球囊导管扩张,后行经皮胆道支架成形术;然后经支架置入8~10F胆道引流管;再将装有粒子条的导管在透视下经胆道引流管送入所需照射部位,包敷固定引流管体外部分或包埋于皮下。结果 38例中36例成功施行经皮胆道支架成形术及放射性粒子条置入术,术后患者的胆红素均降至正常或接近正常(P<0.05),未出现明显不良反应。讨论 经皮胆道支架成形术后联合放射性粒子条置入术治疗恶性胆道梗阻是一种安全有效的方法。
黄疸,梗阻性; 碘125粒子; 近程[放射]治疗; 支架; 治疗
恶性梗阻性黄疸系由恶性肿瘤引起的胆道梗阻致皮肤巩膜黄染,常见于各种肿瘤引起的肝胆管受压。经皮肝穿刺胆管引流和支架植入具有创微性、可重复性等优点,已经成为恶性胆道梗阻非手术保守治疗的首选疗法。金属胆道内支架的远期疗效显著优于塑料支架或鼻胆管外引流[1-3]。但支架对肿瘤本身无治疗作用,而且随着时间推移,金属内支架会发生不同程度的阻塞。125I粒子是一种疗效肯定的低能量放射性粒子,广泛应用于肿瘤的治疗。我们采用经皮胆道支架成形术后经支架腔内置入放射性粒子条,取得满意疗效,现报道如下。
对象与方法
一、一般资料
2009年3月—2012年4月入住我院的恶性梗阻性黄疸患者。男性27例,女性11例,年龄39~78岁,平均56岁,所以病例均经过临床病理,影像学及血液生化,肿瘤标志物等检查证实。全部患者均有明显黄疸表现,病灶均为外科不可切除。血清总红素67~680 μmol/L(平均306.4 μmol/L),直接胆红素48~530 μmol/ L(平均210.2 μmol/L)。38例胆道恶性梗阻的患者中13例为肝胆管细胞癌,5例为壶腹部周围癌,11例为肝癌,5例为胰头癌,4例为胃肠癌肝转移。经皮穿刺活检及腔内活检刷或活检钳夹取组织为获得病理的主要方法。
二、材料
应用中国宁波君安药业科技有限公司生产的125I粒子,每个碘125I粒子长4.5 mm、直径0.8 mm,活度为18~22 MBq,其半衰期为59.43 d。支架选用美国Cordis公司的SMART金属裸支架,8 mm× 8 cm 13个,8 mm×6 cm 11个,8 mm×4 cm 5个,6 mm×8 cm 4个,6 mm×6 cm 3个。将粒子排列成一直线送入4F无菌医用塑料管,用来制备放射性粒子条, 每个粒子条由6~20个粒子串连而成,并用细丝线缝合塑料管内粒子条的前后端,防止管内粒子的移位及脱落。
三、方法
术前检查对患者行CT、MR或MRCP等影像学检查,了解肿瘤或病变部位及梗阻段的部位、长度和范围;同时检查患者的生化、凝血功能、血常规。将患者影像学导入TPS(treatment planning system)系统,根据TPS系统的规划,准备不同粒子个数及间距的碘125I粒子制备的不同长度的放射性粒子条,用细小的针线固定粒子在导管的位置。先行经皮肝穿刺胆管造影(percutaneous transhepatic cholangiography, PTC)术,确认胆管狭窄的范围及长度;行胆道造影,造影所示病例均为胆总管狭窄或阻塞,左右肝胆管通畅。然后经导管将导丝越过狭窄部到达胆道金属支架预定留置部位的远端。留置6F鞘管,送入球囊导管对狭窄段行胆道扩张术后,选择长度和直径适应的胆道金属支架,沿导丝将其送至胆管狭窄段,待位置确定厚,准确置入胆管的狭窄段。通过导管鞘管注入造影剂,了解胆道的开通情况。如果胆道金属支架展开良好,造影剂很顺畅地进入十二指肠,则可以置入8~10F的胆道引流管,胆道引流管必须通过狭窄段到达狭窄近端;将装有粒子条的导管在透视下经8~10F胆道引流管送入所需照射部位,成串的粒子条的长度,即放射线照射范围,可以超过病灶所致狭窄段1~2 cm,以防胆道支架内导管移动造成照射范围的不足;包敷固定引流管露出体外部分。对于局限或孤立病灶所导致的胆道梗阻,可在留置放射性粒子条4~6个月后予以拔除;对于多发梗阻及肝内病灶复发或进展的,可予以长期留置放射性粒子条并适时更换放射性粒子条,以保证新发病灶的治疗剂量。如果胆道造影效果较差,仍有狭窄,造影剂进入十二指肠欠通畅,则需要留置内外引流管,暂不经过引流管置入放射性粒子条,待1~2周后根据造影通畅程度再决定是否放置放射性粒子条。对于直径大于20 mm的肿瘤及非包绕胆管生长的肿瘤,则配合经皮穿刺放射性粒子植入的方式来达到进一步控制肿瘤的目的。所有病例在接受经胆道支架放射性粒子条治疗恶性胆道梗阻的同时,均配合相应的抗肿瘤治疗。本研究采用Kaplan-Meier法评估患者的生存期和支架通畅率。
结 果
1.成功率:1例胰头癌和1例胆管细胞癌患者因导丝未能通过狭窄段而未能施行上述治疗,仅施行经皮肝穿刺胆道引流(percutaneous transhepatic cholangial drainage, PTCD);其余36例胆道恶性梗阻的患者均成功放置胆道支架及放射性粒子,围术期未发现大出血及急性肝功能损害等严重并发症。术后1个月,血清总胆红素降至38.4 μmol/L,直接胆红素降至21.8 μmol/L,患者的胆红素均降至正常或接近正常(图1、2,P<0.05)。
2. 生存率:对支架的通畅期和患者的生存曲线用Kaplan-Meier法进行评估。患者的中位支架通畅期是12个月,患者的生存期是4~40个月,中位生存期是10.5个月。其中5例肝癌患者,4例胆管细胞癌患者及2例胰头癌患者因肿瘤进展及远处转移引起多脏器功能衰竭或出血而无黄疸死亡;2例肝癌患者,4例胆管细胞癌患者及2例胰头癌患者,2例胃肠癌肝转移患者及2例壶腹部周围癌因肿瘤弥漫侵犯肝脏内小胆管而再发生黄疸,其余病例均未见黄疸复发,继续随访中。
讨 论
恶性梗阻性黄疸常见于肝门胆管癌、肝癌、胰头癌、壶腹癌、胃癌肝转移等造成的肝胆管受压。若黄疸得不到及时改善,肝功能、肾功能、凝血机制会迅速恶化,危及患者生命。大部分患者就诊时已经丧失手术机会,尽管目前恶性梗阻性黄疸的手术切除率有了很大提高,但仍仅为20%左右[4]。化疗联合放疗仍是目前最佳保守治疗病灶的方案。
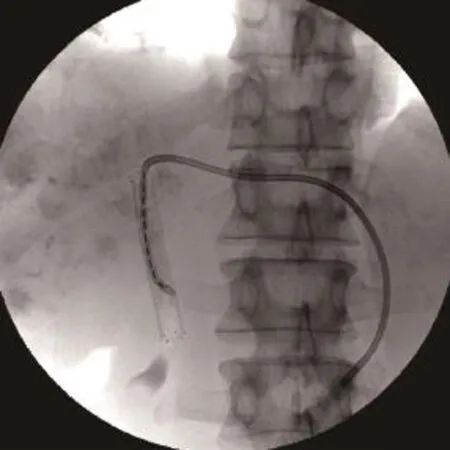
图1 原发性肝癌伴梗阻性黄疸,行PTCD+EMS植入 ,经胆道支架粒子条置入术,现为无黄疸存活

图2 壶腹部周围癌,行PTCD+EMS植入,经胆道支架粒子条置入术。现已拔除粒子条,无黄疸存活3年余
PTCD和支架植入具有创微性、可重复性等优点,已经成为恶性胆道梗阻的首选疗法。大量临床应用发现,金属胆道内支架的远期疗效显著优于塑料支架或鼻胆管外引流。支架对肿瘤本身无治疗作用,而且随着时间推移,金属内支架会发生不同程度的阻塞。其可能原因包括:①肿瘤向支架网眼内生长;②肿瘤过度生长超过支架近端或远端形成新的狭窄;③肿瘤碎片或胆泥阻塞支架等[5-6]。传统处理支架阻塞的方案:对于支架再狭窄可以采用原支架内再次置入支架及电热疗法,激光探头等方法,但是整体效果欠佳,不良反应较大。为控制肿瘤向胆管腔内发展,采用腔内置入放射源的放射治疗方法应运而生。目前临床上报道的腔内放射源为192Ir(铱192),临床应用取得了满意的疗效,较好地解决了再梗阻的问题[7-9]。但192Ir 存在诸多不足之处。由于靶器官接受照射剂量是有限的,同时为减少对正常组织的放射性损伤,不得不采用不连续的方式。治疗期间肿瘤细胞的大量繁殖使肿瘤难以得到有效控制,导致治疗失败。
125I粒子具有能量较低(27~35 keV),半衰期长(约59.43 d),易防护等特点,故目前永久性植入方式中以125I使用最为广泛。125I放射性粒子抑癌机制:125I放射性粒子能持续发射低剂量γ射线,γ射线对DNA分子链具有直接作用:单链断裂、双键断裂;同时具有间接作用:对机体内水分子电离产生自由基。自由基与生物大分子相互作用,引起组织细胞损伤。使肿瘤组织内分裂周期不同的肿瘤细胞得到均匀的照射治疗,周围正常组织由于处于细胞分裂的静止期,对放疗不敏感,仅有轻微损伤。同时,由于粒子放射活度低,可使肿瘤之外的正常组织所受剂量锐减,突出局部“适形”治疗,肿瘤靶区高剂量,而周围正常组织受量较低,这就有效地提高治疗增益系数,减少并发症,增加疗效,从而减少了周围正常组织的损伤。这种低剂量,较长时间持续的放射源,更容易杀死肿瘤细胞,控制病灶[10]。放射性粒子植入体内后,随着距放射源距离的增大,剂量当量迅速减小,所有病例在体表距离为50 cm时,测得的剂量当量已接近天然本底辐射剂量;同时粒子植入体内的深度极大的影响体外测量的γ射线剂量当量大小,如植入深度超过15 cm,在体外0 cm测得数值已基本接近天然本底剂量当量。我们施行的经胆道放射性粒子条植入,置入深度接近15 cm,因此术后对患者不必采取特别的防护措施,同时对周围的医护人员及家属亦是安全的。
胆管放射性粒子支架为塑料支架基础上外捆绑放射性粒子。由于本身塑料支架蛋白样坏死物质的脱落和沉积,造成放射性粒子支架较普通塑料支架可能更易于发生堵塞。而我科首创的金属支架植入+后装粒子条内放射的方法则做到支架通畅和肿瘤治疗的统一。该方法可长期保持支架的通畅;不同程度控制导致恶性梗阻的病灶;如果病灶发展,可通过调整粒子条的长度及位置以及间距来达到进一步控制肿瘤的目的;方便地通过更换粒子条以提高内放射治疗剂量;或取出粒子条而终止内放射治疗。根据以往的报道,胆道金属支架的中位支架通畅期是4.8~10个月,患者的中位生存期是4.5~6.5个月[11-12]。本研究中患者的肿瘤类型与之较相似,但患者的中位支架通畅期是12个月,生存期是4~40个月,中位生存期是10.5个月,患者的支架通畅期及生存期均明显优于单纯支架置入。这与放射性粒子所起的组织间近距离治疗肿瘤的作用不无相关。
该研究所观察病例在生存期内未发现再阻塞。在一定程度上还可控制甚至杀灭引起梗阻性黄疸的肿瘤。具有创伤小,并发症少,手术简单无痛苦,费用低。使介入技术同管腔内近距离放射治疗相结合,发挥两者的优势,在保持胆道引流的同时,通过放射性125I粒子的内照射起到治疗肿瘤的作用。临床观察发现,经皮胆道支架成形术后联合放射性粒子条置入术治疗恶性胆道梗阻是一种安全有效的方法。但在粒子条的组织间近距离治疗时间的控制,以及如何进一步提高对粒子作用范围以外肿瘤的疗效,延长患者的生存时间,有待于进一步临床研究。
(本文图1,2见光盘)
1 Arguedas MR, Heudebert GH, Stinnett AA, et al. Biliary stents in malignant obstructive jaundice due to pancreatic carcinoma: a costeffectiveness analysis[J]. Am J Gastroenterol, 2002,97(4):898-904.
2 Wasan SM, Ross WA Staerkel GA, et al. Use of expandable metallic biliary stents in resectable pancreatic cancer[J]. Am J Gastroenterol, 2005,100(9):2056-2061.
3 Stern N, Sturgess R. Endoscopic therapy in the management of malignant biliary obstruction[J]. Eur J Surg Oncol, 2008,34(3):313-317.
4 Cheng JL, Bruno MJ ,Bergman JJ, et al. Endoscopic palliation of patients with biliary obstruction caused by nonresectable hilar cholangiocarcinoma:effcacy of self-expandable metallic wallstents[J]. Gastrointest Endosc, 2002,56(1):33-39.
5 Eschelman DJ, Shapiro MJ, Bonn J, et al. Malignant biliary duct obstruction: long-term experience with Gianturco stents and combinedmodality radiation therapy[J]. Radiology, 1996, 200(3):717-724.
6 Bethge N, Sommer A, Gross U, et al. Human tissue responses to metal stents implanted in vivo for the palliation of malignant stenoses. Gastrointest Endosc, 1996,43(6):596-602.
7 Fletcher M, Brinkley D, Dawson J, et al. Treatment of high bileduct carcinoma by internal radiotherapy with iridium-192 wire[J]. Lancet, 1981,2(8239):172-174.
8 Bruha R, Petrtyl J, Kubecova M, et al. Intraluminal brachytherapy and selfexpandable stents in nonresectable biliary malignancies-the question of long-term palliation[J]. Hepatogastroenterology, 2001, 48(39):631-637.
9 Levitt MD, Laurence BH, Cameron F, et al. Transpapillary iridium-192 wire in the treatment of malignant bile duct obstruction[J]. Gut,1988, 29(2):149-152.
10 Mohiuddin M, Rosato F, Barbot D, et al. Long-term results of combined modality treatment with I-125 implantation for carcinoma of the pancreas[J]. Int J Radiat Oncol Biol Phys, 1992,23(2):305-311
11 Kaassis M, Boyer J, Dumas R, et al. Plastic or metal stents for malignant stricture of the common bile duct? Results of a randomized prospective study[J]. Gastrointest Endosc, 2003,57(2):178-182.
12 Misra SP, Dwivedi M, Reflux of duodenal contents and cholangitis in patients undergoing self-expanding metal stent placement[J]. Gastrointest Endosc, 2009,70(2):317-321.
Treatment of malignant biliary obstruction by percutaneous transhepatic insertion of biliary stent combined with radioactive seed implantation therapy
Huang Jingyao, Yang Weizhu, Jiang Na, Zheng Qubing, Huang Ning, Xie Hang. Department of Interventional Radiology, Fujian Medical University Union Hospital, Fuzhou 350001, China
Yang Weizhu, Email: ywzjn2012@163.com
Objective To explore effect of percutaneous transhepatic insertion of biliary stent implanted with radioactive seeds in treatment of alignant biliary obstruction. Methods125I seed, each of which was 4.5 mm in length and 0.8 mm in diameter, was applied in 38 patients with malignant biliary obstruction. They were led to a catheter for preparing125I seed sliver. The patients were given percutaneous transhepatic cholangial drainage (PTCD) at the frst step; then a percutaneous puncture was done through the obstructed section by a guide wire. The patients were given balloon catheter dilatation therapy before percutaneous transhepatic insertion of biliary stent (PTIBS). Biliary drainage catheter with the size of 8—10F were implanted. Finally the catheter with125I seeds sliver was sent to the part to be radiated via the biliary drainage catheter and the exposed part of the biliary drainage catheter which stretched outside the patients’body was wrapped or imbedded beneath the skin. Results Among 38 patients, the successful implementation of PTIBS and radioactive seed implantation treatment in 36 cases. All these patients had their bilirubin values return to or very close to normal level (P<0.05). No obvious side effect was obsreved. Conclusions PTIBS combined with radioactive seed implantation therapy in treatment of malignant biliary obstruction is safe and effective.
Jaundice, obstructive; Iodine-125 seed; Brachytherapy; Stents; Therapy
2013-12-05)
(本文编辑:钱晓军)
10.3877/cma.j.issn.2095-5782.2014.02.013
350001 福州,福建医科大学附属协和医院介入科
杨维竹,Email: ywzjn2012@163.com
