液相色谱-质谱联用法和高效液相色谱法研究参附注射液中的核苷类成分*
2014-05-05周学兴
周学兴 张 彬
(1.四川大学化学工程学院,四川 成都 610065;2.雅安三九药业有限公司,四川 雅安 625000)
液相色谱-质谱联用法和高效液相色谱法研究参附注射液中的核苷类成分*
周学兴1张 彬2△
(1.四川大学化学工程学院,四川 成都 610065;2.雅安三九药业有限公司,四川 雅安 625000)
目的对参附注射液中核苷类成分进行研究。方法采用液质联用技术(LC-MS),以乙腈-水(用冰醋酸调pH至2.65)为流动相梯度洗脱,以Waters symmetry shieldTMRP18色谱柱为分析柱,通过电喷雾电离源(ESI),选择正离子模式全扫描方式检测,对参附注射液中核苷类成分进行分析鉴定。采用高效液相色谱法(HPLC),以乙腈-水为流动相梯度洗脱,以Phenomenex Gemini 5 μ C18色谱柱为分析柱,流速1.0 mL/min,柱温30℃,检测波长260 nm,对所鉴定的核苷类成分进行含量测定。结果参附注射液中检测到尿苷(Uridine)、鸟苷(Guanosine)、腺苷(Adenosine)3种核苷类成分。HPLC测定3种核苷类成分精密度良好(RSD<1.0%),平均回收率为97.2%~98.7%,RSD<1.0%(n=6),在选定的范围内线性关系良好(r≥0.9998)。结论参附注射液中含有尿苷、鸟苷、腺苷3种核苷类成分,用HPLC测定3种核苷类成分方法可靠。
参附注射液 核苷 液相色谱-质谱联用法 高效液相色谱法
参附注射液是依据宋代严用和《济生方》参附汤研制成的现代中药制剂,具有回阳救逆,益气固脱功能,主治阳气暴脱的厥脱症(感染性、失血性、失液性休克等),也可用于阳虚(气虚)所致的惊悸、怔忡、喘咳、胃疼、泄泻、痹证等。参附注射液由红参、附片经提取、精制、配制、灌封、灭菌制成。对于参附注射液中人参皂苷类、生物碱类、糖类等成分早已有研究及文献报道,但对于其中核苷类物质的研究尚未查到。为此,笔者通过高效液相-质谱联用技术对本产品中极性较大的物质成分进行研究,鉴定出了参附注射液中尿苷(Uridine)、鸟苷(Guanosine)、腺苷(Adenosine)等核苷类成分,其中,腺苷可直接进入心肌经磷酸化生成腺苷酸,参与心肌能量代谢,同时还参与扩张冠脉血管,增加血流量,对心血管系统和肌体的其他系统及组织均有生理作用。腺苷和鸟苷由红参提供,尿苷由附片提供。同时,建立了高效液相色谱法同时测定尿苷、鸟苷、腺苷3个成分含量的方法[1-7]。现报告如下。
1 仪器与试剂
1.1 仪器
METTLER TOLEDO AE-240电子天平(梅特勒-托利多公司)、Thermo LCQ FLEET高效液相色谱-质谱联用仪及Xcalibur软件(赛默飞世尔科技公司)、Waters e2695高效液相色谱仪和Waters 2998二级阵列管检测器、Agilent 1100高效液相色谱仪、Agilent 1260高效液相色谱仪及ChemStation化学工作站。
1.2 对照品
尿苷(Uridine,99%,Lot:A017402701,C.A.S.:58-96-8,ACROS ORGANICS,New Jersey,USA)、 鸟苷(Guanosine,99%,Lot A018147001,C.A.S.118-00-3,ACROS ORGANICS,New Jersey,USA)、腺苷(Adenosine,110879-200202,中国药品生物制品检定所)。
1.3 试剂
乙腈(色谱纯,Merck),试验用水为纯化水。
1.4 药物
参附注射液为雅安三九药业有限公司生产(规格为 10 mL/支,批号分别为 Z-100402、Z-100403、Z-100404、Z-100405、Z-100406、Z-100703;规格为50 mL/瓶,批号为Z-100702)。
2 方法与结果
2.1 液相色谱-质谱联用鉴定参附注射液中尿苷、鸟苷、腺苷成分
2.1.1 色谱-质谱条件[8-10]色谱柱Waters symmetry shieldTMRP18色谱柱(4.6 mm×250 mm,5.0 μm),柱温30℃;样品盘温度30℃,进样量10 μL;以水(用冰醋酸调pH值2.65)为流动相A,以乙腈为流动相B,按0 min,流动相A100%,30 min流动相A90%、流动相B10%进行梯度洗脱;UV检测波长:254 nm;PDA扫描200~600 nm。离子化方式:电喷雾离子源(ESI);质量分析器:离子肼。扫描方式:50~2000 m/z全扫描一级质谱(full scan)和选择离子二级扫描质谱(SIM)244 m/z(尿苷[′M+H]);283 m/z(鸟苷[′M+H]);268 m/z(腺苷[′M+H])等方式。扫描模式:正离子模式。ESI源温度:350℃;喷雾电压35 V。
2.1.2 溶液的制备 取腺苷对照品、鸟苷对照品和尿苷对照品适量,精密称定,加50%甲醇制成每1 mL各含20 μg的混合溶液,即得对照品溶液的制备。取参附注射液作为供试品溶液。
2.1.3 结果 采用上述液相色谱-质谱联用技术测得参附注射液中尿苷、鸟苷、腺苷色谱图、PDA图、总离子流图(TIC)。
2.2 参附注射液中尿苷、鸟苷、腺苷含量测定

鉴于2.1条件下质谱图中各分子离子峰明显,但色谱图中鸟苷峰和腺苷峰分离不好,故另建分离度好的色谱方法进行含量测定,方法见2.2。
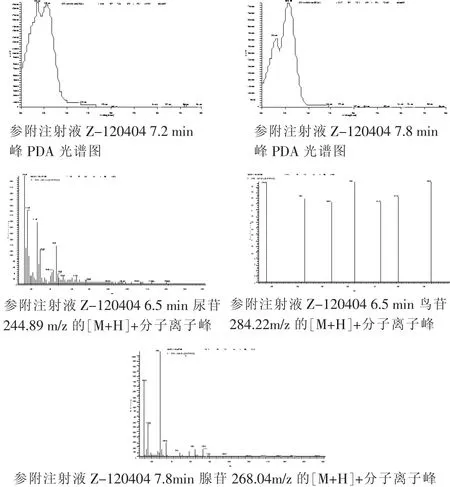
图1 尿苷、鸟苷、腺苷色谱图、PDA图、总离子流图(TIC)
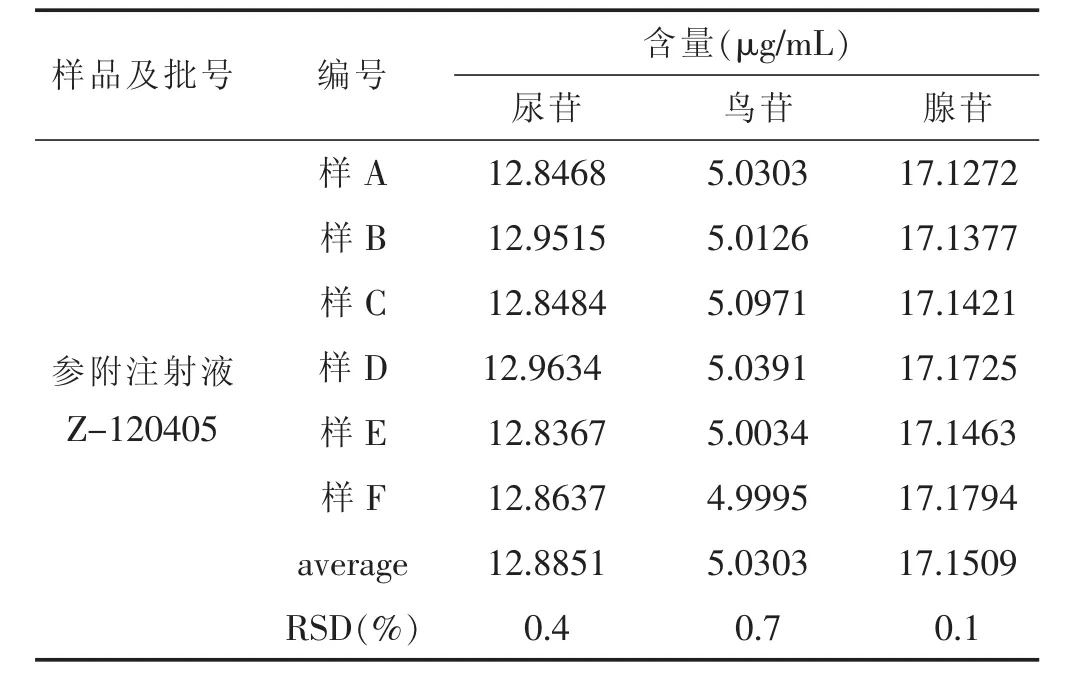
表1 重复性试验

图2 尿苷、鸟苷、腺苷含量测定色谱图
2.2.1 色谱条件 色谱柱 Phenomenex Gemini C18(250mm×4.6mm,5μm);柱温30℃;检测波长260nm[4-9];以水为流动相A,以乙腈为流动相B[4-5],按0~7 min流动相A 98%、流动相B 2%、流速1.000 mL/min,7.01~30 min流动相A96%、流动相B4%、流速1.000 mL/min进行梯度洗脱;进样量10 μL。
2.2.2 溶液的制备 取尿苷、鸟苷、腺苷对照品适量,精密称定,加50%甲醇制成每1 mL分别约含20 μg、8 μg、20 μg的混合溶液,即得对照品溶液。取参附注射液作为供试品溶液。
2.2.3 系统适应性试验 取含尿苷20.84 μg/mL、鸟苷8.304 μg/mL、腺苷20.92 μg/mL的对照品混合溶液,连续进样6次,以峰面积计算RSD值分别为0.20%、0.40%、0.13%(n=6)。以腺苷峰计理论塔板数均大于10000。
2.2.4 重复性试验 见表1。取参附注射液Z-120405共6份分别作为供试品溶液,以含尿苷20.84 μg/mL、鸟苷8.304 μg/mL、腺苷20.92 μg/mL的对照品混合溶液为外标,测定,以含量计算RSD值均小于1.0%,表明方法重复性好。
2.2.5 中间精密度及供试品溶液稳定性试验 取上述供试品溶液样A于室温(23℃)下放置,分别于0、6、
12、24、48 h测定。含量在48 h内无明显变化,表明供试品溶液在48 h内是稳定的。以含量计算RSD值均小于1.0%,表明方法精密度好。
2.2.6 加样回收试验 按“2.2.2”项下的方法操作,配制成含尿苷 20.84 μg/mL、鸟苷8.304 μg/mL、腺苷20.92 μg/mL的对照品混合溶液,分别精密吸取6份对照品溶液各1~2 mL容量瓶中,分别精密加入参附注射液Z-120405供试品1 mL,分别混匀,即得。照“2.2.1”项下的色谱条件各进样10 μL,按外标法计算供试液浓度,并计算回收率(n=6)为97.2%~98.7%及RSD值均小于1.0%,表明该方法准确度高。

表2 加样回收试验
2.2.7 线性关系考察 按“2.2.2”项下分别配制成如下表浓度不等的对照品溶液,按上述色谱条件各进样10 μL,以对照品溶液的浓度Y(μg/mL)对峰面积X(AU)进行线性回归分析。尿苷回归方程和相关系数分别为:y=0.065x+0.0415,R2=0.9999。鸟苷回归方程和相关系数分别为:y=0.0724x-0.2692,R2=0.9998。腺苷回归方程和相关系数分别为:y=0.0324x-0.2473,R2= 0.9998。结果表明。尿苷在2.61~333.44 μg/mL、鸟苷在1.04~132.864 μg/mL、腺苷在2.62~334.72 μg/mL范围内线性关系良好。
2.2.8 耐用性试验 保持其他色谱条件不变,分别改变下述色谱条件进行检测:(1)改变流速为 0.7 mL/min、1.0 mL/min、1.3 mL/min;(2)改变柱温为25℃、30℃、35℃;(3)改变色谱柱品牌及型号为Waters symmetry shieldTMRP18 (4.6 mm×250 mm;5.0 μm)、Agilent ZORBAX Extend-C18(4.6 mm×250 mm,5.0 μm)、Phenomenex Gemini 5μ C18(110 A 250 mm×4.6 mm 5 micron)、Phenomenex Synergi 4μHydro-RP80A(110 A 250 mm×4.6 mm 4 micron);(4)改变仪器品牌及型号为Waters e2695、Agilent 1100、DIONEX U-3000。
由系统耐用性试验得知该方法对流速、柱温、仪器品牌及型号无选择性,用其中任何一种都能达到分离效果并满足检测需求;但对色谱柱有选择性,使用Phenomenex Gemini 5μ C18(110 A 250 mm×4.6 mm 5micron)色谱柱才能达到很好的分离效果,因此将色谱柱型号规定于检测方法色谱条件中。
3 讨论
本研究中尿苷、鸟苷、腺苷相对分子质量较小,采用离子肼质谱进行小分子物质二级扫描时不容易被打碎。可能是由于离子肼进行二级打碎扫描时实际上仍是采取scan扫描方式,只是这次扫描范围比一级扫描(full scan)范围更窄,它在打碎母离子的同时一部分能量也会打碎范围内的其他离子,实际能量很弱,打出的碎片很多很复杂,信号强度也弱,灵敏度也低,故离子肼用作尿苷、鸟苷、腺苷这3个小分子量成分的MS/MS二级扫描检测效果不理想。今后可以改用三重四级杆质谱作这类小分子量物质成分的MS/MS二级质谱分析针对性会更强一些。
本研究通过UV检测发现尿苷、鸟苷、腺苷3个成分,检测用254 nm波长比203 nm波长噪声更小;由于3种成分均为核苷类成分,PDA扫描发现3种成分光谱图基本一致,且最大吸收都在260 nm波长处。由此,建立含量测定方法时选择260 nm作为UV检测波长。笔者通过液相-质谱联用技术鉴定出参附注射液中尿苷、鸟苷、腺苷成分,建立了参附注射液中尿苷、鸟苷、腺苷含量同时测定的方法,并经过方法验证:该方法重复性好、精密度好、回收率(n=6)均大于97.0%、尿苷在2.61~333.44 μg/mL、鸟苷在1.04~132.864 μg/mL、腺苷在2.62~334.72 μg/mL范围内线性关系良好、该方法对流速、柱温、仪器品牌及型号无选择性,对色谱柱有选择性。该方法用于参附注射液中尿苷、鸟苷、腺苷含量同时测定准确可靠。
[1]彭日煌,谢明勇,王远兴,等.RP-HPLC测定虫草菌粉中核苷类成分[J].食品与机械,2005,21(1):61-63.
[2]卢端萍,蒋婷婷,陈硕,等.高效液相色谱法测定灵芝提取物中尿苷和腺苷含量[J].中国药业,2013,22(14):17-19.
[3]刘红,陈燕芹,邓峰,等.反相高效液相色谱法同时测定小根蒜中尿苷、鸟苷和腺苷[J].现代食品科技,2013,29(5):1128-1130,1191.
[4]宋细忠,习梅兰.HPLC法同时测定灵芝浸膏片中尿苷和腺苷的含量[J].江西中医学院学报,2011,23(1):62-63.
[5]隋利强,吴水生.RP—HPLC法测定不同贮存年限半夏饮片中腺苷和鸟苷的含量[J].黔南民族医专学报,2012,25(3):157-159.
[6]赵杨,靳凤云,伍庆,等.高效液相色谱法测定贵州不同产地半夏药材中鸟苷和腺苷的含量[J].时珍国医国药,2007,18(1):23-24.
[7]胡晓茹,孙磊,戴忠,等.高效液相质谱法和超高效液相色谱法研究红花注射液中的核苷类成分[J].中国药学杂志,2013,48(12):1022-1026.
[8]谢显珍,黄兰芳,王小玉.液相色谱一电喷雾离子化一质谱测定蛹虫草子实体中腺苷含量[J].光谱实验室,2009,26(3):631-634.
[9]黄兰芳,郭方遒,梁逸曾.高效液相色谱一质谱法测定人体滑液中腺苷的含量[J].分析化学,2004,32(8):1124.
[10]余辉,徐兰,林永勉,等.液相色谱一质谱联用分析发酵液中的阿糖腺苷及其有关物质[J].海峡药学,2009,21(3):52-55.
Nucleosides in Shenfu injection by LC-MS and HPLC
ZHOU Xuexing,ZHANG Bin.College of Chemical Engineering,Sichuan University,Sichuan,Chengdu 610065,China
Objective:To study nucleosides in Shenfu injection.Methods:Nucleosides in Shenfu injection were identified by LC-MS.The separation was performed on Waters symmetry shieldTM RP18 column.Gradient elution was carried out with mobile phase consisting of acetonitrile-water(adjusted pH=2.65 with acetic acid).Electrospray ionization source was applied and operated in the positive ion mode.Three nucleosides in Shenfu injection were simultaneously determined by high performance liquid chromatography(HPLC)with Phenomenex Gemini 5μ C18 column.Gradient elution was carried out with mobile phase consisting of acetonitrile-water at the flow rate of 1.0 mL/min.The assay was carried out at 30℃with detection at 260 nm.Results:Adenosine,guanosine and uridine in Shenfu injection were identified.The relationship between the injection quality and the peak areas of the three nucleosides was all linear.The precisions were better and the RSDS were less than 1.0%.The average recoveries(n=6)were in the range of 97.2%~98.7%and the RSDS were all less than 1.0%.Conclusion:There are three nucleosides in Shenfu injection.The method is effective which can be applied in quantitative determination of nucleosides in Shenfu injection by HPLC.
Shenfu injection;nucleosides;LC-MS;HPLC
R285.5
A
1004-745X(2014)08-1411-04
10.3969/j.issn.1004-745X.2014.08.006
2014-04-20)
“重大新药创制”科技重大专项“十二五”第三批课题(2013ZX09201018)
△通信作者
