重组人粒细胞集落刺激因子对化疗后中性粒细胞缺乏的有效性和安全性研究
2014-05-02李波曹原司继刚
李波,曹原,司继刚
山东淄博市中心医院,淄博 255036
重组人粒细胞集落刺激因子对化疗后中性粒细胞缺乏的有效性和安全性研究
李波,曹原,司继刚*
山东淄博市中心医院,淄博 255036
目的:评价重组人粒细胞集落刺激因子(rhG-CSF)对化疗所致中性粒细胞缺乏的恶性血液病患者的临床疗效和安全性。方法:对2012年1~12月我院73例化疗后出现中性粒细胞缺乏的恶性血液病患者进行调查分析,均在粒缺发生后使用rhG-CSF,用SPSS统计软件对信息进行分析。结果:rhG-CSF可以有效缓解化疗后的中性粒细胞缺乏,使白细胞和中性粒细胞数目明显升高,平均恢复时间为(7.77±5.14)d,总有效率为95.9%,研究中根据病人中性粒细胞缺乏发生程度、阶段及持续时间进行个体化给药。结论:rhG-CSF对化疗所致的中性粒细胞缺乏症安全有效。
重组人粒细胞集落刺激因子;中性粒细胞缺乏;疗效;安全性
化学药物治疗(简称“化疗”)对肿瘤细胞有很强的杀伤力,但多数化疗药物会导致不同程度的骨髓抑制,使化疗方案无法按计划进行[1]。因血细胞中中性粒细胞平均生存时间最短,约为6~8 h,因此骨髓抑制常最先表现为白细胞下降,当中性粒细胞计数低于0.5×109/L时,称为中性粒细胞缺乏症(A-granulocytosis),此时患者易发生感染,应使用抗菌药物和造血生长因子以及采取保护性隔离等措施,促使中性粒细胞数目恢复[2]。本文对我院73例恶性血液病患者使用重组人粒细胞集落刺激因子(Recombinanthumangranulocytecolony-stimulating factor,rhG-CSF)化疗后中性粒细胞缺乏的病例进行研讨和总结。
1 资料与方法
1.1 一般资料
收集我院2012年1~12月化疗后发生中性粒细胞缺乏的恶性血液病患者73例,男29例,女44例,年龄15~84岁,平均年龄(47.9±15.9)岁。其中急性髓系白血病59例,急性淋巴细胞性白血病5例,淋巴瘤6例,多发性骨髓瘤1例,骨髓增生异常综合征2例。
1.2 中性粒细胞减少程度划分标准
根据WHO抗肿瘤药物血液系统急性及亚急性毒性反应分度标准,中性粒细胞减少程度分为Ⅰ度、Ⅱ度、Ⅲ度、Ⅳ度。Ⅰ度:1.5~1.9×109/L;Ⅱ度:1.0~1.4×109/L;Ⅲ度:0.5~0.9×109/L;Ⅳ度:<0.5×109/ L。其中Ⅳ度减少即为中性粒细胞缺乏症。本研究选取的均为中性粒细胞缺乏症病例。
1.3 辅助检查
化疗后监测患者体温和血常规,如出现中性粒细胞缺乏症,每日复查血常规。
1.4 中性粒细胞缺乏症用药方案
患者出现中性粒细胞缺乏时,立即使用抗菌药物及造血生长因子。73例恶性血液病患者在化疗后发生中性粒细胞缺乏时使用的造血生长因子为rhG-CSF,皮下注射给药。复查白细胞和中性粒细胞的变化情况,中性粒细胞计数≥0.5×109/L为有效,并观察感染和不良反应情况。
1.5 统计学方法
应用SPSS17.0统计软件进行分析,用药前后比较采用配对t检验,结果以平均数±标准差(±s)表示,P<0.05为差异有统计学意义。
2 结果
2.1 治疗与效果
(1)73例中,治愈10例,好转60例,无效3例,总有效率为95.9%,无效的患者因感染不能控制、呼吸循环衰竭而死亡,见表1。患者化疗后中性粒细胞缺乏伴发热29例,经治疗后体温恢复正常的有24例,退热率为82.8%;44例体温正常,未发生感染。从中性粒细胞缺乏开始至中性粒细胞计数≥0.5× 109/L所需时间平均为(7.77±5.14)天。

表1 患者中性粒细胞缺乏用药后疗效情况
(2)排除死亡病例,患者化疗后开始发生中性粒细胞缺乏时和使用rhG-CSF后白细胞计数(WBC)分别为(1.07±0.49)×109/L和(2.65±1.57)× 109/L;中性粒细胞计数(NEU)分别为(0.25±0.19)× 109/L和(1.41±1.01)×109/L,用药前后比较差异有统计学意义(P<0.05),见表2。
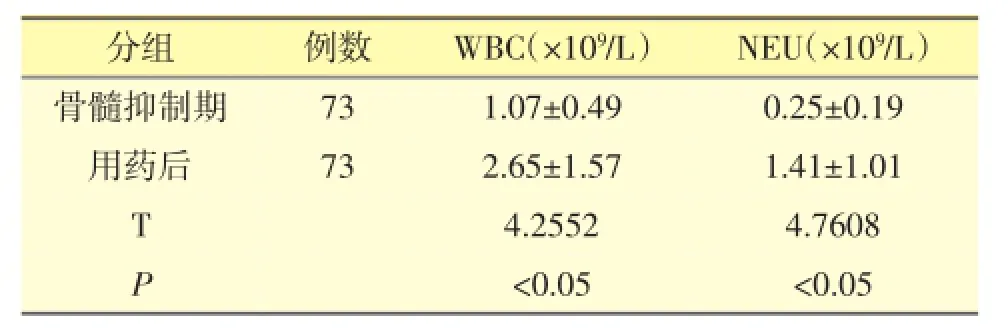
表2 患者化疗后开始发生中性粒细胞缺乏时和用药后WBC和NEU检测结果
(3)根据病人中性粒细胞缺乏发生程度、发生阶段及持续时间进行个体化给药。中性粒细胞缺乏时间较长,且中性粒细胞增长缓慢,给予rhG-CSF 5 μg·kg-1或300 mg·d-1,一日一次或一日两次。化疗后中性粒细胞下降至最低值期间用量较大,平均日用量为(413.51±149.37)μg;中性粒细胞增长期用量减少为100 μg,一日一次或者停药。
2.2 病原学检查
中性粒细胞缺乏初始感染的病原菌,常见的革兰阳性菌有凝固酶阴性的葡萄球菌、草绿色链球菌、肠球菌、金黄色葡萄球菌等;常见的革兰阴性菌有大肠埃希氏菌、肺炎克雷伯菌、铜绿假单胞菌等。本调研中49例做了标本培养,送检率为67.1%,经咽拭子、痰、血、分泌物等培养,15例检出病原菌,检出率为20.5%,其中4例肺炎克雷伯菌;1例金黄色葡萄球菌;2例嗜麦芽窄食单胞菌;2例铜绿假单胞菌;1例洋葱伯克霍德菌;1例鲍曼不动杆菌;1例嗜麦芽窄食单胞菌和铜绿假单胞菌;1例肺炎克雷伯菌和阴沟肠杆菌;2例肺炎克雷伯菌和大肠埃希菌。
2.3 安全性评价
研究病例中,偶发骨痛和肌肉酸痛、食欲不振、皮疹、乏力,患者可耐受,停药后短时间内缓解,无需特殊处理。
3 讨论
化疗药物最为严重的不良反应是抑制骨髓造血功能,其发生率高达50%~91.3%[3],化疗所致白细胞和中性粒细胞水平急剧下降可导致院内感染[4]。肿瘤患者自身抵抗力较低,若发生中性粒细胞缺乏症,感染几率将大大增加,并可能引发肿瘤患者死亡[5]。rhG-CSF是通过重组DNA技术,在植入人GCSF基因的大肠埃希菌内表达产生,与天然G-CSF具有相同的氨基酸序列和生物活性[6]。能较特异性地作用于中性粒细胞的前驱细胞,可促进粒系祖细胞的增殖、分化与成熟,并增加成熟中性粒细胞的趋化吞噬和免疫杀伤能力,刺激骨髓造血干细胞向外周血释放,有利于控制感染和降低死亡风险,且生物稳定性好,毒副作用少,是化疗后骨髓抑制的主要治疗药物[7]。
73例恶性血液病患者在化疗后发生中性粒细胞缺乏时使用rhG-CSF,结果显示:患者用药前后WBC和NEU的比较差异有统计学意义(P<0.05),rhG-CSF可以有效地促进中性粒细胞的恢复,该结果与之前的研究结果相符合。rhG-CSF的用量和用药时间应根据患者化疗强度和中性粒细胞下降程度决定,rhG-CSF平均日用量为(281.65±96.50)μg,中性粒细胞降至最低值时平均日用量为(413.51± 149.37)μg,对于化疗强度大和/或中性粒细胞计数极低的患者应给予大剂量、足疗程,并监视病情,复查血常规后调整用药。用药后,中性粒细胞缺乏持续时间为(7.77±5.14)天,总有效率为95.9%,退热率为82.8%。
根据IDSA指南,在肿瘤患者第一个化疗周期时使用rhG-CSF进行预防,可降低发热和中性粒细胞减少的发生率,对于老年患者,或具有其他危险因素者,例如合并内科疾病、营养不良、有发热和中性粒细胞减少史、无抗菌药物预防史等,尤其应考虑预防使用rhG-CSF[8]。当中性粒细胞减少性发热危险与化疗药物有关时,使用rhG-CSF的累积临床获益≥20%。本调研中,均在中性粒细胞缺乏发生时使用rhG-CSF联合抗菌药物进行治疗,并取得了良好的效果。
rhG-CSF出现的不良反应主要有骨痛、肌肉酸痛、食欲不振、皮疹、乏力等,程度均较轻,停药后短时间内缓解。
综上所述,rhG-CSF可以有效地缓解恶性血液病患者在化疗后发生的中性粒细胞缺乏,使白细胞和中性粒细胞数目明显升高,缩短中性粒细胞减少的持续时间,帮助患者渡过感染高危期,从而使化疗方案得以按计划进行,且大剂量、足疗程使用,有效率高,安全性好。
[1] 苏同义.肿瘤化疗粒细胞减少38例的临床分析[J].中外医学研究,2013,11(2):109.
[2] 盖绿华,冯其梅,左大鹏,等.中性粒细胞缺乏伴发热与感染鉴别诊断及治疗[J].中华医院感染学杂志,2013,23(05):1027-9.
[3] 王新帅,秦玲,高社干,等.rhG-CSF对TP方案化疗后骨髓抑制的有效性和安全性研究[J].中国现代药物应用,2011,5(16):7-8.
[4] 阮燕萍,张文英.化疗致粒细胞缺乏症患者感染的危险因素研究[J].中华医院感染学杂志,2010,20(1):38-40.
[5] 张强.细胞集落刺激因子和抗菌药物预防化疗所致粒细胞缺乏症患者院内感染的疗效观察[J].中华实验和临床感染病杂志,2013,7(4):597-8.
[6] 夏修远,房文铮,宋洪涛.重组人粒细胞集落刺激因子预防肿瘤化疗后骨髓抑制的疗效分析[J].中南药学,2012,10(3):229-32.
[7] Xia F,Zhang QY,Jiang YP.Chronic toxicity of a novel recombinant human granulocyte colony-stimulating factor in rats[J].Chin Med Sci J,2011,26(1):20-7.
[8] WingardJR,ElmongyM.Strategiesforminimizing complicationsofneutropenia:prophylacticmyeloid growth factors or antibiotics[J].Crit Rev Oncol Hematol, 2009,72(2):144-54.
Analysis of Efficacy and Safety of Recombinant Human Granulocyte Colony-stimulating Factor Used for Agranulocytosis Patients after Chemotherapy
LI Bo,CAO Yuan,SI Ji-gang*
Central Hospital of Zibo,Zibo 255036,Shandong,China
Objective:To evaluate the efficacy and safety of recombinant human granulocyte colonystimulating factor(rhG-CSF)used for chemotherapy induced agranulocytosis in patients with hematological malignancies.Methods:Seventy-three patients with hematological malignancies suffering from agranulocytosis after chemotherapy were given rhG-CSF in our hospital during 2012.Data were statistically analyzed.Results:It was effective for chemotherapy induced agranulocytosis with rhG-CSF and the number of neutrophile granulocytes and white blood cells(NEU and WBC)increased significantly.The average duration of recovery was 7.77±5.14 d and the effective rate was 95.9%.Individualized administration was based on the severity,phase and duration of agranulocytosis.Conclusion:rhG-CSF can be effective and safe to treat agranulocytosis after chemotherapy.
Recombinant human granulocyte colony-stimulating factor;Agranulocytosis;Efficacy;Safety
R969.4
A
1673-7806(2014)06-545-03

李波,男,主任医师,内科学和药物临床应用
*通讯作者 司继刚,副主任药师,药学硕士 E-mail:sjg1019@163.com
2014-04-24
2014-08-31
