重组人血管内皮抑制素联合吉西他滨与吉西他滨单药一线治疗老年晚期非小细胞肺癌的随机对照研究
2014-04-30陈群石琴谢强肖松
陈群石琴谢强肖松
作者单位:350008 福州1福建医科大学临床教学医院 福州肺科医院肿瘤科;350001 莆田2福建莆田市涵江医院呼吸内科
临床研究
重组人血管内皮抑制素联合吉西他滨与吉西他滨单药一线治疗老年晚期非小细胞肺癌的随机对照研究
陈群1石琴1谢强1肖松2
作者单位:350008 福州1福建医科大学临床教学医院 福州肺科医院肿瘤科;350001 莆田2福建莆田市涵江医院呼吸内科
目的 观察重组人血管内皮抑制素(恩度)联合吉西他滨(GEM)和GEM单药治疗老年晚期非小细胞肺癌(non-small cell lung cancer,NSCLC)的疗效和安全性。方法128例经病理证实的符合入选标准的老年晚期NSCLC患者,采用前瞻性、开放性、随机对照的临床研究设计,按1∶1比例随机分为联合组和单药组,联合组66例接受恩度联合GEM治疗,单药组62例只用GEM单药治疗。化疗2个周期后按照实体瘤评价标准评价疗效,记录疾病控制率(DCR)、中位无疾病进展生存时间(mPFS)、中位生存时间(mOS)。每个周期按照NCICTC 3.0标准评价毒副反应。结果 治疗后联合组 PR 11例,SD 36例,PD 15例。单药组PR 6例,SD 26例,PD 24例。联合组与单药组的客观有效率(ORR)按意向性分析(intention to treat analysis,ITT)分别为16.7%、9.7%,(P=0.326),按符合方案集分析(per-protocol,PP)分别为17.7%、10.7%,(P=0.278),差异均无统计学意义。DCR按PP分析分别为75.8%、57.1%,(P=0.031),差异具有统计学意义。mPFS分别为4.0个月、3.7个月,(P=0.027),差异具有统计学意义。mOS分别为9.1个月、8.5个月,(P=0.418),差异无统计学意义。两组主要毒副反应以骨髓抑制发生率较高,但多为Ⅰ级/Ⅱ级,Ⅲ级/Ⅳ级少见,差异无统计学意义。结论 恩度联合GEM一线治疗老年NSCLC具有一定的抗肿瘤活性和较好的疾病控制率,安全性较好,临床受益率高,是一种有临床应用前景的治疗方法。
肺肿瘤;非小细胞肺癌;重组人血管内皮抑制素;老年;单药化疗
肺癌是当今发病率和病死率最高的恶性肿瘤[1,2]。临床上肺癌的中位诊断年龄在逐渐增加,目前为69~72岁[3,4]。在老年肺癌中,非小细胞肺癌(non-small cell lung cancer,NSCLC)占85%[2],其中以临床分期ⅢB期或Ⅳ期为常见[5]。中国流行病学研究中通常将年龄≥65岁定义为老年人[6]。化疗是老年晚期NSCLC不可替代的常用治疗手段。其治疗目标是延长患者总生存期(OS)、提高生活质量(QOL)、降低疾病相关并发症的发生。因此如何将治疗方案优化配置,达到更佳的治疗目的是当前老年晚期NSCLC的研究热点。重组人血管内皮抑制素注射液(Rh-Endostar,恩度)联合化疗能提高晚期NSCLC的疗效[7,8],2008年以来,被中国版NSCLC临床实践指南推荐为一线治疗药物[8]。为此,本研究选择重组人血管内皮抑制素联合吉西他滨(GEM)方案,治疗66例老年晚期NSCLC,以期达到既提高患者生活质量,保证安全,又能提高疗效的目的。现将结果报道如下。

表1 128例老年晚期NSCLC的临床病理特征
1 资料与方法
1.1 研究对象
2009年4月1日至2013年5月31日,选取128例65~85岁的老年晚期NSCLC患者,经病理组织学和(或)细胞学检查确诊,临床分期为ⅢB期或Ⅳ期的晚期NSCLC初治患者,按1∶1随机分为联合组66例和单药组62例。两组患者临床病理特征比较差异均无统计学意义(P均>0.05),具可比性。见表1。
入选标准及排除标准 ⑴入选标准:至少具有1个双径可测量的病灶,胸片、普通CT或MRI扫描检查病灶≥20 mm,螺旋CT或PET-CT扫描检查病灶≥10 mm;体力状况尚好(ECOG评分0~1分);预计生存期≥3个月;符合化疗指征和检查基本要求,包括外周血象检查基本正常,心、肝、肾功能无明显异常,心电图基本正常,机体没有未愈合的创伤;外周血象:WBC≥4.0×109/L,PLT≥80×109/L,Hb≥90 g/L;肾功能:Cr≤2.0×UNL(正常上限);肝功能:BIL≤2.0× UNL,ALT/AST≤5.0×UNL;配合随访,依从性好,同意化疗并签署知情同意书。⑵排除标准:孕期或哺乳期患者;急性感染;腹泻(水样便)或麻痹性肠梗阻;主要器官功能衰竭,如失代偿的心肺功能衰竭;有症状的脑转移、胸膜转移;仅有不可测量且不可评价的病灶,如腹水、胸腔积液、心包积液、骨转移;未得到控制的糖尿病;合并第二原发恶性肿瘤。⑶剔除标准:未按上述标准入组并完成有关检查、治疗者;观察期间对靶病灶同时进行放疗者;观察期间合并使用其他抗肿瘤化疗药物者;因故或无故明显推迟给药时间超过2周者。⑷退出情况:联合组66例患者中有2例分别因恩度Ⅲ级变态反应,于第1个周期化疗开始1~3天即退出试验;2例因Ⅲ级心悸和心律不齐,心电图T波下降明显,于第1个周期化疗开始后1~3天退出试验;单药组62例患者均能至少完成两个周期化疗。以上4例退出试验患者均可评价毒副反应,按意向性分析(intention to treat analysis,ITT)原则纳入统计分析,按符合方案集分析(per-protocol,PP)时不纳入统计分析。本研究经医学伦理委员会通过。
1.2 治疗方案
采用简单随机分组方式,分成联合组66例和单药组62例。联合组采用恩度7.5 mg/m2或15 mg/m2,每天1次,连续输注14 d,休息1周后开始新的疗程。联合GEM 1.0 g/m2,静脉注射,d1,d8;每3周重复,直至疾病进展,最多不超过6个周期。单药组采用GEM 1.0 g/m2,静脉注射,d1,d8;每3周重复,直至疾病进展,最多不超过6个周期。恩度为江苏先声药业有限公司产品,GEM为江苏豪森医药公司产品。
1.3 疗效评价
观察治疗后两组患者的疗效、毒副反应、客观有效率、生活质量、中位无疾病进展生存时间(mPFS)、中位生存时间(mOS)、疾病控制率(DCR)、症状缓解率(CBR)。⑴近期疗效按照实体瘤近期客观疗效评价标准(RECIST):完全缓解(CR),部分缓解(PR),稳定(SD),进展(PD)。客观有效率(ORR)=CR+PR/总例数×100%;疾病控制率(DCR)=CR+PR+SD/总例数× 100%。近期疗效同时采用ITT和PP分析法。ITT是对所有符合方案要求经随机分组进入研究,开始治疗的病例进行统计分析(包括对退出病例的评价),以评价总的处理效果。PP只对依从性好(一般用药量在80%~ 120%),遵照治疗方案基本完成治疗计划的受试者进行统计分析,评价处理措施的效能。无疾病进展生存时间(PFS)是指患者随机入组给药时至任何有记录的病变进展之日或任何原因引起的死亡之日的时间。自判定疗效有效(CR和PR)或稳定(SD)之日开始,每2个月定期随访1次,以观察有效或稳定患者的PFS。⑵毒副反应按NCICTC 3.0毒性反应标准进行评价,每个周期记录毒性反应。
1.4 统计学分析
采用SPSS 17.0统计学软件处理数据。计数资料的比较用χ2检验,生存时间用Kaplan-Meier法分析。以P<0.05为差异有统计学意义。
2 结果
2.1 总体疗效
所有患者共完成340个周期化疗,联合组患者完成174个周期,平均2.80个周期;单药组患者完成166个周期,平均2.96个周期。联合组66例患者中62例可评价疗效,按ITT分析ORR为16.7%(11/66),PP分析ORR为17.7%(11/62)。单药组62例患者中56例可评价疗效,按ITT分析ORR为9.7%(6/62),PP分析ORR为10.7%(6/56)。两组患者ORR比较差异均无统计学意义(P>0.05)。DCR按PP分析联合组、单药组分别为75.8%、57.1%,差异有统计学意义(P<0.05)。见表2。
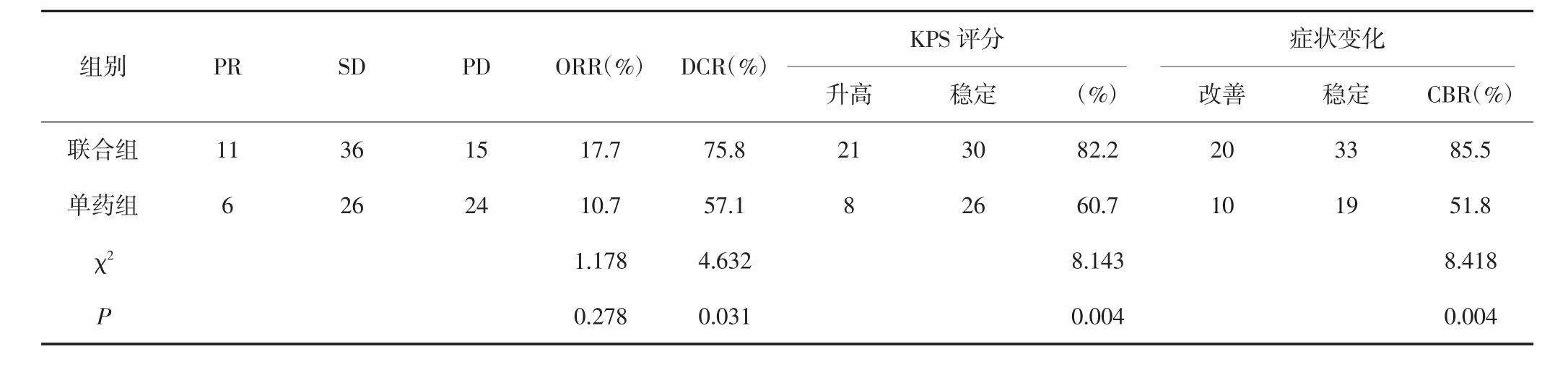
表2 PP分析两组老年晚期NSCLC患者临床疗效的比较(n)
2.2 不同病理类型的疗效
联合组鳞癌与腺癌之间ORR(χ2=0.597,P=0.440)和DCR(χ2=1.608,P=0.205)比较,差异均无统计学意义。腺癌中联合组与单药组的ORR和DCR比较,差异均无统计学意义(P均>0.05),而鳞癌中联合组与单药组的ORR和DCR比较,差异均有统计学意义(P均<0.05)。见表3。
2.3 毒副反应
两组患者治疗后对其血液毒性、非血液毒性和相关生化指标进行比较,差异均无统计学意义(P均>0.05);尤其Ⅲ~Ⅳ级毒性反应的差异无统计学意义;联合组患者中有8例(12.1%)治疗后出现心悸,心电图表现为心律失常,经使用心电监测和输液微注泵控制滴速后可恢复,说明恩度联合GEM治疗老年晚期NSCLC并不增加毒副反应。见表4。
2.4 随访和预后
自2009年5月起,对每例患者每2个月复检1次,截至2013年12月,依据可供评价的病例108例,中位随访时间8.6个月。其中,联合组57例,失访5例,已死亡35例,mPFS为4.0个月[95%CI(3.911~4.099)],mOS为9.1个月[95%CI(7.745~10.455)]。单药组51例,失访5例,已死亡33例,mPFS为3.7个月[95%CI(3.489~3.911)],mOS为8.5个月[95%CI(7.188~9.812)],两组mPFS比较,χ2=4.879,P=0.027,差异有统计学意义。见图1。两组mOS比较,χ2=0.656,P=0.418,差异无统计学意义。见图2。

表3 PP分析两组不同病理类型老年晚期NSCLC的疗效比较(n)

表4 两组老年晚期NSCLC患者治疗后主要毒副反应比较(n)
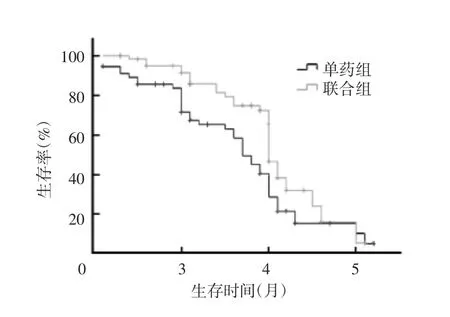
图1 两组患者mPFS的生存曲线比较
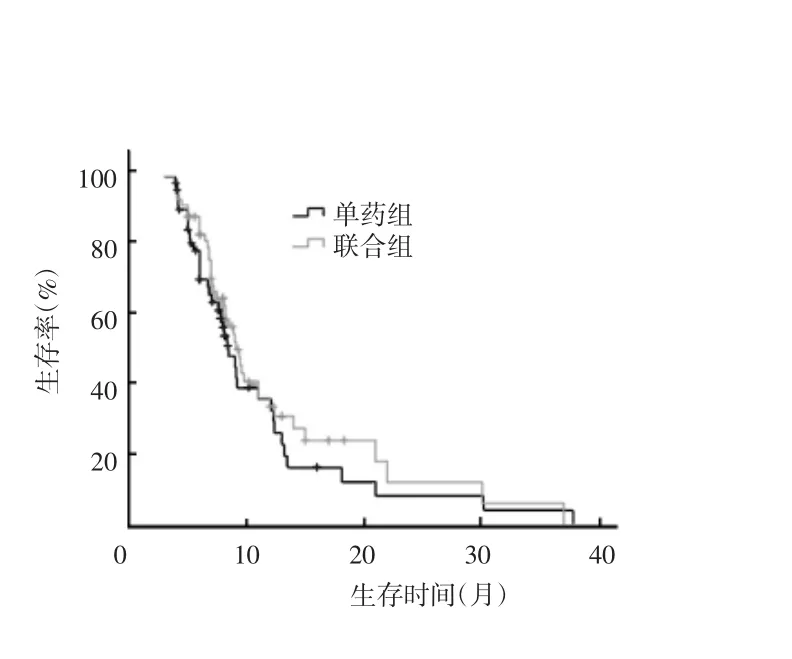
图2 两组患者mOS的生存曲线比较
3 讨论
2013年以来,NCCN的NSCLC临床实践指南指出[9],对于EGFR和ALK突变状况未明或野生型的NSCLC患者,推荐使用血管靶向联合化疗。而对于老年或功能状态评分差(KPS≥2分)的晚期NSCLC患者则不建议使用以铂类为基础的联合化疗标准方案。因为老年患者的肝、肾、骨髓储备功能相对较低,功能状态评分差的患者一般均合并其他疾病,这两类患者在治疗过程中都会使铂类化疗相关的毒副反应增加。因此,临床指南推荐老年晚期NSCLC患者使用单药化疗[9]。
MILES试验是迄今入组人数最多针对老年晚期NSCLC的多中心Ⅲ期临床研究,共计入组698例患者,结果显示吉西他滨与长春瑞宾联合治疗组与两种单药治疗组相比,ORR、肿瘤进展时间(TTP)、mOS及患者生活质量均未显示出优势,且联合用药组其毒性高于两种单药治疗组[10]。Hainsworth等[11]报道GEM联合多西紫杉醇(DOC)与DOC单药治疗老年晚期NSCLC患者的Ⅲ期临床试验结果,发现两组患者总中位生存时间和1年生存率相似,但毒性高于单药治疗组。由此可见,单药治疗仍然是老年晚期NSCLC的标准方案。
2010年JCO发表的IFCT0501研究表明[12],两组中位年龄均接近80岁的451例患者,一线联合化疗组在ORR、PFS及OS均显著优于单药化疗组,PFS改善了1倍(6.3个月vs 3.2个月),OS延长了4个月(10.3个月vs 6.2个月)。联合化疗Ⅲ级/Ⅳ级骨髓抑制发生率均显著高于单药化疗组,毒性相关性死亡发生率高达6%。由此可见,毒性反应仍是铂类为基础联合化疗治疗老年患者临床实践中必须面对的问题。而单药治疗又制约了效果,因此如何在不增加毒副反应的同时,提高老年肺癌的治疗效果,是目前老年肺癌治疗需要解决的问题。血管靶向治疗与化疗联合应用可明显提高抗癌药物疗效[13],包括对老年晚期NSCLC[14]。恩度Ⅲ期临床研究的结果表明[7],治疗组与对照组比较,ORR分别为35.4%、19.5%,mTTP分别为6.3月、3.6月,1年生存率分别为62.8%、31.4%,几乎不增加毒副反应。这为进一步提高老年NSCLC单药治疗效果提供了契机。
本研究选择恩度联合单药GEM一线治疗老年晚期NSCLC,并通过随机抽样的方法设立单药对照组进行对比。结果显示,虽然两组ORR和mOS比较差异无统计学意义,但是DCR、mPFS、症状缓解率、QOL改善率与对照组比较差异均有统计学意义,表明恩度联合单药GEM的方案可以较好地控制老年晚期NSCLC的疾病进展,缓解肺癌临床症状,改善患者的生活质量,并且延长疾病进展时间。在血液毒性、非血液毒性、相关生化指标方面,尤其Ⅲ级/Ⅳ级毒性反应,两组比较差异无统计学意义。毒副反应主要源于化疗药物本身,本组联合组患者在治疗后出现心悸8例(12.1%),心电图表现为心律失常7例(10.6%),经使用心电监测和输液微注泵控制滴速即可恢复正常,并未停药。说明恩度联合GEM治疗老年晚期NSCLC并不增加毒副反应。
本研究联合组评价SD的病例中主病灶缩小10%~25%,或缩小≥30%,但次要病灶增多、增大和发现新病灶的患者共有12例,占19.4%;单药组相应病例仅为5例,占8.9%。联合组5例肺部细小转移结节,治疗后显著减少或消失,充分说明恩度联合GEM单药化疗对老年晚期NSCLC临床症状和生活质量的改善优于单药组。
本研究在病理分型的亚组统计分析时,发现鳞癌亚组的ORR、mPFS联合组优于单药组,差异有统计学意义,提示老年晚期肺鳞癌可能在恩度+GEM治疗中获益。分析可能的原因是GEM是当前肺鳞癌化疗的首选,而血管靶向药物能提高疗效和延长生存,故恩度+GEM构成优化配置。另外,OS受后续治疗的影响较大,尤其受靶向药物治疗的影响,因此,当前国内外大多数的临床研究虽在ORR、mPFS获得优势,但在mOS上往往差异无统计学意义。而鳞癌并非靶向治疗的优势人群,受到后续治疗的影响较少,预示肺鳞癌患者使用恩度+GEM方案,有可能延长OS,因此有必要设立专门的对照研究以进一步明确,有关方面值得深入研究。
[1] Vander walde A,Pal SK,Reckamp KL.Management of non-small-cell lung cancer in the older adult[J].Maturitas,2011,68(4):311-321.
[2] Quoix E,Westeel V,Zalcman G,et al.Chemotherapy in elderly patients with advanced non-small cell lung cancer[J].Lung Cancer,2011,74(3):364-368.
[3] Gajra A,Lichtman SM.Treatment of advanced lung cancer in the elderly[J].Hosp Pract,2011,39(2):107-115.
[4] Owonikoko TK,Ragin CC,Belani CP,et al.Lung cancer in elderly patients:an analysis of the surverillance,epidemiology,and end results database[J].J Clin Oncol,2007,25(35):5570-5577.
[5] Weiss J,Stinchcombe TE.Treatment of elderly patients with stage IV non-small-cell lung cancer[J].Expert Rev Anticancer Ther,2012,12(1):111-120.
[6] 张明云,张菁华,李兴德,等.老年肺癌流行病学及临床治疗现状[J].现代肿瘤医学,2010,18(12):2505-2507.
[7] 王金万,孙燕,刘永煜,等.重组人血管内皮抑素联合NP方案治疗晚期NSCLC随机、双盲、对照、多中心Ⅲ期临床研究[J].中国肺癌杂志,2005,8(4):283-290.
[8] 杨林,王金万,孙燕.重组人血管内皮抑制素YH-16治疗晚期非小细胞肺癌的临床研究[J].中华肿瘤杂志,2006,2:138-141.
[9] Ettinger DS,Akerley W,Borghaei H,et al.Non-small cell lung cancer,version 2.2013[J].J Natl Compr Canc Netw,2013,11(6):645-653.
[10]Gridelli C,Cigolari S,Gallo C,et al.Activity and toxicity of gemcitabine and gemcitabine+vinorelbine in advanced non-small-cell lung cancer elderly patients:PhaseⅡ data from the Multicenter Italian Lung Cancer in the Elderly Study(MILES)randomized trial[J].Lung Cancer,2001,31(2-3):277-284.
[11]Hainsworth JD,Spigel DR,Farley C,et al.Weekly docetaxel versus docetaxel/gemcitabine in the treatment of elderly or poor performance status patients with advanced non-small cell lung cancer:a randomized phase 3 trial of the Minnie Pearl Cancer Research Network[J].Cancer,2007,110(9):2027-2034.
[12]Quoix E,Zalcman G,Oster JP,et al.Carboplatin and weekly paclitaxel doublet chemotherapy compared with monotherapy in elderly patients with advanced non-small-cell lung cancer:IFCT-0501 randomised,phase 3 trial[J].Lancet,2011,378(9796):1079-1088.
[13]Sandler A,Gray R,Perry MC,et al.Paclitaxel-carboplatin alone or with bevacizumab for non-small-cell lung cancer[J].N Engl J Med,2006,355(24):2542-2550.
[14]Leighl NB,Zatloukal P,Mezger J,et al.Efficacy and safety of bevacizumab-based therapy in elderly patients with advanced or recurrent nonsquamous non-small cell lung cancer in the phaseⅢBO17704 study(AVAiL)[J].J Thorac Oncol,2010,5(12):1970-1976.
[2014-07-24收稿][2014-08-15修回][编辑 阮萃才]
Comparison of gemcitabine alone and gemcitabine combined with Rh-endostatin as firstline treatment for elderly with advanced non-small cell lung cancer:a randomized controlled trial
CHEN Qun1,SHI Qin1,XIE Qiang1,XIAO Song2(1Department of Oncology,Fuzhou Pulmonary Hospital,The Teaching Hospital of Fujian Medical University,Fuzhou 350008,P.R.China;2Department of Respiratory Medicine,Putian City Hanjiang Hospital,Putian 350001,P.R.China)
Objective To compare the efficacy and safety of gemcitabine alone or in combination with Rh-endostatin as a first-line treatment for elderly patients with advanced non-small cell lung cancer(NSCLC).Methods A total of 128 elderly patients with pathologyconfirmed,advanced NSCLC were recruited between 1 April 2009 and 31 May 2013 and randomized to receive gemcitabine alone(n=62)or gemcitabine with Rh-endostatin(n=66).Therapeutic efficacy was evaluated strictly according to RECIST criteria after 2 treatment cycles,and median survival time(mOS)and median progression-free survival(mPFS)were recorded.Per-cycle safety and efficacy were evaluated for all subjects according to NCICTC 3.0 criteria.Results In the group receiving combination therapy,11 cases were PR,36 were SD,and 15 were PD.In the gemcitabine-alone group,6 cases were PR,26 were SD,and 24 were PD.Overall response rate was similar between the combination group and gemcitabine-alone group,in terms of both ITT(16.7%vs 9.7%,P=0.326)and PP(17.7%vs 10.7%,P=0.278).However,the two groups differed significantly in DCR(PP)(75.8%vs 57.1%,P=0.031)andmPFS(4.0 vs 3.7 months,P=0.027),and mOS was similar between the two groups(9.1 vs 8.5 months,P=0.418).Major toxic effects included bone marrow aplasia,such as neutropenia and anemia,which generally correlated with the chemotherapy regimen(most were G 1/2;a few were G 3/4).Conclusion The combination of gemcitabine and Rh-endostatin offers therapeutic benefits to elderly patients with advanced NSCLC and may be reasonably tolerated by most patients.
Lung neoplasm;Non-small cell lung cancer;Recombinant human endostatin;Elderly;Single-agent chemotherapy
R734.2
A
1674-5671(2014)03-06
10.3969/j.issn.1674-5671.2014.03.10
