三维泡沫石墨烯在抗坏血酸的干扰下检测尿酸
2014-04-27栾汝水岳红彦俞彦飞张博文杨洋吕品
栾汝水,岳红彦,俞彦飞,张博文,杨洋,吕品
(哈尔滨理工大学材料科学与工程学院,黑龙江哈尔滨 150040)
三维泡沫石墨烯在抗坏血酸的干扰下检测尿酸
栾汝水,岳红彦*,俞彦飞,张博文,杨洋,吕品
(哈尔滨理工大学材料科学与工程学院,黑龙江哈尔滨 150040)
该文采用化学气相沉积法在泡沫镍上生长石墨烯,通过扫描电镜、X射线衍射、拉曼光谱对生成产物的形貌和结构分别进行了表征。结果表明:所制得的石墨烯为具有三维网状结构且层数较少的石墨烯。将三维泡沫石墨烯转移到ITO玻璃上制成生物传感器的工作电极,利用电化学工作站对尿酸和抗坏血酸进行检测,电化学测试结果表明:三维泡沫石墨烯修饰电极在抗坏血酸的干扰下可以准确的检测尿酸,其灵敏度为0.274 μA/(μmol/L),线性范围为10~100 μmol/L。
三维泡沫石墨烯;化学气相沉积法;尿酸;抗坏血酸;生物传感器
0 引言
尿酸,是人体的一个主要嘌呤代谢产物,被视为是重要的天然抗氧化剂[1]。尿酸水平异常可导致一些常见疾病的发生,如痛风、高尿酸血症和帕金森氏病等[2]。抗坏血酸是人类饮食中的一种重要维生素,其抗氧化的特性是众所周知的[3]。尿酸、抗坏血酸这两种物质,在人体的中枢神经系统和血清中的细胞外液中共存。然而,当使用传统固体电极的生物传感器时[4],因为他们的氧化电位彼此重叠,比表面积不足,很难检测到这两种物质混合在一起时的每种物质,使其选择性和灵敏度都很差。虽然高性能液相色谱法、酶方法、微流体系统可用于定量地检测这些物质并具有高度的灵敏性,但这些方法由于成本高、实验条件复杂等[5~7]大多都不被采用。目前,电化学方法已引起人们高度的重视,电化学传感器结构简单、成本较低、灵敏度高、选择性好,以及具有良好的重复性和稳定性,并且具有低的检测限[8~9],已被广泛应用到科学研究、临床检测和工业分析中。
石墨烯,又称单层石墨,是一种由碳原子以sp2杂化轨道组成六角型呈蜂巢晶格的平面薄膜,是只有一个碳原子厚的二维材料。因具有优异的电学、力学、光学、化学、热学以及高比表面积等特性,石墨烯被认为是“后硅时代”的新潜力材料,其潜在应用领域包括高速晶体管、透明电极、印刷电子、新型复合材料、超灵敏传感器、新型催化剂、基因测序、储能装置等[10]。石墨烯这种物质在外界条件下具有十分稳定的化学性质,并在许多科学领域和实际应用中具有许多潜在的用途。
该文采用化学气相沉积法制备三维泡沫状石墨烯,并将其用于构建修饰电极,利用其具有高孔隙率、导电性能良好等优点实现了对尿酸和抗坏血酸的检测,揭示三维泡沫状石墨烯修饰电极的生物传感器对尿酸具有高度的选择性和灵敏度。
1 实验
1.1 实验材料
泡沫镍(Alantum公司);聚甲基丙烯酸甲酯(PMMA,Sigma-Aldrich公司);乳酸乙酯(Sigma-Aldrich公司);尿酸(UA,Sigma-Aldrich公司);抗坏血酸(AA,Sigma-Aldrich公司)。
1.2 三维泡沫石墨烯电极的制备
首先,以泡沫镍为模板制备出三维泡沫石墨烯。具体工艺如下:将泡沫镍(所用泡沫镍密度为420 g/m3,厚度为1.6 mm)置于石英管式炉中央,在氩气和氢气(氩气的流速为500 sccm,氢气的流速为200 sccm)的保护下从室温以40℃/min的升温速率加热至温度为1 010℃,保温30 min,然后向管式炉中以20 sccm的速率通入甲烷气体10 min,然后将石英管式炉以100℃/min的冷却速率冷却至室温,得到被石墨烯包裹的泡沫镍。
然后,去除泡沫镍,制备三维泡沫石墨烯。具体工艺如下:第一步,将得到的被石墨烯包裹的泡沫镍切割成表面积为1×1 cm2的小块;第二步,将PMMA(质量分数为4%)溶于乳酸乙酯中,并且在温度为100℃的条件下加热搅拌2 h得到混合溶液,按每平方厘米200 μL的使用量利用加样枪将混合溶液滴加到泡沫石墨烯上,在室温下自然干燥,然后在温度为180℃的条件下保温0.5 h得到表面包覆PMMA的泡沫石墨烯,并将其完全浸泡于温度为90℃、浓度为3 mol/L的盐酸溶液中6 h磁力搅拌100 r/min,得到去除镍的三维泡沫石墨烯;第三步,将得到的去除镍的三维泡沫石墨烯浸泡于温度为60℃的丙酮中1 h,得到去除PMMA的泡沫石墨烯,然后用蒸馏水将去除PMMA的泡沫石墨烯清洗干净,并将清洗干净的泡沫石墨烯转移到干净的ITO玻璃(所用的ITO玻璃是先后依次在丙酮中超声清洗15 min,乙醇中超声清洗15 min和去离子水中超声清洗15 min,在室温下自然干燥得到的)上;第四步,将样品置于冷冻干燥机中,冷冻到40℃后真空干燥5 h;第五步,将冷冻干燥后的样品进行热处理1 h,温度为450℃。具体步骤如图1所示。
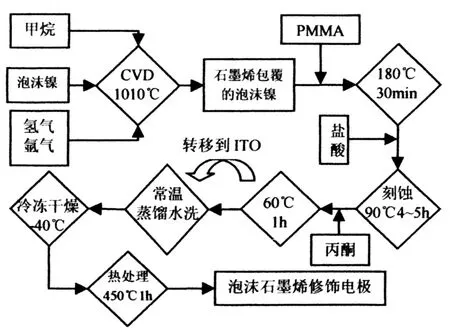
图1 泡沫石墨烯生物传感器制备流程Fig.1Graphene foam biosensor preparation process
最后,将热处理后的三维泡沫石墨烯用作生物传感器的工作电极。
1.3 表征方法
扫描电子显微镜(SEM)采用JSM-7000F型扫描电镜;XRD衍射分析仪采用日本RIGAKU公司的D/Max-RB衍射仪(Cu靶,Kα辐射,λ= 0.154 056 nm),扫描范围5°~80°;拉曼光谱(Raman)分析采用英国RENISHAW公司的RM-1000型显微共焦激光拉曼光谱仪,激光波长为514 nm。
1.4 电化学性能测试
所有的电化学测量,包括循环伏安曲线(CV)和差分脉冲伏安曲线(DPV)都是在0.1 mol/L的PBS缓冲溶液(pH=7.4)中进行的,采用CS350型电化学工作站(武汉科思特公司)和三电极体系在室温下进行检测。三维泡沫石墨烯作为工作电极,Ag/AgCl电极作为参比电极,Pt电极作为安全电极。CV的扫描速率为50 mV/s,其他说明除外。DPV的记录范围为-0.2~+0.6 V,基本参数如下:脉冲幅度:50 mV,脉冲宽度:0.2 s,时间间隔:0.5 s,脉冲宽度:4 mV。
2 结果与分析
2.1 三维泡沫石墨烯的表征
图2-A为用于制备三维泡沫石墨烯的泡沫镍的SEM图。图中可以清晰地看出,泡沫镍具有疏松多孔的三维立体结构,其孔径均匀约为200 μm,且表面光滑。图2-B为泡沫镍被刻蚀后三维泡沫石墨烯的结构,去除镍后的石墨烯结构相对泡沫镍虽然略有变化,似乎有部分结构塌陷,但整体看来能够保持原来的三维结构,并且孔径大小与泡沫镍模板一致。说明镍支架结构已经被完全去除,所形成的结构为碳自支撑结构。通过化学气相沉积发制备的三维石墨烯能够保持泡沬镍的三维连通网络结构。

图2 泡沫镍A及泡沫石墨烯B的SEM图Fig.2A,SEM images of nickel foam,B,SEM images of GF
将化学气相沉积法制得的泡沫石墨烯进行XRD测试,得到如图3-A所示的XRD图谱。图上可见清晰2个特征衍射峰,依次为26.5°、54.6°。这些衍射峰分别对应(002)及(004)晶面。通过对比标准PDF卡片JCPDS75-1621可知,以上衍射峰都与石墨的晶面指数相对应。在衍射峰中没有观察到其它杂质的衍射峰值说明产物较为纯净。XRD结果证明化学气相沉积法生产出的样品为石墨烯且足够纯净。图3-B为三维泡沫石墨烯的Raman测试,可以看出在1 578 cm-1,及2 685 cm-1处有明显的特征峰。两个强峰分别对应G带和2D带,前者是由sp2杂化的碳原子的共面振动引起的G峰。而后者则是双共振拉曼散射引起的2D峰。2D峰的出现表明我们制备的3D石墨烯具有高质量。另外,此峰对石墨烯的厚度很敏感。在谱图中没有发现由缺陷引起的D峰(1 350 cm-1左右),再次证明样品具有高质量。
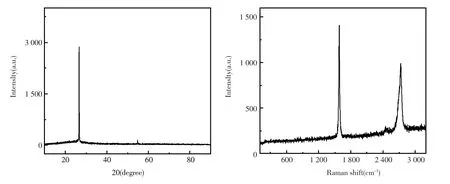
图3 三维泡沫石墨烯的表征A,XRD图谱;B,Raman图谱Fig.3A,XRD patterns of GF.B,Raman spectrum of GF
2.2 电化学性能测试
2.2.1 CV测试
图4中A和B分别表示的是扫描电位在-0.2~+0.6 V之间,扫描速率为50 mV/s,三维泡沫石墨烯修饰电极及裸玻碳电极在1 mmol/L的 UA和1 mmol/L的AA中测得的CV曲线图。石墨烯修饰电极得到UA及AA的氧化峰大概为0.51 V和0.49 V,而裸玻碳电极观察到的氧化峰约为0.37 V和0 V。明显看出,石墨烯修饰电极测得的UA和AA的电流峰值比裸玻碳电极测得的高很多。这可能是高导电的三维石墨烯网络结构提供了一个巨大的比表面积,从而提高从生物分子到离子和电子传输能力。图4-C为石墨烯修饰电极在1 mmol/L的AA和50 μmol/L的UA混合溶液中的CV曲线,UA的氧化峰明显比AA高很多,说明三维泡沫石墨烯对UA的灵敏度要比AA好。
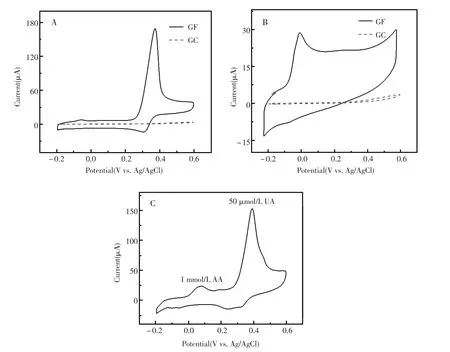
图4 三维泡沫石墨烯修饰电极和裸玻碳电极在A,1 mmol/L UA中的CV曲线和B,在1mmol/L AA中的CV曲线;C,三维泡沫石墨烯修饰电极在含有1mmol/L AA和50 μmol/L UA中的CV曲线Fig.4Curves of GF electrcode and GC electrcode t a scan rate of 50 mV/s A,in UA and B,1 mmol/L AA;C,CV curves of GFelectrode in 1 mmol/L AA and 50μmol/L UA
图5-A是UA在扫描速率为10~100 mV/s测得的CV曲线。从循环伏安曲线中可以看出,氧化峰电流随着扫描速率的增加而增加,同时氧化峰电流位置正移。氧化峰电流与扫描速率的平方根成正比,如图5-B所示,拟合曲线方程为:Ip (μA)=0.061+1.926 v1/2(mV/s),线性相关系数:r= 0.990 2。根据Randles-Sevcik方程:Ip=kn2/3AD1/2cv1/2式中k为Randles-Sevcik常数,n为交换电子数,A为电极面积,D为扩散系数,c为浓度。由公式可知,若氧化峰电流Ip与扫描速率的平方根v1/2成正比,则这个反应是准可逆氧化还原反应,电极反应是扩散型。这说明UA是通过扩散作用扩散到电极表面的,可通过此传感器对UA进行电化学检测。
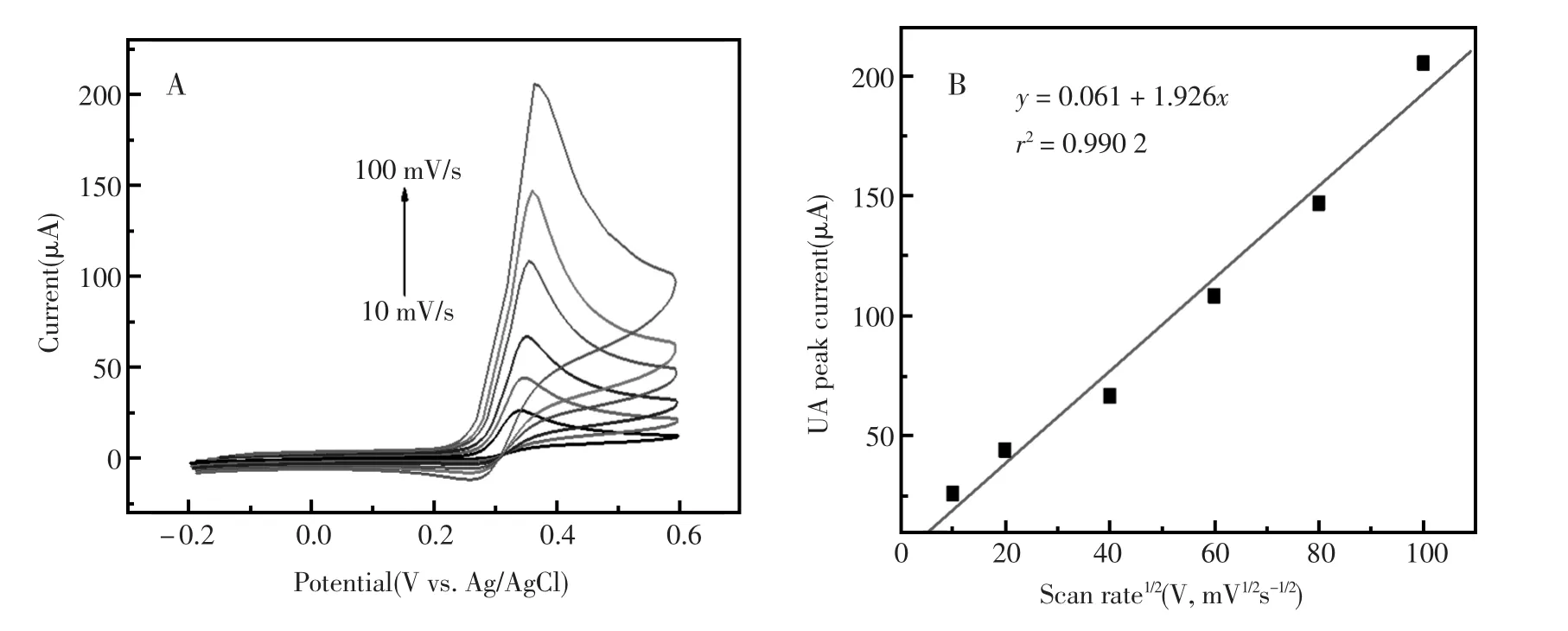
图5 A,不同扫描速率下的CV曲线,其扫描速率分别为10,30,50,75,100 mV/s;B,扫描速率平方根与氧化峰电流的关系图Fig.5CV curves of GF in 1 mmol/L UA at different scan rates.A,Scan rates are 10,30,50,75 and 100 mV/s; B,Relationship of the oxidation peak currents of UA versus the square-root of the scan rate
图6-A为不同浓度UA的CV曲线,可以明显地观察看到,随着UA浓度的增大,循环伏安曲线中对应的氧化峰电流值也逐步增大,并且氧化峰位置逐渐升高,并且不断向正电极方向偏移。由图观察发现这些点呈线性关系,拟合曲线方程为:IUA(μA)=47.419+0.633cUA(μmol/L),线性相关系数为:r=0.992 2。这说明在UA的浓度为25~100 μmol/L的范围内,氧化峰电流与UA的浓度呈线性关系。
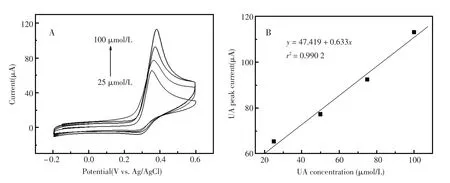
图6 A,不同浓度UA的CV曲线;B,UA浓度与氧化峰电流的线性图Fig.6CV curves of UA at different concentrations.A,UA concentrations from bottom to top:25,50,80,100 μmol/L;B,Relationship of the oxidation peak currents of UA versus UA concentrations
2.2.2 DPV测试
为了进一步研究该传感器对UA检测的灵敏度,我们使用DPV法对该修饰电极进行测试。图7-A为在0.1 mmol/LAA干扰的不同浓度UA的DPV曲线。图中由下至上UA的浓度依次为2.5 μmol/L、5 μmol/L、10 μmol/L、20 μmol/L、40 μmol/L、60 μmol/L、80 μmol/L、100 μmol/L。由图可以看出,不同浓度UA的氧化峰位置均在+0.4 V左右,。随UA浓度的增加,氧化峰电流也逐步增加,AA对UA的影响逐渐变弱。氧化峰电位与UA的浓度呈线性关系,如7-B所示拟合曲线方程为:IUA(μA)=15.003+0.274cUA(μmol/L),线性相关系数:r=0.995 9,灵敏度为0.276 μA/(μmol/L)。说明在UA的浓度为10~100 μmol/L的范围内,氧化峰电流与UA的浓度呈线性关系。
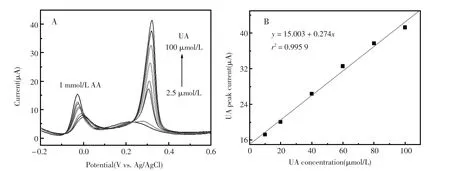
图7 A,不同浓度UA的DPV曲线;B,UA浓度与氧化峰电位的线性图Fig.7DPV measurements of GF in UA with low concentrations.a,UA concentrations from bottom to top:2.5,5, 10,20,40,60,80 and 100 μmol/L;B,Relationship of the oxidation peak currents of UA versus UA concentration. DPV conditions:pulse height:50 mV;pulse width:200 ms;step height:4 mV;step time:500 ms
3 结论
该文采用化学气相沉积法在泡沫镍上生长石墨烯,制备出层数较少、质量较高的三维多孔状、导电性能良好的石墨烯,将其转移到ITO玻璃上制成修饰电极,对UA和AA进行电化学性能测试。在10~100 μmol/L的UA浓度范围内,三维泡沫石墨烯的灵敏度为0.274 μA/(μmol/L)。
[1]Young J S,Alexander F O,Young K.High-resolution Tunnelling spectroscopy of a Graphene Quartet Metal matrix Composites–From Science to Technological significance[J].Natrue,2011,467:185~189.
[2]Zhao J,Zhang W,Sherrel P,et al.Carbon Nanotube Nanoweb-Bioelectrode for Highly Selective Dopamine Sensing[J].ACS Appl.Mater.Interfaces,2012,4:44~48.
[3]Khan M M I,Haque A M J,Kim K.Electrochemical Determination of Uric Acid in the Presence of Ascorbic Acid on Electrochemically Reduced Graphene Oxide Modified Electrode[J].J.Electroanal.Chem.,2013,600: 54~59.
[4]Bryan T,Luo X,Forsgren L,et al.The Robust Electrochemical Detection of a Parkinson's Disease Marker in Whole Blood Sera[J].Chem.Sci.,2012,3:3 468~3 473.
[5]Zheng G,Patolsky F,Cui Y,et al.Multiplexed Electric Detection of Cancer Markers with Nanowire Sensor Arrays[J].Nature Biotech.,2005,23:1 294~1 301.
[6]Wang J,Hoekstra J G,Zuo C,et al.Biomarkers of Parkinson’s disease:Current Status and Future Perspectives [J].Drug Discov Today,2013,18:155~162.
[7]Ge L,Wang S,Yu J,et al.Molecularly Imprinted Polymer Grafted Porous Au-Paper Electrode for an Microfluidic Electro-Analytical Origami Device[J].Adv.Funct. Mater.,2013,23:3 115~3 123.
[8]Sun C C,Luo F F,Wei L,et al.Association of Serum Uric Acid Levels with the Progression of Parkinson’s Disease in Chinese Patients[J].Chin.Med.J.(Engl),2012,125: 583~587.
[9]Li S,Qian T,Wu S,et al.Controllable Fabrication of Polystyrene/Graphene Core-Shell Microspheres and its Application in High-Performance Electrocatalysis[J]. Chem.Commun.,2012,48:7 997~7 999.
[10]Hu Y,Lin L,Zhang Y,et al.Replacing a Battery by a Nanogenerator with 20V Output[J].Adv.Mater.,2012, 24:110~114.
Detection of uric acid in the presence of ascorbic acid with a 3D graphene foam modified electrode
Luan Ru-shui,Yue Hong-yan*,Yu Yan-fei,Zhang Bo-wen,Yang Yang,Lv Pin
(College of Materials Science and Engineering,Harbin University of Science and Technology,Harbin 150040, China)
By using the chemical vapor deposition,the three dimensional porous high conductivity of graphene foam (GF)was fabricated on nickel foams as a template.GF was characterized by scanning electron microscopy,X-ray diffraction and Raman spectroscopy.Then the GF was transferred onto ITO coated glass,acting as an electrode to detect uric acid and ascorbic acid by electrochemical methods.Electrochemical results showed that the GF modified exhibited high selectivity for the detection of UA in the presence of AA,the sensitivity for detection of UA was 0.274 μA/(μmol/L),and the UA concentration ranges from 10 to 100 μmol/L.
graphene foam;nickel foam;chemical vapor deposition;uric acid;ascorbic acid
哈尔滨理工大学青年拔尖人才项目(201306)
*通讯联系人,E-mail:hyyue@hrbust.edu.cn
