靛玉红自乳化释药系统的制备
2014-04-01王云红张传辉柯秀梅周文杰杨荣平
刘 楠, 王云红, 张传辉, 柯秀梅, 周文杰, 杨荣平*
(1.成都中医药大学,四川 成都 611137;2.重庆市中药研究院重庆市中药资源学重点实验室,重庆 400065)
靛玉红(Indirubin)为双吲哚类生物碱成分,临床主要用于治疗慢性粒细胞白血病(Chronic Myelogenous Leukemia,CML)。早期经中国医学科学院对中成药当归芦荟丸进行拆方研究确定青黛中的靛玉红为治疗CML的有效成分,对肿瘤细胞具有明显的抑制作用[1-2]。靛玉红片为重庆市中药研究院制药厂早期产品,多年临床应用表明其对CML有明显疗效,但由于靛玉红的水溶性与脂溶性均较差,存在生物体内溶解度低、生物利用度差、肠胃刺激性较大等问题而限制其临床应用[3-4]。
自乳化给药系统(Self-emulsifying Drug Delivery System,SEDDS)是由药物、油相、乳化剂和助乳化剂组成的固体或液体剂型,口服后能在胃肠道蠕动或环境温度(37℃)及温和搅拌的条件下自发形成水包油型乳剂,能够显著提高难溶性药物的溶解和溶出,提高口服给药的相对生物利用度[5-9]。本实验在文献报道基础上,通过测定靛玉红在辅料中的溶解度,筛选增溶效果较好的油相、表面活性剂、助表面活性剂,绘制三元相图并结合星点设计优化获得最佳自乳化处方,并对比原料药设计相关自乳化制剂体外溶解度和溶出度试验,并对其验证,初步探讨自乳化制剂的增溶机制,为制剂开发提供方向,也为自乳化释药系统的机理研究奠定一定基础。
1 仪器与试药
1.1 仪器 高效液相色谱仪(安捷伦 1200 Series,VWD 检测器190~600 nm,在线脱气,二元泵,安捷伦公司);BS-224S电子天平(十万分之一,赛多利斯公司);Anke TGL-16 C高速离心机(上海安亭仪器厂);SK-1快速混匀器(金坛市城东新瑞仪器厂);HZ-881S台式水浴恒温振荡器(江苏太仓市实验设备厂);DF-101 S 集热式恒温加热磁力搅拌器(郑州市长城科工贸有限公司);RC 806 溶出试验仪(天津市天大天发科技有限公司)。
1.2 试药 靛玉红对照品(飞宇生物科技有限公司,批号FY 11830306,纯度 98.30%);靛玉红原料药(杭州华东医药集团康润制药有限公司,批号120101,纯度>90%);中链甘油三酸酯(MCT,铁岭北亚药用油有限公司);蓖麻油(Castor Oil,成都科龙化工试剂厂);吐温-80(Tween-80,成都科龙化工试剂厂);吐温-20(Tween-20,成都科龙化工试剂厂);吐温-85(Tween-85,成都科龙化工试剂厂);聚乙二醇-200(PEG-200,成都科龙化工试剂厂);聚乙二醇-400(PEG-400,成都科龙化工试剂厂);无水乙醇(成都科龙化工试剂厂);丙二醇(成都科龙化工试剂厂);玉米油(Corn Oil,上海宝曼生物科技有限公司);薄荷油(Mint Oil,西安悦来医药科技有限公司);油酸(Oleic Acid,国药集团化学试剂有限公司);油酸乙酯(Ethyl Oleate,国药集团化学试剂有限公司);油酸正丁酯(Butyl oleate,国药集团化学试剂有限公司);乳化剂-OP(OP,国药集团化学试剂有限公司)、肉豆蔻酸异丙酯(IPM,国药集团化学试剂有限公司);棕榈酸异丙酯(IPP,国药集团化学试剂有限公司);聚氧乙烯蓖麻油(Cremophor EL,上海运宏化工制剂辅料技术有限公司);油酸聚乙二醇甘油酯(Labrafil M 1944CS,法国嘉法狮公司);辛/癸酸聚乙二醇甘油酯(Labrasol,法国嘉法狮公司);二乙二醇单乙基醚(Transcutol P,法国嘉法狮公司);聚甘油油酸酯(Oleique CC497,法国嘉法狮公司);甲醇为色谱纯,其余试剂均为分析纯。
2 方法与结果
2.1 靛玉红含量测定方法
2.1.1 色谱条件 Waster XTerra C18色谱柱(250 mm×4.6 mm,5 μm);流动相甲醇-水(75∶25);检测波长290 nm;体积流量1 mL/min;柱温35 ℃;进样量10 μL。
2.1.2 对照品溶液的制备 精密称取靛玉红对照品 13.12 mg于 100 mL棕色量瓶中,加乙酸乙酯溶解并稀释至刻度,摇匀,即得对照品母液(每1 mL含靛玉红0.131 2 mg),备用。
2.1.3 供试品溶液的制备 取 1 g 靛玉红自乳化乳,精密称定,置10 mL量瓶,加乙酸乙酯溶解并稀释至刻度,配制成一定质量浓度的供试品溶液,摇匀,即得。
2.1.4 空白溶液的制备 按处方比例称定 油酸聚乙二醇甘油酯、聚氧乙烯蓖麻油、二乙二醇单乙基醚置37℃恒温振荡箱震荡 48 h,制得空白自乳化乳。取空白自乳化乳 1 g,按“2.1.3”项方法制备空白辅料溶液。
2.1.5 方法专属性考察 分别取空白溶液、靛玉红对照品溶液、供试品溶液,按上述色谱条件进样测定,结果见图1。如图可见,辅料对靛玉红的测定无干扰。
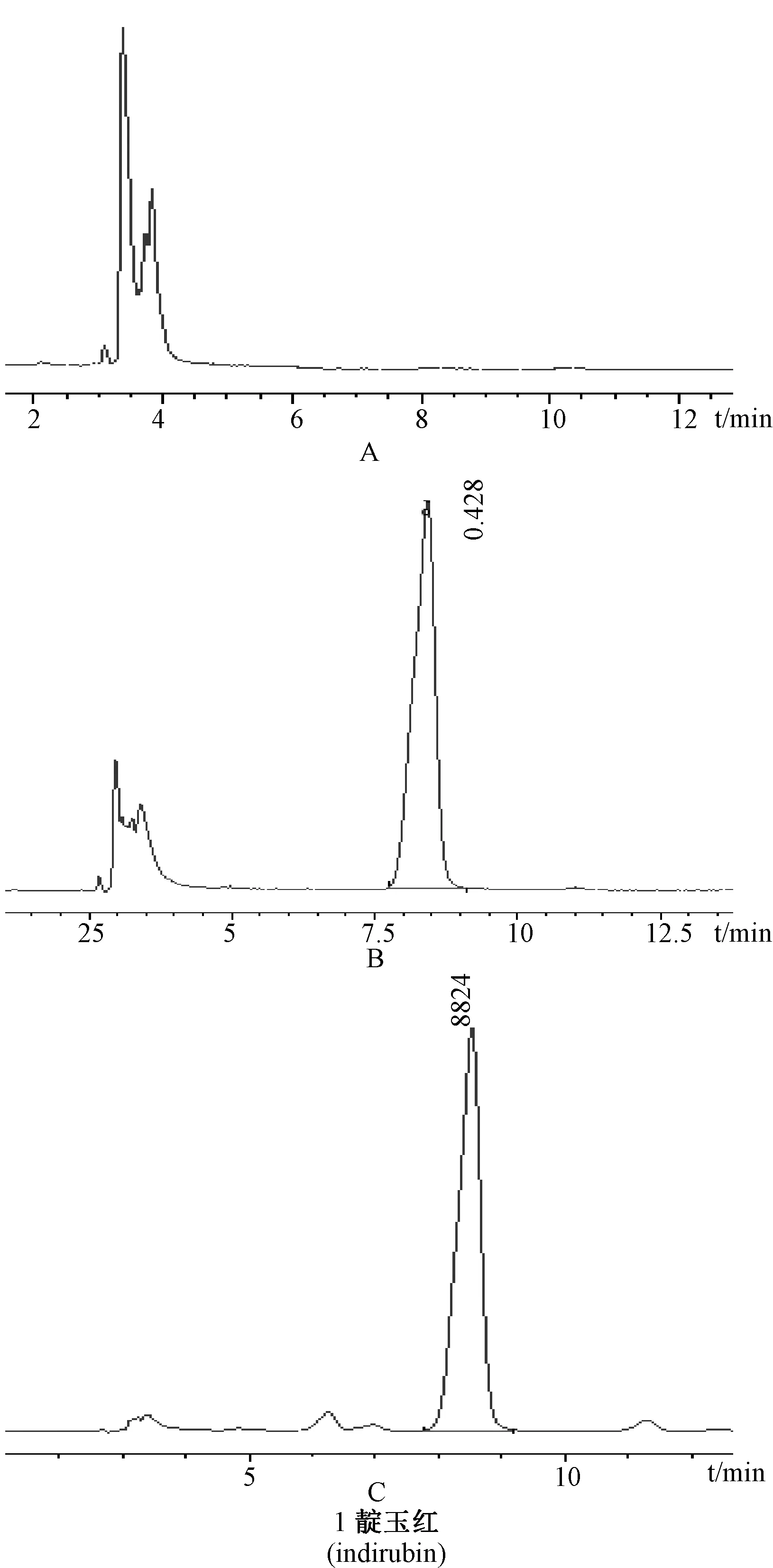
图1 空白溶液(A)、靛玉红对照品溶液(B)、供试品溶液(C)的HPLC色谱图
2.1.6 线性关系考察 精密吸取“2.1.2”项靛玉红对照品溶液 0.2、0.5、1、1.5、2、3、4 mL置 10 mL棕色量瓶中,加乙酸乙酯至刻度,摇匀,滤过,配制成系列对照品溶液。分别精密吸取10 μL注入高效液相色谱仪,于上述色谱条件下测定,记录峰面积。以对照品质量浓度(μg/mL)为横坐标(x),峰面积为纵坐标(y)进行线性回归,得标准曲线方程为y=54.917x+1.063 4,r=0.999 95。表明在 2.624~52.48 μg/mL范围内,靛玉红浓度与其峰面积呈良好的线性关系。
2.1.7 精密度及稳定性试验 分别精密吸取质量浓度为 2.624、19.68、39.36 μg/mL的靛玉红对照品溶液 10 μL,注入高效液相色谱仪连续测定6次,记录峰面积并计算;取同一供试样品溶液,分别于0、2、4、6、8、12、24 h 按色谱条件进样测定,记录峰面积并计算。结果精密度 RSD 分别为 0.30%、0.22%、0.23%,表明仪器的精密度良好;供试品溶液 24 h内稳定性的 RSD 值为 0.17%,表明靛玉红在室温避光保存24 h内基本稳定。
2.1.8 重复性实验 取靛玉红自乳化乳约 0.5 g,精密称定,置 5 mL量瓶中,平行 6 份,分别加乙酸乙酯至刻度,摇匀,滤过,分别精密吸取10 μL,注入液相色谱仪,记录峰面积并计算。结果靛玉红平均含量为 324.3 μg/g,RSD 为0.23%,表明重复性较好。
2.1.9 回收率试验 取靛玉红自乳化乳 0.5 g,精密称定,置10 mL量瓶,平行 6 份,分别加入“2.1.2”项靛玉红对照品溶液 1.2 mL,加乙酸乙酯至刻度,摇匀,滤过,即得。按色谱条件进样测定靛玉红含量并计算回收率。结果平均回收率为 100.64%,RSD 为 0.92%,表明该方法准确度良好。
2.2 靛玉红自乳化制剂的制备
2.2.1 空白自乳化处方的筛选
2.2.1.1 模型药物在各辅料中溶解度测定 分别取不同的油相、表面活性剂、助表面活性剂约 2 mL于具塞刻度试管中,加入过量的靛玉红原料药,涡旋分散,于 37 ℃恒温振荡箱震荡48 h,10 000 r/min 离心 10 min,取上清液用乙酸乙酯适量稀释,按照“2.1”项下建立的方法测定靛玉红在各种辅料中的溶解度,结果见表1。
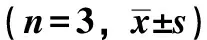
表1 靛玉红在不同油相、乳化剂、助乳化剂中的溶解度
如表1所示,靛玉红在油酸聚乙二醇甘油酯、蓖麻油、中链甘油三酸酯、辛/癸酸聚乙二醇甘油酯、吐温-80、聚氧乙烯蓖麻油、聚乙二醇-400、二乙二醇单乙基醚中的溶解较高,因而拟选用这些辅料做进一步筛选。
2.2.1.2 三元相图的绘制 文献报道[10]自乳化处方中油相一般占 25%~70%、表面活性剂>25%、助表面活性剂 0%~25%。本研究限定自乳化处方各相筛选范围油相0%~30%,表面活性剂20%~80%,助表面活性剂范围 0%~30%。
在如上限定范围内,分别称取不同比例的油相、表面活性剂、助表面活性剂,涡旋混匀。于室温放置 24 h,将不分层且呈均一透明状的处方乳进行下一步筛选。结果筛选出符合条件的如下7个处方:
1.油酸聚乙二醇甘油酯—吐温-80—二乙二醇单乙基醚
2.油酸聚乙二醇甘油酯—聚氧乙烯蓖麻油—二乙二醇单乙基醚
3.蓖麻油—辛/癸酸聚乙二醇甘油酯—二乙二醇单乙基醚
4.蓖麻油—吐温-80—二乙二醇单乙基醚
5.蓖麻油—聚氧乙烯蓖麻油—二乙二醇单乙基醚
6.中链甘油三酸酯—吐温-80—二乙二醇单乙基醚
7.中链甘油三酸酯—聚氧乙烯氢化蓖麻油—二乙二醇单乙基醚
分别取各处方中不同比例0.5 mL 空白乳,加入到 100 mL 37 ℃ 恒温的双蒸水中,磁力搅拌,观察是否成乳。分别以表面活性剂、助表面活性剂、油相各为一边,将能形成澄清透明、半透明及淡蓝色乳光或牛奶状乳且无漂浮油滴的比例确定为相图中有效自乳化区域,绘制三元相图,结果见图 2(黑点:实验点;黑线内区域:有效自乳化区)。
实验结果:在限定范围内处方 1、2 成乳面积较大,处方4~7 成乳区较小,处方 3 不能成乳。其中 2 号处方成乳面积最大,其成乳区的油相范围 20%~80%,表面活性剂范围 20%~80%,助表面活性剂范围 0%~30%。同时结合组成处方的个辅料对药物的溶解度,选择 2 号处方进行优化。
2.2.2 星点设计-效应面法优化处方
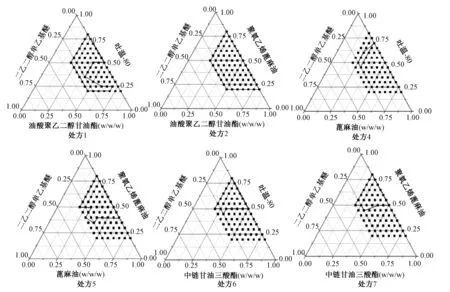
图 2 三元相图
2.2.2.1 星点设计 在三元相图基础上进行处方优化,以油相质量X1、表面活性剂质量X2、助表面活性质量X3为自变量因素,以靛玉红载药量Y1、自乳化时间Y2、总评 OD 值Y3为指标,利用 Design Expert 统计软件进行三因素、五水平的星点设计,实验因素水平、设计及结果见表 2 和表 3。按照星点设计表比例称取油酸聚乙二醇甘油酯、聚氧乙烯蓖麻油、二乙二醇单乙基醚,并加入过量的靛玉红原料药漩涡混匀,置 37 ℃ 振荡仪中振荡 48 h,取出,10 000 r/min 离心 10 min,称取上清乳液用乙酸乙酯适量稀释后按“2.1”项下方法测定溶解度。同时在溶出试验仪上,取上述含药乳 0.2 mL 加入到 400 mL 37 ℃ 去离子水中,用桨法以桨转速 50 r/min 轻微搅拌使自乳化,目测法用秒表记录乳化时间,结果见表 3。

表 2 星点设计的因素及水平
2.2.2.2 模型拟合 数据处理分析引入 OD 值,采用“归一化法”。采用Hassan[11-13]方法分别进行数学转换求“归一值”dmin和dmax,dmin=(ymax-yi)/(ymax-ymin),dmax=(yi-ymin)/(ymax-ymin);OD=(d1d2…dn)1/n,n为指标数。以总评 OD 值为效应进行优化,最后得到综合效应最佳的处方配比。
运用 Design Expert 8.0.5 软件,对实验数据进行多元线性、两因素相互作用(2FI)、二次多项式或更高次项的模型拟合非线性拟合处理,以相关系数(r)和置信度(P)为模型判定标准。结果表明,实验数据采用二项式模型有极显著性差异,相关系数较高,拟合度好。二次项方程如下:
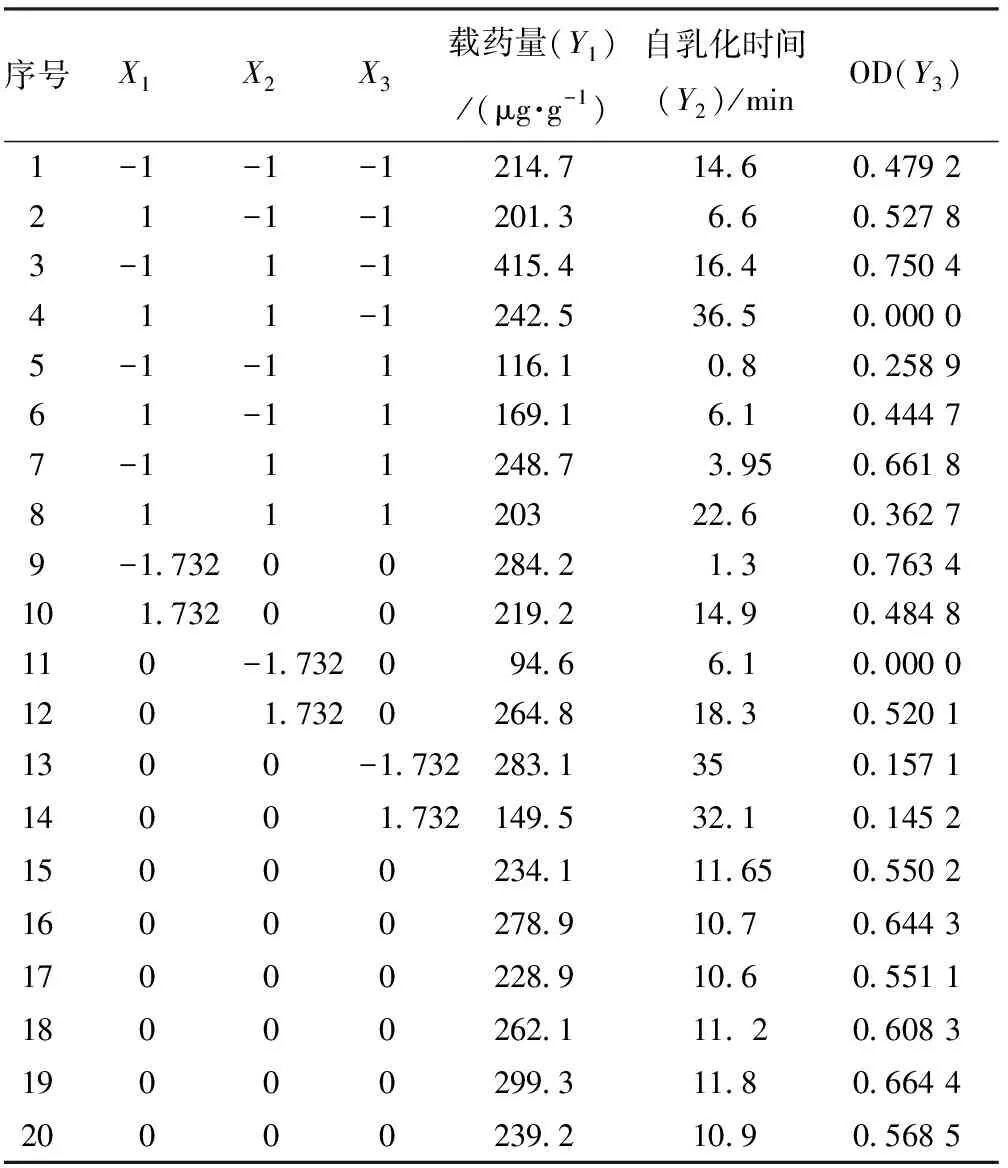
表 3 星点设计与结果


2.2.2.3 结果分析 根据二次多项式模型方程拟合结果作出 OD 值对三个因素中任意两个因素的效应面三维图和二维等高线图(见图 3~5),利用效应面和等高线分析各因素的相互作用。等高线的密度和形状可以反映因素对响应值的影响大小和因素之间的交互强弱[14]。从图 3~5 可以看出油相X1、表面活性剂X2、助表面活性剂X3各因素间交互作用显著。减小油相X1比例,OD 值增大;增大表面活性剂X2比例,OD 值增大;随着助表面活性剂X3比例增加,OD 值呈现出先增大后减小的趋势。根据效应面预测,三因素的较佳范围为:X1:20~35;X2:51~80;X3:12~17。
2.2.2.4 最优处方预测与验证 本研究先以载药量大、自乳化时间最短对靛玉红自乳化制剂处方组成进行预测的最佳处方质量配比为:X1(油酸聚乙二醇甘油酯)=25,X2(聚氧乙烯蓖麻油)=80,X3(二乙二醇单乙基醚)=12.83,预测载药量 337.9 μg/g,自乳化时间为 7.66 min;再以 OD 值最佳对靛玉红自乳化制剂处方组成进行预测,得最佳处方质量配比:X1(油酸聚乙二醇甘油酯)=25,X2(聚氧乙烯蓖麻油)=80,X3(二乙二醇单乙基醚)=15.41,预测载药量 325.9 μg/g,自乳化时间为 6.49 min。两种方式预测结果相差不大,说明采用归一化法进行多指标综合评定方法可行。

图3 油相A、表面活性剂B对OD值的三维效应面图及等高线图
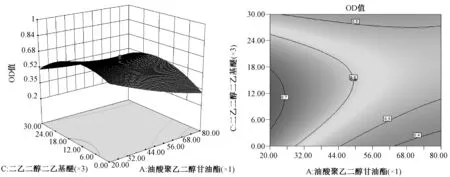
图4 油相A、助表面活性剂C对OD值的三维效应面图及等高线图

图5 表面活性剂B、助表面活性剂C对OD值的三维效应面图及等高线图
以 OD 值最佳预测的处方比例按“2.2.2(1)”项下操作进行验证试验,结果各指标的偏差绝对值均 < 5%,证实所建数学模型预测性良好,结果见表 4:
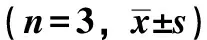
表 4 星点设计-效应面优化法的验证
2.3 靛玉红自乳化释药系统的体外初步评价
2.3.1 外观性状 按星点优选处方比例称取油酸聚乙二醇甘油酯 20 g,聚氧乙烯蓖麻油 80 g,二乙二醇单乙基醚 15.41 g,漩涡混匀,加入40 g 靛玉红原料药,置 37 ℃ 振荡仪中振荡 48 h,制得靛玉红自乳化乳,取适量对其外观性状进行评价。
结果:该自乳化制剂的外观为紫红色均匀透亮的油状液体。在体外溶出实验中,该自乳化制剂完全乳化后形成均一澄明透亮的淡紫色溶液且无药物析出现象。
2.3.2 溶解度
2.3.2.1 靛玉红自乳化制剂在不同分散介质中溶解度的测定 称取 4 份 1 g 靛玉红自乳化乳,分别以水、pH 1.2盐酸溶液、pH 4.5、pH 6.8 磷酸缓冲液为分散介质,稀释 10 倍(v/m),混匀,取 2 mL溶液,加入过量的靛玉红,涡旋 5 min,按“2.1”项下方法测定溶解度。
结果:含药乳在不同分散介质中的溶解度分别为(32.72±0.09)、(32.62±0.06)、(31.97±0.13)、(33.66±0.43)μg,RSD 为 2.13%,表明不同分散介质对自乳化制剂的溶解度测定无明显影响。
2.2.2.2 稀释倍数与溶解度相关性研究 称取 5 份 1 g 靛玉红自乳化乳,以水为分散介质,分别以 10、50、100、200、500 倍(v/m)37 ℃的蒸馏水稀释,混匀,取 2 mL 溶液,加入过量的靛玉红原料药,涡旋 5 min,按“2.1”项下方法测定溶解度:含药乳在各稀释倍数下溶解度分别为(32.72±0.09)、(6.53±0.07)、(3.26±0.06)、(1.63±0.07)、(0.65±0.08) μg/mL,与稀释倍数呈反相关。
2.2.2.3 考察含药乳和空白乳对溶解度测定的影响 各称取 1 g空白自乳化乳和靛玉红自乳化乳,分别以 10、200 倍(v/m) 37 ℃的蒸馏水稀释,混匀,各取 2 mL溶液,加入过量靛玉红原料药,涡旋 5 min,8 000 r/min 离心 5 min,按“2.1”项下方法测定溶解度;另外各取 2 mL 10、200 倍水稀释的含药乳溶液,按“2.1”项下方法测定其中靛玉红含量。
结果:含药乳和空白乳以水稀释 10、200 倍测得的平均溶解度分别为32.72和 0.86、1.63 和 0.19 μg/mL,以10、200倍稀释含药乳液测定的溶解度比相应空白乳液测定的溶解度分别高出 38.05;8.58 倍;测定含药乳 10、200 倍水溶液的靛玉红平均质量浓度为 32.68 和 1.62 μg/mL。
2.3.3 靛玉红自乳化制剂在不同分散介质中的稳定性考察
称取 4 份 1 g 靛玉红自乳化乳,分别以水、pH 1.2盐酸溶液、pH 4.5、pH 6.8 磷酸缓冲液为分散介质,稀释 10 倍(v/m),分别于 0、2、4、6、8、12、24 h 按“2.1”项下方法测定峰面积,计算靛玉红剩余百分含量及 RSD。
结果:不同稀释介质中 24 h 内 RSD 分别为0.52%、0.32%、0.86%、0.28%,表明靛玉红自乳化制剂在不同释放介质中 24 h 内基本稳定,结果见表 5。
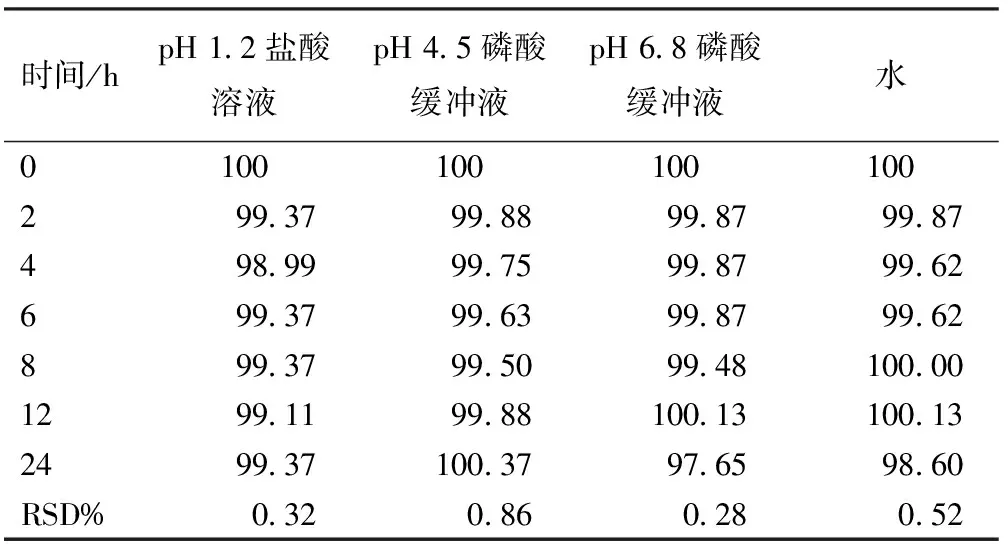
表5 靛玉红自乳化制剂在不同释放介质中24 h稳定性(%)
2.3.4 靛玉红自乳化制剂体外溶出曲线的绘制 由于目前已无市售靛玉红片,因此采用靛玉红原料药与本研究自乳化制剂进行体外释药性对比。取等含药量的自乳化释药系统与靛玉红原料药,照《中国药典》2010 年版(二部)附录XC“溶出度测定法”第三法,以 200 mL 0.1 mol/L HCl 为溶出介质,温度为(37±0.5)℃,转速为 50 r/min,分别于 3、5、10、15、20、30、45、60、90、120 min 时取样 2.0 mL,同时补充等体积释放介质,测定并计算靛玉红累积溶出百分率,绘制溶出曲线,结果见图6。

图6 靛玉红自乳化制剂及原料药的溶出曲线
2.3.5 稳定性 取适量靛玉红自乳化乳置离心管中,10 000 r/min 离心10 min,结果未出现分层现象;取适量靛玉红自乳化乳用蒸馏水稀释 100 倍,于室温密闭避光放置10 d,微乳仍保持均一澄明淡紫色外观;取适量靛玉红自乳化乳置安瓿瓶中,于75%湿度、40 ℃条件下密闭避光贮存,每隔一个月测定靛玉红百分含量,结果3个月内含量依次为(98.47±0.23)%、(97.86±0.36)%、(97.85±0.28)%,且外观均为均一澄明淡紫色溶液,未有明显变化。
3 讨论
难溶性药物的口服吸收决定于溶出速率以及药物在介质中的溶解程度,靛玉红属于生物药剂分类系统 Ⅳ(BCS Ⅳ)类药物,其胃肠道吸收机制属于被动扩散过程,其制剂的切入点在于改善其溶解性能及提高黏膜通透性,进而提高口服生物利用度。自乳化释药系统能提高药物的溶解度且粒径小,比表面积大,易于通过胃肠壁的水化层,增加通透性,促进药物体内吸收。但有文献报道某些自乳化处方口服后由于胃液稀释以及肠道的消化,自乳化处方中各组分的浓度及比例会发生一定变化,降低系统的增溶能力,致使药物沉淀析出,降低制剂的生物利用度[15]。目前对于自乳化释药系统的增溶机制尚无统一定论,实验过程中发现靛玉红自乳化制剂的载药量与其溶解度不同,溶解量大于载药量,因此猜测自乳化增溶机制可能为类似“催化剂”的效应,进而针对本假设进行了验证,考察了含药乳不同稀释倍数与溶解度相关性试验。“2.3.2.2”项实验结果表明,在本研究的条件下,自乳化释药系统的增溶机制不是简单的“催化剂”效应。在此基础上,又考察含药乳和空白乳对溶解度的影响,实验数据提示药物与辅料在自乳化制备过程中的相互作用影响增溶效果,推测可能为自乳化制备过程中药物与辅料形成饱和的 o/w 乳,遇水形成 o/w 乳化体系,药物已经被包裹在其中,因此再加入过量的靛玉红原料药增溶效果不明显;而空白乳与水先形成 o/w 乳化体系,再加入过量的靛玉红原料药,药物进入不到 o/w 体系内核,空白乳稀释10、200倍测得的溶解度相差不大,应该是自乳化辅料改善了药物的润湿性而溶解部分药物。可见这一增溶过程并非简单的物理混匀效果。本研究的假设及结果均为自乳化制剂的增溶机制研究提供一定的思路及方法。
本研究优化出的处方载药量为 324.3 μg/g,自乳化释药系统显著提高了靛玉红的溶解度和溶出度,由于靛玉红原料药的溶解未检测出来,因而以本研究中的最低检测限计算,本研究优化的自乳化处方将靛玉红的溶解度至少提高了 4 000倍,达到了对其增溶的目的,这为后期靛玉红自乳化乳进一步制剂成型提供一定指导意义。
参考文献:
[1] 莲 明,杨尧平,朱传先,等.青黛治疗慢性粒细胞自血病有效成分的研究(I)报[C].中草药研究资料,1979:17:1-6.
[2] 李锡春,汪 英,郭志雄.中药治疗慢性粒细胞白血病的研究进展[J].实用癌症杂志,2011,26(2):213-216.
[3] 籍秀娟,张福荣.靛玉红类化合物的抗肿瘤作用及构效关系的研究[J].药学学报,1985:20(2):137-139.
[4] 李珂佳.靛玉红口服吸收机理研究[D].成都:四川大学,2007.
[5] Mezghrani O, Ke X, Bourkaib N,etal.Optimized self-microemulsifying drug delivery systems(SMEDDS) for enhanced oral bioavailability of astilbin[J].Pharmazie,2011,66(10):754-760.
[6] Guo F, Zhong H, He J,etal.Self-microemulsifying drug delivery system for improved oral bioavailability of dipyridamole:preparation and evaluation[J].ArchPharmRes,2011, 34(7):1113-1123.
[7] Wang Y, Sun J, Zhang T,etal.Enhanced oral bioavailability of tacrolimus in rats by self-microemulsifying drug delivery systems[J].DrugDevIndPharm,2011,37(10):1225-1230.
[8] Setthacheewakul S, Mahattanadul S, Phadoongsombut N,etal.Development and evaluation of self-microemulsifying liquid and pellet formulations of cureumin,and absorption studies in rats[J].EurJPharmBiopharm,2010,76(3):475-485.
[9] Shen Q,Li X,Yuan D,etal.Enhanced oral bioavailability of daidzein by self-micro-emulsifying drug delivery system[J].ChemPharmBull(Tokyo),2010,58(5):639-643.
[10] 沈 熊,吴 伟.自乳化和自微乳化释药系统[J].复旦学报:医学版,2003,30(2):180-183.
[11] 杨 勇,奉建芳,张 慧,等.星点设计效应面法优化蟾酥固体脂质纳米粒制备工艺[J].中国中药杂志,2006,31(8): 650-652.
[12] 周文杰,傅 亚,王云红,等.中心复合设计-效应面法优化玄参的炮制工艺[J].中国实验方剂学杂志,2013,19(4):6-10.
[13] 吴 伟,崔光华,陆 彬.实验设计中多指标的优化:星点设计和总评“归一值”的应用[J].中国药学杂志,2000,35(8):530-533.
[14] 李东东,放茂良,刘 琼,等.星点设计-响应面法优化超声提取青竹标多酚[J].中药材,2011,34(1):129-133.
[15] Attama A A,Nkemnele M O.Invitroevaluation of drug release from self-microe-mulsifying drug delivery systems using a biodegradable homolipid from Caprah-ireus[J].IntJPharm,2005,304(1/2):4-10.
