热熔挤出法制备布渣叶提取物固体分散体
2014-04-01涂瑶生孙冬梅徐文杰
涂瑶生, 朱 颖,2, 孙冬梅*, 徐文杰
(1. 广东省中医研究所,广东 广州 510095;2.广州中医药大学,广东 广州 510405)
布渣叶,又名破布叶,为椴树科破布叶属植物破布叶Microcospaniculata. L的叶。课题组前期研究发现布渣叶提取物能显著降低高脂血症小鼠模型血清中总胆固醇(TC)和甘油三酯(TG)的含有量[1]。但是布渣叶提取物在0.1 mol/L盐酸、水和磷酸盐缓冲液(pH 6.8)中的表观溶解度分别为1.78 g/100 mL,1.73 g/100 mL和1.80 g/100 mL,根据《中国药典》2010版凡例“项目与要求”项下溶解度的规定属于略溶。布渣叶提取物溶解性差,导致其口服生物利用度低。
固体分散体(solid dispersion, SD)作为一种新型的载药系统,主要用于改善难溶性药物的溶出与吸收,提高生物利用度[2-3]。固体分散技术在改善药物溶出方面有突出的效果,但由于制备方法存在工艺复杂、重现性低、有机溶剂残留等问题,工业化推广难度较大[4]。热熔挤出技术(hot-melt extrusion technique, HME)又称熔融挤出技术(melt extrusion technique),它本身是一种工业化大生产技术,工艺简单,自动化程度高,不使用有机溶剂,恰好弥补了以上不足,又因为它具有独特的混合机理,使药物和载体达到了分子水平的混合。通过优选载体,可以使药物以无定形状态分散在载体中或者以分子状态溶解在载体中。因此 HME技术用于制备速释制剂有着明显的优势[5-8]。HME技术作为一种新的制剂方法,已成为国外制备固体分散体的主导技术。
本研究利用热熔挤出技术将布渣叶提取物制备成固体分散体,提高其体外溶出度,以达到促进其体内释放和吸收,提高其生物利用度的目的,为中药有效部位新剂型的开发提供一定的参考。
1 材料
HaakeMini CTW微量混合挤出机(美国赛默飞世尔公司);Nicolet 6700型傅立叶变换红外光谱仪(美国赛默飞世尔公司);TG 209型热重分析仪(德国NETZSCH公司);锐影(Empyrean)X-射线衍射仪(荷兰帕纳科公司);UV 2550紫外分光光度计(日本岛津公司);Agilent1200高效液相色谱仪(美国Agilent公司),Waters Xbridge C18(4.6 mm×250 mm,5 μm)色谱柱(美国Waters公司)。
芦丁对照品(批号080-9303,纯度≥99.99%)、牡荆苷对照品(批号111687-200602,纯度≥99.99%)均购于中国食品药品检定研究院;异牡荆苷对照品(批号Y-127-110705,HPLC分析纯度≥98%)、水仙苷对照品(批号S-127-110705,HPLC分析纯度≥98%)均购于成都瑞芬思生物科技有限公司;布渣叶药材为广东市售,经广东省中医研究所刘法锦研究员鉴定为椴树科植物破布叶MicrocospaniculataL.的干燥叶,其提取物为自制(总黄酮含有量≥50%);泊洛沙姆407、PEG6000均购于ISP公司。
2 方法和结果
2.1 HME技术制备布渣叶提取物固体分散体
2.1.1 药物与载体热稳定性的考察 采用热重分析(thermal gravitational analysis, TGA)法,分别取药物和载体适量,置于铝盘中,以氧化铝为参比物,在空气流中,从室温到700 ℃,以10 ℃/min的速率升温。
药物和载体的失重曲线见图1。结果显示,药物和载体在150 ℃以下稳定,提示热熔挤出操作温度低于150 ℃为宜。
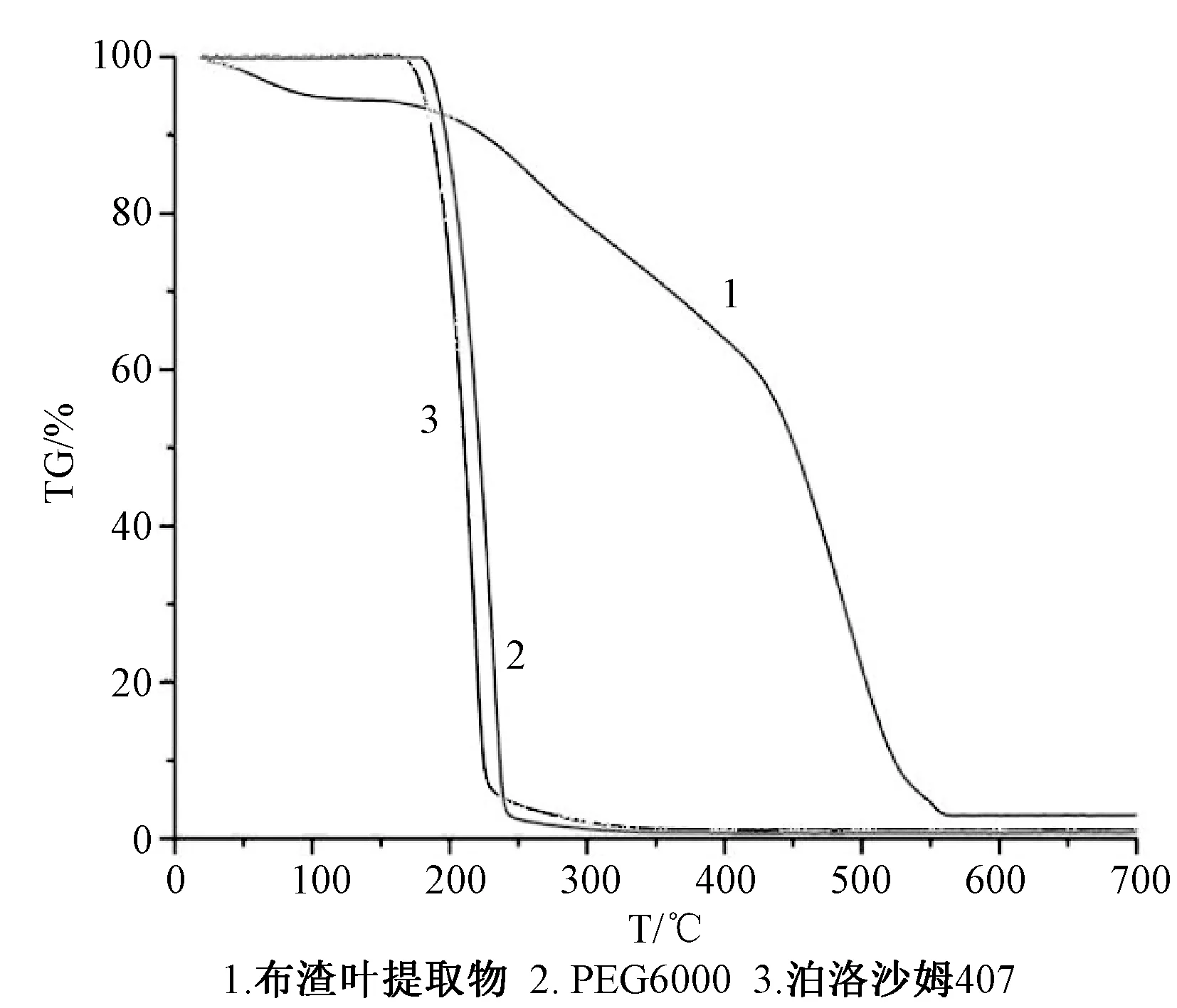
图1 药物和载体的热重分析图
2.1.2 热熔挤出操作 设定温度均为110 ℃;设定螺杆转速为100 r/min。将药物与各载体按试验设计的比例混合均匀,得物理混合物,称取10 g物理混合物投入加料斗中,待物料由模孔挤出后,盛接于不锈钢盘中,-20 ℃条件下放置24 h后,置干燥器中干燥,粉碎,过60目筛,备用。
2.1.3 单一载体固体分散体的制备 按药物与载体质量比为1∶1,1∶2,1∶4,1∶6,1∶8,分别准确称取布渣叶提取物、PEG6000和泊洛沙姆407,按“2.1.2”项下所述方法分别制备布渣叶提取物与PEG6000、泊洛沙姆407固体分散体。
2.1.4 二元载体固体分散体的制备 固定药物与载体的质量比为1∶2,PEG6000与泊洛沙姆407质量比为4∶1,2∶1,1∶1,1∶2,1∶4称取,按“2.1.2”项下所述方法制备布渣叶提取物与PEG6000、泊洛沙姆407二元载体的固体分散体。
2.1.5 物理混合物的制备 按药物与载体的质量比为1∶2准确称取布渣叶提取物与二元载体(PEG6000与泊洛沙姆 407质量比1∶4)置于乳钵中研细,混匀,过60目筛,置干燥器内保存备用。
2.2 体外溶出度测定
2.2.1 UV法测定总黄酮的量
2.2.1.1 标准曲线的绘制 取芦丁对照品适量,精密称定,加70%乙醇制成每1 mL含0.306 mg的对照品溶液。精密量取芦丁对照品溶液1.0、2.0、3.0、4.0、5.0、6.0 mL,分别置25 mL量瓶中,按照参考文献方法[9-10]测定,绘制标准曲线,得回归方程:A=13.27×10-3C-30.46×10-3,r=0.999 7,在14.188~85.128 μg/mL呈良好线性关系。
2.2.1.2 专属性试验 取芦丁对照品溶液、PEG6000/泊洛沙姆407(1∶4)-布渣叶提取物溶液、PEG6000/泊洛沙姆407(1∶4)溶液测定。结果见图2,对照品溶液和布渣叶提取物的最大吸收波长一致,两者在(500±2) nm处有最大吸收,载体材料对总黄酮的含量测定没有干扰,故选择500 nm为测定波长。
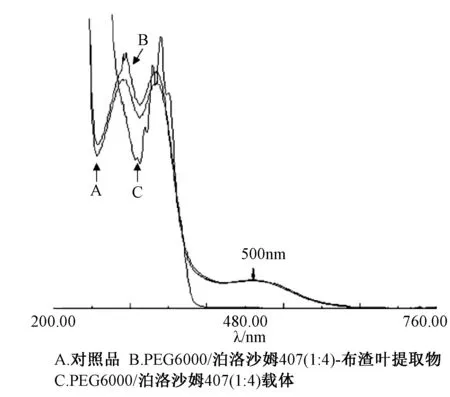
图2 对照品、样品及载体UV扫描图
2.2.2 HPLC法测定牡荆苷、异牡荆苷、水仙苷的量
2.2.2.1 标准曲线的绘制 色谱条件参照参考文献[11],取牡荆苷对照品、异牡荆苷对照品、水仙苷对照品适量,精密称定,加甲醇制成每1 mL含牡荆苷192.6 μg、异牡荆苷 210.4 μg、水仙苷229.1 μg的混合对照品贮备液。精密量取贮备液1.0、2.0、4.0、6.0、8.0、10.0 mL置于10 mL量瓶中,用甲醇稀释至刻度,摇匀,滤过,分别取10 μL注入液相色谱仪,进行线性回归,得回归方程分别为:
牡荆苷Y=3.202×103X+3.707(r=0.999 5);
异牡荆苷Y=3.605×103X+4.933 (r=0.999 5);
水仙苷Y=10.088×103X+5.610 (r=0.999 5)。
结果表明牡荆苷、异牡荆苷和水仙苷分别在7.704~77.040 ng、8.416~84.160 ng和9.165~91.650 ng范围呈良好的线性关系。
2.2.2.2 专属性试验 精密吸取混合对照品溶液、PEG6000/泊洛沙姆407(1∶4)-布渣叶提取物溶液、PEG6000/泊洛沙姆407(1∶4)溶液各10 μL,HPLC测定。结果表明各辅料对牡荆苷、异牡荆苷和水仙苷含量测定没有干扰,见图3。
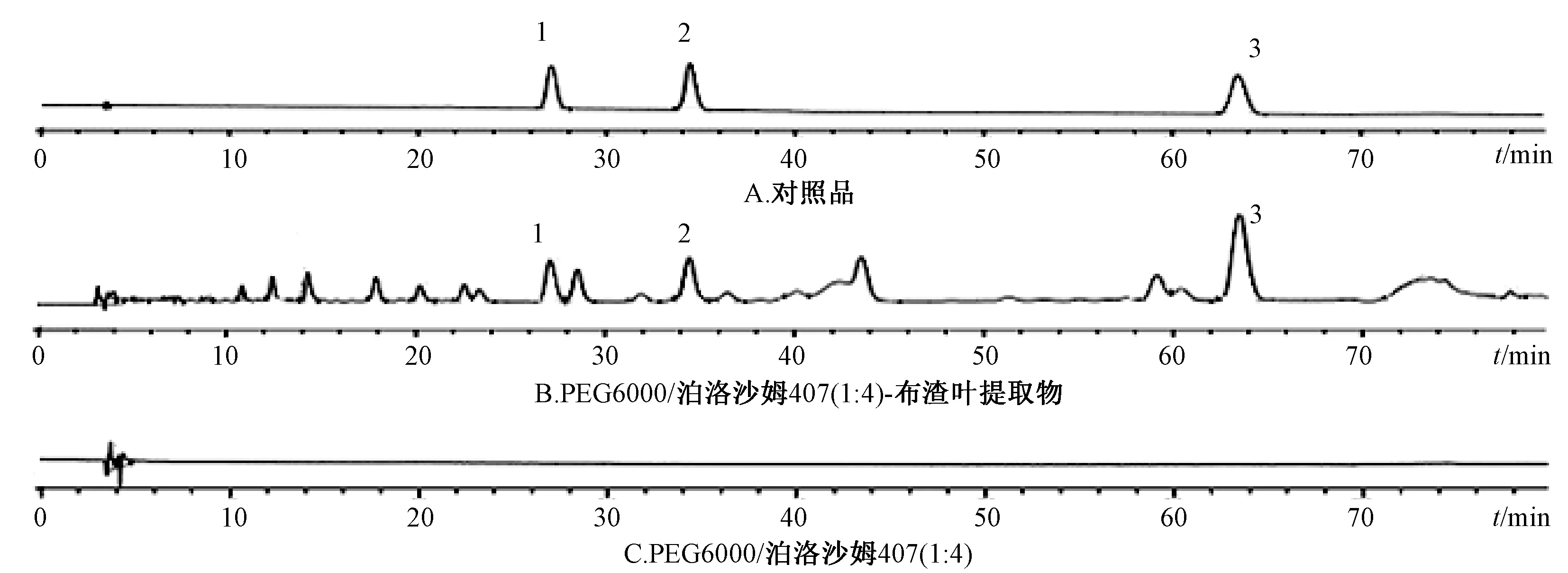
1.牡荆苷 2.异牡荆苷 3.水仙苷 1.vitexin 2.isovitexin 3.narcissi
2.2.3 药物的溶出度测定 精密称取布渣叶提取物和各种固体分散体(相当于含布渣叶提取物0.8 g),按溶出度测定方法(《中国药典》2010 年版二部附录 XC 桨法),以水(900 mL)为溶出介质,转速100 r/min,温度(37±0.5)℃,分别于5、10、15、30、45、60 min 取样 5 mL(同时补加同温度等量溶出介质),以0.45 μm滤膜过滤,进行 HPLC 和UV测定,计算累积溶出率,结果见表1~表3和图4。
由表1可知,PEG6000作为布渣叶提取物(Bzy)的载体材料,可以显著提高牡荆苷、异牡荆苷、水仙苷的溶出度和溶出速率,且随着PEG6000用量的增加溶出度增大。但是,对总黄酮的溶出度影响不大,当药辅比为1∶6时,总黄酮溶出度为63%,较原料药溶出度增加12%,随着PEG6000用量再增加时,总黄酮溶出度并未增加。
由表2可知,泊洛沙姆407作为布渣叶提取物的载体材料,可以显著增加总黄酮的溶出度,且随着泊洛沙姆407用量的增加,总黄酮的溶出度也随之增大。泊洛沙姆407也可增加牡荆苷、异牡荆苷、水仙苷的溶出度,但均低于PEG6000为载体制备的固体分散体;牡荆苷、异牡荆苷的溶出度随着泊洛沙姆407用量的增加而增加;45 min内,水仙苷的溶出速率随着泊洛沙姆407用量的增加而降低。
为了同时增加总黄酮、牡荆苷、异牡荆苷、水仙苷的溶出度,以及尽量减少辅料用量,拟将PEG6000和泊洛沙姆407作为联合载体应用。在固定药物和辅料质量比为1∶2的情况下,又对PEG6000和泊洛沙姆407之间的质量比例进行了考察,结果表3。由表3和图4可知,随着泊洛沙姆407的用量增加,总黄酮的溶出度明显增加,当PEG6000与泊洛沙姆407质量比为1∶4时,总黄酮的溶出度最好,达到了80%;较相同药辅比情况下单一载体(PEG6000、泊洛沙姆407)制备的固体分散体中总黄酮溶出度分别增加20%和30%。PEG6000和泊洛沙姆407各质量比均可显著提高牡荆苷、异牡荆苷、水仙苷的溶出度,且不受PEG6000和泊洛沙姆407比例的影响;当PEG6000与泊洛沙姆407质量比为1∶4时,牡荆苷、异牡荆苷、水仙苷的溶出度分别为100%、100%、90%。所以,确定采用PEG6000与泊洛沙姆407质量比为1∶4作为二元载体,药物与辅料的质量比为1∶2制备固体分散体。

表1 PEG6000不同比例对总黄酮、牡荆苷、异牡荆苷、水仙苷溶出的影响(n=6)
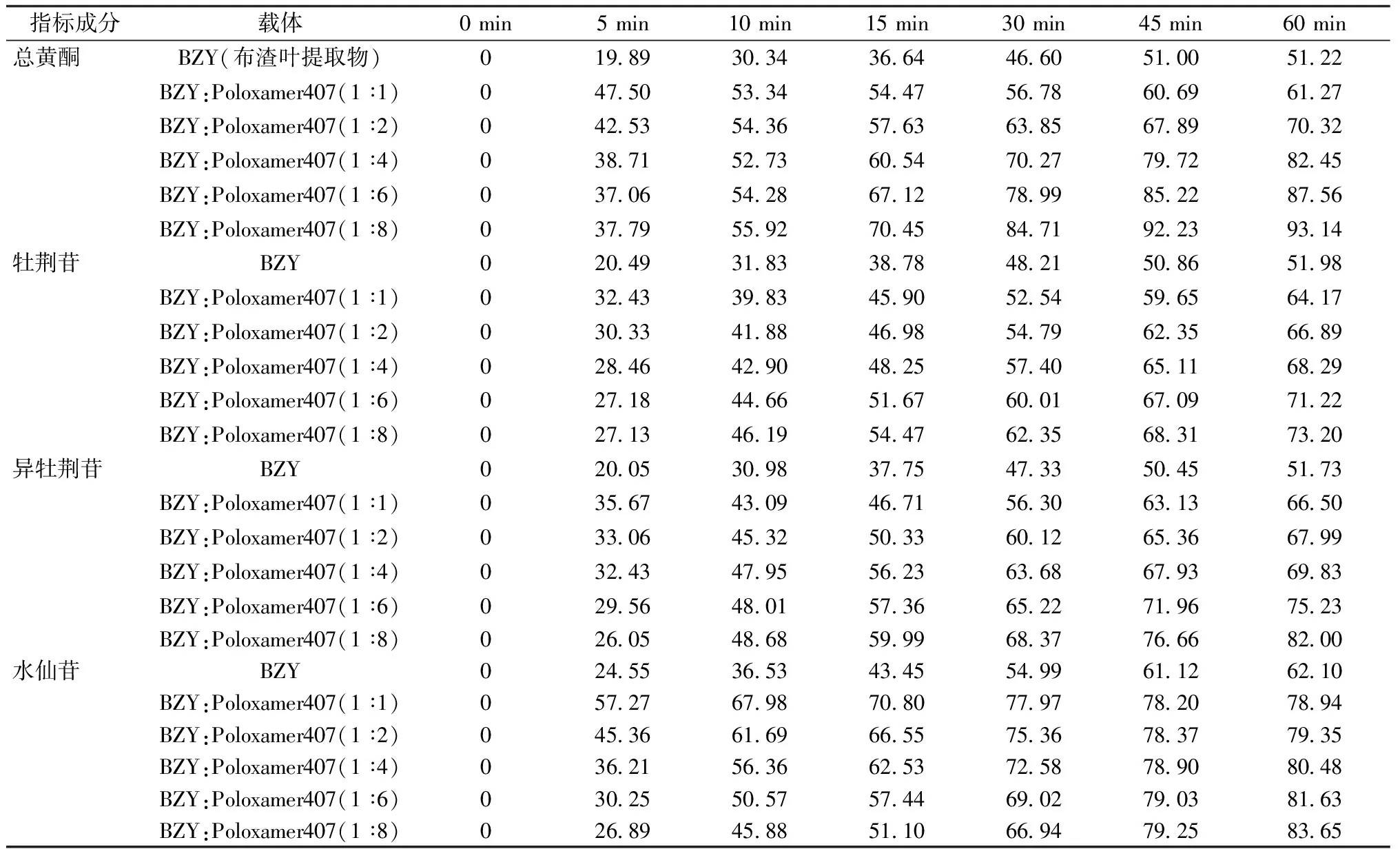
表2 泊洛沙姆407不同比例对总黄酮、牡荆苷、异牡荆苷、水仙苷溶出的影响(n=6)
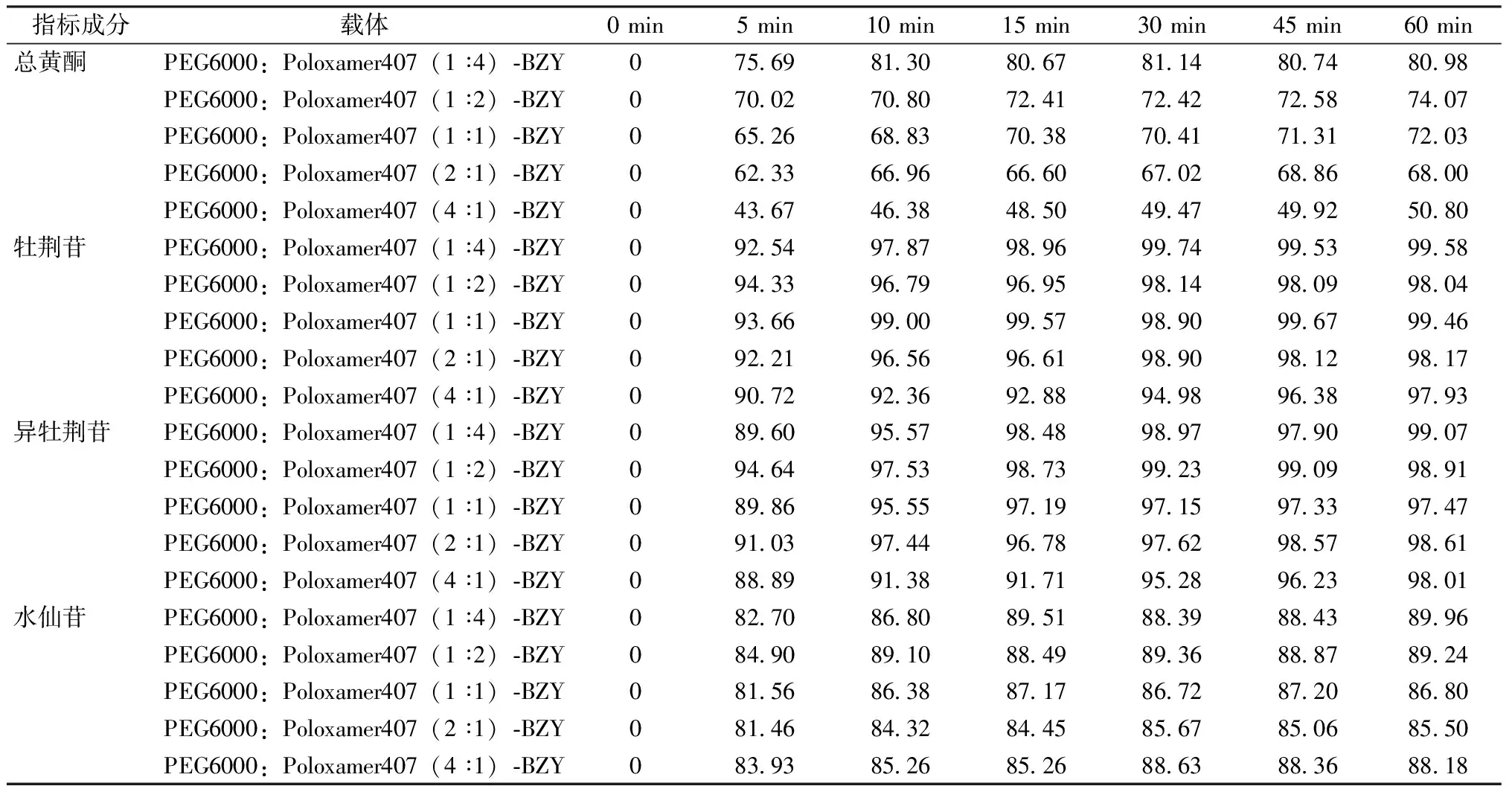
表3 二元载体PEG6000与泊洛沙姆407不同比例对总黄酮、牡荆苷、异牡荆苷、水仙苷溶出的影响(n=6)
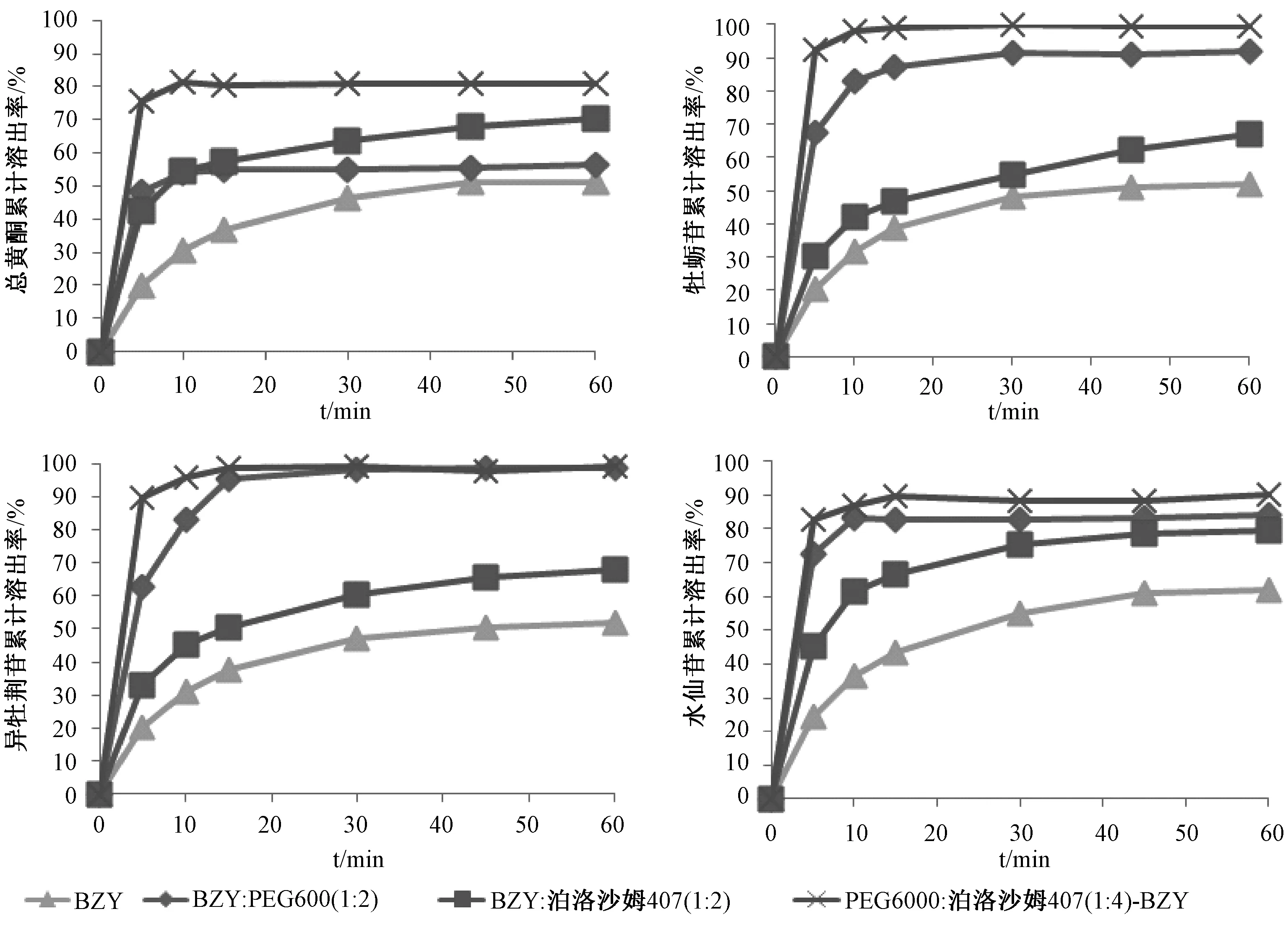
图4 单一载体和二元载体对总黄酮、牡荆苷、异牡荆苷、水仙苷溶出的影响(n=6)
2.4 固体分散体的鉴别
2.4.1 红外光谱分析 采用Nicolet 6700傅立叶红外光谱仪,采用KBr压片法制备样品,扫描范围为 400~4 000 cm-1,分别对布渣叶提取物、PEG6000、泊洛沙姆407、PEG6000/泊洛沙姆407(1∶4)-布渣叶提取物物理混合物及其固体分散体进行红外光谱分析。
由图5可知,物理混合物在3 405.75 cm-1波数有-OH的吸收峰,而固体分散体中的吸收峰向高波数发生位移(3 420.27 cm-1),强度也大幅降低,认为可能由于布渣叶提取物与载体以氢键的形式结合。
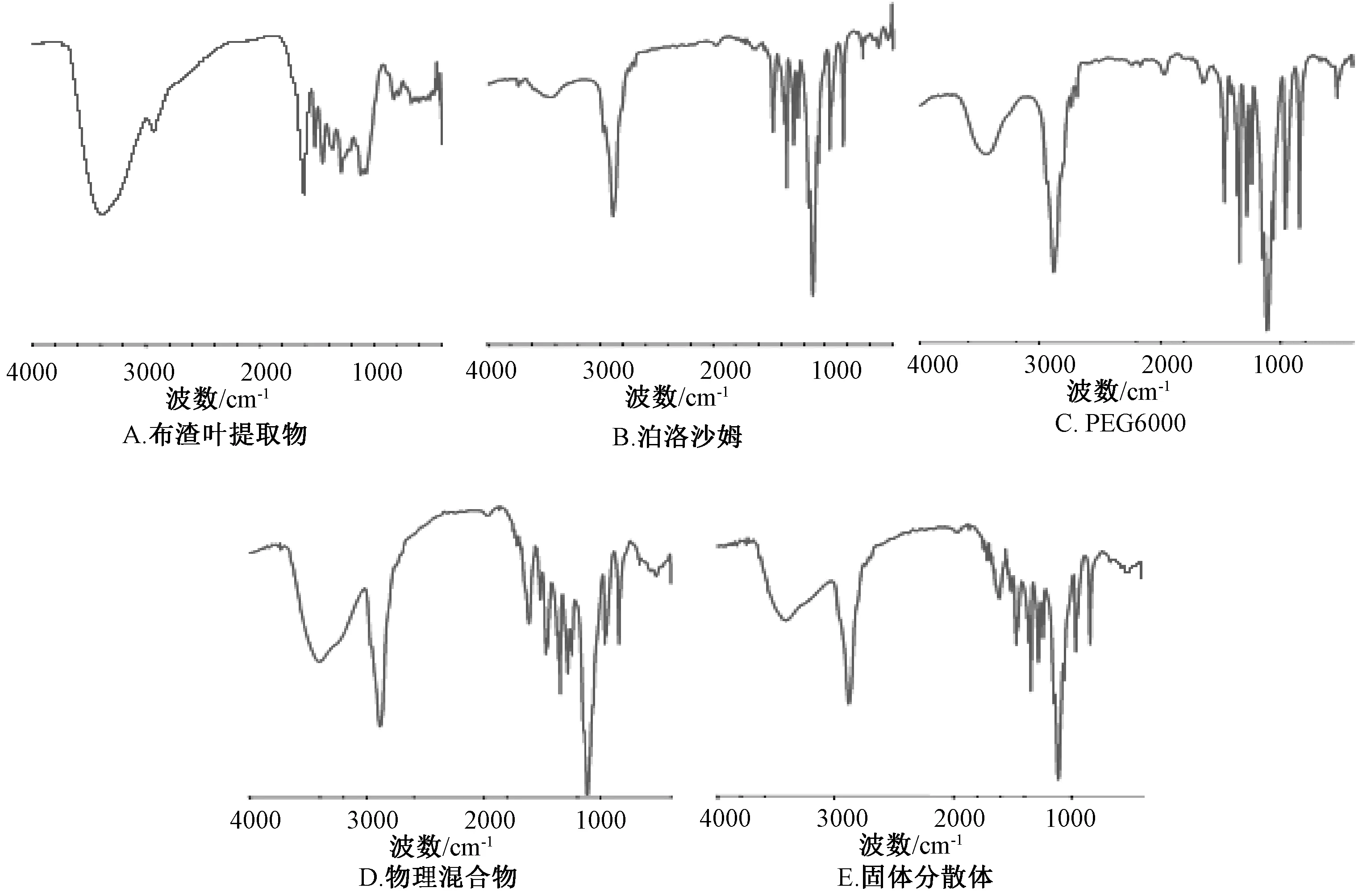
图5 药物、载体、固体分散体和物理混合物IR图
2.4.2 X-射线粉末衍射分析 Cu 靶 Kα1射线,电压 40 kV,电流 40 mA,发射狭缝1/32°,防散射狭缝1/16°,防散射狭缝7.5 mm,2θ范围:3°~50°,步长0.02°,每分钟停留40 s。分别对布渣叶提取物、PEG-6000、泊洛沙姆407、物理混合物和固体分散体进行 X-射线粉末衍射分析。
由结果可知,泊洛沙姆407在19.14°,23.41°出现强衍射峰,PEG-6000在19.19°,23.08°,23.44°出现强衍射峰,而布渣叶提取物没有明显的晶体衍射峰,三者的固体分散体中仍有晶体衍射峰出现,但峰强度明显减弱,与物理混合物的X-射线衍射曲线类似,提示固体分散体没有形成新的物相。
3 讨论
布渣叶是广东道地药材,具有消食化滞,清热利湿之功效,临床常用于治疗饮食积滞,感冒发热,湿热黄疸等。其保健作用虽得到广泛认可,但作为药用的历史不长,对其研究报道也不多,多数集中于化学成分研究[12-13]以及粗提物药理作用研究[14],对其有效部位的开发尚未见报道,本实验对布渣叶有效部位进行制剂研究,利用热熔挤出技术制备得到固体分散体,提高其体外溶出速率。中药有效部位成分复杂,单一指标考察很难体现药物作用的整体效果。所以,本实验采用多个指标同时评价体外溶出度的方法,进行载体的筛选。结果表明,采用不同的单一指标进行体外溶出度评价就会得出不同的结果,最后所选用的辅料及辅料用量亦不同;采用多个指标同时评价,结合各辅料优势,以PEG6000和泊洛沙姆407联合应用为载体,既提高了溶出度,又减少了辅料的用量。
差示扫描量热法(DSC)、红外光谱法(IR)、X-射线衍射为固体分散体常用物相鉴别的方法,通过观察药物的DSC、IR、X-射线衍射这几个谱图的变化,可以观察到药物存在状态的改变。但目前固体分散技术和物相鉴别技术主要用于药物单体的制备和鉴别。由于本研究的药物是从布渣叶中提取的混合物,并非单体药物,DSC方法并不适用,所以仅采用IR和X-射线衍射对制备的固体分散体进行物相鉴别。本实验为中药提取物或中药有效部位固体分散体的研究提供参考。
参考文献:
[1] 谭志灿.广东道地药材布渣叶质量评价及调血脂物质基础研究[D].广州:广州中医药大学,2012:66-69.
[2] 戴春兰,王光发,廖正根,等.柚皮素-PVPK30固体分散体的制备及体外特性研究[J].中成药,2011,33(1):45-49.
[3] 李维峰,翟永松,杜守颖.芦丁固体分散体的制备及其溶出性能研究[J].中成药,2010,32(12):2071-2075.
[4] 杨 睿,唐 星,黄惠锋.热熔挤出技术及其在药物传递系统中的应用[J].中国新药杂志,2007,16(4):279-284.
[5] He H B, Yang R,Tang X.Invitroandinvivoevaluation of fenofibrate solid dispersion prepared by hot-melt extrusion[J].DrugDevIndPharm,2010,36(6):681-687.
[6] Gryczkeb A, Schminkeb S, Maniruzzamana M,etal. Development and evaluation of orally disintegrating tablets (ODTs) containing Ibuprofen granules prepared by hot melt extrusion[J].ColloidsSurfBBiointerfaces,2011,86(2):275-284.
[7] Fu J J, Xu L S, Wang X L,etal. Nimodipine (NM) tablets with high dissolution containing NM solid dispersions prepared by hot-melt extrusion[J].DrugDevIndPharm, 2011,37(8): 934-944.
[8] 林 瑶,顾 宜,严筱楠,等.热熔挤出技术提高安宫牛黄固体分散体中黄芩苷溶出速率的研究[J].中成药,2012,34(1):38-41.
[9] 马婉婉,骆开荣,班 颖,等.十二烷基硫酸钠协同微波-酶法提取布渣叶总黄酮[J].生物加工过程,2011,9(6):35-39.
[10] 韩 伟,马婉婉,骆开荣,等.表面活性剂协同微波提取布渣叶总黄酮[J].南京工业大学学报,2012,34(2):91-94.
[11] 孙冬梅,陈雪婷,谭志灿.HPLC同时测定布渣叶提取物中3种黄酮苷的含量[J].中国实验方剂学杂志,2013,19(11):102-104.
[12] 曾聪彦,戴卫波.布渣叶化学成分研究新进展[J].海峡药学,2010,(22)7:12-14.
[13] Fan H, Yang G Z,Zheng T,etal. Chemical constituents with free-radical-scavenging activities from the stem of Microcos paniculata[J].Molecules, 2010, 15, 5547-5560.
[14] 曾聪彦,梅全喜,戴卫波.布渣叶药理作用研究的新进展[J].中华中医药学,2010,28(9):1927-1929.
