响应面法优化克氏原螯虾虾壳中钙提取工艺的研究
2014-03-27陈丽丽袁美兰胡火根
魏 颖,刘 华,陈丽丽,赵 利*,袁美兰,苏 伟,胡火根
(1.江西科技师范大学 生命科学学院,国家淡水鱼加工技术研发分中心(南昌),江西 南昌 330013;2.江西省水产技术推广站,江西 南昌 330046)
0 引言
目前我国的克氏原螯虾以出口为主,而出口产品主要以虾仁的形式,因此在对虾的加工过程中会产生大量的虾头、虾壳等下脚料 (占整虾的30%~40%)[1].这些副产物含有丰富的蛋白质、虾红素、不饱和脂肪酸等营养物质[2-3],同时含有各种氨基酸以及人体必需的微量元素[4].虾头、虾壳是一种优质的可再利用的资源,但长期以来,我国对这部分资源没有进行有效的利用,除少量被用于生产肥料、饲料和制备几丁质之外,大部分被作为垃圾丢掉,这样不仅使资源严重浪费,而且也会造成环境污染.
钙是人体内必需的元素之一,它是组成人体骨骼、牙齿、脏器和肌肉组织的重要成分[5].当人体中钙缺乏时,会发生各种生理功能障碍,如失眠、疲劳、抽筋、骨痛等.虾壳中的钙是一种天然绿色的钙源.张祥刚等[6]对南美白对虾虾壳(干重)进行矿物元素含量的测定,发现其中钙元素含量约占总金属元素含量的92.06%.但虾壳中的钙主要以不易被人体吸收利用的碳酸钙形式存在.本研究目的就是寻求一种能直接提取的方法替代以往的高温锻烧法,将虾壳中的无机碳酸钙转化成易于被人体吸收利用的具有含钙量高、易溶解、吸收快、安全性好、价格合理等优点[7]的乳酸钙,使其作为一种安全的添加剂、稳定剂、营养增补剂和组织凝固剂等[8],广泛应用于食品和医药行业中[9],为科学地开发虾壳资源提供一条有效的技术途径.
1 材料与方法
1.1 材料与试剂
虾壳:江西海浩鄱阳湖水产有限公司.
乳酸、氨水、氯化铵、三乙醇胺、乙二胺基四乙酸二钠(EDTA)、铬黑T、氯化钙、盐酸、氯化铵、氨水、氢氧化钠等均为分析纯.
1.2 仪器与设备
数显智能控温磁力搅拌器:巩义市予华仪器有限责任公司;电子分析天平:赛多利斯科学仪器(北京)有限公司;粉碎机:上海比朗仪器有限公司;电热恒温鼓风干燥箱:上海一恒科学仪器有限公司.
1.3 虾壳预处理
虾壳预处理:用4%的氢氧化钠溶液浸泡虾壳4 h,用水洗至中性,重复1 次.将经过初分的虾壳置于100 ℃的鼓风干燥机中干燥12 h.再将干燥好的虾壳粉碎,过40 目筛,贮存备用.
1.4 钙含量的分析[10]
钙标准溶液的配制:准确称取已恒质量的无水氯化钙2.774 6 g,用蒸馏水定容至250 mL 配成0.1 mol/L 的氯化钙溶液,此时钙离子的浓度为4 mg/mL.
钙标准曲线的测定:分别取1.0、2.0、3.0、4.0、6.0、8.0、10.0 mL 的氯化钙溶液于50 mL 的三角瓶中,均用蒸馏水定容至总体积为10 mL.分别在待测溶液中加入3 mL 的三乙醇胺溶液,5 mL pH 10的氨性溶液和两滴铬黑T 指示剂,然后以0.021 5 mol/L 的EDTA 标准溶液滴定到溶液由紫蓝色变成蓝色.以EDTA 滴定体积和钙浓度作图,得到钙标准曲线.通过实验计算钙的标准曲线为y=2.978 6x+0.590 5(y 代表EDTA 的滴定体积,x 代表钙离子浓度,R2=0.998).
虾壳浸酸溶液中钙含量的测定:取1 mL 浸酸溶液加9 mL 蒸馏水,分别加入3 mL 三乙醇胺和5 mL 氨性溶液,两滴铬黑T 指示剂,以标准EDTA溶液滴定到溶液由紫蓝色转为蓝色.根据标准回归方程计算浸酸溶液中钙含量.
1.5 单因素试验
根据参考文献[11]中的测定方法略作修改.
(1)乳酸添加量的确定:虾壳粉用量为10 g,加水量为100 mL,提取时间为2 h,提取温度为35℃,乳酸添加量分别为13.5 mL、16.0 mL、18.5 mL、21.0 mL、23.5 mL.待反应结束后,分别测定浸提液中钙的含量.
负面清单模式能够极大地赋予市场主体从事经济活动的自由,这可能会造成社会资本流向热点行业、热点地区,导致行业发展不平衡,地区发展不均衡。适当的管制可以引导市场主体的行为,避免市场主体之间的恶性竞争,更合理、有效地配置社会资源,促进行业和地区经济的均衡发展,防止垄断的发生。
(2)提取温度的确定:虾壳粉用量为10 g,加水量为100 mL,提取时间为2 h,乳酸添加量为(1)试验中较适宜的结果,提取温度分别为25 ℃、35 ℃、45 ℃、55 ℃、65 ℃.待反应结束后,分别测定浸提液中钙的含量.
(3)提取时间的确定:虾壳粉用量为10 g,加水量为l00 mL,乳酸添加量和提取温度分别采用(1)和(2)试验中较适宜的结果,提取时间分别为10 min、20 min、30 min、40 min、50 min.待反应结束后,分别测定浸提液中钙的含量.
1.6 响应面法优化提取工艺试验[12-15]
根据单因素试验的结果,采用乳酸添加量、提取时间、提取温度3 个因素与钙提取量进行响应面试验设计优化虾壳钙提取工艺.通过Design-Expert 8.0.6 软件对试验结果数据进行回归分析,预测最优的工艺参数.在分析得到的最佳工艺提取条件下,做3 组平行试验验证响应面分析法的可靠性.
2 结果与分析
2.1 单因素试验
2.1.1 乳酸添加量对虾壳钙提取量的影响(图1)
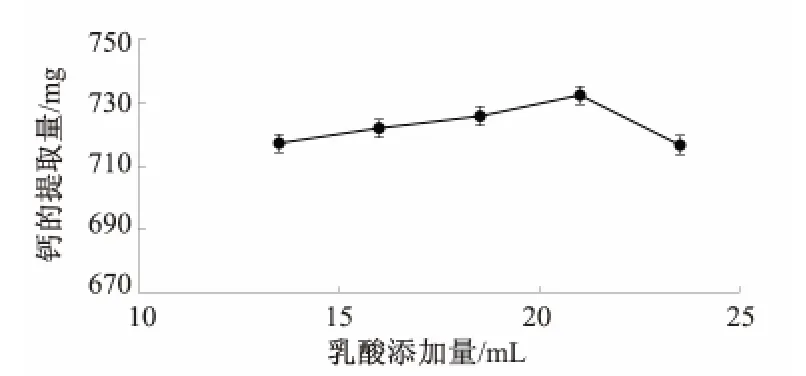
图1 乳酸添加量对虾壳钙提取量的影响
由图1 可以看出,在乳酸添加量达到21 mL之前,钙的提取量随着乳酸的体积增加而增加并达到最大值,之后又随着乳酸添加量的增加而减少.产生这种现象的原因可能是乳酸添加量为21 mL 时,转化制取的乳酸钙的产率和含量已经达到了一种平衡的饱和状态,处在具有较好产率的范围内.但是当乳酸添加量继续增加时,乳酸钙的产率减少,主要是因为当乳酸过量时会在反应时形成乳酸酐,并吸附在乳酸钙表面上,使其钙的含量降低.因此,21 mL 乳酸添加量最佳.
2.1.2 反应温度对虾壳钙提取量的影响(图2)
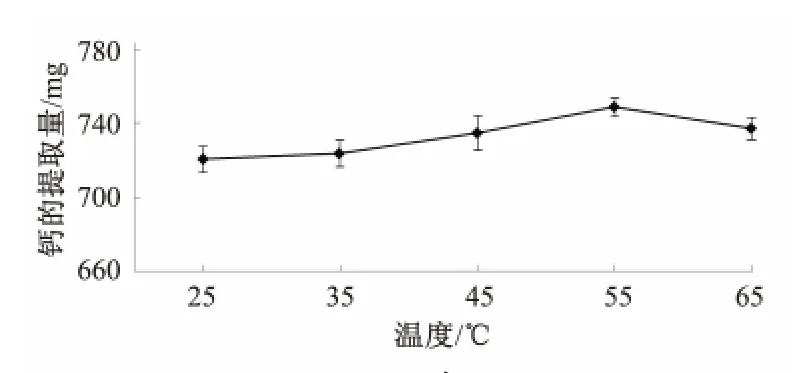
图2 提取温度对虾壳钙提取量的影响
由图2 可知,在25~55 ℃范围内,虾壳钙提取量随着温度的升高而增加,继续升高温度钙提取量下降.这主要是由于温度的升高可以增加大分子间的碰撞几率,使得反应向乳酸钙生成的方向进行,但是随着温度的不断升高,乳酸发生酯化反应生成乳醛乳酸,并与钙离子结合生成对应的钙盐,导致生成的乳酸钙含量逐渐下降[16].由此可知,最佳提取温度是55 ℃.

图3 反应时间对虾壳钙提取量的影响
由图3 可以看出,在提取30 min 之内,钙提取量随着反应时间的延长而增加,主要是由于在反应刚开始时,系统中存在较多的乳酸和虾壳,在这时系统中生成乳酸钙的浓度比较小,其正反应速率大于逆反应速率,促使反应向正反应方向进行,即生成乳酸钙的方向.在20~30 min 时间内,由于正反应速率在逐渐减小,使得乳酸钙的增长速率缓慢.当反应时间达到30 min 后曲线逐渐趋于平缓,表明系统中的反应已经趋于平衡,随着反应时间的继续增加,反应体系中逆反应的发生几率增加,曲线有下降的趋势.因此,虾壳中钙提取最佳时间为30 min.
2.2 响应面法优化试验
2.2.1 试验设计及结果
在单因素试验的基础上,通过Design-Expert 8.0.6 软件设计3 因素3 水平进行响应面试验,设计方案见表1,试验结果见表2.
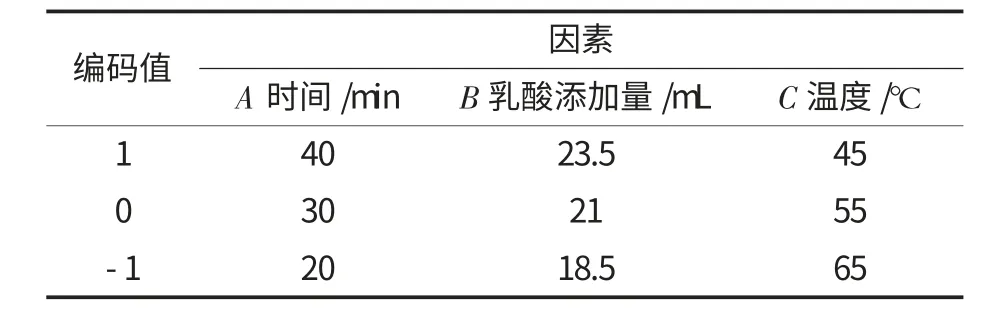
表1 虾壳钙提取工艺Box-Behnken设计试验因素、水平及编码

表2 Box-Behnken 设计方案及钙的提取量的测定结果
2.2.2 模型的建立及显著性检验
利用Design Expert 8.0.6 对表3 中数据进行多元回归拟合得到提取量(Y)对时间(A)、乳酸添加量(B)、温度(C)的二次多项回归方程模型如下:

观察回归方程可以看出虾壳中乳酸钙提取影响因素的大小顺序为:温度>时间>乳酸添加量.由表3 可知,模型的F=8.77,P<0.01,说明本试验所采用的二次模型是显著的.比较表3 中的P 值可知,C 极显著,BC 交互项显著.二次项B2、C2都极显著表明各影响因素对提取量不是简单的线性关系.

表3 钙提取量回归模型的方差分析
2.2.3 响应面分析(图4)


图4 各因素对虾壳钙提取量的响应面图
响应曲面分析法优化图形为响应Y 与对应的因素间构成的三维图及在二维平面上的等高图,综合直观地反映各因素对响应值的影响,每个响应面对其中两个因素进行分析,另外一个因素固定在零水平上.由图4 可知,响应面开口向下,随着每个因素的值的增大,与其对应的响应值增大,然而当响应值增大到极值后,随着因素的增大响应值随之减小.该模型有稳定点,且稳定点是最大值.等高线的形状可反映出交互作用的强弱,椭圆形表示两因素交互作用显著,而圆形则与之相反.从其等高线图可以直观地看出时间和乳酸添加量、时间和温度、温度和乳酸添加量这3 组的两因素交互作用显著.从图4 可以看出,3 因素的交互作用均有最大值,说明响应面优化设计能够较好地反映出试验所设定的3 因素对钙提取量的影响.
2.2.4 最佳工艺条件的验证
由上述软件分析得到最大的响应值为765.12 mg,即每10 g 虾壳中最大的钙提取量为765.12 mg,与之对应的最佳工艺条件为:乳酸添加量21.43 mL、温度61.34 ℃、时间40 min.根据实际操作,对工艺条件进行简化处理,在乳酸添加量21.43 mL、温度61 ℃、时间40 min 条件下进行验证试验,经过3 组平行试验所得到的每10 g 虾壳钙的提取量分别为760.29 mg、765.08 mg 和762.07 mg.平均值为762.48 mg,与模型的预测值765.12 mg基本相符.
3 结论
本试验采用响应面Box-Behnken 试验设计优化了用乳酸提取法从克氏原螯虾虾壳中提取乳酸钙的最佳工艺条件:10 g 虾壳粉,100 mL 水,乳酸添加量为21.43 mL,温度61.34 ℃,时间40 min,此条件下的钙提取量为762.48 mg.
[1]曹文红,章超桦,谌素华,等.中国毛虾营养成分分析与评价[J].福建水产,2001(1):1-5.
[2]罗梦良,钱名.虾仁加工废弃的头[J].淡水渔业,2003,33(6).
[3]高建华,苏应全.虾壳蛋白质营养价值的评价[J].食品与发酵工业,1998,24(3):29-32.
[4]彭燕,曾霞.南美白对虾虾头的营养成分分析及评分[J].茂名学院学报,2007,17(1):25-27.
[5]Cooper C,Melton III L J.Epidemiology of osteoporosis[J].Trends in Endocrinology &Metabolism,1992,3(6):224-229.
[6]张祥刚,周爱梅,林晓霞,等.南美白对虾虾头,虾壳化学成分的对比研究[J].现代食品科技,2009,25(3):224-227.
[7]江敏,李鉴,梁洁玲,等.牡蛎壳合成L-乳酸钙的工艺研究[J].食品科技,2008,33(3):123-125.
[8]Irmaos Hoffmeister,Cia Ltda.Industrial cold meat processing to suit market requirements comprises treatment with e.g.sodium alginate and calcium lactate and controlled storage:America,BR200502988[P].2007.
[9]白海涛.鸡蛋壳制备食品级乳酸钙的新工艺研究[D].西安:西北大学化工学院,2006.
[10]GB 6226—2005,食品添加剂乳酸钙[S].
[11]刘小玲,许时婴,王璋.鸡骨明胶生产中浸酸工艺的控制[J].食品工业与发酵,2004,25(8):109-111.
[12]试验设计与Design-Expert,SPSS 应用[M].北京:科学出版社,2010.
[13]Chin L H,Hameed B H,Ahmad A L.Process optimization for biodiesel production from waste cooking palm oil(Elaeis guineensis)using respo nse surface methodology[J].Energy &Fuels,2009,23(2):1040-1044.
[14]刘晶晶,赵泓筠,韩曜平,等.响应面法优化菊花脑黄酮提取工艺[J].食品科学,2012,33(16):68-71.
[15]Lim J Y,Yoon H S,Kim K Y,et al.Optimum conditions for the enzymatic hydrolysis of citron waste juice using response surface methodology(RSM)[J].Food Science and Biotechnology,2010,19(5):1135-1142.
