物理精炼工艺对亚麻籽油和葡萄籽油品质的影响研究
2014-03-27李桂华王向云康雪梅
祝 品,李桂华*,赵 芳,王向云,康雪梅
(1.河南工业大学 粮油食品学院,河南 郑州 450001;2.河南省产品质量监督检验院,河南 郑州 450008)
0 引言
亚麻籽又称胡麻籽,是亚麻科、亚麻属的一年生或多年生草本植物亚麻的种子,为世界十大油料作物之一,我国亚麻籽年产量已达到50 万t,处于世界第二位[1].亚麻籽油主要是由压榨法提取,成品油呈橙黄色,澄清透明,具有亚麻籽油固有的气味和滋味.亚麻籽油中含有90%的不饱和脂肪酸,而被誉为“植物脑黄金”,具有重要的生理功能和保健功能的α-亚麻酸的含量高达40%~60%[2-3].
葡萄是葡萄科葡萄属植物,葡萄籽的主要来源是葡萄酒厂、果汁饮料厂等葡萄加工企业的下脚料,我国每年可用于开发利用的葡萄籽约4.5 万t[4].葡萄籽含油量14%~17%,葡萄籽油中不饱和脂肪酸含量达90%以上,其中亚油酸含量高达75%,与红花油中亚油酸含量接近[5],属于高亚油酸型油脂.
亚麻籽油和葡萄籽油作为n-3 和n-6 型多不饱和油脂,其营养价值已经得到国内外学者的普遍认可[6-7].但压榨或浸出制取的亚麻籽油和葡萄籽毛油含有非食用的游离脂肪酸等杂质,需精炼加工才能食用.近年来,学者们探讨了不同的精炼方法如化学精炼、物理精炼、酶促酯化脱酸精炼对高级食用保健油品质裂变的影响[8-10].采用常规化学精炼工艺加工时,会存在碱炼脱酸较难控制、精炼损耗高、污染物排放量大、油中营养物质减少等特点;酶促酯化脱酸因分离难,成本高,脱酸技术不成熟尚未推广应用;而物理精炼的特点在于油中游离脂肪酸靠蒸馏法去除,污染物排量少,营养物质损失少,还可降低油脂损耗,备受人们的青睐,但由于物理脱酸温度高、易使含不饱和脂肪酸的油脂产生反式脂肪酸,因此,对富含n-3 和n-6 不同类型不饱和脂肪酸的亚麻籽油和葡萄籽油采用物理精炼脱酸乃是人们研究和关注的热点.
作者以亚麻籽毛油和葡萄籽毛油为原料,采用物理工艺精炼,由于多不饱和脂肪酸含量高,高温下易裂变,选用略低大宗油脂脱酸的温度220℃,研究不同精炼阶段油脂的酸价、过氧化值、p-茴香胺值、反式脂肪酸和生育酚等品质质量的变化,为富含不同类型的多不饱和脂肪酸的油脂采用物理精炼的加工工艺提供参考.
1 材料与方法
1.1 试验材料
压榨葡萄籽油、压榨亚麻籽油:晨光生物科技集团股份有限公司.
正己烷、异辛烷、冰乙酸、甲醇、异丙醚为色谱纯;碘化钾、硫代硫酸钠、淀粉、对甲氧基苯胺、甲醇钠等为分析纯;生育酚和各脂肪酸标准样品:美国Sigma 公司.
1.2 主要仪器设备
GC-2010 型气相色谱仪、10-AT 系列高效液相色谱仪:日本岛津公司;2XZ-1 型旋片式真空泵:浙江黄岩天龙真空泵厂;BS21OS 分析天平(感量0.000 1 g):北京赛多利斯天平有限公司;转动式真空计:中国浙江嘉兴玻璃厂.
1.3 试验方法
1.3.1 脱胶
称取毛油200 g 置于500 mL 的烧杯中,将搅拌器的搅拌翅放进油中(搅拌器浸入油中2/3 处)待油样升温至60~65 ℃,适当调快搅拌速度,用滴管缓慢加入油重0.1%磷酸和3%蒸馏水,搅拌25 min 脱胶,于3 500 r/min 离心20 min 分离出脱胶油.将脱胶油转移到三口烧瓶中,放入磁力转子,在真空度0.09 MPa、105 ℃条件下脱水,直到油面上看不到水汽为止.
1.3.2 脱色
脱水结束后,将油温降至90 ℃,加入油重2.5%脱色剂(酸性白土/活性炭=8/2),使油和活性白土均匀混合,搅拌20 min 脱色,冷却后将混合物真空过滤除去脱色剂.
1.3.3 蒸馏脱酸、脱臭
连接真空脱酸装置,启动真空泵,将油预先预热到100 ℃,开启直接蒸汽导管上的旋塞,通入直接蒸汽,并调节蒸汽量(在不引起油飞溅的情况下,通汽量尽量加大),使油进行汽提(搅拌),使油不断升温到220 ℃,在真空残压≤50 Pa、220 ℃条件下将脱色油脱酸2 h、4 h 和6 h,得脱酸脱臭油.
1.4 分析方法
1.4.1 理化指标的测定
酸价按照GB/T 5530—2005 动植物油脂酸值和酸度测定;过氧化值按照GB/T 5538—2005 动植物油脂过氧化值测定;p-茴香胺值按照GB/T 24304—2009 茴香胺值测定;磷脂含量按照GB/T 5537—2008 磷脂含量测定.
1.4.2 反式脂肪酸测定方法
(1)甲酯化:参照GB/T 17376—2008 动植物油脂脂肪酸甲酯制备.
(2)反式脂肪酸组成分析条件:参照GB/T 17377—2008 动植物油脂脂肪酸甲酯气相色谱分析.
(3)脂肪酸组成成分定性、定量方法:根据各脂肪酸标样的保留时间定性,根据峰面积归一化法定量.
1.4.3 生育酚含量分析
(1)试样前处理及分析条件:参照国标GB/T 26635—2011 动植物油脂生育酚及生育三烯酚含量测定高效液相色谱法.
(2)生育酚的定性和定量方法:用各生育酚标样的保留时间定性,用外标法定量,即根据油样测定的生育酚峰面积在标准曲线上查其含量.
2 结果与讨论
2.1 亚麻籽油和葡萄籽油的理化指标(表1)

表1 亚麻籽毛油和葡萄籽毛油的理化指标
2.2 脱胶脱色工序对亚麻籽油和葡萄籽油的影响
对亚麻籽毛油和葡萄籽毛油采用物理方法精炼,前道仅作脱胶处理,既保证具有生理活性的物质如维生素E 不受损失,又不加入任何化学物质,进入脱色工段后,利用吸附剂的吸附作用可以将油脂中的色素和部分残留胶质一起脱除,经脱胶脱色处理后的亚麻籽油和葡萄籽油理化指标如表2 所示.
脱胶效果的好坏直接影响到物理精炼的效率和产品的质量.对比表2 和表1 可知,经脱胶脱色后的亚麻籽油和葡萄籽油的色泽明显变淡,酸价略有下降,生育酚损失很少,磷脂的含量大大降低.亚麻籽油的磷脂含量由0.166%降低到0.021%,葡萄籽油由0.328%降低到0.027%,亚麻籽油和葡萄籽油的含磷量都达到15 mg/kg 以下,均满足物理精炼的要求.

表2 经脱胶脱色后亚麻籽油和葡萄籽油的理化指标
2.3 物理精炼过程对亚麻籽油和葡萄籽油酸价的影响
采用1.3.3 的工艺方法,对酸价分别为3.80 mg/g 和14.06 mg/g 的亚麻籽油和葡萄籽油进行脱酸,亚麻籽油和葡萄籽油酸价变化如图1 所示.
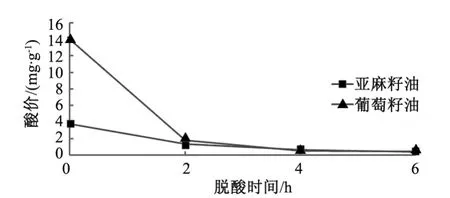
图1 物理精炼过程对亚麻籽油和葡萄籽油酸价的影响
图1 表明,采用物理脱酸法精炼,随着脱酸时间的延长,亚麻籽油和葡萄籽油的酸价均不断降低.前2 h 是物理脱酸的主要阶段,葡萄籽油的酸价下降较亚麻籽油更加明显,脱酸2 h 后亚麻籽油和葡萄籽油的酸价分别为1.37 mg/g 和1.82 mg/g;4 h 后酸价分别为0.67 mg/g 和0.49 mg/g;均达到了一级亚麻籽油(GB/T 8235—2008)和一级葡萄籽油(GB/T 22478—2008)对酸价的要求,脱酸6 h 后酸价分别降为0.41 mg/g 和0.44 mg/g.
2.4 物理精炼过程对亚麻籽油和葡萄籽油过氧化值的影响
亚麻籽油含有大量亚麻酸和亚油酸,葡萄籽油富含亚油酸,在物理精炼过程中易氧化生成氢过氧化物,其中过氧化值是衡量亚麻籽油和葡萄籽油氧化裂变的重要品质指标.采用1.3.3 所述工艺方法分别对亚麻籽油和葡萄籽油进行真空残压≤50 Pa、220 ℃的条件下脱酸2 h、4 h、6 h.不同阶段油样的过氧化值,其变化趋势见图2.
由图2 可以看出,经脱胶脱色后的亚麻籽油和葡萄籽油过氧化值分别为5.20 mmol/kg 和6.16 mmol/kg.随着脱酸时间的延长,葡萄籽油的过氧化值不断降低,精炼4 h 后,过氧化值降低到2.27 mmol/kg,6 h 后持续下降;亚麻籽油的过氧化值前2 h 降低到3.43 mmol/kg,4 h 时又略有升高,6 h时过氧化值为3.76 mmol/kg,整个脱酸过程中过氧化值变化不大.由此可看出:在高温220 ℃精炼时,葡萄籽油中氢过氧化物分解速率大于其生成速率;而亚麻籽油氢过氧化物分解速率与其生成速率基本相等.

图2 物理精炼过程对亚麻籽油和葡萄籽油过氧化值的影响
2.5 物理精炼过程对亚麻籽油和葡萄籽油p-茴香胺值的影响
油脂氧化生成的氢过氧化物不稳定易分解产生醛、酮、酸等小分子二次生成物,测定物理精炼过程中亚麻籽油和葡萄籽油茴香胺值的变化,可评价这两种油氧化裂变的程度.相同脱酸条件下亚麻籽油和葡萄籽油p-茴香胺值变化情况如图3所示.
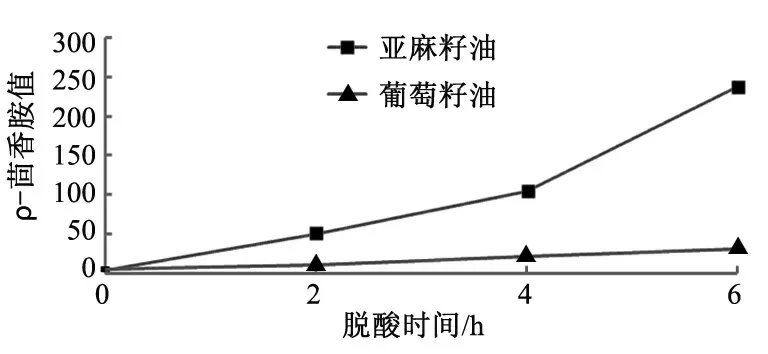
图3 物理精炼过程对亚麻籽油和葡萄籽油p-茴香胺值含量的影响
由图3 可看出,随着时间的延长,亚麻籽油和葡萄籽油的p-茴香胺值均呈升高趋势.亚麻籽油的p-茴香胺值升高很快,脱酸4 h,p-茴香胺值达到105.32,6 h 后,升到238.45;而葡萄籽油的p-茴香胺值升高较慢,脱酸前2 h 茴香胺值变化不大,脱酸4~6 h 茴香胺值从21.66 升高到31.25.相同脱酸时间下,亚麻籽油的p-茴香胺值均高于葡萄籽油的p-茴香胺值,这说明在此脱酸条件下亚麻籽油样的醛类生成速率远大于葡萄籽油样的醛类生成速率.
2.6 物理精炼过程对亚麻籽油和葡萄籽油反式脂肪酸的影响
富含亚麻酸和亚油酸的油脂采用高温物理脱酸工艺,可能使其中不饱和脂肪酸发生异构化和双键重排,反式酸产生几率增加.在真空残压≤50 Pa、220 ℃条件下分别对亚麻籽油和葡萄籽油脱酸2~6 h,不同脱酸时间的亚麻籽油和葡萄籽油脂肪酸组成分别见表3、表4,总反式酸含量随时间变化见图4.

表3 亚麻籽油物理脱酸后脂肪酸组成和反式脂肪酸的含量 %

表4 葡萄籽油物理脱酸后脂肪酸组成和反式脂肪酸的含量 %

图4 物理精炼过程对亚麻籽油和葡萄籽油总反式酸含量的影响
图4 表明,随脱酸时间的延长,亚麻籽油和葡萄籽油反式脂肪酸含量呈现不同的增加趋势.亚麻籽油脱酸时间由2 h 延长到4 h,反式脂肪酸含量增加2.2~2.7 倍,延长到6 h 时增加3.2~3.8 倍,总反式脂肪酸含量达到5.25%,远高于国外目前对油脂中反式脂肪酸的含量标准;葡萄籽油脱酸时间2 h 时总反式酸含量为0.16%,4 h 为0.27%,6 h 达到0.41%,总反式脂肪酸增加缓慢,脱酸6 h时葡萄籽油中总反式脂肪酸含量远低于亚麻籽油脱酸6 h 时总反式酸含量,说明亚麻籽油不适合进行长时间的物理脱酸.
2.7 物理精炼过程对亚麻籽油和葡萄籽油生育酚含量的影响
生育酚是油脂中的天然抗氧化剂,对人体具有重要的生理功能.采用高效液相色谱仪测定不同物理精炼条件下亚麻籽油和葡萄籽油中生育酚含量,结果如图5 所示.

图5 物理精炼过程对亚麻籽油和葡萄籽油生育酚含量的影响
由图5 可看出,亚麻籽油和葡萄籽油中生育酚含量分别为36.09 mg/100 g 和49.04 mg/100 g.随着脱酸时间延长,亚麻籽油和葡萄籽油氧化裂变程度加深,生育酚含量不断减少.脱酸的前2 h,物理精炼对亚麻籽油生育酚含量影响不大,4 h 损失了22.28%,6 h 损失了41.42%;葡萄籽油生育酚含量基本匀速下降,2 h 损失了24.04%,4 h 损失了46.51%,6 h 后,葡萄籽油生育酚含量降低到16.48 mg/100 g,结果表明,物理精炼亚麻籽油中生育酚含量的损失比葡萄籽油少.但脱酸4 h 后,两种油中生育酚的损失都很严重,这对油脂的储存和食用是不利的.
3 结论
物理方法精炼亚麻籽毛油和葡萄籽毛油的结果表明:精炼4 h 后,两种油均能达到一级油的国家标准.此时的亚麻籽油酸价为0.67 mg/g,过氧化值为4.25 mmol/kg,茴香胺值为105.32,反式脂肪酸含量为3.62%,生育酚为28.05 mg/100 g;葡萄籽油酸价为0.49 mg/g,过氧化值为2.27 mmol/kg,茴香胺值为21.66,反式脂肪酸含量为0.27%,生育酚26.23 mg/100 g.
相同脱酸条件下,亚麻籽油氧化裂变较为严重,反式脂肪酸生成速率达到葡萄籽油的十几倍.这跟亚麻籽油和葡萄籽油本身的脂肪酸组成密切相关,富含高亚麻酸的亚麻籽油不饱和度大于高亚油酸的葡萄籽油,油脂的不饱和度越高,越容易发生氧化裂变,越不易采用物理脱酸的方法精炼.
[1]张方英,庄峰,李阳,等.新疆亚麻油的理化性质及脂肪酸组成分析[J].食品研究与开发,2013,34(12):13-14.
[2]Guil-Guerrero J L,Campra-Madrid P,Belarbi E H.γ-Linolenic acid purification from seed oil sources by argentated silica gel chromatography column[J].Process Biochemistry,2000,36(4):341-354.
[3]Dwivedi C,Natarajan K,Matthees D P.Chemopreventive effects of dietary flaxseed oil on colon tumor development[J].Nutrition and Cancer,2005,51(1):52-58.
[4]刘传富,董海洲,李向阳,等.超声波辅助提取葡萄籽油工艺条件的优化[J].中国粮油学报,2010(3):54-58.
[5]李桂华,刘若瑜,李珺.葡萄籽油理化特性及组成分析的研究[J].河南工业大学学报:自然科学版,2009,30(6):37-40.
[6]张学文,单连青,符诒诚,等.酿酒葡萄籽的化学成分及综合利用[J].中外葡萄与葡萄酒,2006(4):52-54.
[7]Nykter M,Kymäläinen H R,Gates F,et al.Quality characteristics of edible linseed oil[J].Agricultural and Food Science,2006,15(4):402-413.
[8]袁榕,张丽新,王宝刚,等.油茶籽油物理精炼工艺实践[J].粮食与食品工业,2011,18(4):8-11.
[9]Martinello M,Hecker G,Carmen Pramparo M.Grape seed oil deacidification by molecular distillation:Analysis of operative variables influence using the response surface methodology[J].Journal of Food Engineering,2007,81(1):60-64.
[10]张明,李桂华,赵芳,等.精炼工艺对亚麻籽油中反式酸含量的影响[J].农业工程学报,2011,27(10):388-392.
