纳米金光度法测定维生素B1
2014-03-20王瑞勇范淑敏康小慧葛宝玉贾雪雷
王瑞勇, 范淑敏, 康小慧, 王 瑞, 葛宝玉, 贾雪雷
(郑州大学化学与分子工程学院 河南郑州450001)
0 引言
纳米金以其独特的物理和化学性质成为研究热点[1-3],近年来主要用作光学探针及电化学传感器.纳米金具有很好的生物相容性,能够和生物分子发生相互作用产生聚集,吸收峰红移至600~700 nm之间,溶液的颜色由原来的酒红色变为紫色或蓝色.纳米金比色法已用于多种物质的检测,包括DNA、蛋白质、农药和金属离子等[4-9],在生物分析、环境检测等方面具有很大的应用前景.
维生素B1能够构成辅酶维持体内的正常生理代谢,在临床上主要用于防治脚气病,辅助治疗神经炎、消化不良、全身感染、高热、糖尿病、甲状腺功能亢进等各种疾病.目前国内外报导的测定维生素B1的方法主要有高效液相色谱法[10]、光度法[11]、荧光法[12]、化学发光法[13]、电化学法[14-15]等,还没有用纳米金作探针应用于分子光谱法测定维生素B1的报道,本实验用纳米金测定维生素B1,灵敏度较高,而且操作简单,拓宽了纳米金在药物分析中的应用.
1 实验部分
1.1 实验药品与仪器
氯金酸(阿拉丁试剂有限公司),维生素标准品(中国药品生物制品检定所),柠檬酸钠、盐酸、乙酸钠(天津市科密欧化学试剂有限公司),维生素B1片剂(10 mg,国药准字H12020592)和注射液(100 mg,国药准字H14022171),二次蒸馏水、亚沸水(本实验室提供),实验用玻璃容器均用新配制的王水(HCl/HNO3=3∶1)浸泡,洗涤后使用.
UV-1800PC紫外-可见分光光度计(中国上海美谱达),F-4500荧光分光光度计(日本日立),PHS-3C酸度计(上海雷磁仪器厂),STP FA1004电子分析天平(上海上平仪器有限公司),Tecnai G220s-twin高分辨型透射电子显微镜.
1.2 实验方法
采用柠檬酸钠法制备纳米金.取250 mL三口烧瓶,加入100 mL 0.01%氯金酸溶液,在磁力搅拌加热器上加热至沸,加入2.75 mL 1%柠檬酸钠溶液,继续煮沸12 min,停止加热,自然冷却至室温,转移至100 mL容量瓶中,4℃保存.
取2 mL制备的纳米金于5 mL容量瓶中,加入800 μL pH 2.3的盐酸-柠檬酸钠缓冲溶液,定容至刻度线.取2 mL加入缓冲的纳米金于比色皿中,依次加入1~13 μL维生素B1标准溶液,混合均匀,以水为参比测定各自的吸光度.根据纳米金溶液与维生素B1作用前后吸光度的变化值Δ(A625/A518)绘制标准曲线.Δ(A625/A518)=纳米金与维生素B1作用后的吸光度比值A625/A518-纳米金与维生素B1作用前的吸光度比值A625/A518.
2 结果与讨论
2.1 纳米金的表征
制备的纳米金为酒红色,其粒径及表观颜色都符合文献报道.纳米金的吸收曲线如图1所示,最大吸收波长在518 nm处,这是球形的纳米金粒子特有的表面等离子吸收峰,从而估算出纳米金粒子的粒径约为13 nm,浓度约为3.72 nM[16].利用透射电镜(TEM)对制备的纳米金进行表征,从图中可以看出制备的纳米金为球形,粒径均匀,分散很好.

图1 纳米金的紫外-可见吸收光谱及透射电镜图Fig.1 The absorption spectra and photograph of TEM of gold nanoparticles
2.2 纳米金测定维生素B1
实验制备的纳米金粒子表面被大量的柠檬酸根离子包裹,由于静电排斥力纳米金能够稳定存在而不发生凝聚.维生素B1分子上带有氨基(—NH2),在弱酸溶液中,维生素B1带正电(—NH+3),由于静电作用力,维生素B1能够和纳米金发生相互作用,使纳米金粒子之间的距离变小,发生凝聚,利用透射电镜观察到作用后的纳米金,如图2所示,纳米金发生凝聚.凝聚后纳米金的紫外-可见吸收光谱发生红移和展宽,纳米金和维生素B1本身的共振散射峰很弱,凝聚后共振散射光谱增强,在此过程中,颜色由酒红色变为紫色最终变为蓝色.纳米金的凝聚程度用Δ(A625/A518)来表示,在一定范围内与维生素B1的浓度呈现良好的线性关系,据此建立了一种简单、快速测定维生素B1的比色分析新方法.

图2 纳米金与55 ng/mL维生素B1相互作用的透射电镜图,紫外-可见吸收光谱图及共振散射光谱图Fig.2 The photograph of TEM,absorption spectra and RRS spectra of gold nanoparticles with 55 ng/mL VB1
2.3 实验条件优化
在pH 2.0~7.0范围内,对比加入等体积等浓度的盐酸-柠檬酸钠缓冲溶液、盐酸-乙酸钠缓冲溶液和BR缓冲溶液对体系测定的影响(图3),其中盐酸-柠檬酸钠缓冲溶液对纳米金的聚集及变色效果最好,在此基础上,考察了不同缓冲溶液加入量对体系测定的影响(图4),最终选定800 μL pH为2.3的盐酸-柠檬酸钠缓冲溶液时,Δ(A625/A518)最大.这主要是因为pH过低,纳米金表面吸附的负电荷减少,不利于它与维生素B1的结合,pH过高时,维生素B1中质子化的氢解离,正电荷减少,也不利于与纳米金结合.
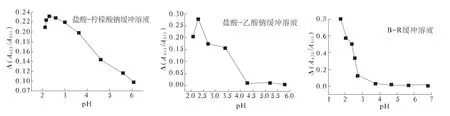
图3 不同缓冲溶液对体系的影响Fig.3 Effect of pH on the absorption ratio
考察纳米金的用量对体系测定的影响.改变纳米金的用量(1~3 mL),实验结果表明,纳米金的浓度增大时,其最大吸收峰值增大,而Δ(A625/A518)降低,考虑到纳米金容易染色,因此实验选择2 mL纳米金.
考察反应时间对体系测定的影响.分别对加入不同浓度的维生素B1前后的纳米金体系连续测定1 h,结果表明,加入维生素B1前,其吸收光谱基本不变,加入维生素B1后,在20 min时凝聚程度都达到最大,20 min后吸收光谱基本不再变化,反应时间定为20 min.
2.4 标准工作曲线
在最优条件下,按照实验方法测定维生素B1,由Δ(A625/A518)对维生素 B1的浓度 c作图(如图5所示),线性范围为5~55 ng/mL,线性回归方程为 Δ(A625/A518)= -0.073 4+0.019 7c(维生素 B1,ng/mL),相关系数为 0.998,检出限(3σ)为 0.74 ng/mL.

图4 不同盐酸-柠檬酸钠加入量对维生素B1测定的影响Fig.4 Effect of buffer solution amount on the absorption ratio

图5 不同浓度维生素B1存在下纳米金的紫外-可见吸收光谱图Fig.5 UV-vis absorption spectra of GNPs in the presence of different concentrations of VB1
2.5 常见物质的干扰
按照试验方法,考察了常见的金属离子、氨基酸和结构类似的药物分子的干扰情况(表1).结果表明,对于55 ng/mL维生素B1,常见的阴离子、金属离子、氨基酸和糖类对体系基本不干扰,表明该体系具有较好的选择性.
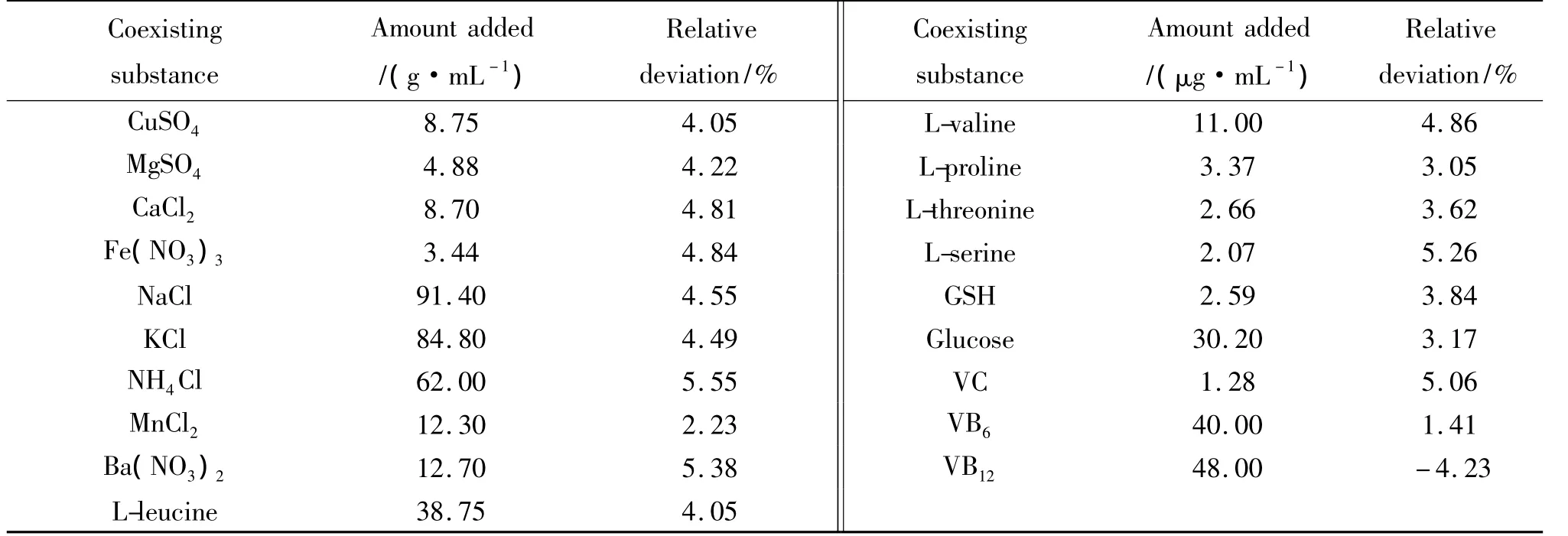
表1 常见物质的干扰(55 ng/mL维生素B1)Tab.1 Effects of coexistent substances(containing[VB1]=55 ng/mL)
2.6 样品分析
2.6.1 回收率试验
取维生素B1片剂20片,研细,精密称取适量(约相当于维生素B110 mg),加少量盐酸溶解,滤纸过滤后,转移至棕色容量瓶中.按实验方法进行标准加入回收实验,精密量取适量样品溶液,分别加入标准溶液10 ng/mL、30 ng/mL,测定吸光度值,计算回收率,并重复测定3次.精密量取1 mL维生素B1注射液于100 mL棕色容量瓶中,同样按实验方法进行标准加入回收实验,精密量取适量样品溶液,分别加入标准溶液15 ng/mL、30 ng/mL,测定吸光度值,计算回收率,并重复测定3次,回收率均在95% ~105%之间,说明该方法可以用于实际样品的分析.
2.6.2 含量测定
精密量取适量维生素B1片剂及注射液样品溶液,按试验方法测定吸光度,并计算ΔA,根据标准工作曲线计算样品中维生素B1的含量.结果见表2.由以上测定结果可知,购买的维生素B1片剂及注射液含量均在标示范围90.0% ~110%之内,RSD较小,符合药品质量管理规定.

表2 维生素B1片剂及注射液中维生素B1的测定Tab.2 Results for the determination of VB1in tablet and injection
3 结论
本文采用柠檬酸钠还原氯金酸的方法制得粒径约为13 nm的纳米金.在酸性环境中纳米金与维生素B1发生相互作用,纳米金产生凝聚,使其最大吸收峰发生红移,由此建立维生素B1的比色测定方法.优化了溶液pH、纳米金的浓度以及反应时间.在最佳条件下,方法的线性范围为5~55 ng/mL,结果令人满意.用此方法分析了维生素B1片剂和注射液,所测结果和按药典方法测定结果相一致.实现了维生素B1的测定,方法简单,测定速度快,而且不需要昂贵的仪器及大量的分析试剂,在食品分析及环境监测方面有很好的应用前景.
[1] Long M S,Christine D K.Nanoparticle conjugation increases protein partitioning in aqueous two-phase systems[J].Anal Chem,2006,78(2):379-386.
[2] Arūnas J,Kęstutis M,Jonas R,et al.Annealing effects on the transformations of Fe nanowires encapsulated in the alumina template pores[J].Mater Chem Phys,2009,115(1):217 -222.
[3] Khalid M B,Shalendra K,Chan G L.Influence of Al doping on electrical properties of Ni-Cd nano ferrites[J].Curr Appl Phys,2009,9(4):826 -832.
[4] Wang M,Gu X G,Zhang G X,et al.Continuous colorimetric assay for acetylcholinesterase and inhibitor screening with gold nanoparticles[J].Langmuir,2009,25:2504 -2507.
[5] Hurst S J,Han M S,Lytton-Jean A K R,et al.Screening the sequence selectivity of DNA-binding molecules using a gold nanopartiele-based colorimetric approach[J].Anal Chem,2007,79(18):7201-7205.
[6] Xu Qin,Du Shi,Jin Gendi,et al.Determination of acetamiprid by a colorimetric method based on the aggregation of gold nanoparticles[J].Microchim Acta,2011,173(3/4):323 –329.
[7] Huang K W,Yua C J,Tseng W L.Sensitivity enhancement in the colorimetric detection of lead(Ⅱ)ion using gallie acidcapped gold nanoparticles:improving size distribution and minimizing interparticle repulsion[J].Biosens Bioeleetron,2010,25(5):984-989.
[8] 温桂清,梁爱惠,吴宝玲,等.锑磷钼蓝-纳米金共振散射光谱法测定抗坏血酸[J].广西师范大学学报:自然科学版,2008,26(4):95 -98.
[9] 邓祥,黄小梅.基于L-半胱氨酸/纳米金固定酶的过氧化氢生物传感器[J].四川师范大学学报:自然科学版,2011,34(2):236-239.
[10]曹红,王浩.HPLC法快速测定婴幼儿配方奶粉中维生素B1[J].中国乳品工业,2010,38(11):46-47.
[11]高青.紫外分光光度法测定维生素B1片含量以及方法验证[J].中国医药指南,2012,(20):455-457.
[12]谢秀娟,葛笑兰,张振新.痕量维生素B1的双水相萃取与荧光测定[J].环境与健康杂志,2010,27(9):818-819.
[13]汪敬武,谢志鹏,杨伟平.流动注射化学发光法测定维生素B1[J].药物分析杂志,2005,25(8):996-998.
[14] 邹晓莉,丁宇,曾红燕,等.示波极谱法测定保健食品中维生素 B1[J].理化检验,2006,42(2):109-112.
[15]孙炳耀,赵蕾,钟红舰,等.维生素B1的电化学性质研究及测定[J].郑州大学学报:理学版,2002,34(3):74-76.
[16]Wolfgang H,Nguyen T K,Thanh J A,et al.Determination of size and concentration of gold nanoparticles from UV-vis spectra[J].Anal Chem,2007,79(11):4215-4221.
