浅析广东高考热点之一
——阿伏伽德罗常数
2014-03-18谢意纯衷明华
谢意纯 衷明华
(韩山师范学院 化学系,广东 潮州 521041)
阿伏伽德罗常数是中学化学一个比较重要的概念,用于建立宏观物理量与微观粒子之间的关系。它作为广东高考改革后的一个重要的知识点,从2010年广东高考分文理科以来,每年的高考卷都会出现,一般是以单项选择题的形式出现。而在近几年广东高考卷中,其主要考察的内容有:考生对物质的量、阿伏加德罗常数、气体摩尔体积、物质的量浓度等概念的含义的理解;考查考生根据物质的量、质量、微粒数目、气体体积之间的相互关系进行有关计算的能力;考查考生对常见氧化还原反应及其电子转移数的了解以及是否熟悉常见物质的聚集状态等。这类题型涉及的知识面广,几乎整个高中化学每一个模块都会有所涉及,这就要求考生要有较全面的能力。特别是自从2010年广东高考分文理科以来,试题题量虽然减少了,但是知识面的考察还是比较全面的,很多考生对此无从下手,为此,本文通过对近几年广东的高考卷以及模拟题的研读总结了10个常考点,旨在帮助高考考生和老师的备考。
考点一:考查物质的状态
考生要特别注意一些特殊物质在标准状况下的状态,例如:标准状况下,H2O为液态;SO3为固态;烃类有机物中碳的个数≤4的为气态;HF为液态;CH3Cl,HCHO为气态等。例如:
(2007广东高考)D.标准状况下,33.6LH2O含有9.03×1023个H2O分子 (χ,标况下水为液态。)
(2013中山一模)B.标准状况下,22.4L辛烷中分子数目为nA个 (χ,标况下辛烷为液态。)
(2014广州一模)D.标准状况下,2.24L乙醇含有0.1nA个CH3CH2OH分子(χ,标况下乙醇分子为液态。)
(2014茂名二模)D.标准状况下,22.4 L 的CCl4含有4 nA个Cl原子(χ,标况下四氯化碳为液态。)
考点二:只有在标准状况下的气体摩尔体积为:Vm =22.4lL/mol,其余情况下气体摩尔体积不一定为:Vm =22.4lL/mol,这是近几年来高考的一个热点。例如:
(2010年广东高考)D、常温常压下,22.4L CO2中含有nA个CO2分子(χ,常温常压下,气体的摩尔体积不一定为22.4lL/mol)
(2011年广东高考)C、常温常压下,22.4LCCl4含有nA个CCl4分子(χ,理想气体摩尔体积Vm =22.4lL/mol只适用于标准状态下的气体)
(2013年广东高考) C.标准状况下,22.4L盐酸含有nA个HCl分子(,HCl分子在标况下为气体。)
(2014湛江一模)A.标准状况下,22.4L汽油含有nA个分子(χ,标况下,汽油为液态。)
考点三:考察物质的微粒数
(1)分子中的原子数:①单原子数:Ne等稀有气体; ②双原子数:O2,N2等;③三原子数:O3等;④四原子数:P4等;等等。
(2)10电子结构:NH4+,CH4,NH3,H2O, H3O+,OH+。
(3)Na2O2的阴阳离子的个数比为1:2。
(2014汕头一模)D.1 mol CH5+所含电子数为8nA(χ,该物质所含的电子数为6+5-1=10个)
(2013东莞一模)A.2.24L NO2含有氧原子数0.2nA(χ,若为标况下则该选项成立)
(2013广州一模)C.7.8g Na2O2中含有的阳离子数目为0.1nA(χ,该物质所含的阳离子数目为0.2nA)
考点四:特殊物质摩尔质量:H(1g/mol);D(2g/mol);T(3g/mol);D2O(20g/mol)等。
(2014深圳一模)D.20 g重水(D2O)中所含电子总数为8nA(χ,重水跟水一样为10电子物质)
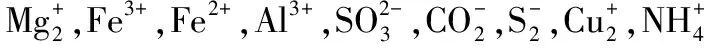
(2013广东高考)B.1L0.1mol/L的氨水中有nA个NH4+(χ,NH4+会发生部分水解)
(2011广东高考)B、1L0.1mol·L-1的氨水含有0.1nA个OH-(χ,氨水为弱电解质只发生部分电离)
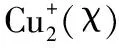
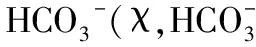
考点六:氧化还原反应中转移的电子数目:
①1molCl2与NaOH转移1mol电子。
②Na2O2与CO2或H2O的反应转移的电子数=Na2O2前的系数。
③1molCu与S反应转移1mol电子。
④1molFe与I2反应转移2mol电子。
⑤1molS与O2反应转移4mol电子(生成SO2,只有催化剂的存在才会生成SO3)
⑥1molFe与少量Cl2反应转移2mol电子;1molFe与足量Cl2反应转移3mol电子。
(2014汕头一模)B.标准状况下,22.4 L Cl2参加任何化学反应转移的电子数都是2nA(χ,1molCl2与NaOH转移1mol电子)
(2008年广东高考)C.标准状况下,氯气与足量氢氧化钠溶液反应转移的电子数为nA()
(2013潮州一模)B.1 mol Na2O2与水完全反应时转移的电子数为2NA(,2Na2O2+2H2O=4NaOH+O2↑)
(2013茂名一模)B.1molCl2与足量Fe反应,转移的电子数为3nA(χ,1molFe与足量Cl2反应转移3mol电子)
考点七:化学键的数目:
P4(空间正四面体结构)——6mol共价键
CH4(正四面体结构)——4mol共价键
SiO2(原子晶体)——(1molSi中含有4molSi—O键)
Si(原子晶体)——(1molSi中含有2molSi—Si键)
金刚石(原子晶体)——(1molC中含有2molC-C键)
对于1mol烷烃(CnH2n+2)中含有的共价键为(3n+1)mol
(2010广东高考)A、16gCH4中含有4nA个C-H键()
(2012广东高考)A、常温下,4gCH4含有nA个C-H共价键()
(2013东莞一模)C.1molC2H6分子中含有极性键为7nA(χ,因为乙烷分子中n=2,故该分子中含有的共价键为7nA,极性键为6nA)

(2011广东高考)A、常温下,23g NO2含有nA个氧原子()

(2008广东高考)C.常温常压下,46 g NO2和其混合气体含有的原子数为3 nA(,说其混合气体即包括了NO2和N2O4)


(2013茂名一模)C.0.1mol/L的 FeCl3溶液中含Fe(OH)3微粒的数目是0.1nA(χ,多个胶体分子才能形成一个胶粒)
考点十:对于存在混合气体的物质的量的计算:这种题一般只出现两种不同的物质。首先采用“定一法”即把所有已知的量看成是全部是某一物质的量,再求出该物质的物质的量,对于第二种物质也采用同样的方法。最后看看得出的两种物质的物质的量是否相等,若相等则取平均值,否则该题一定判断为错误的。
(2012广东高考)D、常温常压下,22.4L的NO2和CO2混合气体含有2nA个O原子 (χ,常温下,NO2和CO2不一定为1mol)
(2013东莞一模)B.常温常压下,乙烯和环丙烷(C3H6)组成的28 g混合气体中含氢原子4nA(,n乙烯=28/28*4=4mol,n环丙烷=28/42*6=4mol)
(2013肇庆一模)C.2.24LCO和CO2混合气体中含有的碳原子数目为0.1nA()
(2013中山一模)D.氧气和臭氧组成的4.8g混合气体中含有0.3 nA个氧原子()
总之,有关阿伏加德罗常数考题仍为高考的热点之一,而且综合性更强,特别注意考查的新特点:由纯净物到混合物,由无机物到有机物,由单一到综合的考查特点。在进行判断时首先要以“物质的量”为中心;以“标准状况”和“气体”这两个前提为基本条件(混合气体也适用);明确“三个关系”:(1)直接构成物质的粒子与间接构成物质的粒子(原子,电子)数目间的关系;(2)摩尔质量与相对分子质量的关系;(3)强电解质、弱电解质、非电解质与溶质粒子(分子或离子)数之间的关系。搞清“两个无关”物质的量、质量、粒子数的多少均与温度、压强的高低无关;物质的量浓度的大小与所取该溶液的体积多少无关(但溶质粒子数的多少与溶液体积有关)[1]。
[1]王海华,高考热点阿伏伽德罗常数[J].中国校外教育,2012年17期:124.
