燕麦秸秆还原浸出低品位软锰矿及其动力学
2014-03-17满瑞林薛建荣
满瑞林,常 伟,吴 奇,薛建荣
(中南大学 化学化工学院,长沙 410083)
锰矿是我国重要的矿产资源之一,目前利用最多的就是碳酸锰矿,随着多年的大量开采,碳酸锰矿石资源日益紧缺,在我国一些锰系产品生产集中的地区,所使用的碳酸锰矿的品位已由含锰 18%~20%降低到13%~15%[1]。而另一方面,大量含锰20%~25%的软锰矿却得不到利用。这主要是由于当前处理软锰矿最常用的工艺是煤还原焙烧-硫酸浸出法,采用约 800 ℃的焙烧温度,此时煤会自燃,还原效率低,存在成本高、粉尘大和污染环境等缺陷[2]。
有效地开发利用低品位软锰矿,以部分替代碳酸锰矿,扩大电解锰生产原料,已成为我国电解锰工业可持续发展亟待解决的问题。直接还原酸浸法是低品位软锰矿加工利用的有效途径和发展方向,但包括最受关注的两矿一步法[3]、二氧化硫吸收法[4],在大规模工业化的推广上并不成功。为此,人们越来越注重还原剂的选取,而生物质还原剂以其廉价、高效、来源广泛等特点,很有可能解决这一技术困境。TIAN等[5]利用玉米棒在硫酸体系中还原浸出复杂氧化锰矿,锰的浸出率达到 92.8%;牛莎莎等[6]提出利用桔子皮作还原剂在硫酸中浸出电解锰阳极渣的工艺,锰的浸出率可达96%;另外还有利用木屑[7]、稻草[8]、酒糟[9]、蔗渣[10]等纤维素类物质作还原剂的相关报道。
中国的纤维素原料很丰富,仅农作物秸秆就可达7亿多t,其中燕麦秸秆占3%[11]。燕麦秸秆大部分用作燃料或在田间烧掉,不但污染环境,对资源也是极大的浪费。本文作者将燕麦秸秆用作还原剂,在硫酸体系中还原浸出低品位软锰矿,最大限度地提高锰的浸出率,兼顾浸出液中杂质铁和低分子降解物含量的控制,还着重考察了燕麦秸秆在浸出前后的变化,为实现锰的选择性高效溶出,以及燕麦秸秆的综合利用,提供了理论依据。
1 实验
1.1 实验材料与试剂
实验所用软锰矿来自湖南湘西,其平均粒度为31.6 μm,其主要成分见表1。由表1可知,该低品位软锰矿的硅、铁含量较高,但实验中硅的最大浸出率低于0.3%,不影响浸出过程和后续净化过程。
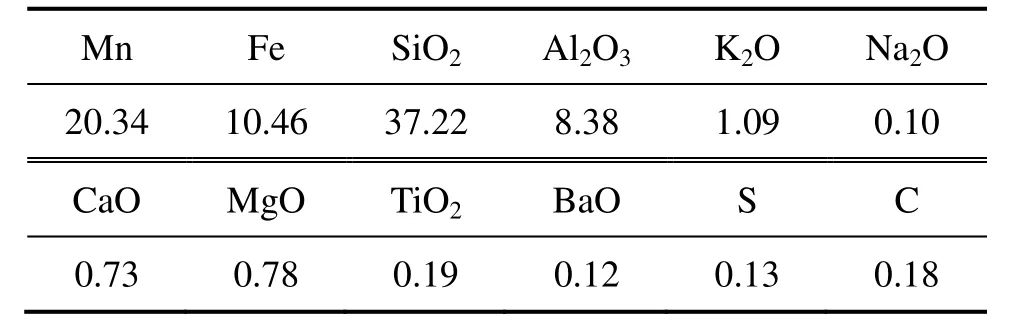
表1 软锰矿的主要化学成分Table 1 Chemical compositions of pyrolusite (mass fraction, %)
燕麦秸秆取自河北张家口地区,经干燥,粉碎至粒径小于150 μm,其主要成分分析如表2所列。秸秆中金属元素含量较少,其中锰含量为0.0012%(质量分数),铁含量为0.032%,在计算锰、铁浸出率时,均可忽略不计。实验所用硫酸为分析纯,所用水为蒸馏水。

表2 燕麦秸秆主要成分Table 2 Main compositions of oat straw (mass fraction, %)
1.2 实验过程与步骤
1.2.1 软锰矿的浸出条件实验
将三口烧瓶置于恒温水浴中,三口瓶一侧开口放置温度计和取样器,另一侧开口固定一个冷凝器,中间开口放置机械搅拌,其中搅拌速率固定为 400 r/min。取原矿10 g,与秸秆按一定比例混合,投入到三口瓶中,再将一定浓度硫酸按液固比配入,开启搅拌,在一定温度下反应一定时间,抽滤料浆,得浸出液,采用高氯酸-硫酸亚铁铵容量法测定其锰含量、EDTA 容量法测定铁含量[12]及快速密闭催化消解-分光光度法测定COD值。
1.2.2 软锰矿的浸出动力学实验
使用与条件实验相同的装置,搅拌速率为 400 r/min,待三口瓶中盛有的90 mL、150 g/L稀硫酸升温至90 ℃,将10 g原矿迅速倒入溶液中,开始计时。每隔一定时间吸取料浆3 mL,离心后取上清液,分析其锰含量,每次实验取样次数不超过3次。矿石中酸溶性MnCO3的锰含量为1.2%,在进行数据处理时,酸溶解的锰不计入氧化还原反应的锰浸出率。
1.3 实验原理
燕麦秸秆-硫酸直接浸出软锰矿,反应属多相氧化还原反应,其反应机理与其以玉米棒、木屑等植物还原剂酸浸反应机理大致相同[5,7]。秸秆中含有纤维素、半纤维素等成分,纤维素在硫酸介质中发生酸性水解,形成低聚糖和葡萄糖,其水解形成葡萄糖的反应如下:半纤维素反应情况比纤维素复杂,以聚木糖为例,

其完全水解反应如下:
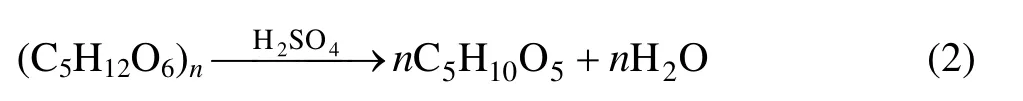
MnO2在酸性条件下具有较强的氧化性,秸秆水解生成的还原性糖与MnO2发生氧化还原反应,MnO2被还原为Mn2+而进入溶液中。主要反应如下:
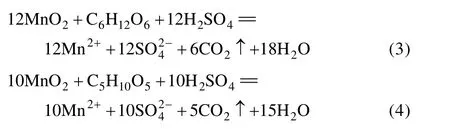
2 结果与讨论
2.1 硫酸浓度对还原酸浸过程的影响
在液固比为9 mL/g、麦秆与软锰矿质量比为0.3、浸出温度90 ℃、浸出1 h的条件下,考察硫酸浓度对锰、铁浸出率以及浸出液 COD值的影响,实验结果如图1所示。
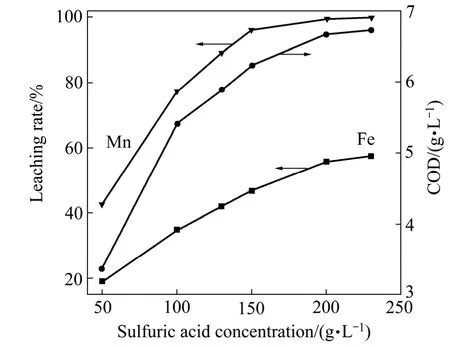
图1 硫酸浓度对锰、铁浸出率以及浸出液COD值的影响Fig. 1 Effect of sulfuric acid concentration on leaching rates of Mn, Fe and COD in lixivium
由图1可知,硫酸浓度对锰、铁浸出率和浸出液COD的影响较大。当硫酸浓度为50g/L时,锰浸出率为42.7%,铁浸出率19.1%,COD值为3.4 g/L。因为硫酸既是锰和铁的浸出剂,又是麦秆水解生成还原性糖的催化剂,所以,随着硫酸浓度的增大,锰、铁的浸出率以及 COD值均显著升高。当硫酸浓度为 150 g/L,锰、铁的浸出率分别为96.1%和46.8%,COD值为6.2 g/L。此后,增大硫酸浓度,锰浸出率升高缓慢,而铁浸出率和 COD值仍然增加明显。为控制铁浸出率和浸出液中小分子降解物在较低水平,硫酸的初始浓度不宜超过150 g/L。
2.2 液固比对还原酸浸过程的影响
当硫酸浓度为 150 g/L、麦秆与软锰矿质量比为0.3、浸出温度为90 ℃、浸出1 h时,改变浸出反应的液固比,考察液固比对锰、铁浸出率以及浸出液COD值的影响,结果如图2所示。
由图2可知,当液固比由5 mL/g增大至9 mL/g,锰浸出率由85.1%升高至96.1%,进一步增大液固比,锰浸出率基本保持不变。总体上铁浸出率随液固比的增加而逐渐升高。当液固比由5 mL/g增大至12 mL/g,浸出液COD值由9.6 g/L急剧减小至4.9 g/L,而COD总量却增大了 22.3%。这主要是由于硫酸浓度一定的情况下,增大液固比,增大了麦秆与硫酸的接触面积,促进了麦秆的酸性水解。考虑到每1 g秸秆粉末的吸水量为4.1 g,若液固比太小,矿浆黏度增大,反应体系很难搅拌均匀,适宜的液固比为7~9 mL/g。
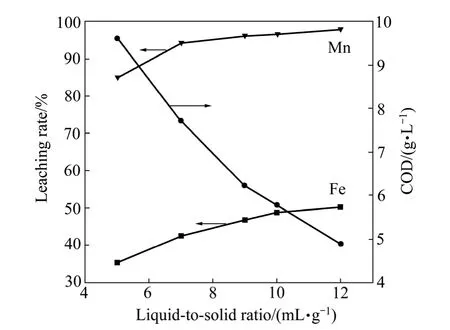
图2 液固比对锰、铁浸出率以及浸出液COD值的影响Fig. 2 Effect of liquid-to-solid ratio on leaching rates of Mn,Fe and COD in lixivium
2.3 燕麦秸秆用量对还原酸浸过程的影响
控制硫酸浓度为150 g/L、液固比为9 mL/g、浸出温度为90 ℃、浸出1 h时,考察不同麦秆用量对锰、铁浸出率以及浸出液COD值的影响,结果如图3所示。
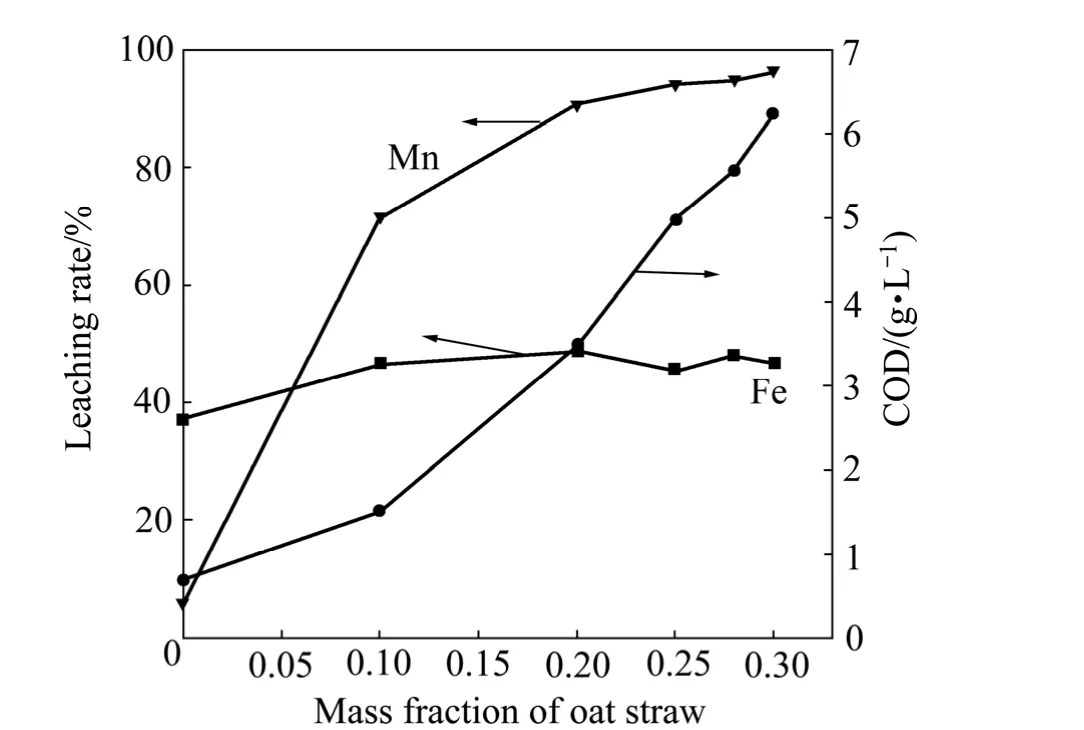
图3 麦秆用量对锰、铁浸出率以及浸出液COD值的影响Fig. 3 Effect of mass fraction of manganese dioxide ore to oat straw on leaching rates of Mn, Fe and COD in lixivium
由图3可知,随着麦秆用量的增加,Mn浸出率逐渐增大,增加幅度越来越小;浸出液 COD值也逐渐增大,但相应的增幅却越来越大。当还原剂用量不足时,麦秆水解生成的还原性物质可充分地与软锰矿反应,锰浸出率较低,COD值也较低;当还原剂足量时,锰矿反应更彻底,而水解生成的有机糖类则残余较多,所以锰浸出率较高,相应的 COD值也较高。在还原剂与软锰矿质量比为 0.3时,锰浸出率为96.1%,COD值为6.2 g/L。
未加入麦秆时,铁浸出率为 36.8%;加入麦秆可在一定程度上提高铁的浸出率,但加大麦秆用量时,铁浸出率没有明显的变化。由此可知,铁的浸出主要是通过酸性溶解、只有少部分铁是通过还原酸浸的方式溶出的[13]。在还原剂与软锰矿质量比为0.3时,可测得浸出液中Fe2+约占总铁量的4.6%。
2.4 不同温度下时间对锰浸出率的影响
在硫酸浓度为150 g/L、液固比为9 mL/g、麦秆与软锰矿质量比为0.3时,考察了不同温度下时间对锰浸出率的影响,结果如图4所示。
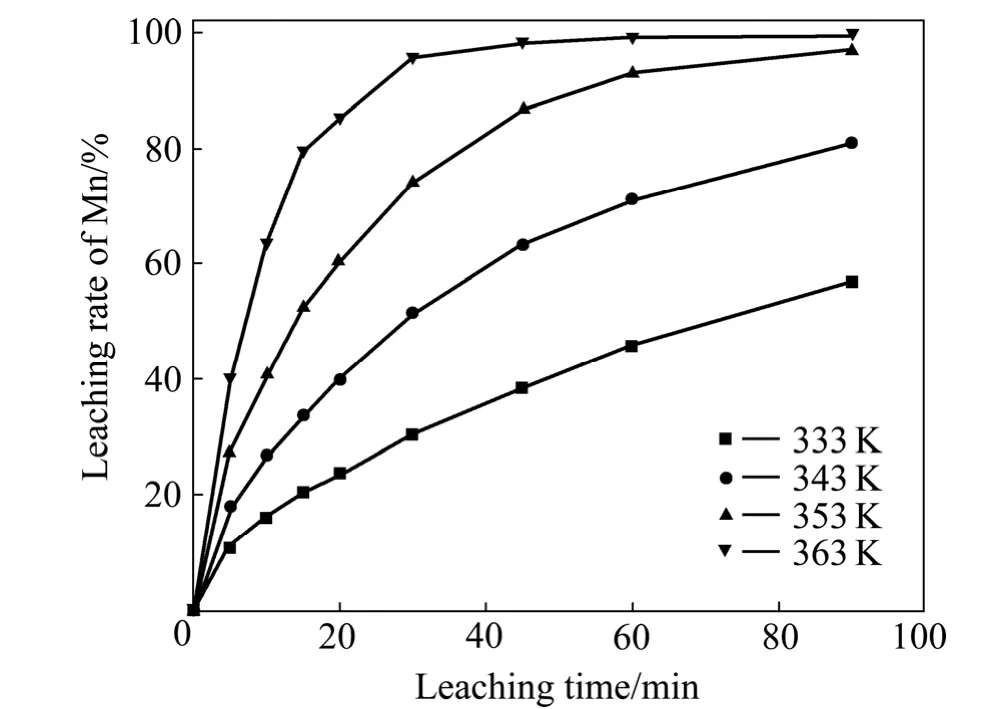
图4 不同温度下时间对锰浸出率的影响Fig. 4 Change of leaching rate of manganese with time at different temperatures
由图4可知,温度对锰浸出率的影响很大。当浸出温度低于353 K时,在0~90 min的整个时间段内,锰浸出率随着时间较缓慢的升高,浸出率较低;而在353~363 K时,反应在刚开始的前30 min内最为强烈,锰浸出率急剧上升;30 min后,锰浸出率则趋于稳定。升高温度促进了麦秆的酸性水解,且反应物活度增加,有利于浸出反应速率的提高。当浸出温度为353 K、反应时间为90 min时,锰浸出率为95.0%;而当浸出温度为 363 K、反应时间为 60 min时,锰浸出率为96.1%。
2.5 锰的浸出动力学
对于大多数液固反应,其最常见的反应模型为未反应核缩减模型[14-15]。当浸出过程为化学反应控制时,其动力学方程如下:

当浸出过程为内扩散控制时,其动力学方程如下:

式中:X为反应物浸出率;t为反应时间;k1和k2均为表观反应速率常数。
将图 4的实验数据代入特性式(5)和(6)进行模型及控制步骤判断,发现以t对1-(1-X)1/3作图,各温度下浸出动力学曲线的线性相关系数均大于0.99,且大体通过Y轴上同一点,如图5所示,说明各温度下浸出过程属于化学反应控制类型。
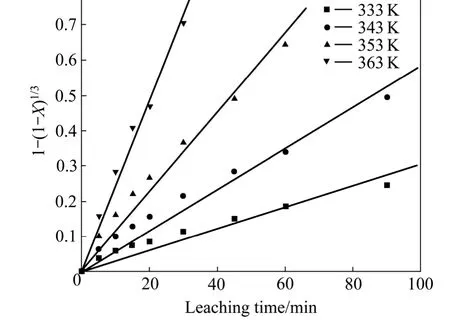
图5 不同反应温度下1-(1-X)1/3与反应时间的关系Fig. 5 Relationship between 1-(1-X)1/3 and reaction time at different temperatures
对缩核模型进行线性回归,所得直线的斜率即为反应速率常数k1。以lnk1对1/T作图可得浸出过程的阿仑尼乌斯曲线,见图6。
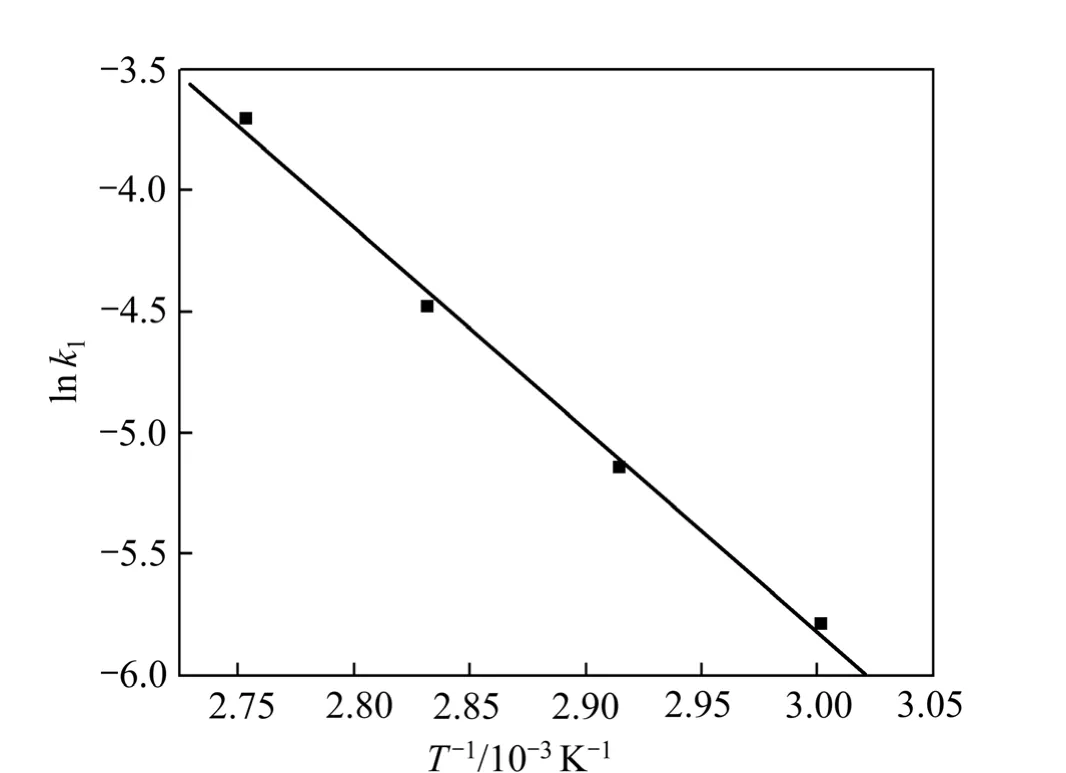
图6 ln k1与1/T的关系Fig. 6 Relationship between ln k1 and 1/T
在化学反应中,反应速度常数k是温度的函数,温度对反应速度常数的影响可用阿仑尼乌斯公式表示:

式中:k0为频率因子;Ea为活化能;T为热力学温度;R为摩尔气体常数。
结合式(3)和图6,可求得浸出过程的活化能Ea为69.4 kJ/mol,k0为224.9。对于多数浸出反应,化学反应控制时其表观活化能大于40 kJ/mol[16],这就进一步证明了还原浸出过程总体反应速率受化学反应控制。
2.6 燕麦秸秆酸性水解过程的分析
为了考察燕麦秸秆在浸出反应前后的变化,用双层纤维织物隔膜将秸秆紧紧包裹成一小团,投进矿浆中进行反应。当硫酸浓度为150 g/L,液固比为9 mL/g,麦秆与软锰矿质量比为0.3,浸出温度为90 ℃时,研究浸出时间对锰、铁浸出率、浸出液COD值的影响,结果如图7所示,并研究浸出时间对麦秆纤维素和半纤维素水解率的影响,结果如图8所示。
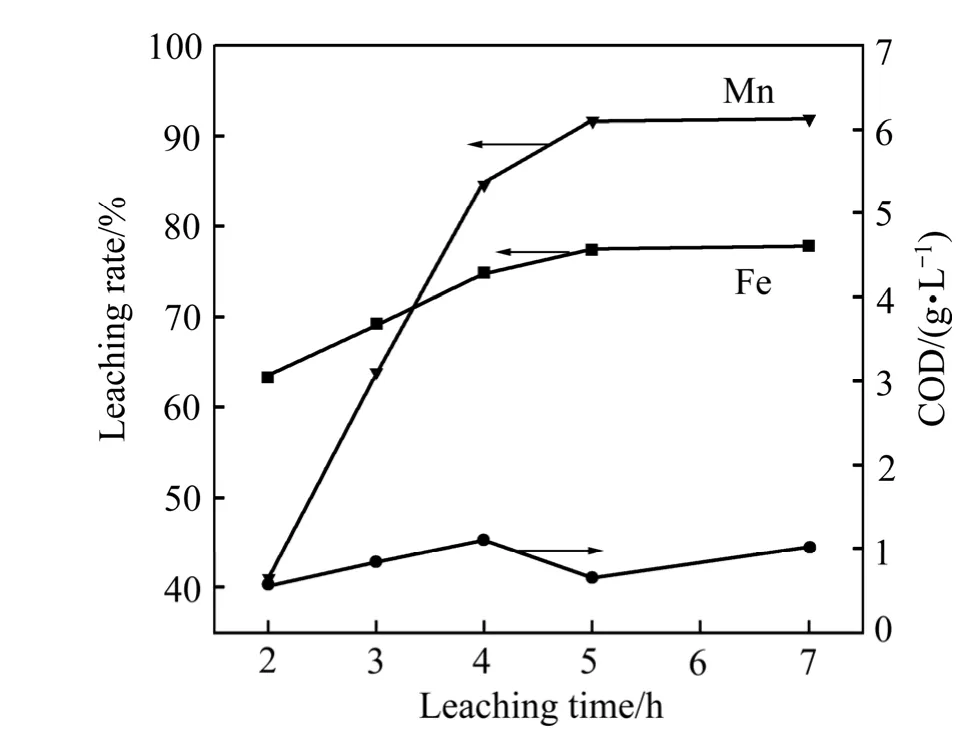
图7 浸出时间对锰、铁浸出率以及浸出液COD值的影响Fig. 7 Effect of time on leaching rates of Mn, Fe and COD in lixivium
由图7可知,随着时间的延长,锰、铁浸出率随之提高,当浸出时间由1 h延长至5 h时,锰浸出率由41.1%升高至91.8%,铁浸出率由63.4%升高至77.4%。当时间超过5 h时,继续延长时间,锰铁浸出率均变化不大。值得注意的是,浸出液COD值基本维持在1 g/L左右,远小于前述实验中的6.2 g/L。在前述浸出过程中,软锰矿和麦秆在稀硫酸介质中是均匀分散的,整个体系实际上是以还原促进水解,以水解反应维持还原,边水解边反应。而当隔膜将麦秆包成小团,完全或部分隔断其与软锰矿和硫酸的接触,增大了硫酸向麦秆扩散的阻力,同时增大了水解产物向软锰矿扩散的阻力,最终减缓了麦秆的水解速率和还原浸出反应的速率。换言之,麦秆的水解产物只够维持软锰矿的还原反应,不会有较多的残余。
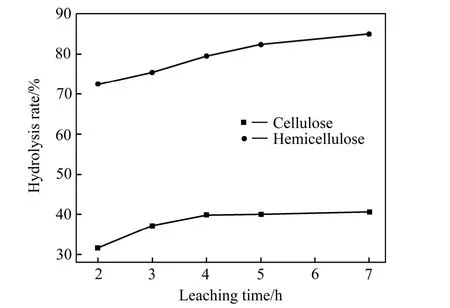
图8 浸出时间对秸秆纤维素和半纤维素水解率的影响Fig. 8 Effect of time on hydrolysis rates of cellulose and hemicellulose
由图8可知,随着时间的延长,纤维素水解率逐渐增大,浸出时间为4 h时,纤维素水解率为39.9%,再延长时间,纤维素水解率没有明显增加。而在浸出时间为2 h时,半纤维素的水解率已达到72.6%,且随着时间延长至7 h时,水解率达到84.9%。相对而言,半纤维素的水解更充分一些,主要是由于其聚合度低,在酸性介质中比纤维素易降解[17]。由于半纤维素的水解率接近 100%,而浸出液 COD值却不到1 g/L,可推知,前述浸出液COD值达6.2 g/L主要由纤维素的过量水解造成,因此,采用一定的措施适度调控纤维素的水解,对生物质直接还原浸出软锰矿的工业化进程是有重要意义的。本实验中,水解7 h后,秸秆总的水解率为40%左右,约60%的秸秆残留在浸渣中。
3 结论
1) 采用燕麦秸秆为还原剂,在硫酸介质中直接浸出低品位软锰矿,当硫酸浓度 150 g/L、液固比为 9 mL/g、麦秆与软锰矿质量比为0.3、浸出温度90 ℃、浸出1 h时,锰浸出率可达96.1%,铁浸出率为46.8%,浸出液COD值为6.2 g/L。
2) 锰的浸出过程符合未反应核缩减模型,主要受界面化学反应步骤控制,其浸出表观活化能为 69.4 kJ/mol。
3) 用双层纤维织物隔膜将秸秆包裹成小团,投进矿浆中进行反应,其他实验条件相同,使浸出时间延长至7 h,锰浸出率为91.8%,铁浸出率为77.4%,浸出液COD值由原来6.2 g/L降低至1 g/L左右。
[1] 李同庆. 低品位软锰矿还原工艺技术与研究进展[J]. 中国锰业, 2008, 26(2): 4-14.LI Tong-qing. Technology of low grade pyrolusite ore reduction process and recent advances[J]. China’s Manganese Industry,2008, 26(2): 4-14.
[2] ISMAIL A A, ALI E A, IBRAHIM I A, AHMED M S. A comparative study on acid leaching of low grade manganese ore using some industrial wastes as reductants[J]. The Canadian Journal of Chemical Engineering, 2004, 82(6).
[3] LAN Yao-zhong. Laboratory study: simultaneous leaching silver-bearing low-grade manganese ore and sphalerite concentrate[J]. Minerals Engineering, 2004, 17(9/10):1053-1056.
[4] PARTENOV D, STEFANOVA V, AVRAMOV A, CHIMBULEV M. Kinetics of leaching of polymetallic concretions in an aqueous solution of SO2[J]. Bulletin of the Higher Education Institutions: Series Non-ferrous Metals, 2004(1): 15-19.
[5] TIAN Xi-ke, WEN Xiao-xia, YANG Chao, LIANG Yu-jun, PI Zheng-bang, WANG Yan-xin. Reductive leaching of manganese from low-grade manganese dioxide ores using corncob as reductant in sulfuric acid solution[J]. Hydrometallurgy, 2010,100(3/4): 157-160.
[6] 牛莎莎, 王志兴, 郭华军, 李新海, 彭文杰, 胡启阳, 张云河.电解锰阳极渣还原浸出锰[J]. 中国有色金属学报, 2012, 22(9):2662-2666.NIU Sha-sha, WANG Zhi-xing, GUO Hua-jun, LI Xin-hai,PENG Wen-jie, HU Qi-yang, ZHANG Yun-he. Reductive leaching of manganese from manganese anode slag[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(9): 2662-2666.
[7] HARIPRASAD D, DASH B, GHOSH M K, ANAND S.Leaching of manganese ores using sawdust as reductant[J].Minerals Engineering, 2007, 20(14): 1293-1295.
[8] 黄欢喜. 稻草秸秆硫酸水解还原浸出低品位软锰矿及其电解金属锰的初步研究[D]. 吉首: 吉首大学, 2011: 26-33.HUANG Han-xi. Studies on hydrolysis reducing leaching low-grade pyrolusite by rice straw with sulfuric acid and electrolytic manganese[D]. Jishou: Jishou University, 2011:26-33.
[9] 粟海锋, 蒋 娜, 陈 超, 文衍宣. 木薯酒糟还原浸出低品位软锰矿工艺研究[J]. 无机盐工业, 2011, 43(9): 46-48.SU Hai-feng, JIANG Na, CHEN Chao, WEN Yan-xuan.Reductive leaching of manganese from low grade pyrolusite by cassava lees[J]. Inorganic Chemicals Industry, 2011, 43(9):46-48.
[10] 崔益顺. 蔗渣还原硫酸浸取低品位软锰矿工艺研究[J]. 无机盐工业, 2013, 45(10): 45-47.CUI Yi-shun. Study on sulfuric acid leaching process of manganese from low-grade pyrolusite with bagasse as reducing agent[J]. Inorganic Chemicals Industry, 2013, 45(10): 45-47.
[11] 陈洪章. 纤维素生物技术[M]. 北京: 化学工业出版社, 2005:1.CHEN Hong-zhang. Biotechnology of cellulose[M]. Beijing:Chemical Industry Press, 2005: 1.
[12] 地质矿产部. 锰矿石分析[M]. 北京: 地质出版社, 1991.Department of Geology and Mineral Resources. Manganese ore analysis[M]. Beijing: Geological Publishing House, 1991.
[13] 粟海锋, 孙英云, 文衍宣, 童张法, 裴锐南, 薛敏华. 废糖蜜还原浸出低品位软锰矿[J]. 过程工程学报, 2007, 7(6):1089-1093.SU Hai-feng, SUN Ying-yun, WEN Yan-xuan, TONG Zhang-fa,PEI Rui-nan, XUE Min-hua. Reductive leaching of manganese from low-grade pyrolus ore using cane molasses[J]. The Chinese Journal of Process Engineering, 2007, 7(6): 1089-1093.
[14] 倪 冲, 赵燕鹏, 阮福辉, 卢 娜, 杜冬云. 氨浸法从含砷石灰铁盐渣中回收铜的动力学[J]. 中国有色金属学报, 2013,23(6): 1769-1774.NI Chong, ZHAO Yan-peng, RUAN Fu-hui, LU Na, DU Dong-yun. Kinetics of copper recovery from As-contained solid waste by ammonia leaching method[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(6): 1769-1774.
[15] LEVENSPIEL O. Chemical reaction engineering[M]. New York:John Wiley & Sons, 1999.
[16] 莫鼎成. 冶金动力学[M]. 长沙: 中南工业大学出版社, 1987:298-301.MO Ding-cheng. Kinetics of metallurgical process[M].Changsha: Press of Central South University of Technology,1987: 298-301.
[17] 詹怀宇. 纤维化学与物理[M]. 北京: 科学出版社, 2005:196-197.ZHAN Huai-yu. Chemistry and physics of fibers[M]. Beijing:Science Press, 2005: 196-197.
