Fenton法分解NG/TEGDN废水研究①
2014-03-15张银玲王中合李念云臧乐丹
刘 亮,张银玲,王中合,李念云,臧乐丹
(西安航天化学动力厂,西安 710025)
0 引言
硝酸酯增塑聚酯推进剂代表了当今推进剂的发展方向[1-2],硝化甘油/二缩三乙二醇二硝酸酯(NG/TEGDN)作为新一代廉价、高能推进剂的含能增塑剂,得到广泛应用。NG/TEGDN混合硝酸酯中TEGDN亲水性较强,废水中酯含量大于0.5%,析出的硝酸酯沉积在管道、罐体、阀门及地下排放管线中,在撞击、摩擦或其他外力的作用下易爆炸。因此,需要对废水进行处理,使其达标排放[3-5]。
目前,针对含硝基化合物火炸药的废水处理有紫外光照法、组合臭氧法、Fenton试剂氧化法等几种方法[3]。Fenton法在去除水中有毒有害有机污染物方面十分有效,其最主要的优势是能彻底破坏有机化合物的分子结构,生成CO2、H2O和无机盐。因此,对Fenton法处理水体中难降解有机物的研究和应用己十分广泛,并取得了良好效果[6]。在近十几年的研究中,Fenton试剂已成功用于多种工业废水的处理,并日益受到国内外的关注。研究证明,Fenton试剂可有效处理含油废水、含醇废水、含苯系物废水、含硝基废水及含酚废水等[7]。王浩伊等[8]采用Fenton法处理丙二醇(PG)废水,PG的降解率可达99.1%。余宗学[9]利用Fenton试剂处理间二硝基苯废水,硝基苯去除率达88%,废水可生化性也明显提高。Bin等[10]对几种AOPs(O3,O3+H2O2,O3+UV,Fenton法)进行比较发现,对于含有硝基苯、二硝基甲苯(DNT)与TNT混合废水进行AOPs处理,O3与Fenton法最为有效。Zoh等[11]用Fenton法处理炸药废水时发现,在合适的条件下,废水中的污染物可完全降解。
针对含硝化甘油/1,2,4-丁三醇三硝酸酯(NG/BTTN)的废水,目前国内主要采用加碱水高温蒸煮进行分解破坏,但此法对NG/TEGDN废水处理不彻底。西安航天化学动力厂曾进行过Na2S2O3还原法分解NG/TEGDN废水研究,但由于分解产物中含单质S,会造成二次污染,未得到实际应用。目前,国外少见处理NG/TEGDN废水的报道和研究。本文采用Fenton试剂氧化法处理NG/TEGDN废水,通过实验得到了降低废水酯含量的工艺参数,从而使废水可达标排放。
1 实验
1.1 试剂和仪器
废水:自制,混合酯含量0.56%,酸度0.15~0.30(主要为HNO3);氢氧化钠:工业级,固体颗粒;Fenton试剂:自制;AB104-S型电子天平:METTLER TOLEDO;HH.S21型数显式电热恒温水浴锅:上海跃进医疗器械厂;UV-2550型紫外分光光度计:日本岛津公司。
1.2 实验方法
取水样50 ml加入到300 ml的锥形瓶中,用NaOH调节pH值,加入一定量的催化剂(Fe2+)和氧化剂(H2O2),置于一定温度的恒温水浴锅中恒温加热一定时间进行L16(45)正交实验,取样分析处理后酯含量[12],计算出酯去除率,根据酯去除率确定各因素对处理效果的影响程度和初步实验数据,然后进行单因素实验,确定最佳实验数据。因素及水平见表1。
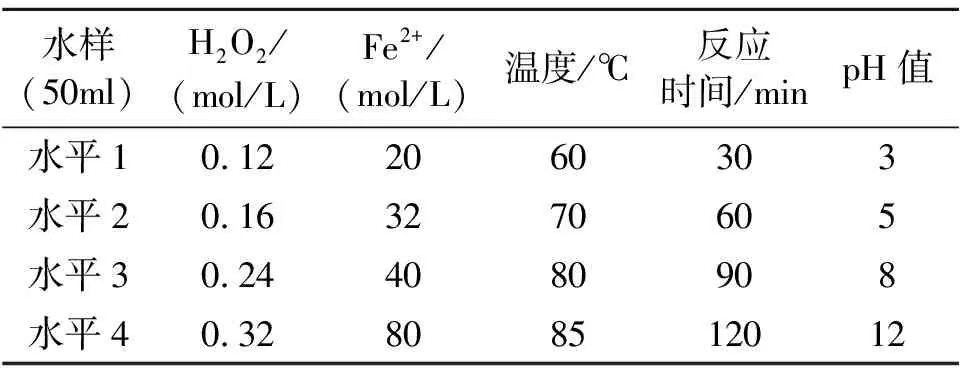
表1 正交实验因素水平
1.3 实验原理
1.3.1 Fenton氧化法的作用机理[12]
Fenton法属于高级氧化技术,是由H2O2与催化剂Fe2+所构成的氧化体系,其反应机理如下:
Fe2++H2O2→Fe2++·OH+OH-
Fe3++H2O2→Fe2++HO2·+H+
Fe2++·OH→Fe3++OH-
Fe3++HO2·→Fe2++H++O2
在Fenton体系中,H2O2在Fe2+的催化作用下,产生2种活泼的氢氧自由基(HO2·和·OH)。其中,·OH的氧化能力仅次于氟,具有很强的加成反应特性,从而引发和传播自由基链反应,加快有机物和还原性物质的氧化。因此,Fenton试剂可氧化水中的大多数有机物。
1.3.2 酯含量测定原理[13]
硝酸酯在浓硫酸的作用下与硫酸亚铁铵(FeSO4(NH4)2·6H2O)作用,生成紫红色络合物[Fe(NO)]SO4,硝酸酯的含量越高,溶液颜色越深,溶液颜色的深浅在分光光度计上对应一定的光度,通过测试光度比较溶液颜色深浅(比色法),则可确定硝酸酯的含量。主要反应式如下:
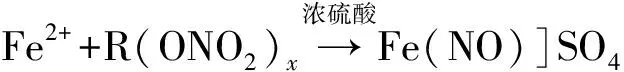
其中,Fe2+由硫酸亚铁铵离解而得。
2 结果与讨论
2.1 正交实验确定初步实验数据
取自制废水,按实验方法中设计的L16(45)正交实验进行实验,详见表2。从表2可看出,选定的影响因素中,H2O2的投加量对处理效果影响最大,然后依次是pH值、反应时间、Fe2+浓度、温度;初步实验数据如下:H2O2浓度为0.32 mol/L、pH值为5、反应时间为60 min、Fe2+浓度为80 mol/L、反应温度为80 ℃。
2.2 单因素实验优化废水处理工艺参数
下面通过研究H2O2浓度、pH值、反应时间、Fe2+浓度、温度等一系列单因素实验,对NG/TEGDN废水处理工艺参数进行优化。
2.2.1 H2O2浓度
改变H2O2浓度,分别为0.15、0.25、0.32、0.40、0.45、0.55 mol/L,然后进行实验,结果如图1所示。
从图1可看出,随H2O2浓度增加,酯含量先下降、后升高,最后趋于稳定。这是因为:(1)H2O2浓度较低时,随H2O2浓度增加,产生的·OH自由基的量增加,与废水中硝酸酯的反应速率增加,酯去除率随之升高;(2)H2O2浓度过高时,氧化性变强,反应一开始就把Fe2+转化为Fe3+,即:Fe2++H2O2Fe3++H2O+OH-,而降解则是在Fe3+的催化下进行,这样既消耗了H2O2又抑制了·OH自由基的产生,使酯去除率反而下降。(3)过量的H2O2加入后,废水中产生大量小气泡,这是因为发生副反应H2O2+2·OH→2H2O+O2↑,这样不仅消耗了·OH,而且使H2O2无效分解,降低了反应速率。实验证明,H2O2浓度为0.30~0.35 mol/L时,处理效果较好,酯去除率最高可达98.0%。
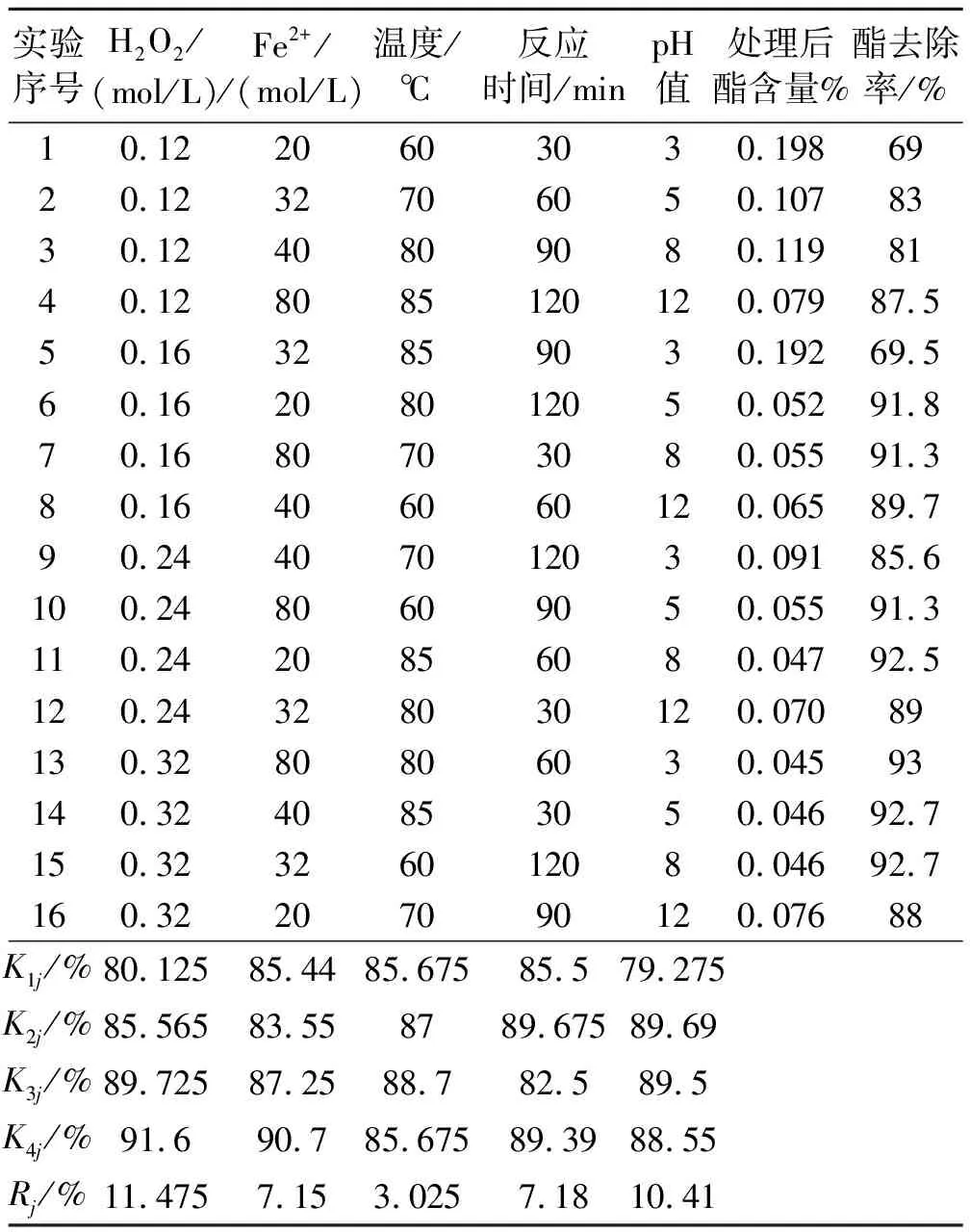
表2 正交实验数据统计表

图1 H2O2浓度对酯含量的影响
2.2.2 pH值
改变pH值分别为1、3、5、7、9、11,然后进行实验,结果如图2所示。从图2可看出,反应环境为酸性时,酯含量更低,随pH增大,酯含量先降低、后升高,当pH=5时,酯含量最低。这是因为Fenton试剂是在酸性条件下发生作用的,在中性或碱性环境中,Fe2+不能催化H2O2产生·OH自由基。经典的Fenton试剂反应理论[14]认为,当pH高于5时,随pH升高,不仅抑制了·OH自由基的产生,而且使溶液中Fe2+以氢氧化物的形式沉淀,即Fe2++OH-→Fe(OH)2↓,从而失去了催化能力;而当pH低于5时,溶液中H+浓度过高,Fe3+不能被顺利地还原成Fe2+,催化反应受阻。可见,pH直接影响到Fe2+、Fe3+综合平衡体系,从而影响到Fenton试剂的氧化能力。实验证明,pH为4~6时,处理效果较好,酯去除率最高可达97.8%。
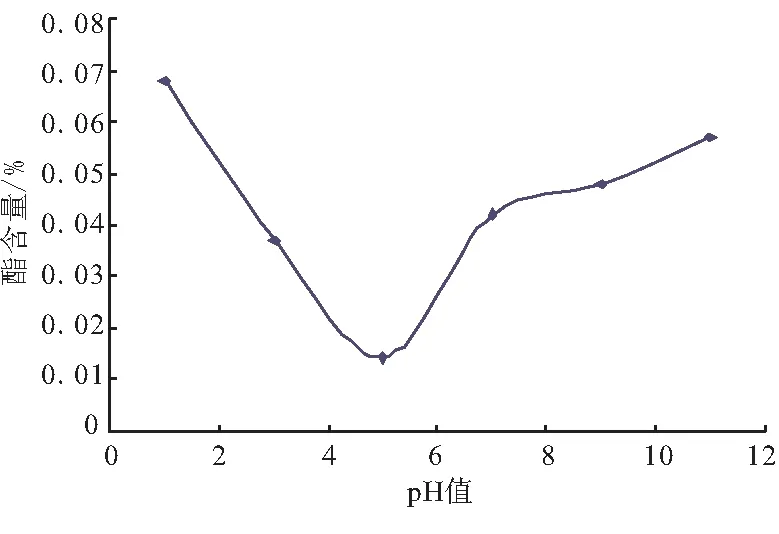
图2 pH值对酯含量的影响
2.2.3 反应时间
改变反应时间分别为0、20、40、60、80、100 min,然后进行实验,结果如图3所示。

图3 反应时间对酯含量的影响
从图3可看出,反应进行40 min时,酯含量就降至0.015,去除率达97%,说明在反应初期反应速率很快,在50~80 min时,酯含量随时间基本不再降低,表明反应速率基本稳定,80 min后,酯去除效果不明显,说明Fenton试剂处理含酯废水基本完成。化学反应进行的程度,在反应速率一定的情况下,直接受制于反应时间的长短,不同的废水所需的氧化时间不同。实验证明,对于本实验废水样品,反应时间为50~80 min即可达到最佳处理效果,酯去除率最高可达97.9%。
2.2.4 Fe2+浓度
配制Fe2+浓度分别为10、20、40、60、80、100 mol/L的溶液,然后进行实验,结果如图4所示。

图4 Fe2+浓度对酯含量的影响
从图4可看出,当Fe2+浓度低于20 mol/L时,废水中酯含量随Fe2+浓度增大迅速降低,但当Fe2+浓度高于20 mol/L时,酯含量变化缓慢,甚至略微升高。这是因为在Fe2+投加初期,随着Fe2+的增加,·OH自由基的数量不断增加,酯含量降低速度较快。但随着Fe2+的投加量进一步增加,虽然反应速度也会有所提高,但酯含量却在升高。这是因为Fe2+不仅起催化作用,而且可发生下列副反应:
Fe2++·OH+2H2O→Fe(OH)3↓+2H+
2Fe3++3H2O2+2H2O→2H2FeO4+6H+
2H2FeO4+3H2O2→2Fe(OH)3↓+2H2O+3O2↑
实验证明,Fe2+浓度为20~30 mol/L较好,酯去除率最高可达98.0%。
2.2.5 温度

综上所述,优化后的Fenton法处理NG/TEGDN废水条件如下:H2O2浓度为0.30~0.35 mol/L、pH值为4~6、反应时间为50~80 min、Fe2+浓度为20~30 mol/L、反应温度为80~90 ℃。酯去除率均在97.8%以上,最高可达98.2%。
2.3 Fenton氧化法与硫化钠还原法的比较
硫化钠与硝酸酯发生还原分解反应,反应速率较快。前期研究发现,在pH=10的条件下,硝化甘油浓度为0.015 mol/L,投入硫化钠剂量为320 mg/L,30 min可将硝酸酯分解至最低含量。取生产线上废水做5个样,用硫化钠还原法对其进行处理,各个样的酯含量及酯去除率情况详见表3。
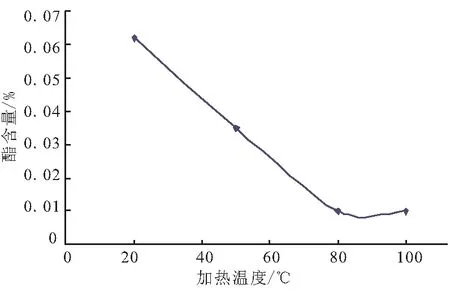
图5 反应温度对酯含量的影响
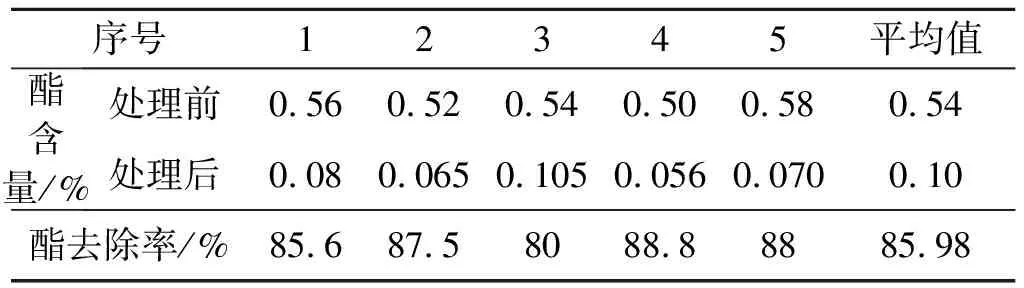
序号12345平均值酯含量/%处理前0.560.520.540.500.580.54处理后0.080.0650.1050.0560.0700.10酯去除率/%85.687.58088.88885.98
从表3可看出,采用硫化钠还原法,酯去除率平均值为85.98%,处理效果明显。硫化钠与硝酸酯反应具有低浓度、低投入、工艺简单的特点,但由于反应完毕后废水中含有胶体硫,造成了二次污染。而采用Fenton法处理NG/TEGDN废水,只要处理条件合适,酯去除率可达97.8%以上。处理后,酯含量可低于0.05%,不仅可使废水达标排放,而且反应产物无污染,有望在工业上推广应用。
3 结论
(1)研究发现,Fenton法处理NG/TEGDN废水时,H2O2浓度、pH值、反应时间、Fe2+浓度、温度对处理效果的影响程度依次减弱。
(2)Fenton法处理NG/TEGDN废水的条件:H2O2浓度为0.30~0.35 mol/L、pH值为4~6、反应时间为50~80 min、Fe2+浓度为20~30 mol/L、反应温度为80~90 ℃。在此条件下,废水处理效果最好,酯去除率最高可达98.2%。
(3)处理后,废水中混合酯含量低于0.05%,最低可达0.01%。
(4)与硫化钠还原法相比,Fenton法处理废水的效率更高,且更环保,有望在工业上推广应用。
参考文献:
[1] 李上文,赵凤起,袁潮,等.国外固体推进剂研究与开发的趋势[J].固体火箭技术,2002,25(2):36-42.
[2] 王泽山.火炸药科学技术[M].北京:北京理工大学出版社,2002.
[3] 韩光烈,黎留鑫,赵长友,等.硝化甘油生产安全技术与管理[M].北京:国防工业出版社,1988:88-95.
[4] 方维吾.硝化甘油[M].北京:国防工业出版社,1984: 12-16.
[5] 黎留鑫.论硝化甘油生产安全技术[M].北京:兵器工业出版社,2002: 99-101.
[6] Neyens E,Baeyens J. A review of classic Fenton's peroxidation as an advaneed oxidation technique[J].Hazardous Materials,2003,98:33-50.
[7] 孙晓君.废水难降解有机物的高级氧化技术[J].化工环保,2002,21(5):268.
[8] 王浩伊.Fenton试剂高级氧化法处理丙二醇废水研究[D].华东理工大学,2011.
[9] 余宗学.利用Fenton试剂预处理间三硝基苯生产废水[J].环境污染与防治,2002,24:282-284.
[10] Bin A K,Machniewski,Sakowicz P,et al.Degradation of nitroaromatics(MNT,DNT and TNT) by AOPs,Ozone[J].Science and Engineering,2001,23(5):343-349.
[11] Zoh K D,Stenstrom M K. Fenton oxidation of hexahy-dro-l,3,5-trinitro-1,3,5-triazine(RDX) and octahydro-l,3,5,7-tetranitro-1,3,5,7-tetrazoeine(HMX)[J].Water Research,2002,36(5):1331-1341.
[12] 武智,石晶晶,陈旭东.Fenton试剂氧化法在工业废水处理中的研究及应用进展[J].河北化工,2009,32(1):61-63.
[13] Q/GZ 443.6-2002. 废水中硝酸酯含量的测试[S].2002.
[14] Pignatello J J,Sun Y.Complete oxidation of atrazine by Fenton's reagent:condition optimization and product quantification[J].Environmental Science & Technology,1995,29(8):2083-2089.
