纳米羟基磷灰石制备与催化乙酸/乙醇酯化反应研究
2014-03-14陆秀凤殷恒波孔芙蓉卢志鹏尹海旭薛武平
陆秀凤,殷恒波,孔芙蓉,卢志鹏,尹海旭,薛武平
(江苏大学化学化工学院,江苏 镇江 212013)
纳米羟基磷灰石(Ca10(PO4)6(OH)2,HAP)在活体组织中具有良好的生物活性和表面活性,被广泛的应用于生物功能材料,如外科整形和口腔医学[1-2]。近年来人们发现,HAP可作为潜在的催化剂或催化剂载体应用于催化反应中,例如:丙烷[3-4]、苯[5]、醇类[6,7]、石蜡、不饱和酮类[8]以及甲烷[9]等氧化反应,甲基硫醇[10]和二甲基硫醚[11]的光致氧化反应以及硫醇制备查尔酮衍生物的Michael加成反应[12]。HAP的形貌、颗粒尺寸以及表面性质对其催化活性有重要的影响。
目前合成纳米HAP的方法有:溶胶-凝胶法[13-17]、化学沉淀法[18]、水热合成法[19-21]以及化学沉淀/水热合成法[22-24],其中沉淀法与水热法相结合可以制备出结晶性能良好的纳米HAP颗粒[22-24],添加含有不同官能团的有机修饰剂可以改变颗粒的大小与形貌。
乙酸乙酯作为一种有机溶剂被广泛地应用在油漆、涂料、油墨等有机产品中。在工业生产中常用无机质子酸如硫酸和磷酸作为催化剂催化乙酸和乙醇合成乙酸乙酯。其缺点是对设备的腐蚀性强、有毒、不易与产物分离[25-26]。固体碱催化剂在醇类和羧酸的酯化反应中具有较高的催化活性和选择性[27],是一种环境友好、新型催化剂。
笔者以柠檬酸三钠、十二烷基磺酸钠、乙醇胺以及聚乙二醇6 000为有机修饰剂,在不同pH值条件下,采用化学沉淀与水热合成法相结合的方法,合成了不同粒径的HAP纳米颗粒。采用XRD、FT-IR、TEM、BET与CO2-TPD等技术对合成的纳米HAP进行了表征。研究了纳米HAP作为碱催化剂在乙酸与乙醇的酯化反应中的催化活性。
1 实验部分
1.1 原 料
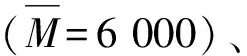
1.2 HAP的制备
在室温下,将70 mL 1.0 mol/L Ca(NO3)2·4H2O的水溶液加入到250 mL三口烧瓶中,按照Ca/P(摩尔比)为1.67的比例滴加0.6 mol/LH3PO4水溶液,滴加时间约30 min。再向反应混合液中加入占反应物总质量5%的有机修饰剂。然后,滴加氨水,调节反应液的pH值分别为7与10,室温(25 ℃)下搅拌反应4 h。将上述悬浮液移入内衬聚四氟乙烯的不锈钢水热反应釜中,于100 ℃反应12 h。反应结束后,得到的乳白色沉淀经过滤,蒸馏水洗涤至滤液的电导率低于2 mS/m。滤饼在80 ℃烘干8 h,干燥后的试样存放在干燥器中。
1.3 表 征
试样结构分析用Rigaku D-max 2200型X射线粉末衍射仪(XRD),放射源为CuKα(λ=1.540 6×10-10),管电压为50 kV。用高分辨透射电子显微镜(HRTEM,JSM-2100,加速电压为200 kV)观察制得样品粒子的形貌及颗粒的尺寸。用NOVA2000比表面仪测试试样的比表面积。采用KBr压片法(Nicolet Nexus470) 对试样进行FT-IR分析。
1.4 CO2程序升温脱附
采用CO2程序升温脱附(CO2-TPD)测定HAP试样的碱性。称取0.1 g试样于400 ℃烘干1 h脱除吸附水,于60 ℃通入CO2气体0.5 h,再以30 mL/min的流速通入N20.2 h,吹扫样品物理吸附的CO2。以20 ℃/min的升温速率程序升温至700 ℃进行CO2脱附。通过对峰面积积分,计算出脱附CO2的量。CO2脱附量代表试样碱量。
1.5 纳米HAP催化酯化反应
在100 mL三口烧瓶中加入摩尔比为1∶2乙酸和乙醇,回流温度85 ℃,以纳米HAP为催化剂催化该酯化反应,搅拌速率为300 r/min。将1 g HAP加入到50 mL乙酸和乙醇的混合液中。用气相色谱(SP-6800A) TCD检测器分析反应物组成。
2 结果分析与讨论
2.1 XRD分析
图1是添加不同有机修饰剂、不同pH值条件下制备的纳米HAP试样的XRD谱,与HAP的标准卡(Ca10(PO4)6(OH)2,JCPDS No.9-432)一致。从图1可看出:没有氢氧化钙和磷酸钙的特征峰,表明在本实验条件下制备的试样为纯相纳米HAP。
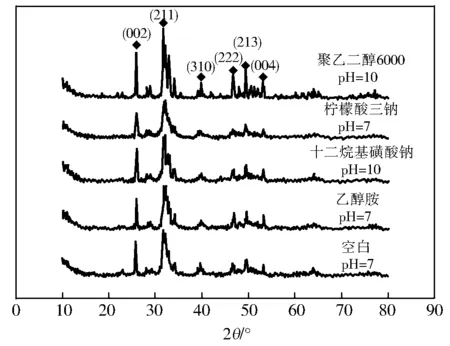
图1 纳米HAP试样的XRD谱
2.2 透射电镜分析
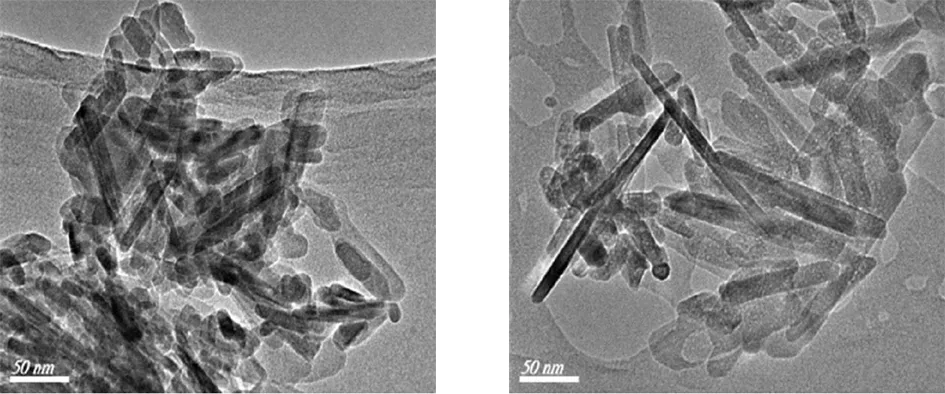
图2是HAP试样的透射电镜照片。通过透射电镜图测出的HAP颗粒的平均颗粒尺寸列于表1。由图2可知:不同pH值条件下,合成的HAP试样均为棒状纳米颗粒。

空白,pH=7 空白,pH=10

柠檬酸三钠,pH=7 柠檬酸三钠,pH=10
聚乙二醇 6 000,pH=7 聚乙二醇 6 000,pH=10

十二烷基磺酸钠,pH=7 十二烷基磺酸钠,pH=10

乙醇胺,pH=7 乙醇胺,pH=10
由表1可知:修饰剂存在时,随着溶液pH值的增加,棒状HAP试样的平均直径和平均长度随之增大,说明高pH值有利于棒状HAP晶体的生长。与无修饰剂时制备的HAP相比,修饰剂的存在有利于形成较小尺寸的HAP棒状颗粒。修饰剂对降低颗粒粒径影响为柠檬酸三钠>乙醇胺>十二烷基磺酸钠>聚乙二醇。由于有机修饰剂与HAP晶体的相互作用抑制了HAP晶体的生长。
2.3 比表面积分析
图3为无修饰剂与有修饰剂时制备的HAP试样的N2吸脱附等温线。从表1可看出:无修饰剂制备的HAP试样pH值为7时比表面积为69.5 m2/g,添加有机修饰剂制备的HAP的比表面积与未加修饰剂制备的HAP比表面积相比均变大,说明添加修饰剂有利于合成比表面积大的HAP试样。有机修饰剂对提高HAP颗粒比表面的影响为柠檬酸三钠>乙醇胺>十二烷基磺酸钠>聚乙二醇,与对粒径影响一致。HAP颗粒的粒径越小,其比表面积越大。
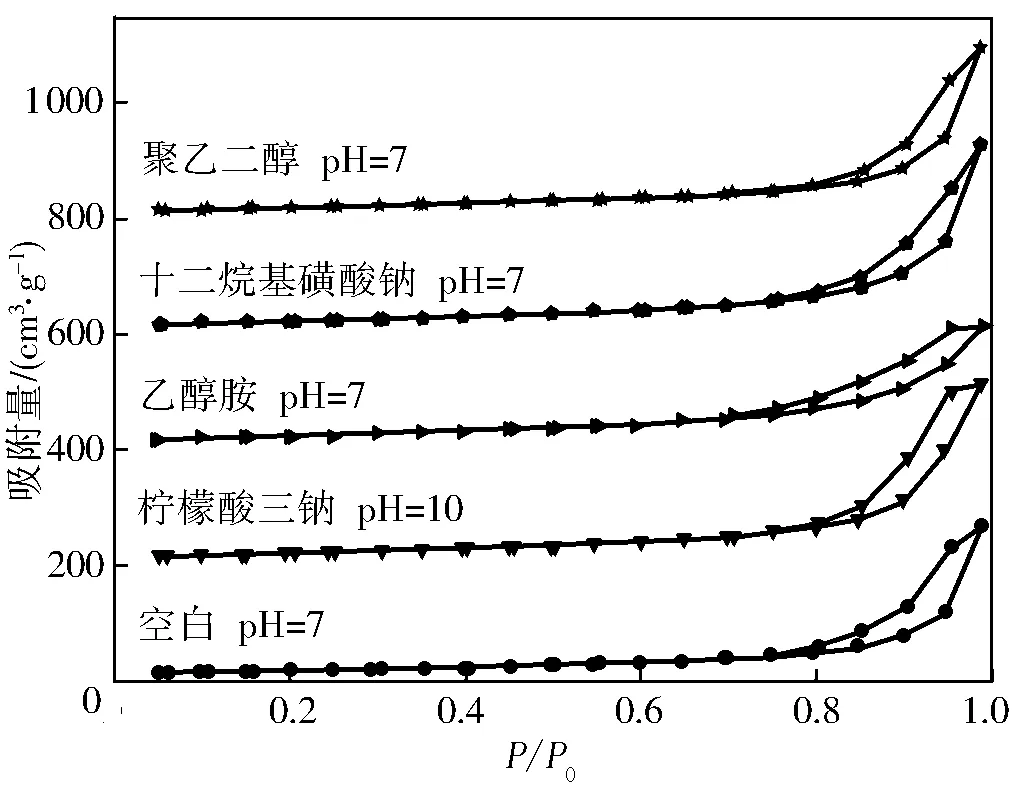
图3 HAP试样的N2吸脱附等温线

表1 HAP颗粒的平均粒径尺寸
2.4 FT-IR分析
图4是HAP试样的红外光谱。由图4可见:在3 569和634 cm-1处为—OH的振动吸收峰;1 088,1 036和962 cm-1处为PO43-的伸缩振动吸收峰;601,556和476 cm-1处为PO43-的弯曲振动吸收峰。由上可知,所制备的试样具有HAP晶体结构[22-24]。在872 cm-1处出现吸收峰,说明合成的HAP晶体中有CO32-离子,这是由于试样与空气中的CO2发生相互作用的结果。
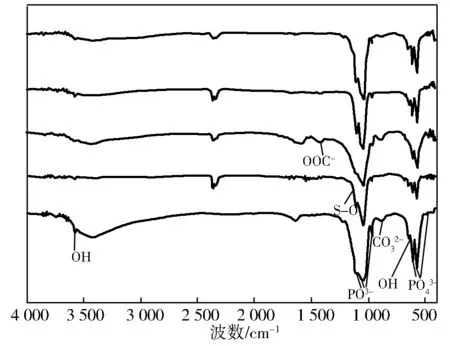
图4 纳米HAP试样的FT-IR

2.5 HAP试样的碱性测定与催化活性研究
图5为pH值分别为7和10时,添加不同修饰剂制备的HAP试样的CO2-TPD曲线。不同温度下CO2脱附量列于表2。
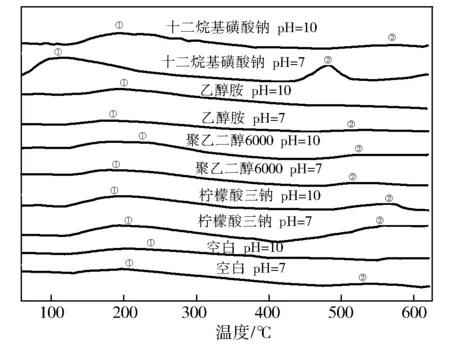
图5 HAP试样的CO2-TPD曲线
从图5可知:当pH值为7时,不添加修饰剂制备的HAP的TPD有双峰,CO2-TPD在204 ℃和536 ℃出峰;CO2脱附量分别为1.53和0.24 mmol/g。当pH值为10时,制备的HAP的CO2-TPD峰出在244 ℃,CO2脱附量为1.47 mmol/g。表明在pH值为7时,不添加修饰剂制备的HAP试样具有高的碱量。

表2 添加不同修饰剂制备的HAP催化剂的碱量与催化乙酸与乙醇反应中乙酸转化率
由表2可知:随着pH值的增加,试样CO2脱附量减小,表明制备的HAP碱量随着pH值的升高而减小。HAP试样的碱量顺序为HAP(十二烷基磺酸钠)>HAP(柠檬酸三钠)>HAP(聚乙二醇)>HAP(乙醇胺)>HAP(未加修饰剂)。修饰剂的种类影响了制备试样的表面碱性。
在回流温度(85 ℃)下,使用不同粒径的纳米HAP为催化剂,催化乙酸与乙醇酯化反应。酯化产物主要是乙酸乙酯,无副产物生成。反应15 h后,乙酸转化率见表2。由表2可知:与高pH值条件下制备的纳米HAP催化活性相比,低pH值条件下制备的纳米HAP具有高的催化活性。CO2-TPD实验表明,低pH值条件下制备的纳米HAP具有高的碱量。表明具有高碱量的纳米HAP有高的催化酯化反应活性。
有机修饰剂种类对制备的纳米HAP催化剂催化酯化反应活性有明显影响,在pH值为7条件下制备的纳米HAP催化剂,其催化活性依次为HAP(十二烷基磺酸钠)>HAP(乙醇胺)>HAP(未加修饰剂)>HAP(聚乙二醇)>HAP(柠檬酸三钠)。在pH=10条件下制备的HAP催化剂,其催化活性依次为HAP(乙醇胺)>HAP(未加修饰剂)>HAP(十二烷基磺酸钠)>HAP(柠檬酸三钠)>HAP(聚乙二醇)。十二烷基磺酸钠、乙醇胺、未加修饰剂条件下制备的纳米HAP有较高的催化活性。柠檬酸三钠存在时制备的纳米HAP具有较小的颗粒尺寸与较高的表面碱性,但是其催化活性较低,可能是由于表面吸附的柠檬酸根影响了其催化活性。聚乙二醇存在下制备的纳米HAP催化活性最低,可能与其颗粒直径较大有关。无修饰剂存在时制备的纳米HAP有较大的颗粒粒径和较低的表面碱量,但其催化活性较高,表明洁净的纳米HAP具有高的催化活性。
3 结 论
通过化学沉淀与水热合成相结合的方法,在不同pH值,不同有机修饰剂的作用下,合成了不同粒径的棒状纳米HAP。随着pH值增加,纳米HAP颗粒尺寸也增加。当柠檬酸三钠作为有机修饰剂时,柠檬酸根离子与HAP相互结合,抑制了HAP晶粒长大,合成的纳米HAP具有较小的颗粒尺寸,且其比表面积较大。在乙酸和乙醇的酯化反应中,纳米棒状HAP作为碱催化剂具有良好的催化活性,纳米HAP催化活性与其表面性质有关。
参 考 文 献
[1] Yeong K C B,Wang J,Ng S C.Mechanochemical synthesis of nanocrystalline hydroxyapatite from CaO and CaHPO4[J].Biomaterials,2001,22: 2705-2712.
[2] Chen F,Wang Z C,Lin C J.Preparation and characterization of nano-sized hydroxyapatite particles and hydroxyapatite/chitosan nano-composite for use in biomedical materials[J].Mater Lett,2002,57: 858-861.
[3] Shigeru S,Etsushi N,Hiromu H,et al.The oxidation of propane on nonstoichiometric calcium hydroxyapatites in the presence and absence of tetrachloromethane[J].Appl Catal A: Gen,2000,198: 171-178.
[4] Shigeru S,Tomotaka S,Daisaku M,et al.Enhancement of the catalytic activities in propane oxidation and H-D exchangeability of hydroxyl groups by the incorporation with cobalt into strontium hydroxyapatite[J].J Catal,2003,214: 8-14.
[5] Liptáková B,BáhidskM,Hronec M.Preparation of phenol from benzene by one-step reaction[J].Appl Catal A: Gen,2004,263: 33-38.
[6] Kohsuke M,Kazuya Y,Takayoshi H,et al.Controlled synthesis of hydroxyapatite-supported palladium complexes as highly efficient heterogeneous catalysts[J].J am Chem Soc,2002,124: 11572-11573.
[7] Kohsuke M,Takayoshi H,Tomoo M,et al.Hydroxyapatite-supported palladium nanoclusters: a highly active heterogeneous catalyst for selective oxidation of alcohols by use of molecular oxygen[J].J am Chem Soc,2004,126: 10657-10666.
[8] Unnikrishnan R P,Endalkachew S D.Epoxidation of olefins andα,β-unsaturated ketones over sonochemically prepared hydroxyapatites using hydrogen peroxide[J].Appl Catal A: Gen,2004,261: 69-76.
[9] Jun J H,Lee T J,Lim T H,et al.Nickel-calcium phosphate/hydroxyapatite catalysts for partial oxidation of methane to syngas: characterization and activation[J].J Catal,2004,221: 178-190.
[10] Harumitsu N,Koichi O.Photocatalytic activity of hydroxyapatite for methyl mercaptane[J].J Mol Catal A: Chem,2002,179: 193-200.
[11] Harumitsu N.A high active type of hydroxyapatite for photocatalytic decomposition of dimethyl sulfide under UV irradiation[J].J Mol Catal A: Chem,2004,207: 149-153.
[12] Zahouily M,Abrouki Y,Bahlaouan B,et al.Hydroxyapatite: new efficient catalyst for the Michael addition[J].Catal Commun,2003,4:521-524.
[13] Han Y C,Li S P,Wang X Y,et al.Synthesis and sintering of nanocrystalline hydroxyapatite powder by citric acid sol-gel combustion method[J].Mater Res Bull,2004,39: 25-32.
[14] Kim I S,Kumta P N.Sol-gel synthesis and characterization of nanostructured hydroxyapatite powderMater[J].Mater Sci Eng B,2004,111: 232-236.
[15] Bezzi G,Celotti G,Landi E,et al.A novel sol-gel technique for hydroxyapatite preparation[J].Mater Chem Phys,2003,78: 816-824.
[16] Liu D M,Troczynski T,Tseng W J.Water-based sol-gel synthesis of hydroxyapatite: process development[J].Biomaterials,2001,22: 1721-1730.
[17] Liu D M,Troczynski T,Tseng W J.Aging efect on the phase evolution of water-based sol-gel hydroxyapatite[J].Biomaterials,2002,23: 1227-1236.
[18] Kumar R,Prakash K H,Cheang P,et al.Temperature driven morphological changes of chemically precipitated hydroxyapatite nanoparticles.Langmuir,2004,20: 5196-5200.
[19] Liu J B,Ye X Y,Wang H,et al.The influence of pH and temperature on the morphology of hydroxyapatite synthesized by hydrothermal method[J].Ceram Int,2003,29: 629-633.
[20] Yoshimura M,Sujaridworakun P,Koh F,et al.Hydrothermal conversion of calcite crystals to hydroxyapatite[J].Mater Sci Eng C,2004,24: 521-525.
[21] Yan L,Li Y D,Deng Z X,et al.Surfactant-assisted hydrothermal synthesis of hydroxyapatite nanorods[J].Int J Inorg Mater,2001,3: 633-637.
[22] Wang A L,Liu D,Yin H B,et al.Size-controlled synthesis of hydroxyapatite nanorods by chemical precipitation in the presence of organic modifiers[J].Mater Sci Eng C,2007,27: 865-869.
[23] Wang A L,Yin H B,Liu D,et al.Effects of organic modifiers on the size-controlled synthesis of hydroxyapatite nanorods[J].Appl Surf Sci,2007,253: 3311-3316.
[24] Wang A L,Yin H B,Liu D,et al.Size-controlled synthesis of hydroxyapatite nanorods in the presence of organic modifiers[J].Mater Lett,2007,61: 2084-2088.
[25] Peters T A,Benes N E,Holmen A,et al.Comparison of commercial solid acid catalysts for the esterification of acetic acid with butanol[J].Appl Catal A: Gen,2006,297: 182-188.
[26] Dias J A,Caliman E,Dias S C L,et al.Preparation and characterization of supported H3PW12O40on silica gel: a potential catalyst for green chemistry processes[J].Catal Today,2003,85: 39-48.
[27] 曾韬,刘玉鹏,梁静谊.固体酸碱催化马来松香酯化反应[J].林产化工通讯,2001,35(6):18-21.
