内消瘰疬丸(浓缩丸)质量标准提高研究
2014-03-14魏立晓赵建邦刘兰生
魏立晓,赵建邦,刘兰生
内消瘰疠丸(浓缩丸),由夏枯草、玄参、大青盐、海藻、浙贝母、薄荷、天花粉、哈壳(煅)、白蔹、连翘、熟大黄、甘草、地黄、桔梗、枳壳、当归、玄明粉制成。原标准鉴别项收载有熊果酸对照品、玄参对照药材、大黄对照药材、甘草对照药材、当归对照药材、橙皮苷对照品的薄层色谱鉴别,含量测定项采用薄层扫描法测定夏枯草中熊果酸的含量。为了更有效地控制该药的质量,本实验对薄荷、连翘进行鉴别,采用高效液相色谱法测定夏枯草中迷迭香酸的含量和玄参中哈巴俄苷的含量。
1 仪器与试药
日本岛津LC-2010A高效液相色谱仪,DikmaC18(4.6 mm×250 mm,5 μm)。
哈巴俄苷对照品(批号111173-200604)、薄荷对照药材(批号120916-200508)、薄荷脑对照品(批号110729-200506)、连翘对照药材(批号120908-200613)、连翘苷对照品(批号110821-200711)均购自中国药品生物制品检定所。迷迭香酸对照品购自中国食品药品检定研究院(批号111871-201202)。内消瘰疠丸(浓缩丸)采用2家企业的6批样品(兰州佛慈制药股份有限公司,批号12C9-1、12C9-2、12C9-3;兰州太宝制药有限公司,批号73110510、73110524、73110603)实验。甲醇、乙腈为色谱纯,水为超纯水,其余试剂均为分析纯。
2 方法与结果
2.1 薄层色谱鉴别
2.1.1 薄荷的薄层鉴别 取本品粉末10 g,加石油醚(60~90℃)20 mL,密塞,振摇数分钟,放置30 min,滤过,药渣备用,滤液浓缩至1 mL,作为供试品溶液[1]。另取薄荷对照药材0.5 g,加石油醚(60~90℃)5 mL,同法制成对照药材溶液。再取薄荷脑对照品,加石油醚(60~90℃)制成每1 mL含2 mg的溶液,作为对照品溶液。按处方比例及制备工艺,配制不含薄荷的阴性对照品,并照上述供试品溶液的制备方法制成阴性对照溶液。照薄层色谱法[2010版《中华人民共和国药典》(一部)附录ⅥB]实验,吸取对照品溶液5 μL及对照药材溶液、供试品溶液、阴性对照液各10 μL,分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯(19∶1)为展开剂,展开,取出,晾干,喷以香草醛硫酸试液-乙醇(1∶4)的混合溶液,在100℃加热至斑点显色清晰[2]。见图1。

图1 薄荷的薄层鉴别(日光下)
2.1.2 连翘的薄层鉴别 取本品粉末10 g,加石油醚(60~90℃)20 mL,密塞,振摇数分钟,放置30 min,滤过;药渣挥尽石油醚后加甲醇20 mL,密塞,超声处理20 min,滤过,滤液浓缩至5 mL,作为供试品溶液。再取连翘对照药材1 g,同法处理,作为对照药材溶液。另取连翘苷对照品,加甲醇制成每1 mL含0.2 mg的溶液,作为对照品溶液。按处方比例及制备工艺,配制不含连翘的阴性对照品,并照上述供试品溶液的制备方法制成阴性对照溶液。照薄层色谱法[2010版《中华人民共和国药典》(一部)附录ⅥB]实验,吸取对照品溶液10 μL、对照药材溶液10 μL、供试品溶液 5 μL、阴性对照液各 5 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-甲醇(8∶1)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰[3-4]。供试品色谱中,在与对照品色谱和对照药材相应的位置上,显相同颜色的荧光斑点。阴性对照无干扰。见图2。
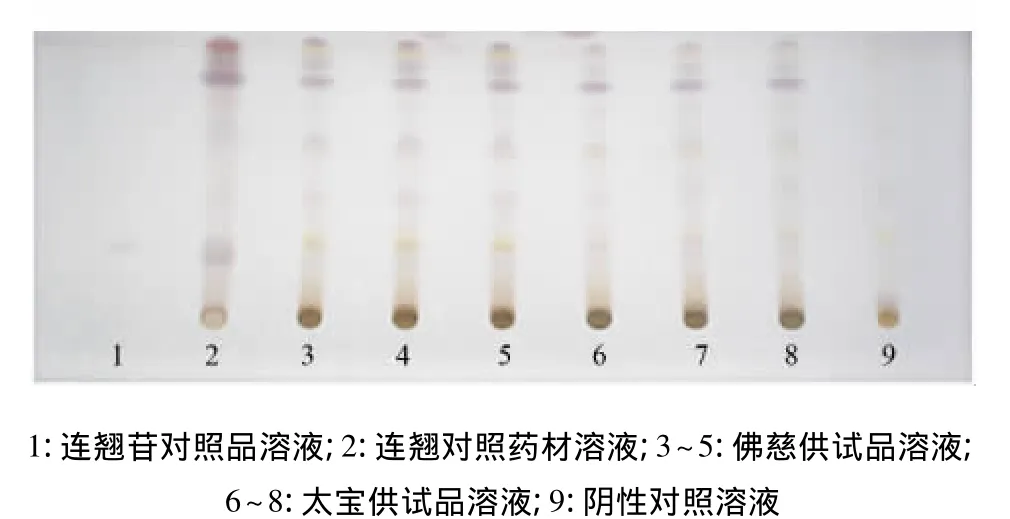
图2 连翘的薄层鉴别(日光下)
2.2 含量测定
2.2.1 夏枯草的含量测定
2.2.1.1 色谱条件 色谱柱DikmaC18(4.6 mm×250 mm,5 μm);以甲醇-0.1%磷酸(35∶65)为流动相,峰形及保留时间均比较理想;检测波长330 nm;柱温 30 ℃;流速 1 mL/min;进样量各 10 μL[5-7]。
2.2.1.2 供试品溶液的制备 取本品,研细,取约1 g,精密称定,精密加稀乙醇50 mL,称定质量;超声处理(功率180 W、频率50 kHz)30 min,放冷,再称定质量;用稀乙醇补足减失的质量,摇匀,用微孔滤膜滤过,即得[8]。
2.2.1.3 对照品溶液的制备 精密称取迷迭香酸对照品适量,精密加入稀乙醇,制成含迷迭香酸19.67 μg/mL的溶液,作为对照品溶液。
2.2.1.4 阴性对照溶液的制备 按处方比例及制备工艺,配制不含夏枯草的阴性对照样品,并按上述供试品溶液的制备方法制成阴性对照溶液。
2.2.1.5 专属性实验 取对照品溶液、供试品溶液与阴性对照溶液,分别按上述色谱条件进行测定,样品与对照品在同一保留时间有相同的波峰出现,而空白溶液则无相应的波峰(图3)。
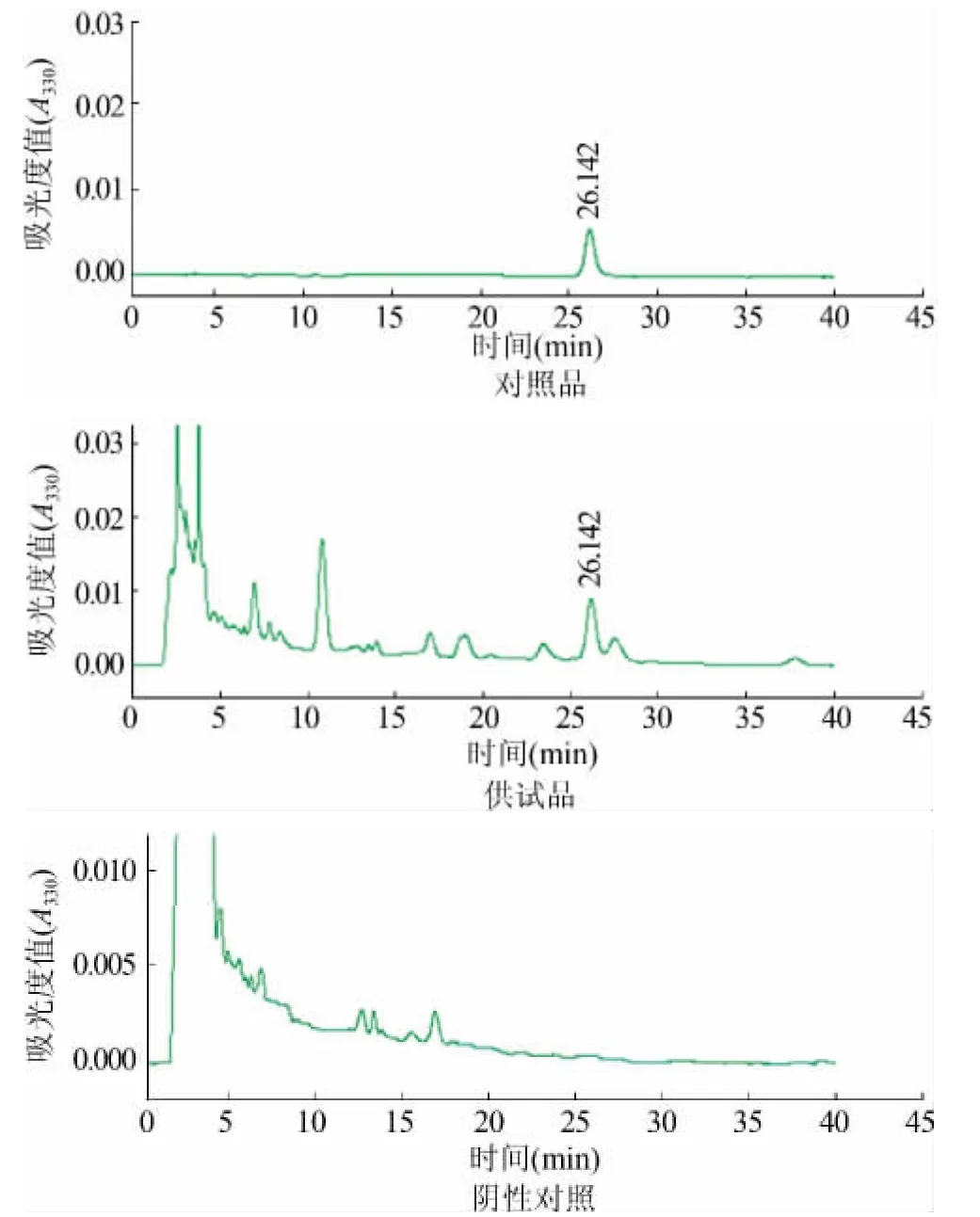
图3 内消瘰疠丸中迷迭香酸高效液相色谱图
2.2.1.6 线性关系考察 精密吸取上述迷迭香酸对照品溶液 2、4、6、8、10、12、14 μL,按上述色谱条件分别注入液相色谱仪,以对照品的进样量为横坐标,相应的峰面积积分值为纵坐标,计算回归方程:Y=3.560 922 9×10-7X-0.000 376 297,r=0.999 98,迷迭香酸在0.039 34~0.275 38 μg内有良好的线性关系。
2.2.1.7 精密度实验 分别精密吸取迷迭香酸对照品溶液10 μL,按上述色谱条件测定,各进样6次,测定峰面积积分平均值为548 398.4,相对标准偏差(relative standard deviation,RSD)为0.49%。表明精密度良好。
2.2.1.8 稳定性实验 取同一供试品溶液(批号12C9-1),分别在 0、2、4、6、8 h,按上述色谱条件各进样1次,每次10 μL,测定峰面积积分平均值为280 451.2,RSD为0.77%。
2.2.1.9 重复性实验 精取同一批供试品(批号12C9-1)6份,按上述供试品溶液制备方法和色谱条件重复实验测定,迷迭香酸含量平均值为0.451 88 mg/g,RSD为0.78%。
2.2.1.10 加样回收率实验 精取6份(批号12C9-1)已知含量的供试品,精加迷迭香酸对照品,按上述供试品溶液制备和色谱条件测定含量,平均回收率98.33%,RSD为2.27%(表1)。
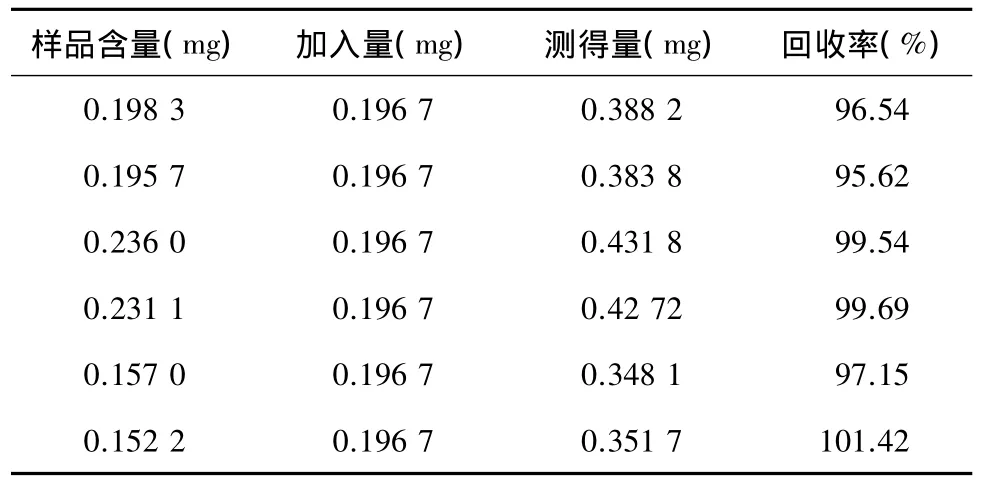
表1 迷迭香酸加样回收率实验
2.2.1.1 1样品测定 精取6批不同厂家的样品,按上述供试品溶液制备和色谱条件测定含量,6批样品 12C9-1、12C9-2、12C9-3、73110510、73110524、73110603 迷迭香酸含量分别为0.450 4、0.456 6、0.466 4、0.422 7、0.360 5、0.375 4 mg/g,均值为0.422 0 mg/g。
2.2.2 玄参的含量测定
2.2.2.1 色谱条件 色谱柱DikmaC18(4.6 mm×250 mm,5 μm);以乙腈-水(25∶75)为流动相,峰形及保留时间均比较理想;检测波长280 nm;柱温30℃;流速 1 mL/min;进样量各 10 μL[9-12]
2.2.2.2 供试品溶液的制备 取本品研细,取约1 g,精密称定,置具塞锥形瓶中,精密加入80%甲醇25 mL,称定质量,浸渍30 min;超声处理(功率180 W、频率50 kHz)30 min,放冷,再称定质量;用80%甲醇补足减失的质量,摇匀,用微孔滤膜滤过,即得[10-12]。
2.2.2.3 对照品溶液的制备 精密称取哈巴俄苷对照品适量,精密加入80%甲醇,制成含哈巴俄苷15.04 μg/mL的溶液,作为对照品溶液。
2.2.2.4 阴性对照溶液的制备 按处方比例及制备工艺,配制不含玄参的阴性对照样品,并按上述供试品溶液的制备方法制成阴性对照溶液。
2.2.2.5 专属性实验 取对照品溶液、供试品溶液与阴性对照溶液,分别按上述色谱条件进行测定,样品与对照品在同一保留时间有相同的波峰出现,而空白溶液则无相应的波峰。样品、对照品、阴性对照高效液相色谱图见图4。
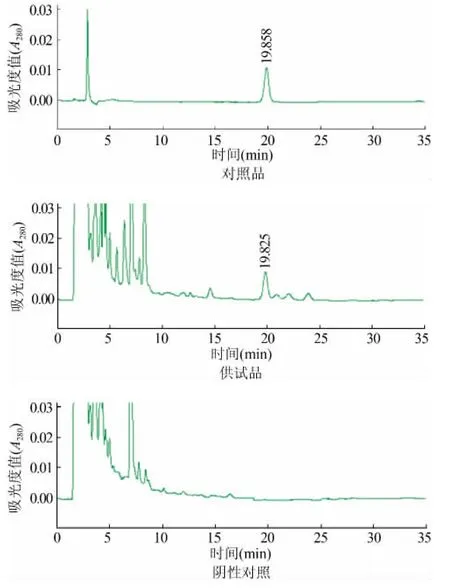
图4 内消瘰疠丸中哈巴俄苷高效液相色谱图
2.2.2.6 线性关系考察 精密吸取上述哈巴俄苷对照品溶液 4、6、8、10、12、14、16 μL,按上述色谱条件分别注入液相色谱仪,以对照品的进样量为横坐标,相应的峰面积积分值为纵坐标,计算回归方程:Y=4.384 076×10-7X-0.000 522 333 4,r=0.999 87,哈巴俄苷在0.060 16~0.240 64 μg内有良好的线性关系。
2.2.2.7 精密度实验 分别精密吸取哈巴俄苷酸对照品溶液10 μL,按上述色谱条件测定,各进样6次,测定峰面积积分平均值为342 483,RSD为0.42%。
2.2.2.8 稳定性实验 取同一供试品溶液(批号12C9-1),分别在 0、2、4、6、8 h,按上述色谱条件各进样1次,每次10 μL,测定峰面积积分平均值为243 265,RSD为1.44%。
2.2.2.9 重复性实验 取同一批供试品6份(批号12C9-1),按上述供试品溶液制备方法和色谱条件重复实验测定,哈巴俄苷含量平均值为0.266 82 mg/g,RSD为1.43%。
2.2.2.10 加样回收率实验 精取6份(批号12C9-1)已知含量的供试品,精加哈巴俄苷对照品,按上述供试品溶液制备和色谱条件测定含量,平均回收率98.26%,RSD为2.17%(表2)。
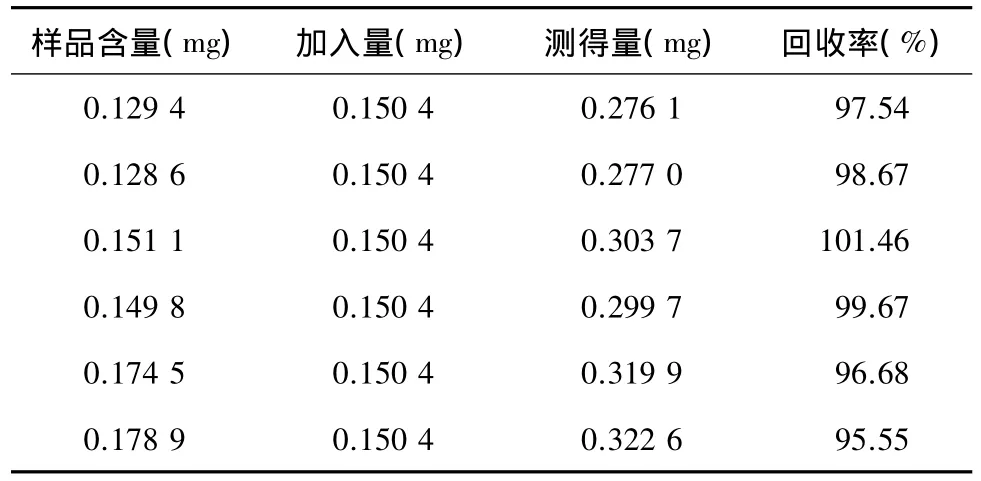
表2 哈巴俄苷加样回收率实验
2.2.2.11 样品测定 精取6批不同厂家的样品,按上述供试品溶液制备和色谱条件测定含量,6批样品 12C9-1、12C9-2、12C9-3、73110510、73110524、73110603 哈巴俄苷含量分别为0.266 3、0.272 5、0.278 1、0.169 8、0.169 5、0.157 7 mg/g,均值为0.219 0 mg/g。
3 讨论
薄荷薄层色谱法鉴别参照2010版《中华人民共和国药典》(一部)薄荷质量标准鉴别(3)项下实验[1]263,结合本品的特性拟定如上述方法。
连翘薄层色谱法鉴别参照2010版《中华人民共和国药典》(一部)连翘质量标准鉴别(2)项下实验[1]159,以石油醚(30~60 ℃)提取,提取效果不佳,斑点不明显,结合本品的特性采用石油醚(60~90℃),薄层色谱斑点清晰。
实验前对本品夏枯草中迷迭香酸成分的提取方法进行研究,分别考察了提取时间、提取溶剂和提取方式(超声提取和加热回流提取),最终确定用稀乙醇超声30 min效果最好。对本品玄参中哈巴俄苷的提取方法也进行了同样的研究,最终确定80%甲醇浸渍30 min后超声30 min效果最佳。
原标准中含量测定项采用薄层扫描法测定夏枯草中熊果酸的含量,中药材如山楂、熊果、车前、女贞子等药材都含有该成分[13],含量检测专属性差,故建立新的方法检测夏枯草中迷迭香酸的含量。玄参是内消瘰疬丸(浓缩丸)中的重要药味之一,玄参中已分离出化学成分有50多种,主要含有环烯醚萜、苯丙素苷、有机酸及挥发油等[14]。本研究采用高效液相色谱法测定环烯醚萜类成分中的哈巴俄苷,有利于提高药品质量标准。
现仅参考对6批实际样品测定的结果,并考虑不同夏枯草原料中迷迭香酸含量的差异、大生产过程的损失、制剂中提取转移的因素及实际操作过程的误差,将其下浮至70%。限度暂定为本品每1 g含迷迭香酸(C18H16O8)不得少于0.30 mg。考虑不同玄参原料中哈巴俄苷含量的差异、大生产过程的损失、制剂中提取转移的因素及实际操作过程的误差,将其下浮至70%。限度暂定为本品每1 g含哈巴俄苷(C24H30O11)不得少于0.15 mg。
[1]国家药典委员会.中华人民共和国药典:一部[M].北京:化学工业出版社,2010.
[2]马俊奇,春阳.薄荷薄荷桉油片(Ⅰ)中薄荷脑薄层色谱鉴别方法的改进[J].北方药学,2014,11(2):7.
[3] 陈雪,董军伟,丁锤,等.芩翘通窍胶囊薄层鉴别[J].河北中医,2012,34(9):1399-1400.
[4]张丽,王凡,刘航.消痤胶囊的质量控制[J].陕西中医,2007,28(10):1406-1407.
[5]李锦淼,吴洪文.HPLC法测定肿节风中绿原酸、异嗪皮啶和迷迭香酸的含量[J].西北药学杂志,2014,29(2):125-127.
[6]花汝凤,姚江雄,黎志坚,等.HPLC同时测定夏桑菊颗粒中迷迭香酸与异迷迭香酸苷的含量[J].中国实验方剂学杂志,2013,19(24):75-77.
[7]张凤霞,张宗宝.祛痤胶囊的制备及其哈巴苷和迷迭香酸含量测定[J].中国药业,2014,23(6):31-33.
[8]张兰珍,秦雯,张小华,等.夏枯草不同部位中咖啡酸和迷迭香酸的含量测定方法研究[J].北京中医药大学学报,2007,30(5):343-345.
[9]陈华国,周欣,赵超,等.HPLC测定养阴清肺颗粒中哈巴俄苷的含量[J].中国实验方剂学杂志,2010,16(7):44-46.
[10]魏庆华,王勤.HPLC测定增液承气口服液中哈巴苷和哈巴俄苷含量[J].中国实验方剂学杂志,2012,18(7):81-83.
[11]王建华,谢丽华,刘洪宇,等.玄参不同加工品中哈巴俄苷与肉桂酸的HPLC含量测定[J].中国药学杂志,2000,35(6):375-378.
[12]焦豪妍,杨燕军,徐吉银,等.HPLC法同时测定玄参破壁粉粒中哈巴俄苷和肉桂酸的含量[J].海峡药学,2011,23(10):71-72.
[13] 孟艳秋,陈瑜,王趱,等.熊果酸的研究进展[J].中国新药杂志,2007,16(1):25-27.
[14]蔡少青,谢丽华,王建华,等.中药玄参中哈巴俄苷和肉桂酸的高效液相色谱法测定[J].药物分析杂志,2000,20(3):191-194.
