硅酸盐水泥在模拟体液中降解和矿化性能
2014-03-13陈耀忠吕晓迎刘根娣
陈耀忠 吕晓迎 刘根娣
(1 东南大学生物电子学国家重点实验室,南京210096)
(2 东南大学附属中大医院,南京210009)
三氧化矿物凝聚体(mineral trioxide aggregate,MTA)是20 世纪90年代发展起来的一种新型的牙髓治疗生物材料.自1993年Lee 等[1]首次报道MTA 以来,由于其具有可湿固化性、良好的封闭性、生物相容性及生物活性等显著优点,受到了国内外学者和临床医生的广泛关注,被认为是一种最有前景的牙髓材料,但其也存在固化时间长、对牙体组织黏结性小、价格高等缺陷[2-4].
MTA 主要是由80%硅酸盐水泥(Portland cement,PC)及20%X 射线阻射剂氧化铋组成[5-6].硅酸盐水泥的主要成分为硅酸二钙、硅酸三钙、铝酸三钙、铁铝酸四钙及二水硫酸钙等,是一种最常见的水泥,主要应用于土木工程.相关研究显示:除了不含X 射线阻射剂氧化铋外,硅酸盐水泥的主要成分、pH 值、抑菌性能、封闭性能及生物相容性等均与MTA 相类似,但其价格低廉、易于获得,因此可视作MTA 的一种替代材料而应用于牙髓治疗术中[7-10].
学者们对硅酸盐水泥的生物相容性、封闭性能及体外抑菌性能等进行了大量的研究,但对其与口腔环境如血液、组织液等直接接触后所引起基本理化反应的研究甚少.模拟体液(simulated body fluid,SBF)的主要成分与人体血浆的无机成分基本相同,是目前体外模拟最常用的溶液,被广泛接受为研究体外矿化过程的介质[11-13].本文将对硅酸盐水泥在模拟体液中的降解性能及其生物矿化性能进行研究,为其在临床上的使用提供数据.
1 试验材料与方法
1.1 材料
硅酸盐水泥购自华新水泥股份有限公司(P.O 52.5),模拟体液为自制(SBF,初始pH 值为7.4).
1.2 样品准备
根据硅酸盐水泥产品说明书,按粉液质量比为3∶1 进行调拌后,置入铜制模型中,玻璃板压平,制备出10 mm×10 mm×1 mm 的片状样品,在100%湿度下完全固化24 h.
1.3 模拟体液制备
根据文献[14-15]的方法制备模拟体液,其离子浓度与人体血浆各离子浓度相近,见表1.即采用 分 析 纯 级 的NaCl,NaHCO3,KCl,K2HPO4·3H2O,MgCl2·6H2O,CaCl2·2H2O,Na2SO4等溶于去离子水中,在37 ℃,采用1 mol/L 盐酸和三(羟甲基)氨基甲烷调节其pH 值为7.4.
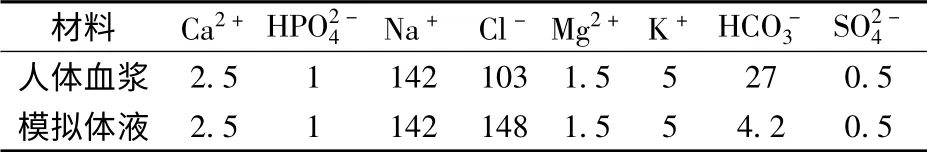
表1 模拟体液和人体血浆的各离子浓度 mmol/L
1.4 体外模拟实验
根据Kamitakahara 等[16]及Bozeman 等[17]方法进行体外模拟实验,即将所制样品(10 mm×10 mm×1 mm)置入37 ℃的模拟体液中,分别浸泡3,7及14 d,每组3 个样品,每个样品浸泡在50 mL 模拟体液中,每周换液2 次.浸泡后的样品从模拟体液中取出,去离子水冲洗,干燥,备用.
1.5 测试
1.5.1 X 射线衍射分析
采用D8-advance 型X 射线衍射仪(XRD,德国Bruker 公司)分析样品表面结构,CuKα 辐射,测试电压为40 kV,管电流为40 mA,扫描速度为5°/min,扫描范围为10°~50°.
1.5.2 红外光谱分析
在样品表面刮取少量材料,按1∶150 与溴化钾混合,充分研磨后压片,使用Nicolet 5700 型傅里叶红外光谱仪(FTIR,美国Nicolet 公司)测试红外光谱,扫描范围为400~4 000 cm-1.
1.5.3 材料表面形貌观察
采用S-3000N 型扫描电子显微镜(SEM,日本Hitachi 公司)观察样品材料表面结构及形貌.
1.5.4 模拟体液浸泡液的pH 值测试
采用PHS-2C 型pH 计(上海雷韵试验仪器制造有限公司)检测将硅酸盐水泥分别浸泡0.02(30 min),1,3,5,7,9,11,13 及14 d 后模拟体液浸泡液的pH 值.
1.5.5 材料的失重率
采用JA-1203 型分析天平(上海金鹏分析仪器有限公司)检测浸泡模拟体液前后样品的质量变化.所有样品在称重前用去离子水冲洗,60 ℃下干燥4 h.硅酸盐水泥材料的失重率按下式计算:
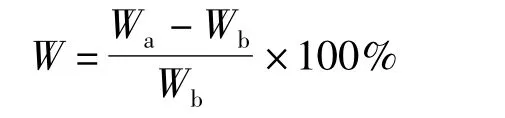
式中,W 为失重率;Wa为浸泡后样品的质量;Wb为未浸泡时样品的质量.
2 结果与讨论
2.1 XRD 表征
图1为硅酸盐水泥浸泡前后的2θ 角(10°~50°)的XRD 谱图.浸泡前的硅酸盐水泥XRD 谱图显示:当2θ=18.1°时,出现氢氧化钙特征峰;当2θ=32.4°时,出现硅酸二钙及硅酸三钙的特征峰;当2θ=34.3°时,出现硅酸二钙及铁铝酸四钙特征峰;在2θ =29.5°,47.1°及48.5°时,出现碳酸钙特征峰,该结果显示硅酸盐水泥除不含X 射线阻射剂氧化铋(2θ =273°及46.3°)的特征峰外,与MTA的XRD 特征峰相一致,这表明2 种材料的主要成分相同[5-6].在硅酸盐水泥浸泡3 d 后,氢氧化钙的特征峰消失,碳酸钙的特征峰增强,说明在碳酸盐水泥表面主要有碳酸钙的形成[18].这是由于硅酸盐水泥材料中的氢氧化钙释出的Ca2+及OH-与模拟体液中的HCO-3发生碳化反应,生成碳酸钙而沉积在材料表面,其反应机理为
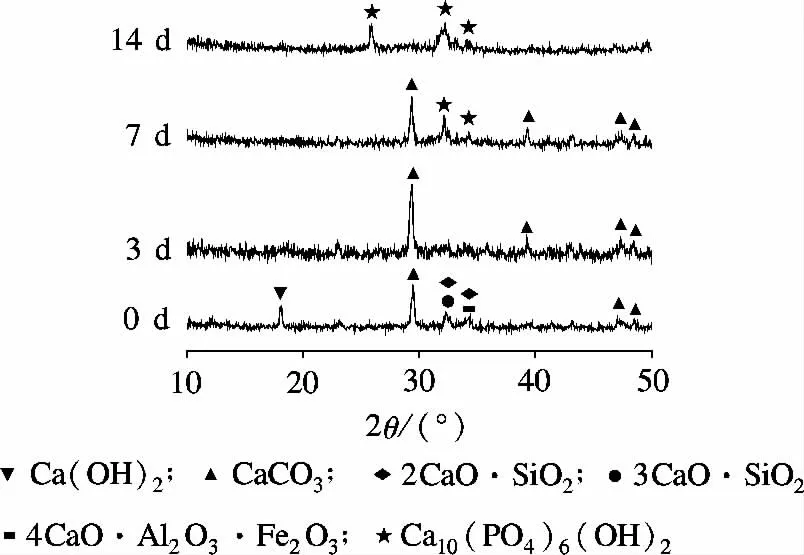
图1 硅酸盐水泥浸泡前后的XRD 表征

硅酸盐水泥浸泡7 d 后,硅酸盐水泥样品材料的XRD 谱图显示,除了出现碳酸钙特征峰外,还出现 羟 基 磷 灰 石 特 征 峰(2θ = 25.9°,32.2° 及34.2°),且随着浸泡时间的延长,碳酸钙特征峰逐渐降低,直至消失,而羟基磷灰石特征峰增强,说明硅酸盐水泥样品在浸泡7 d 后,其表面的碳酸钙含量逐渐减少,而生成羟基磷灰石的量越来越多[11,17-19].这可能是由于碳酸钙与模拟体液中的HPO24-反应生成羟基磷灰石,以及浸泡液内Ca2+,OH-及PO3-4发生反应生成羟基磷灰石所致,其反应机理如下:

2.2 FTIR 表征
硅酸盐水泥浸泡前后的FTIR 谱如图2所示.浸泡前的硅酸盐水泥的FTIR 谱图在波数为3 640 cm-1时出现氢氧化钙的羟基伸缩峰;3 430 cm-1出现结合水及吸收水伸缩峰;1 420 cm-1出现碳酸根吸收峰;1 640,1 150 cm-1出现硫酸根;928,526 cm-1出现无定形硅酸钙等特征峰[20].硅酸盐水泥浸泡3 d 后,氢氧化钙的羟基、无定形硅酸钙及硫酸根等特征峰消失,在1 420,876 cm-1出现强而锐利的碳酸根吸收峰,说明在材料表面有较多的碳酸盐生成;但随着浸泡时间的延长,碳酸根特征峰强度逐渐减弱,说明在材料表面的碳酸盐随着浸泡时间的延长,其含量逐渐降低.硅酸盐水泥浸泡14 d后,除在1 040 cm-1出现强而锐利的P—O 伸缩振动峰,在569,611 cm-1出现了较明显的结晶态的O—P—O 弯曲峰,在1 420,876 cm-1的碳酸根吸收峰明显减弱,这些峰的出现标志着碳酸羟基磷灰石在不断形成[11,18].这一结果与XRD 研究结果相一致,并进一步证实在硅酸盐水泥表面沉积的是碳酸羟基磷灰石.
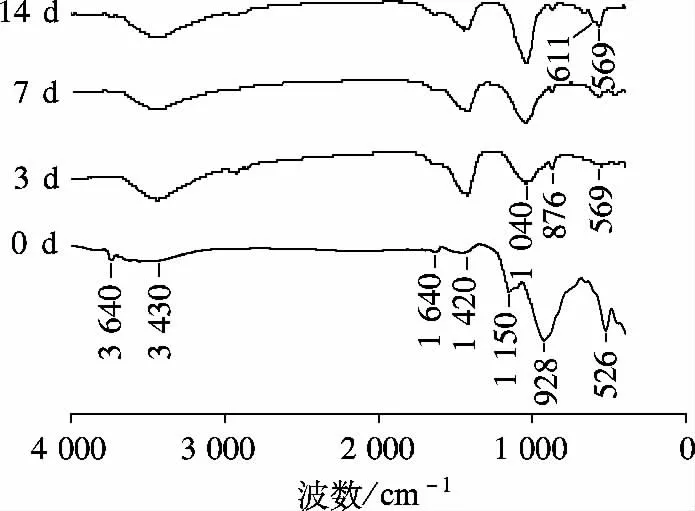
图2 硅酸盐水泥浸泡前后的FTIR 表征
2.3 SEM 表征
图3为硅酸盐水泥浸泡前后的SEM 表征.由图3(a)可见,未浸泡的硅酸盐水泥样品表面呈珊瑚状的方形及针形晶体;样品材料浸泡3 d 后(见图3(b)),其表面部分沉积成簇绒毛状球状颗粒,经XRD 及FTIR 谱图分析这些沉积颗粒为碳酸钙;浸泡7 d 后(见图3(c)),其表面覆盖一层叶状球形颗粒,且随着浸泡时间的延长,叶状球形颗粒逐渐长大增厚(见图3(d)),相关的XRD 及FTIR 谱图分析结果显示这些叶状球形颗粒为碳酸羟基磷灰石.

图3 硅酸盐水泥浸泡前后的SEM 照片
综合硅酸盐水泥浸泡模拟体液前后的XRD,FTIR 及SEM 分析,硅酸盐水泥在模拟体液浸泡后,首先在其表面生成碳酸钙,然后才逐渐生成碳酸羟基磷灰石.Coleman 等[18]研究显示白色硅酸盐水泥在模拟体液中浸泡7 d 后,生成碳酸钙及碳酸羟基磷灰石,但其研究时间仅为7 d,所以并没有能观察到硅酸盐水泥生物矿化的动态过程.Sarkar等[19]及Bozeman 等[17]分别采用磷酸缓冲液(PBS)及合成体液(主要成分与磷酸缓冲液相似)检测MTA 的生物矿化性能,其研究结果显示,MTA 表面仅有磷灰石晶体形成,无碳酸钙的生成,与本研究结果不一致.这主要是由于Sarkar 等[19]采用的磷酸缓冲液(PBS)及合成体液不含HCO-3,MTA 中的氢氧化钙并不能发生碳化作用,生成碳酸钙.然而,在人体的血浆中HCO-3浓度为27.0 mmol/L,要远高于模拟体液中的HCO-3浓度(4.2 mmol/L),因此,当硅酸盐水泥、MTA 等材料植入体内后,其碳化作用可能会更加显著,生成的碳酸钙更多.因此,采用模拟体液研究硅酸盐水泥等材料的生物矿化性能的方案更加接近人体内的情况.
2.4 模拟体液的pH 值测试
由图4可知,硅酸盐水泥的模拟体液浸泡液在0~3 d 时间段,其pH 值迅速升高,在3 d 达到峰值(10.79 ±0.04),呈现较强的碱性,但其pH 值却明显低于其在去离子水中的pH 值(11.97~12.60)[21];且随着浸泡时间的延长,模拟体液的pH 值逐渐下降,浸泡14 d 的模拟体液的浸泡液pH 值为8.42 ±0.08.这主要是由于在去离子水中,硅酸盐水泥释出的Ca2+和OH-使其浸泡液的pH 值迅速升高;但在模拟体液中,不仅有硅酸盐水泥释出的Ca2+和OH-,使其浸泡液pH 值迅速升高;而且其释出的Ca2+,OH-与模拟体液中的HCO3-发生碳化反应,生成的碳酸钙沉积在硅酸盐水泥表面,消耗了浸泡液内大量的Ca2+和OH-,导致其pH 值有所降低;另外,在碱性环境下,CaCO3还可与HPO42-反应生成羟基磷灰石及弱酸H2CO3,使其浸泡液pH 值进一步下降.
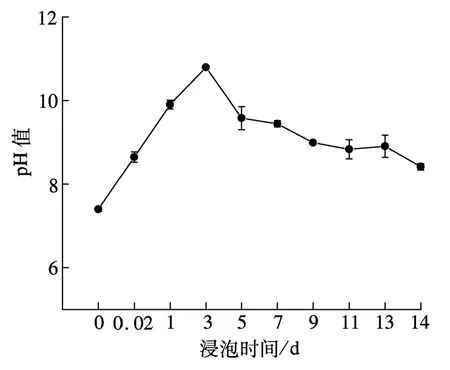
图4 浸有硅酸盐水泥的模拟体液pH 值
2.5 材料的失重率
图5显示,硅酸盐水泥的质量随着其在模拟体液中浸泡时间的延长而增加.当硅酸盐水泥浸入去离子水中,其主要表现为材料的降解作用,即硅酸盐水泥中的Ca2+,OH-释出,使其质量减少,材料的pH 值迅速升高,如Weckwerth 等[22]研究显示,白色硅酸盐水泥在去离子水中的溶解度为0.91%±0.12%.当硅酸盐水泥浸入模拟体液中,不仅有材料的降解作用,而且还存在材料的矿化作用,即模拟体液中的HCO3-,PO34-与硅酸盐水泥中释出的Ca2+,OH-反应,生成碳酸钙及碳酸羟基磷灰石,沉积在样品材料表面,从而导致硅酸盐水泥在模拟体液浸泡后质量增加.Bozeman 等[17]研究显示,MTA 在磷酸缓冲液(PBS)中浸泡后,质量增加,这与本研究结果相一致.由于碳酸钙及碳酸羟基磷灰石沉积于硅酸盐水泥等材料的表面,封闭其表面小的孔隙,以及材料与牙本质之间的间隙,这对提高材料与牙体组织的封闭性能具有非常重要的临床应用价值.

图5 硅酸盐水泥经模拟体液浸泡后的失重率
3 结论
1)随着含有硅酸盐水泥在模拟体液中浸泡时间的延长,模拟体液的pH 值迅速升高后逐渐下降.
2)随着含有硅酸盐水泥在模拟体液中浸泡时间的延长,硅酸盐水泥的质量不断增加.
3)XRD,FTIR 图谱及SEM 图像表明,硅酸盐水泥经模拟体液浸泡后,首先是碳酸钙在其表面形成,其次才是碳酸羟基磷灰石在其表面沉积,因此,硅酸盐水泥具有良好的生物矿化能力.
References)
[1]Lee S J,Monsef M,Torabinejad M.Sealing ability of a mineral trioxide aggregate for repair of lateral root perforations[J].Journal of Endodontics,1993,19(11):541-544.
[2]Parirokh M,Torabinejad M.Mineral trioxide aggregate:a comprehensive literature review—part Ⅲ:clinical applications,drawbacks,and mechanism of action [J].Journal of Endodontics,2010,36(3):400-413.
[3]Torabinejad M,Parirokh M.Mineral trioxide aggregate:a comprehensive literature review—part Ⅱ:leakage and biocompatibility investigations[J].Journal of Endodontics,2010,36(2):190-202.
[4]Parirokh M,Torabinejad M.Mineral trioxide aggregate:a comprehensive literature review—part Ⅰ:chemical,physical,and antibacterial properties [J].Journal of Endodontics,2010,36(1):16-27.
[5]Camilleri J.Characterization of hydration products of mineral trioxide aggregate[J].International Endodontic Journal,2008,41(5):408-417.
[6]Islam I,Chng H K,Yap A U.X-ray diffraction analysis of mineral trioxide aggregate and Portland cement [J].International Endodontic Journal,2006,39(3):220-225.
[7]Hasan Z M,Javidi M,Naderinasab M,et al.Comparative evaluation of antimicrobial activity of three cements:new endodontic cement(NEC),mineral trioxide aggregate(MTA)and Portland[J].Journal of Oral Science,2009,51(3):437-442.
[8]Dreger L A,Felippe W T,Reyes-Carmona J F,et al.Mineral trioxide aggregate and Portland cement promote biomineralization in vivo [J].Journal of Endodontics,2012,38(3):324-329.
[9]Hwang Y C,Kim D H,Hwang I N,et al.Chemical constitution,physical properties,and biocompatibility of experimentally manufactured Portland cement[J].Journal of Endodontics,2011,37(1):58-62.
[10]Shahi S,Yavari H R,Rahimi S,et al.Comparison of the sealing ability of mineral trioxide aggregate and Portland cement used as root-end filling materials [J].Journal of Oral Science,2011,53(4):517-522.
[11]叶心亮,谢宝君,李珍,等.羟基磷灰石/聚乳酸/聚氨酯生物材料的降解性能[J].高分子材料科学与工程,2012,28(5):57-60.
Ye Xinliang,Xie Baojun,Li Zhen,et al.Biodegradation of hydroxyapatite/poly(DL-lactide)/polyurethane biomaterials [J].Polymer Materials Science & Engineering,2012,28(5):57-60.(in Chinese)
[12]Marelli B,Ghezzi C E,Alessandrino A,et al.Silk fibroin derived polypeptide-induced biomineralization of collagen[J].Biomaterials,2012,33(1):102-108.
[13]Wang Q Q,Li W,Yang B C.Regulation on the biocompatibility of bioactive titanium metals by type Ⅰcollagen [J].Journal of Biomedical Materials Research Part A,2011,99(1):125-134.
[14]Kokubo T,Takadama H.How useful is SBF in predicting in vivo bone bioactivity?[J].Biomaterials,2006,27(15):2907-2915.
[15]Kokubo T,Kim H M,Kawashita M.Novel bioactive materials with different mechanical properties[J].Biomaterials,2003,24(13):2161-2175.
[16]Kamitakahara M,Kawashita M,Kokubo T,et al.Effect of polyacrylic acid on the apatite formation of a bioactive ceramic in a simulated body fluid:fundamental examination of the possibility of obtaining bioactive glass-ionomer cements for orthopaedic use[J].Biomaterials,2001,22(23):3191-3196.
[17]Bozeman T B,Lemon R R,Eleazer P D.Elemental analysis of crystal precipitate from gray and white MTA[J].Journal of Endodontics,2005,32(5):425-428.
[18]Coleman N J,Nicholson J W,Awosanya K.Preliminary investigation of the in vitro bioactivity of white Portland cement[J].Cement and Concrete Research,2007,37(11):1518-1523.
[19]Sarkar N K,Caicedo R,Ritwik P,et al.Physicochemical basis of the biologic properties of mineral trioxide aggregate[J].Journal of Endodontics,2005,31(2):97-100.
[20]Gomes C E M,Ferreira O P,Fernandes M R.Influence of vinyl acetate-versatic vinylester copolymer on the microstructural characteristics of cement pastes[J].Material Research,2005,8(1):51-56.
[21]Chen Y Z,Lü X Y,Liu G D.A novel root-end filling material based on hydroxyapatite,tetracalcium phosphate and polyacrylic acid[J].International Endodontic Journal,2013,46(6):556-564.
[22]Weckwerth P H,Machado A C,Kuga M C,et al.Influence of radiopacifying agents on the solubility,pH and antimicrobial activity of portland cement[J].Brazilian Dental Journal,2012,23(5):515-520.
