大豆浸泡动力学研究
2017-07-10刘旭华欲飞陈业明
刘旭 华欲飞 陈业明
摘要 [目的] 探究浸泡条件与大豆之间的关系,寻找适合的浸泡条件,为实际生产提供理论依据。[方法]用Peleg方程,探讨了大豆在不同温度(4~50 ℃)和不同浸泡时间下的吸水动力学性质,并用电泳与质谱的方法对浸泡液中蛋白质的渗出情况进行分析。[结果] 吸水过程可以用数学模型进行较好地拟合,在大豆的吸水模型中,Peleg方程参数k1随温度升高而减小,是浸泡温度的多项函数,说明初始吸水速率与浸泡温度有关。大豆在各个温度浸泡过程中,均有蛋白质释放出,其中分子量为37 kD的蛋白质在50 ℃浸泡时大量释放出,经质谱鉴定后为碱性7S球蛋白,是一种细胞壁蛋白,其大量释放出,说明细胞壁被破坏,故50 ℃浸泡吸水速率明显加快。[结论] Peleg方程可以较好地描述大豆浸泡过程吸水性质,浸泡过程中细胞壁蛋白碱性7S球蛋白大量渗出,细胞壁结构被破坏。
关键词 大豆;吸水;Peleg方程;浸泡液;蛋白质
中图分类号 TS214.2 文献标识码 A 文章编号 0517-6611(2017)18-0077-04
Abstract [Objective] To explore the relationship between soaking conditions and soybean, find suitable soaking conditions and provide theoretical basis for actual production. [Method] Pelegs equation was used to describe the kinetics of water absorption of soybean during soaking at 4 ℃ to 50 ℃ for different duration. The protein exudation in the soaking solution was analyzed by electrophoresis and mass spectrometry. [Result] The result showed high fitting of kinetics to Pelegs equation for predicting the hydration characteristics. This study found that the value of k1 (rate) depended on temperature according to a polynomial function, meaning that the value of the initial rate of hydration was dependent on soaking temperature. Soybean seeds released several proteins during soaking. It was found that the 37 kD protein was identified as the most abundant protein, especially at 50 ℃basic 7S globulin (Bg 7S), which is the cell wall protein. These meant that the structure of cell wall was destroyed to some extent, which could explain why the release rate was quick at 50 ℃. [Conclusion] Peleg equation can describe the water absorption properties of soybean during soaking process well, 7S globulin exude abundantly and the structure of cell wall is destroyed.
Key words Soybean;Water absorption;Pelegs equation;Soaking solution;Protein
大豆浸泡是豆制品加工的重要步骤,在传统豆制品加工中浸泡的主要目的是軟化大豆,便于研磨[1]。大豆浸泡过程对水分的吸收程度直接影响大豆的质构和其在加工过程中的研磨特性。Pan等[2]研究发现,大豆的研磨特性只和大豆最后的吸水率有关,与浸泡条件没有关系;高温浸泡可以显著缩短浸泡时间,但是当浸泡温度由30 ℃上升到40 ℃时,浸泡液中固形物损失严重。通过测量不同浸泡时间种子质量的增加来计算干豆的总吸水率,是评估干豆加工特性的常用方法,并以此为基础,拟合出大豆吸水方程和参数[3]。Joshi 等[4]研究了浸泡过程中,扁豆的硬度与吸水率和浸泡温度有关,与种子大小和种子质量无关。Peleg方程能较高地对吸水过程进行拟合[5],且可以通过阿累尼乌斯方程和经验公式来拟合动力学参数与温度的关系[6]。
大豆在浸泡吸水的同时,大豆中的物质也在向外扩散,Kon[7]研究了不同浸泡温度(20~90 ℃)下,當大豆达到最大吸水率时总固形物、含N物质、总糖、低聚糖、Ca、Mg和3种水溶性维生素(硫胺素、核黄素和烟酸)的损失情况,结果表明,当浸泡温度小于50 ℃时,损失较少,但当浸泡温度高于60 ℃时,损失是低温时的3~4倍。在国内研究中,多研究不同浸泡条件所得豆浆的性质,间接浸泡过程[8-11],对浸泡过程中的变化研究较少。大豆中的营养物质主要是蛋白质,研究蛋白质的浸出情况对于浸泡过程的研究有重要意义。
笔者主要探索大豆在浸泡过程中吸水动力学以及蛋白质浸出动力学,为实际生产提供理论依据。
1 材料与方法
1.1 材料
1.1.1 原料与主要试剂。
大豆,市购。甘氨酸、乙二胺四乙酸二钠(EDTA-2Na)、考马斯亮蓝G-250、甘油、过硫酸铵、乙酸铵均为分析纯;三羟甲基氨基甲烷(Tris)为生化试剂;丙烯酰胺、N,N,-甲叉双丙烯酰胺、四甲基乙二胺(TEMED),购于Sigma-Aldrich;精确分子量双色预染蛋白标准品,购于Bio-Rad。
1.1.2 主要仪器设备。
HH-S数显恒温水浴锅,江苏金坛市医疗仪器厂;DYY-8C型垂直电泳仪,北京六一仪器厂;GelDoc-ItTS 凝胶成像仪,美国UVP公司;豆浆机,九阳股份有限公司。
1.2 方法
1.2.1 浸泡方法。
大豆→脱皮→挑选→豆液比1∶5浸泡。浸泡温度4 ℃下,浸泡6、12、15、18、21、24 h;25 ℃下,浸泡2、6、10、12、14、16 h;50 ℃下,浸泡1、2、3、4、5 h。
1.2.2 大豆吸水率的测定。
20 g大豆,去离子水洗2次,滤纸吸干残余水分,浸泡于100 g浸泡液中,取出不同浸泡温度和浸泡时间的大豆,将大豆捞出,滤纸擦干,称重,按公式(1)计算大豆吸水率。
大豆吸水率=Wt-W0W0×100%(1)
式中,Wt为浸泡t时间后大豆质量(g);
W0为浸泡前大豆质量(g)。
1.2.3 浸泡液SDS-PAGE分析。
样品制备:取不同浸泡条件所得浸泡液2 mL于离心管中,冷冻干燥后加入0.2 mL去离子水溶解,然后加入0.2 mL SDS-PAGE样品溶解液混匀,上样10 μL。
操作步骤主要参考Laemmli[12]的方法并略加修改。
选取浓缩胶浓度为5.0%,分离胶浓度为12.5%。
电泳电极缓冲液:1.44 %(W/V)甘氨酸,0.025 mol/L Tris-HCl和0.1%(W/V)SDS。试验时取上述溶液75 mL,加入200 mL去离子水混合均匀。
样品溶解液:50%(W/V)甘油,0.05 mol/L Tris-HCl,4%(W/V))SDS和1 %溴酚蓝。
固定液:33%(W/V)无水乙醇和12%(W/V)三氯乙酸(TCA)。染色液:0.2%(W/V)考马斯亮蓝G-250,5.3%(V/V)浓硫酸,9.35%(W/V)KOH,12% TCA。脱色液:10%(V/V)乙酸。
电泳电流15 mA,电泳结束后,立即固定凝胶,时间为2 h,然后倒出固定液,换上染色液染色过夜,最后脱色至背景透明,即可拍照,Bio-Rad Image Lab软件分析。
1.2.4 质谱分析。
质谱分析用于鉴定SDS-PAGE凝胶的未知条带,参考闫尊浩[13]的方法并略作修改,具体方法如下:
①用手术刀切下SDS-PAGE凝胶上的目标条带,置于EP管中;②用300 μL NH4HCO3(100 mmol/L)和30%的乙腈(ACN)脱色2 h;③每个管加入90 μL NH4HCO3(100 mmol/L),10 μL现配的DTT(100 mmol/L),56 ℃下孵化30 min;④除去上清,加入100 μL 100% ACN,5 min后吸出;⑤每管加入70 μL NH4HCO3(100 mmol/L)和30 μL IAA(200 mmol/L),避光放置20 min;⑥去除上清,每管加入100 μL NH4HCO3(100 mmol/L),室温下放置15 min;⑦去除上清,加入100 μL 100% ACN,5 min之后吸出,重复2次;⑧酶管中加入5 μL Trypsin溶液(10 μg/μL),4 ℃保温30~60 min;⑨吸出多余酶液,再加25 μL NH4HCO3(25 mmol/L)覆盖胶粒;⑩将酶管倒置,pH 7.8~8.0,37 ℃下反应20 h;B11吸取酶液,转移至新的EP管中,原管中加入60 μL 60% ACN,一并倒入新的EP管中;B12新的EP管中加入20 μL双蒸水,离心浓缩成干粉;B13干粉中加入3 μL 0.1% TFA溶解;B14点靶。整个过程要避免角蛋白污染。
1.2.5 Peleg 数学模型理论基础。
吸水过程可以用Peleg数学模型进行较好地拟合[2,14-15]。Peleg数学模型为两参数、非指数的经验型方程,其主要形式如方程(2)所示,将方程(2)经过一定的转换即得到方程(3):
2 结果与分析
2.1 大豆吸水动力学
2.1.1 大豆吸水过程分析。
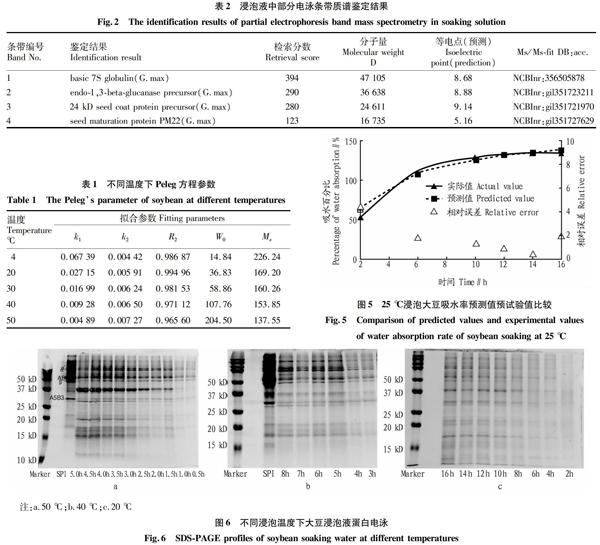
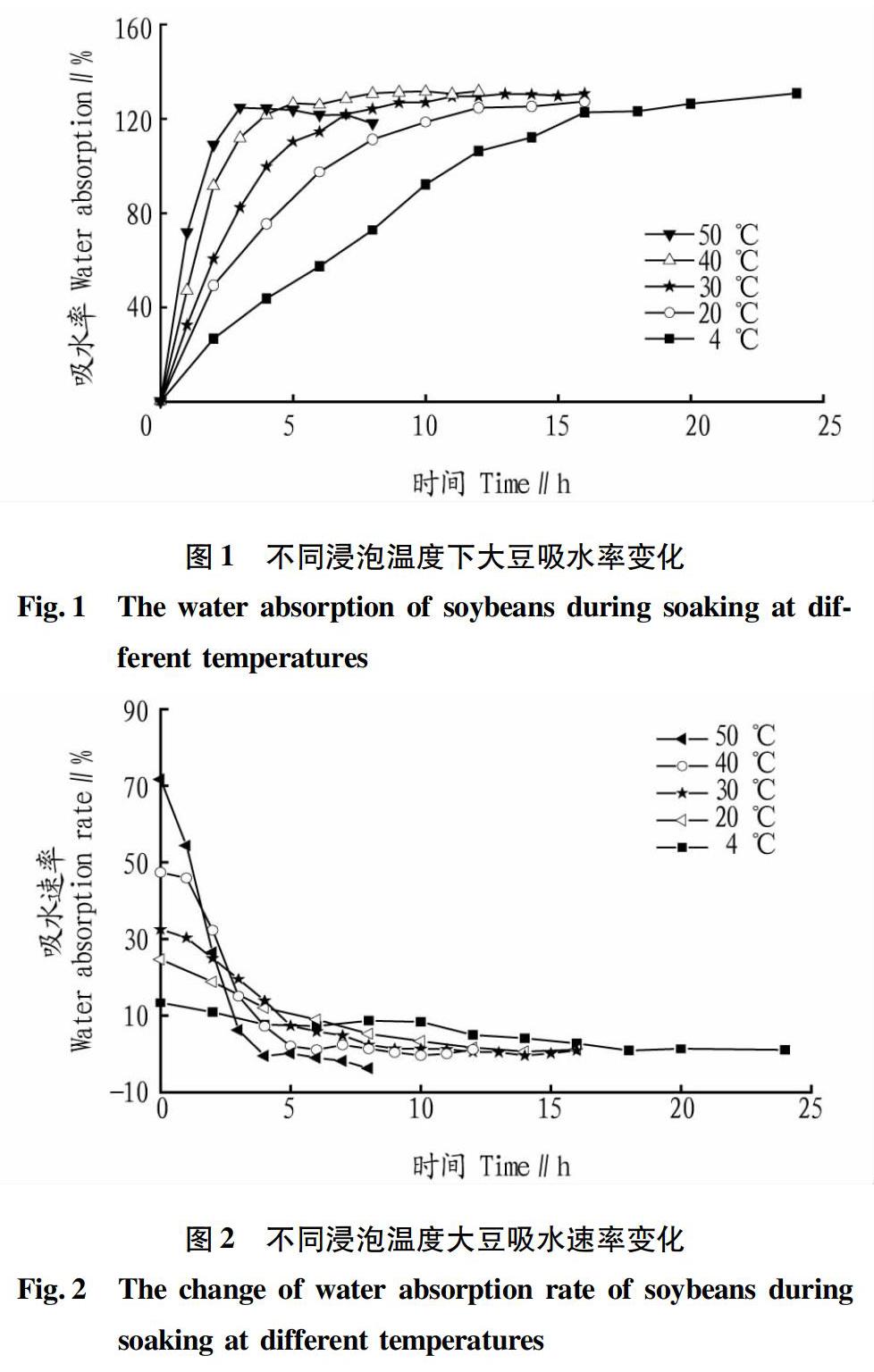
图1展示了不同浸泡温度下大豆吸水率随时间的变化,图2是不同浸泡温度下大豆吸水速率随浸泡时间的变化。由图1、2看出大豆浸泡过程经历3个阶段:第1个阶段,快速吸水,吸水率直線上升,吸水速率最大;而后吸水率缓慢上升,吸水速率减小;最后吸水率曲线趋于平缓,吸水速率接近于0甚至为负值,最终吸水达到饱和。
大豆的浸泡过程是自身的吸水膨胀过程,大豆的吸水速率取决于驱动力(饱和时刻与某一时刻的水分含量差);随着吸水过程进行,大豆水分含量越来越高,降低了驱动力,因而吸水速率下降,当达到饱和水分含量时,吸水过程终止[16],所以理论上不同温度的最大吸水率应该是大约相等的。随着浸泡温度的升高,最大吸水率减小,当浸泡温度为50 ℃时,浸泡3 h后,吸水率降低甚至出现负值,这可能是由于浸泡温度较高,当达到平衡含水量时,大豆水分含量基本不变,但固形物等其他物质仍在释放,导致吸水率降低。
由图1和图2还可以看出,大豆吸水速率受温度的影响明显。50、40、30、20、4 ℃达到100%吸水率分别需要1.5、2.5、4.0、6.0和11.0 h。以连续3个数据相对标准偏差RSD<1.2%作为吸水平衡点,即为最大吸水率点。50、40、30、20、4 ℃达到最大吸水率分别需要3、5、9、12和24 h。可見,浸泡温度越高,豆子吸水速率越快,达到饱和吸水率的时间越短。温度较高时,水分子运动较为剧烈,水分子进入细胞的速度较快。此外,大豆细胞壁是水分子进入细胞的第一道阻碍,细胞壁主要是由纤维素、半纤维素和果胶组成,纤维素会通过分子间氢键相互作用,形成非常稳定的多聚体,同时半纤维素、果胶和木质素也会通过氢键镶嵌在纤维素多聚体中,形成不溶性的微纤维[17],其结构类似于“钢筋混凝土”。当采用较高的温度浸泡时,果胶成分会部分溶解到温水中,“钢筋混凝土”结构被破坏,因此水分更易进入细胞。
2.1.2 Peleg数学模型分析。
使用OriginPro 8.0对所得数据进行拟合,得到方程相关参数如表1所示。
2.1.3 Peleg数学模型评价。
根据拟合方程,可以计算不同温度下的数据,以用来描述浸泡过程中大豆的水分含量与温度和时间的关系,并通过方程求出相应温度和时间下的近似含水量,同时可以大致预测不同浸泡温度下达到相应吸水率所需要的时间。
选取25 ℃对Peleg拟合方程进行检验,结果如图5所示,拟合方程能较好地预测大豆吸水过程,吸水率变化曲线与试验值相差不大。
2.2 浸泡过程中蛋白质浸出动力学
2.2.1 浸泡液SDS-PAGE分析。
为了研究浸泡条件对大豆蛋白质浸出成分的影响,更直观地了解蛋白的溶出量及溶出的蛋白种类,对去离子水浸泡后的浸泡液浓缩后进行电泳分析,结果如图6所示。
由电泳图可知,随着浸泡时间的增加,蛋白含量呈增加趋势,50 ℃浸泡有一个分子量为37 kD的蛋白条带,含量明显大于其他2个温度,且随着时间的增加,含量显著增加;40 ℃浸泡出现了先增加后趋于不变的现象,而且相较于50 ℃,浸泡5 h后的蛋白溶出量较少;20 ℃时,蛋白溶出量比50、40 ℃浸泡条件下的都要少。
2.2.2 浸泡液成分质谱鉴定。
通过与SPI条带对比,可以确定浸泡液中大部分重要蛋白质种类,对不能确定的重要电泳条带进行质谱鉴定,分别为50 ℃浸泡电泳图上的1、2、3、4号电泳条带,结果如表2所示。
24 kD seed coat protein(SC24)是一种新的有羧酸盐结合活性的植物防御蛋白[19]。浸泡温度为50 ℃时,分子量为37 kD的蛋白质大量释放,经质谱鉴定为碱性7S球蛋白(Bg7S)。Bg7S是一种富含Cys(半胱氨酸)的糖蛋白,在57.5~62.5 ℃,豆类种子能迅速释放Bg类蛋白(碱性球蛋白)[20]。在温度为40 ℃及以下时,通过电泳图可以看出,其释放较少,这与Palavalli等[21]报道的结果相一致。Bg7S可溶于高离子强度的盐溶液中,在50~60 ℃热水浸泡液中会大量浸出[22-23]。Bg7S是一种细胞壁蛋白,Bg7S被大量浸出,说明细胞壁结构被破坏,水分更容易通过细胞壁进入到细胞中,大豆吸水速率加快,这和之前推测50 ℃吸水速率加快的原因一致。
3 结论
Peleg方程能较好地描述大豆浸泡过程吸水性质。在大豆的吸水模型中,Peleg方程参数k1随温度升高而减小,是浸泡温度的多项函数,说明初始吸水速率与浸泡温度有关。大豆在各个温度浸泡过程中,均有大量蛋白质渗出,其中分子量为37 kD的蛋白质在50 ℃浸泡时大量浸出,经质谱鉴定后为碱性7S球蛋白,是细胞壁蛋白,其大量浸出,说明细胞壁被破坏,故50 ℃浸泡吸水速率明显加快。
参考文献
[1] DE LIMA F S,KUROZAWA L E,IDA E I.The effects of soybean soaking on grain properties and isoflavones loss[J].LWTFood Science and Technology,2014,59(2):1274-1282.
[2] PAN Z L,TANGRATANAVALEE W.Characteristics of soybeans as affected by soaking conditions[J].LWTFood Science and Technology,2003,36(1):143-151.
[3] WOOD J A,HARDEN S.A method to estimate the hydration and swelling properties of chickpeas(Cicer arietinum L.)[J].Journal of food science,2006,71(4):190-195.
[4] JOSHI M,ADHIKARI B,PANOZZO J,et al.Water uptake and its impact on the texture of lentils(Lens culinaris)[J].Journal of food engineering,2010,100(1):61-69.
[5] 徐杰,張晖,郭晓娜,等.糙米和发芽糙米吸水动力学研究[J].食品工业科技,2011,32(7):150-153.
[6] WARDHANI D H,VZQUEZ J A,PANDIELLA S S.Kinetics of daidzin and genistin transformations and water absorption during soybean soaking at different temperatures[J].Food chemistry,2008,111(1):13-19.
[7] KON S.Effect of soaking temperature on cooking and nutritional quality of beans[J].Journal of food science,1979,44(5):1329-1335.
[8] 李里特,曹薇.大豆浸泡溫度对豆腐加工的影响[J].食品科学,1998,19(6):29-32.
[9] 杨道强,邢建荣,陆胜民.大豆不同前处理方式对豆浆品质的影响[J].食品科学,2016,37(1):69-73.
[10] 孙明玉,张仲欣,王铂涵,等.大豆浸泡时间对豆浆品质的影响[J].农产品加工·学刊,2013(11):42-43.
[11] 趙秋艳,乔明武,宋莲军,等.大豆浸泡温度对腐竹产率及品质的影响[J].湖南农业科学,2011(21):87-89,90.
[12] LAEMMLI U K.Cleavage of structural proteins during the assembly of the head of bacteriophage T4[J].Nature,1970,227(5259):680-685.
[13] 闫尊浩.豆浆制作过程中油体变化规律及其对豆腐性质的影响研究[D].无锡:江南大学,2016.
[14] HUNG T V,LIU L H,BLACK R G,et al.Water absorption in chickpea(C.arietinum)and field pea(P.sativum)cultivars using the peleg model[J].Journal of food science,1993,58(4):848-852.
[15] YILDIRIM A,NER M D,BAYRAM M.Modeling of water absorption of ultrasound applied chickpeas(Cicer arietinum L.)using Pelegs equation[J].Tarim bilimleri dergisi,2010,16(4):278-286.
[16] RESIO A N C,AGUERRE R J,SUAREZ C.Analysis of simultaneous water absorption and waterstarch reaction during soaking of amaranth grain[J].Journal of food engineering,2005,68(2):265-270.
[17] OUHIDA I,PREZ J F,GASA J.Soybean(Glycine max)cell wall composition and availability to feed enzymes[J].Journal of agricultural and food chemistry,2002,50(7):1933-1938.
[18] JIDEANI V A,MPOTOKWANA S M.Modeling of water absorption of Botswana bambara varieties using Pelegs equation[J].Journal of food engineering,2009,92(2):182-188.
[19] DHAUBHADEL S,KUFLU K,ROMERO M C,et al.A soybean seed protein with carboxylatebinding activity[J].Journal of experimental botany,2005,56(419):2335-2344.
[20] 頓新鹏,陈正望.碱性7S球蛋白和豆类胰岛素研究进展[J].植物学报,2005,22(S1):68-74.
[21] PALAVALLI M H,NATARAJAN S S,WANG T T Y,et al.Imbibition of soybean seeds in warm water results in the release of copious amounts of BowmanBirk protease inhibitor,a putative anticarcinogenic agent[J].Journal of agricultural and food chemistry,2012,60(12):3135-3143.
[22] HIRANO H,KAGAWA H,OKUBO K.Characterization of proteins released from legume seeds in hot water[J].Hytochemistry,1992,31(3):731-735.
[23] KAGAWA H,HIRANO H,TOMOTAKE M,et al.A seed protein induced by heattreatment in soybean(Glycine max(L.))[J].Food chemistry,1993,48(2):159-163.
