2013年欧洲卒中组织关于颅内动脉瘤及蛛网膜下腔出血的管理指南(第二部分)
2014-03-07姜睿璇张娟边立衡
姜睿璇,张娟,边立衡
(接上期)
2.5.2 预防再出血的特异性治疗 治疗基本原则——及时处理动脉瘤
高达15%的患者在初次出血后的几小时内会再出血,即出血发生在运送患者途中或治疗小组处理颅内动脉瘤之前。首次SAH后第一天存活的患者,再出血累积风险为35%~40%,死亡率约40%。4周后再出血的风险下降至每年3%。
治疗动脉瘤性SAH的主要目的是处理已破裂的责任动脉瘤,即去除出血源防止再出血。目前有两种主要的治疗方法:神经外科开颅夹闭动脉瘤和血管内弹簧圈栓塞动脉瘤。一篇Meta分析收集了268项相关研究中的11项研究,纳入1814例SAH患者,比较早期和晚期采用外科夹闭术治疗破裂动脉瘤的差异,结果显示对于入院时临床情况/神经系统功能较好(WFNS Ⅰ~Ⅲ级)的患者,早期治疗(SAH后72 h内)较晚期治疗,患者预后更好。在WFNS分级更差(评分4~5)的患者中尽管差异无显著性,但也可发现类似的趋势。即使更早期治疗(SAH后12 h内)WFNS分级Ⅳ和Ⅴ的患者,也不会增加幸存者不能自理的比例。尽管没有明确的循证医学证据,专家共识一直以来认为应该对临床分级较好的(WFNS Ⅰ~Ⅳ;Hunt和Hess分级Ⅰ~Ⅳ)动脉瘤性SAH患者早期(<72 h)处理动脉瘤。对于同时存在多个颅内动脉瘤的患者,如有一个破裂动脉瘤引起SAH,同时发现其他几个非破裂动脉瘤,需优先处理破裂动脉瘤。关于如何治疗偶然发现的未破裂颅内动脉瘤,取决于SAH后的病程变化、预后、患者年龄以及动脉瘤大小、位置和形态。
动脉瘤处理时机的推荐
应在理论和技术允许的情况下,尽快处理动脉瘤以预防再出血;如果条件允许,应该在出现症状后的72 h内进行处理。
临床分级和评分不应该影响动脉瘤的处理方案(Ⅲ类证据,C级推荐)。
已破裂动脉瘤的外科夹闭术和血管内栓塞治疗
在早期的颅内动脉瘤治疗中,外科手术是唯一的方法。开始先从近端结扎血管(中断血流)如颈动脉,然后利用肌肉组织包裹动脉瘤以加强动脉瘤壁防止其再出血,如今外科治疗动脉瘤主要基于夹闭动脉瘤(夹闭)。虽然中断血流和包裹技术单独作为治疗方法有些过时,但这两种技术可联合其他外科技术如动脉瘤夹闭和(或)搭桥处理动脉瘤。自从动脉瘤夹问世后,再出血风险显著降低。显微手术的发明使手术入路变得更小,创伤也更少。此外,术中吲哚菁绿血管造影和多普勒超声检查有助于提供额外的术中质量控制。自1990年G. Guglielmi发明了铂线圈,动脉瘤填塞术作为一种替代外科夹闭术的治疗方法迅速发展。
动脉瘤夹闭术与动脉瘤栓塞术的比较
比较动脉瘤夹闭术和栓塞术两种治疗方法,需要考虑发病率、死亡率、动脉瘤完全闭塞率、闭塞持久性、再出血(术中和术后动脉瘤破裂)及其他一些因素。国际动脉瘤性蛛网膜下腔出血试验(International Subarachnoid Aneurysm Trial,ISAT)是一项比较血管内弹簧圈栓塞和外科夹闭术两种治疗方法的随机对照试验(没有使用球囊扩张或支架技术)。ISAT遵循了“不确定原则”,主要入选标准为外科手术夹闭术和血管内弹簧圈栓塞术同等适用颅内动脉瘤且均可采用两种方法治疗(“临床均势”)。在研究中心接受治疗的RIA患者中,有22.4%(9559例患者中的2143例)符合这项标准。剩余77.6%的颅内动脉瘤患者有的更适合夹闭术或填塞术,这些患者没有被随机化,故被排除。除了患者人群的高度选择性,ISAT的患者中90%临床分级较好(Hunt和Hess分级Ⅰ~Ⅱ),这种现象同样受到质疑,由于大脑中动脉动脉瘤相对其他部位的动脉瘤更难进行血管内弹簧圈栓塞治疗,故这个部位的动脉瘤较少,患者的代表性较差。但是,对这组破裂动脉瘤的亚组人群,接受栓塞术和夹闭术的概率相等,ISAT结果表明血管内栓塞术优于外科夹闭术,临床结局更好:1年后栓塞术较夹闭术的死亡和严重残疾绝对危险度降低率为6.9%,1年后23.7%的血管内弹簧圈栓塞治疗的患者严重残疾或死亡较夹闭术患者低(30.6%)。ISAT经过9年的随访发现,栓塞术患者5年的相对死亡率降低。SAH后夹闭术和栓塞术后生活自理的幸存者的数量差异无显著性(82% vs 83%)。早期及ISAT随访分析显示,血管内弹簧圈栓塞治疗患者的再出血风险更高,相当于新动脉瘤发生SAH的概率。术后再出血的风险似乎与栓塞不全的程度相关。另一项随访研究观察和比较ISAT中患者动脉瘤复发的风险和预后。17.4%经血管内治疗的患者和3.8%经夹闭术治疗的患者再次接受了动脉瘤治疗。血管内栓塞术后二次治疗的概率是夹闭术的6.9倍。血管内栓塞术后需要二次治疗的危险因素包括发病年龄较轻、动脉瘤腔大和不完全栓塞。一项事后分析研究将ISAT研究中患者的死亡率作为唯一的结局参数,认为40岁以下的患者,当不能确定血管内栓塞术优于夹闭术时,从预期寿命的角度,夹闭术可能是更好的治疗选择。
由于ISAT研究对动脉瘤患者亚组人群的高度选择性,其结果不能广泛推广。最近对过去几年逐渐增多的血管内治疗的研究,未发现夹闭术和栓塞术在死亡率和发病率方面差异存在显著性。
治疗后颅内动脉瘤再破裂(Cerebra l Aneurysm Rerupture after Treatment,CARAT)研究是一项非随机化的研究。该研究在1996-1998年入组了1010例SAH患者,随访至2005年。其中299例进行了动脉瘤栓塞术,711例进行了夹闭术。经过平均4年的观察发现,动脉瘤再破裂的风险与动脉瘤栓塞的程度明显相关。血管内弹簧圈栓塞术较夹闭术总体再破裂风险更高一些,但校正后差异消失。行颅内动脉瘤治疗的患者术中再破裂出血很常见。在CARAT研究中,栓塞术术中再破裂发生率为5%,夹闭术为19%。血管内弹簧圈栓塞术中再破裂相关的死亡率/致残率是夹闭术的2倍(栓塞术63% vs 夹闭术31%)。
两项近期刚完成病例收集的研究结果让我们期待:一项为水凝胶弹簧圈血管内动脉瘤栓塞和填充研究(HydroCoil Endovascular Aneurysm Occlusion and Packing Study,HELPS),该研究比较了水凝胶涂层线圈和普通铂线圈,而另一项为Cerecyte Coil研究,比较了聚合物涂层线圈和普通铂线圈。
总结目前的研究结果显示,动脉瘤破裂的损伤是复杂的。治疗的首要目的是尽可能完全闭塞动脉瘤,以减少术后再破裂和出血风险。对于不需要球囊扩张或支架植入,又均可采用栓塞术或夹闭术治疗的动脉瘤(临床均势),应该优先考虑栓塞术。具体的指征和治疗方案应经过多学科的共同讨论制订。对于存在颅内血肿占位效应的病例,优先考虑外科治疗和夹闭术。
一般认为,宽颈动脉瘤、动脉瘤体发出分支血管、大脑中动脉动脉瘤或动脉瘤同时合并血肿的患者应该优先考虑夹闭术,而基底动脉瘤或老年患者(>70岁,窄颈,后循环)应该优先考虑血管内弹簧圈栓塞术(B级推荐)。患者具体的治疗方案应该经过多学科讨论,不仅基于手术医师和介入科医师的经验和治疗效果,同时还应考虑个体化因素如年龄、一般健康情况、动脉瘤部位、形态和大小,以及患者的个人意愿。颅内动脉瘤治疗应在能高质量完成两种术式的医疗中心完成。
预防再出血的推荐
外科手术医师和介入科医师应进行跨学科讨论,以制订最佳的治疗方案。
基于讨论结果,患者应该被告知并在条件允许时参与决策制订。
对于适合血管内弹簧圈栓塞术和开颅夹闭术的动脉瘤,应该优先考虑栓塞术(Ⅰ类证据,A级推荐)。
一般情况下,选择栓塞术还是夹闭术取决于多种因素,大致分为3类:
(1)患者因素:年龄、合并症、是否合并ICH、SAH分级、动脉瘤的大小、部位和形态,侧支循环情况(Ⅲ类证据,B级推荐)。
(2)手术因素:资质、技术水平和可行性(Ⅲ类证据,B级推荐)。
(3)后勤保障:多学科合作的等级(Ⅲ类证据,B级推荐)。
对于动脉瘤性SAH患者:优先选择手术治疗(夹闭术)的因素为:年龄较轻,合并有占位效应的ICH(Ⅱ类证据,B级推荐),以及动脉瘤相关因素,如部位:大脑中动脉和胼周动脉瘤(Ⅲ类证据,B级推荐);瘤径宽(Ⅲ类证据,B级推荐);动脉瘤体直接发出血管分支(Ⅲ类证据,B级推荐);血管和动脉瘤形态不适于血管内弹簧圈栓塞治疗(Ⅳ类证据,C级推荐)。
优先选择血管内介入治疗(栓塞术)的因素包括:年龄>70岁(Ⅱ类证据,B级推荐),不存在有占位效应的ICH(Ⅱ类证据,B级推荐),以及动脉瘤相关的因素,如动脉瘤位于后循环、瘤径窄、动脉瘤不分叶(Ⅱ类证据,B级推荐)。
高龄理论上不应该做为排除条件;是否治疗应结合患者的临床情况决定。
抗纤溶治疗
抗纤溶药物 一篇包括9项随机对照试验的Cochrane系统综述分析了SAH患者使用抗纤溶药物的研究提示:抗纤溶治疗可以减少再出血,但是不能减少各种原因引起的死亡和不良预后。在上一版指南发表后,一项来自瑞典的研究入选SAH患者,他们在社区医院诊断为SAH后,在患者转运前开始接受氨甲环酸治疗,直至动脉瘤闭塞治疗后(通常在72 h内)。研究结果显示,尽管再出血风险显著降低,使用氨甲环酸的患者总体结局同样没有任何改善。将这项研究结果与Cochrane综述的9项研究综合分析,结果仍显示抗纤溶治疗对总体预后没有影响。抗纤溶治疗在临床推广应用之前,尚需要进一步关于超早期和短期使用氨甲环酸的相关研究。
重组凝血因子Ⅶa理论上重组凝血因子Ⅶa可以预防再出血。一项开放式标签剂量增加安全性研究因为入组的第10例患者出现责任动脉瘤对侧大脑中动脉分支阻塞而被中止。在一项非对照研究中,18例患者在破裂动脉瘤栓塞术中接受重组凝血因子Ⅶa治疗,均未发生再出血,但1例出现深静脉血栓,7例出现与外周中心静脉置管相关的上肢静脉血栓。目前,没有证据支持SAH患者在临床试验需要外使用重组凝血因子Ⅶa。
说明
目前没有药物可以通过减少再出血而改善预后(Ⅰ类证据,A级推荐)
一些关于止血剂应用的小样本量规模的临床试验的结果提示,需要进一步研究指导治疗方案的修改(Ⅱ类证据,C级推荐)。
2.5.3 脑积水 脑积水定义为CT上测量双侧尾状核指数超过正常年龄组的95%,SAH急性期约20%的患者发生脑积水,恢复期约10%。急性脑积水可能是由于中脑周围池积血较多或脑室内出血堵塞了CSF回流。其中大约1/3的脑积水患者无症状,一半患者在脑积水初期就出现意识障碍,可在24 h内自行缓解。
急性脑积水患者可能在SAH后立即出现神经功能恶化,CT可见脑室扩大。这种急性脑积水相较SAH,与脑室出血量更相关。
因为半数脑积水患者可以自行改善,且脑室引流存在再出血和感染的风险,故一些神经外科医师不推荐立即进行脑室引流。对不存在其他可以解释意识水平降低(如大体积ICH)的患者,推荐立即进行脑室外引流(保持颅内压在10~20 mmHg)(Ⅳ级证据)。另一方面,脑室造瘘术增加再出血和脑膜炎/脑室炎的风险。
自发性脑出血患者当第三、四脑室无积血,即存在交通性脑积水,有建议对此类患者行分流术前使用腰大池引流作为持续脑室外引流的治疗方法。这种方法可被当作一个替代疗法来减少永久分流术的概率,但需要注意防止幕上脑组织向下形成疝和积液的可能。无论对自发性脑出血患者还是SAH患者,目前还没有前瞻性临床试验证明这种方法的有效性。
脑积水管理的推荐
对于CT证实存在脑积水且第三、四脑室积血的患者,应行脑室外引流;引流可以降低和监测颅内压以及清除积血;对于清除积血作用的证据水平较低(GCP)。
对于未使用镇静药物,考虑由于脑积水引起意识水平下降的患者,其第三、四脑室无积血且可以预防脑疝时,可以考虑行腰椎穿刺引流(Ⅳ类证据,C级推荐)。
对于镇静的患者,CT证实存在脑积水,且第三、四脑室没有积血,应考虑行腰椎穿刺引流(Ⅳ类证据,C级推荐)。
症状性的慢性脑积水患者需要行脑室-腹腔分流术或脑室-心房分流术(GCP)。
2.5.4 迟发性脑缺血(delayed cerebral ischaemia,DCI)的预防
药物预防/治疗
一篇Cochrane综述总结了16项临床研究,包括3361例SAH患者,发现接受钙离子拮抗剂治疗患者死亡或依赖的相对风险为0.81(95%CI 0.72~0.92);相应需要治疗患者的数量为19(95%CI 1~51)。单独口服尼莫地平其RR为0.67(95%CI 0.55~0.81);使用其他钙离子拮抗剂和静脉使用尼莫地平,结果显示差异均无显著性。钙离子拮抗剂减少了继发性脑缺血的发生,且有降低病死率的趋势。尽管统计学上显示明显减少不良预后,但该数据主要基于一项大规模临床试验,因此对尼莫地平可使患者获益的结论并非完全没有质疑。对于动脉瘤性SAH患者,临床建议动脉瘤性SAH患者使用的标准治疗是尼莫地平临床试验的方案(口服60 mg每4小时1次,持续3周)。如果患者吞咽困难,应该使用生理盐水将碾碎的尼莫地平经胃管在几分钟内喂入。制药商建议使用静脉输注,但该方法更昂贵,且没有证据支持这种方法。此外,静脉输注尼卡地平不能改善预后。
手术夹闭动脉瘤后也可以在蛛网膜下腔中应用钙离子拮抗剂,但目前没能证实这种方法可使患者获益。
尼莫地平预防DCI的推荐
应口服尼莫地平(60 mg/4 h)以预防DCI(Ⅰ类推荐,A级证据)。
如果不能口服尼莫地平,可以考虑静脉途径(GCP)。
其他预防DCI的药物治疗
小规模的单中心研究显示他汀类药物可以改善血管痉挛,降低DCI和死亡率。但是,最近发表的安慰剂随机对照研究和Meta分析显示,他汀类药物对SAH后血管痉挛的发展和临床预后没有影响。
镁剂降低DCI的发生率与剂量相关。镁剂治疗动脉瘤性蛛网膜下腔出血(Magnesium for Aneurysmal Subarachnoid Haemorrhage,MASH-2)试验是一项Ⅲ期临床随机对照试验,随机入组606例SAH患者接受静脉硫酸镁治疗(64 mmol/d),另外597例患者接受安慰剂治疗。结果显示镁剂治疗没有改善预后。纳入7项随机对照试验的Meta分析显示镁剂降低不良预后的疗效并不优于安慰剂。
其他预防DCI的推荐
不推荐使用硫酸镁预防DCI(Ⅰ类证据,A级推荐)。
他汀类的效果仍需进一步研究。
DCI的血流动力学管理
缺陷
自35年前第一次有关于诱导性高血压的观察性研究发表以来,目前仍然缺乏相关随机试验,但是根据个案报道和非对照试验的结果,很多医师使用诱导高血压和高容量的方法改善了患者的预后。主动升高动脉压和增加血浆容量增加了脑水肿、梗死的出血转化、可逆性白质脑病、心肌梗死和充血性心力衰竭的风险。
DCI血流动力学的管理推荐
没有相关对照研究的证据证明诱导性高血压或高血容量可以改善DCI患者的预后(Ⅳ类证据,C级推荐)。
3 非动脉瘤性蛛网膜下腔出血
3.1 流行病学和定义 15%的非创伤性SAH患者经DSA检查未发现责任病灶(参见上文中的诊断)。对这类患者,我们需要根据出血部位区分中脑周围性SAH和非中脑周围性SAH,这决定了下一步的治疗方案。
3.2 中脑周围性蛛网膜下腔出血 “中脑周围性SAH”(perimesencephalic SAH,PMSAH)的诊断需排除了动脉瘤性出血,并结合典型的出血部位在中脑周围和环池(即侧裂和脑叶间裂中没有血液)得出。尽管脑室中可能出现血液沉积,但是脑室堵塞或脑实质出血与PMSAH是不一致的。
由于椎基底动脉动脉瘤或动静脉畸形的出血源有可能导致出血,故仅通过影像学检查不足以诊断PMSAH。诊断本身的风险,一方面取决于SAH和PMSAH的年发病率:在年龄≥18岁人群中,SAH及PMSAH发病率分别为8.7/100 000(95%CI 7.9/100 000~9.5/100 000)和0.5/100 000(95%CI 0.3/100 000~0.7/100 000)。
另一方面动脉血管造影本身存在风险(2%~3%)。同时,研究表明CTA和MRA对排除PMSAH中动脉瘤性的出血敏感性较高,但尚需要大样本前瞻性临床试验来证实PMSAH患者是否可以用CTA或MRA代替DSA。由于操作风险超过发现动脉瘤带来的获益,故不推荐对DSA未发现动脉瘤的PMSAH患者重复该检查。
临床上PMSAH患者的症状较非动脉瘤性弥漫性SAH轻且预后较好。出现血管痉挛和DCI的概率可能较低。在更多研究证据支持PMSAH与DCI有关前,不推荐对PMSAH患者预防性使用尼莫地平(或其他钙离子拮抗剂)。
除了DCI和再出血,PMSAH患者出现其他并发症如脑积水、低钠血症和心电图改变的概率与动脉瘤性SAH患者基本相同。这类并发症的治疗与上文相同。
PMSAH患者的再出血似乎对预后影响不大,且患者不会降低生存率。这些现象提示PMSAH的病因并非动脉源性,可能是由于幕下静脉引流的变异引起的。
3.3 非中脑周围性蛛网膜下腔出血 几乎所有基线DSA检查未发现动脉瘤的非中脑周围性SAH的研究都是回顾性的。但是,随访过程中血管造影阳性发现率为5%~35%。因此,建议未对发现出血源的非中脑周围性SAH患者复查血管造影。
3.4 其他原因引起的非创伤性SAH 非创伤性SAH的病因可能有许多(表3)。非创伤性SAH的诊断和治疗需要根据病因来决定。
非动脉瘤性SAH诊断步骤推荐
PMSAH患者仅在CTA不足以诊断或对中脑周围出血的形式存在质疑时才考虑行DSA(Ⅱ类证据,B级推荐)。
对于非中脑周围性SAH,如果没有治疗指征提示需要进行早期复查,建议在首次出血至少3周后复查CTA或DSA(Ⅲ类证据,B级推荐)。
4 未破裂的颅内动脉瘤
4.1 流行病学 由于SAH仍是一种高死亡率和发病率的严重疾病,所以几十年来西方国家仍积极处理偶然发现的未破裂的颅内动脉瘤(unruptured intracranial aneurysm,UIA),这些动脉瘤可能是偶然发现的,也可能与破裂动脉瘤同时发现(多发动脉瘤)。未破裂动脉瘤一般分为以下几类:无症状性偶然发现的动脉瘤、症状性动脉瘤和SAH非责任未破裂动脉瘤(多发动脉瘤)。通过外科手术或介入治疗未破裂动脉瘤,可以降低严重SAH导致的高死亡率和高发病率。但是由于目前研究人群数量小且随访时间不足,故UIA的自然史、血管内介入治疗和手术治疗的风险以及导致动脉瘤破裂的危险因素尚不十分明确。
目前,只有少量前瞻性随访研究和几项小样本回顾性研究评估了UIA的自然史。另外,不同研究在重要的预测因子、手术方式和患者年龄等方面存在选择偏倚。
表4为两项已发表的最大规模的关于UIA破裂风险的前瞻性研究的队列分析结果(Ⅱ/Ⅲ类证据,B级推荐)。国际未破裂颅内动脉瘤研究(International Study of Unruptured Intracranial Aneurysms,ISUIA)的前瞻性研究部分(61家中心在1991-1998年入组患者)与其回顾性研究部分(53家中心1970-1991年的患者)的结果有所不同。在前瞻性研究部分,动脉瘤破裂的总发病率更高(0.8%/年 vs 0.3%/年),椎基底动脉动脉瘤的破裂风险相对较低(与其他动脉瘤相比,RR 2.3 vs 5.1~13.8),每个患者的平均随访时间更短(3.9年 vs 8.3年),未发生过SAH的患者,其动脉瘤破裂风险很小,发生破裂的动脉瘤直径下限更低(<7 mm vs <10 mm),与回顾性研究相比,动脉瘤破裂风险与年龄无直接相关性。
尽管ISUIA入组了大量患者,其前瞻性和回顾性研究部分的结果不同提示存在选择偏倚。因此ISUIA的结果很难在未破裂动脉瘤人群中推广,其结果需要谨慎解释。另外,在30岁以上的成人中,SAH年发病率至少为30/100 000~40/100 000,成人动脉瘤患病率估计为2%~5%。因此,一般成人未破裂动脉瘤的破裂风险预计为每年至少1%。ISUIA报道的破裂风险可能被低估,多数破裂动脉瘤的直径<10 mm也支持这一观点。

表3 非创伤性SAH的罕见原因
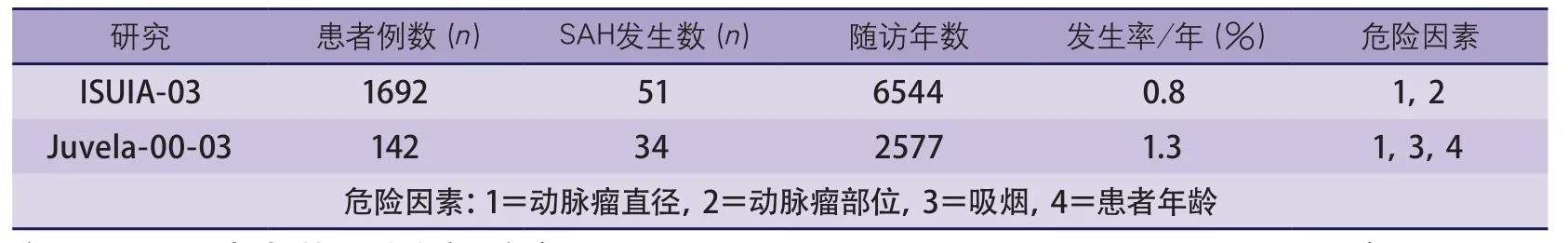
表4 未破裂动脉瘤破裂的风险
ISUIA入组患者的时间正是积极处理UIA的年代,特别是对于工作年龄的患者,研究显示很大比例的患者(58%)接受了开颅手术或血管内介入治疗。进行开颅手术治疗颅内动脉瘤的患者较未手术的患者更年轻且更有可能正在吸烟(P<0.01)。开颅手术、血管内治疗和未治疗3组患者,在其他方面差异具有显著性,如预测动脉瘤破裂或预后的重要预测因子显著不同。这些因素包括动脉瘤大小、位置以及不同的医疗或行为因素。
Helsinki大学中心医院一项关于未破裂动脉瘤自然史的前瞻性研究(单中心入组1956-1978年的患者)自1960年起被报道过多次,因为随着时间的推移,入组的患者人数和随访时间在不断增加。这项队列研究的随访时间较长(每位患者平均随访时间18.2年,中位随访时间19.7年),未经手术治疗,有完整的随访记录的未破裂动脉瘤患者,与ISUIA研究相比,患者数量(n=142)相对较少而且几乎所有患者都是工作年龄人群、有较高的吸烟率且存在多个动脉瘤的患者在随访开始时责任动脉瘤已闭塞。因此这些结果不适用于偶然发现动脉瘤的高龄人群。目前通过MRA或3D CTA偶然发现的动脉瘤越来越多。另外,动脉瘤年破裂率为1.3%(95%CI 0.9%~1.7%)几乎在25年内没有太大变化,与之前小规模回顾性研究的结论(1%~3%)相同。动脉瘤破裂风险的重要因素为吸烟(作为时间依赖性协变量)、动脉瘤直径(线性相关)和年龄(负相关)。随访中存在高收缩压和长期高血压提示动脉瘤一旦破裂,往往是致命性的。尽管多发动脉瘤的患者动脉瘤再形成风险增加,但与仅有一个未破裂动脉瘤的患者相比,动脉瘤破裂风险不增加。
在决定治疗颅内未破裂动脉瘤的方法时,不仅需要考虑动脉瘤的最大直径,还应该考虑患者年龄、动脉瘤的位置(后交通和椎基底动脉动脉瘤破裂风险可能较高)、高血压病史、既往SAH史(不是动脉瘤破裂的独立危险因素)以及吸烟。ISUIA的前瞻性部分研究显示,开颅手术和血管内介入治疗的风险相当。另一方面,选择血管内介入治疗的患者通常是开颅手术风险较高的患者(高龄、较大的动脉瘤、基底动脉尖动脉瘤等)。然而,仅51%的血管内动脉瘤栓塞患者栓塞完全,由于随访时间较短,其治疗效果的持久性还不明确。尽管血管内动脉瘤栓塞治疗能有效预防动脉瘤性SAH后再出血,但因治疗获益需要几十年的随访观察才能明确,故其对未破裂颅内动脉瘤(尤其是年轻患者)的疗效不十分明确。大动脉瘤不完全栓塞(动脉瘤内血栓不完全机化、动脉瘤纤维化不良及动脉瘤口内膜增生异常)可致随访期间出现血管再通和动脉瘤意外变大、破裂,这类动脉瘤很难行开颅手术治疗。然而,未破裂动脉瘤血管内介入治疗对高龄患者的窄颈(<12 mm)基底动脉尖动脉瘤,以及既往有缺血性卒中史的患者可能疗效较好。
ISUIA中未破裂动脉瘤开颅手术治疗的风险(死亡率1.5%~2.3%,致残率10%~12%)与一项Meta分析的结论(全因死亡率2.6%,永久性致残率10.9%)基本一致。开颅手术预后不良的独立预测因素包括动脉瘤大小、后循环动脉瘤、高龄和既往缺血性卒中史。血管内介入治疗不良预后的独立预测因素包括动脉瘤大小和后循环动脉瘤。ISUIA研究中,开颅手术的动脉瘤患者11%出现了脑梗死,而血管内介入治疗患者仅5%。但血管内介入治疗的长期疗效和长期随访中的全因治疗风险仍然未知。因此,推荐由术后出现脑梗死概率≤5%的手术医师进行开颅手术处理未破裂动脉瘤。
在Meta分析中技术处理困难的动脉瘤所占比例过多[巨型动脉瘤(>25 mm)27%,后循环动脉瘤占30%]。因此,这些良好的结果很可能存在发表偏倚。笔者计算了下列特殊动脉瘤组的不利预后:前循环非巨大动脉瘤,死亡率0.8%,发病率1.9%;后循环非巨大动脉瘤,分别为3.0%和12.9%;前循环巨大动脉瘤为7.4%和26.9%,后循环巨大动脉瘤分别为9.6%和37.9%。
综合上述研究结果,未破裂动脉瘤患者接受手术治疗应满足:年龄<50~60岁(开颅手术),动脉瘤直径≥7 mm的老年患者且无禁忌证及严重疾患病史(开颅手术或血管内治疗)。高龄和缺血性卒中史患者应优先考虑血管内治疗。
症状性动脉瘤患者不论年龄如何均应进行动脉瘤闭塞治疗,这是因为症状可能是由于动脉瘤渗血或生长所致,提示近期可能会出现严重的动脉瘤破裂事件。最终治疗颅内动脉瘤的方案由不同中心的神经外科医师和神经放射医师的经验决定。最后,无论选择何种治疗方案,未破裂颅内动脉瘤患者均应戒烟并积极治疗高血压。
4.2 治疗
4.2.1 夹闭术或栓塞术
UIA干预治疗说明
尽管血管内操作的短期风险较少,但是长期风险和疗效尚不明确,需要进一步对接受治疗患者进行长期随访。
研究数据提示相当部分UIA在处理时存在临床均势;不同中心UIA治疗的多样性证实了该现象。
UIA干预治疗的推荐
动脉瘤越大破裂风险越大(Ⅱ类证据,B级推荐)。
要充分考虑风险(手术风险,每年5%~50%vs 自发性破裂风险,每年0~10%)和获益(伴或不伴有小缺陷的寿命),是否采取干预治疗时应综合考虑患者自身因素(年龄、吸烟以及其他动脉瘤破裂的可能)、动脉瘤特点(大小和部位)以及治疗风险;因此,在制订治疗方案时应该针对个体并进行多学科讨论(Ⅲ类证据,C级推荐)。
