紫外光谱法实时测定新枞酸的氧化动力学研究
2014-02-25刘珈伶刘雄民关文龙李伟光
刘珈伶,刘雄民,关文龙,赖 芳,李伟光
(广西大学化学化工学院精细化工研究所,广西南宁530004)
紫外光谱法实时测定新枞酸的氧化动力学研究
刘珈伶,刘雄民*,关文龙,赖 芳,李伟光
(广西大学化学化工学院精细化工研究所,广西南宁530004)
采用了紫外光谱法建立的新枞酸定量分析方法,跟踪测定在连续反应器上的新枞酸氧化反应动力学。在物质的量范围0.6420×10-6~3.854×10-6mol内,新枞酸的吸光度(A1)与物质的量(n1)的线性关系是:A1=0.7390×106n1+0.2403。在反应温度25、30、40、50℃下,新枞酸的氧化反应动力学呈现表观一级反应,氧化速率常数分别为0.0024、0.0040、0.0083、0.0168min-1。反应的表观活化能Ea为61.39kJ·mol-1。
新枞酸,氧化反应,动力学和机理,紫外光谱
新枞酸是松香主要成分之一[1],松香广泛应用于涂料、油墨、造纸、粘合剂、食品添加剂及生物制品等领域[2]。新枞酸是一种天然的抗肿瘤试剂[3]及手性药物合成原料[4],是幼虫的生长抑制剂[5]。松香暴露在空气中会因自氧化变红,影响其使用效果[6],因此,松香和新枞酸的抗氧性研究对产品生产、储存和使用具有重要理论意义,值得关注。
Malevskaya等[7]发现松香氧化反应首先发生在枞酸型树脂酸上。Schuller等[8-11]研究枞酸型树脂酸的光氧化,证明新枞酸光敏氧化反应是:新枞酸氧化得过渡态18-氢过氧化左旋海松酸,而后再氧化得18-氢过氧-8,12-过氧-△13(14)-二氢枞酸。Enoki等[12]发现溶解于α-蒎烯中的松香氧化时,同环共轭树脂酸(左旋海松酸和长夜松酸)生成氧加成物和脱氢枞酸;而异环共轭酸(枞酸和新枞酸)只生成氧加成物。钟国华等[13]指出松香氧化后形成的醌基是其颜色加深的主因。吴宗华等[14-15]发现松香中双键与氧形成环氧基再水解成羟基是松香氧化的主要途径之一,羰基的形成是松香变红的主要原因。尽管国内外学者做了大量的研究,但由于分离鉴定其相关氧化中间产物难度非常大,精确的反应机理至今尚未清楚。
化学动力学是一门研究化学反应动态过程以及机理的学问[16]。但国内外对新枞酸的氧化动力学和其动力学检测方法的研究很少。松香树脂酸常用的检测方法是气相色谱法,该法虽然能准确分析新枞酸含量,但实验条件苛刻,所用的分析时间长,无法长期实时监控新枞酸氧化过程,不是动力学检测的理想方法[17-18]。本课题组[19-20]采用紫外分光光度法对松香和枞酸的热氧化和紫外光氧化动力学进行了初步研究。
本文采用紫外分光光谱法建立了新枞酸的动力学检测方法,并研究了其在不同温度条件下的氧化反应动力学,为今后松香及其产品的耐候性研究提供理论基础。
1 材料与方法
1.1 材料与仪器
松香 特级,工业品,广西梧州日成林产化工有限公司;2-胺基-2-甲基-1,3-丙二醇(≥99%) 阿拉丁试剂(上海)有限公司;丁酮(AR)、丙酮(AR) 成都市科龙化工试剂厂;无水乙醇(AR) 汕头市西陇化工有限公司;乙酸(AR) 广东光华化学有限公司。
UV-2550型紫外分光光度计、GC-MS/QP2010型气相色谱-质谱联用仪 日本岛津公司。
1.2 原料制备
60g松香溶解于丁酮中,加入2-胺基-2-甲基-1,3-丙二醇生成淡黄色新枞酸粗胺盐沉淀物。采用树形重结晶法经丁酮多次重结晶得白色胺盐晶体,在丙酮溶解下以乙酸还原获得白色新枞酸晶体3g[21-22]。用气相色谱-质谱联用仪定量分析[18],新枞酸含量为97.02%。
1.3 反应器及反应室
微量反应器为两块相同大小的长方形薄铝板,内开一个方形小孔,孔与紫外-可见分光光度仪光路通道的位置和尺寸相匹配,将聚乙烯膜固定在孔内,光路可透过聚乙烯膜。氧化反应室为密闭可控温暗室,室内的湿度基本恒定,有管道与大气相通。反应时,将滴加新枞酸样品的微量反应器置于反应器内进行反应,同时用温控器改变室内温度。
1.4 分析方法
新枞酸在乙醇溶液中、新枞酸在薄膜上、新枞酸氧化物在薄膜上及空白薄膜的紫外吸收谱如图1所示,扫描波长为200~400nm。
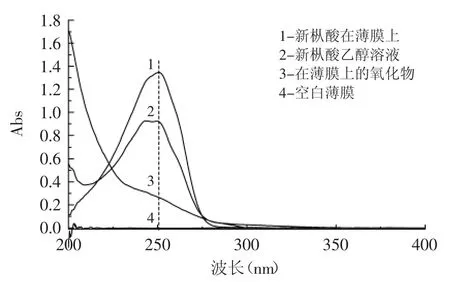
图1 新枞酸和氧化产物的紫外吸收光谱Fig.1 UV spectra of neoabietic acid and its oxides
图1中空白薄膜几乎无紫外吸收,不影响新枞酸样品吸收的吸光度。新枞酸在薄膜上及在乙醇溶液中具有相同的紫外吸收特性,最大吸收峰都在波长251nm处。因此该法不影响新枞酸的紫外吸收特征,可用紫外光谱对其进行跟踪监测,并选择251nm处为检测波长。新枞酸氧化物在此处无特征吸收峰。
定量配制各种浓度的新枞酸乙醇标准溶液,用微量进样器准确量取20μL该溶液均匀滴加到微量反应器薄膜上,扫描其紫外可见光谱,测定标准溶液吸光度,绘制标准曲线。
1.5 氧化动力学方法
准确称取新枞酸0.4000g,以无水乙醇溶解定容至10mL。用微量进样器准确量取新枞酸溶液20μL均匀滴加到微量反应器薄膜上,将反应器置于氧化反应室中进行氧化实验,用紫外光谱(UV)跟踪检测其氧化随时间变化情况。
2 结果与讨论
2.1 紫外光谱法测定新枞酸的浓度
2.1.1 线性方程和范围的确定 分别称取0.0500、0.1001、0.1750、0.2000、0.2501、0.3001g新枞酸,以无水乙醇为溶剂,在5mL的棕色容量瓶中溶解定容。取20μL溶液均匀滴加到薄膜上,待乙醇挥发后,以紫外分光光度计测定其在251nm处的吸光度。以新枞酸物质的量(n1,×10-6mol)为横坐标,吸光度A1为纵坐标绘制标准曲线,如图2所示。
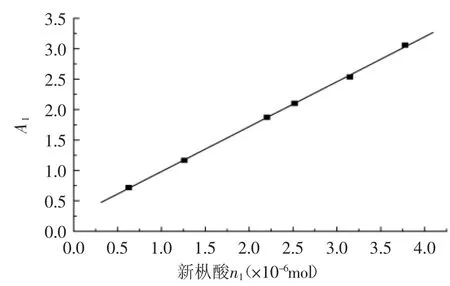
图2 新枞酸标准曲线Fig.2 Standard curve of neoabietic acid
由图2可得新枞酸物质的量n1与最大吸收波长处的吸光度A1的关系曲线方程为:
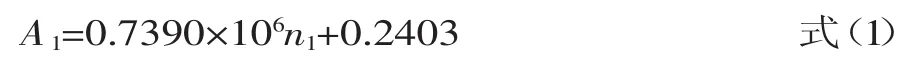
因此,新枞酸浓度在0.6420×10-6≤n1≤3.854× 10-6mol内,线性关系良好,相关系数R2=0.9995。
2.1.2 精密度实验 在线性浓度范围内,配制3个不同浓度的新枞酸溶液50.04、39.98、30.02g/L,取20μL配制好的溶液均匀滴加到反应器薄膜上,分别平行测定6次,结果如表1所示。

表1 精密度测定(n=6)Table.1 Precision of analysis method(n=6)
由表1可见,同一样品平行测定6次的相对标准偏差RSD均小于2.0%,采用紫外标准光谱法测定新枞酸含量的精密度较高。说明使用该方法检测新枞酸含量的检测结果可靠。
2.1.3 稳定性测定 在线性浓度范围内,配制3个不同浓度的新枞酸乙醇溶液19.96、30.02、39.98g/L,取20μL配制好的溶液均匀滴加到反应器薄膜上,分别在0、6、24h测定其吸光度,结果如表2所示。
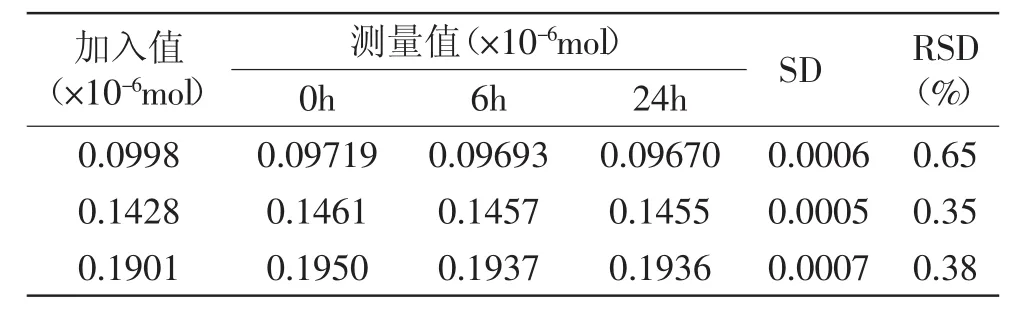
表2 稳定性测定(n=6)Table.2 Stability of analysis method(n=6)
由表2可见,在24h内新枞酸未受氧化反应或异构化反应影响,在紫外光谱检测中相对稳定,相对标准偏差RSD范围为0.35%~0.65%,可认为其在测定时间内较稳定,即采用紫外光谱检测新枞酸的稳定性较高。
2.2 新枞酸的氧化动力学
2.2.1 反应动力学模型的建立 新枞酸与氧气发生如下反应:

假设反应中新枞酸和氧气物质的量的反应级数分别为α和β,则其动力学速率表达式为:

式中,rA为反应速率;k为氧化速率常数;V为反应容积,m3;cA为新枞酸反应浓度,mol·L-1;cB为参与反应的氧气浓度,mol·L-1。反应时反应体系通气管道打开与大气相通,视为氧气过量,cB≫cA,则无变化,动力学表达式简化为为新枞酸氧化表观动力学常数;nA为新枞酸反应摩尔数,mol。

2.2.2 反应级数及速率常数的测定 由图1可见,新枞酸氧化物在251nm处无特征吸收峰,但其微量吸收不可忽视,在进行氧化动力学数据处理时应予以扣除。新枞酸氧化物工作曲线为:

式中,A2为新枞酸氧化物的吸光度;n2为氧化物摩尔数,单位mol。新枞酸氧化动力学数据处理过程如下:
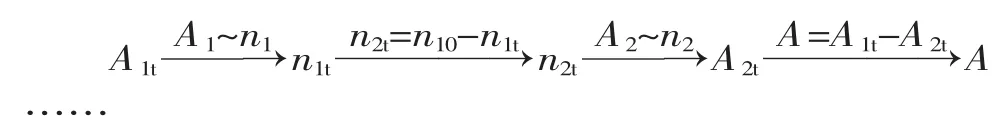
其中,n10为新枞酸初始反应量;A1t为t时刻测得的吸光度值;n1t为曲线求出新枞酸物质的量;n2t为氧化物生成量;A2t为氧化物吸光度值;A为t时刻参与反应的新枞酸吸光度。以此循环迭代,减小计算误差。
以紫外分光光度计跟踪检测新枞酸在在25、30、40、50℃下氧化反应的吸光度变化值,运用上述方法,求得新枞酸的反应摩尔量n。采用积分法作ln(n)与时间t的曲线,如图3所示。

图3 不同温度下ln(n)~t的关系曲线Fig.3 Correlation plots of the natural logarithm of molar weight(ln(n))vs.the reaction time(t)at different temperatures
由图3可见,ln(n)与反应时间t为直线关系,则满足一级反应n与t的关系,该反应级数为一级反应。不同温度下新枞酸的氧化速率常数及动力学方程如表3所示。

表3 不同反应温度下新枞酸的速率常数和动力学方程Table.3 Kinetic data and equation for the oxidation of neoabietic acid at different reaction temperatures
结果表明随着温度升高,反应速率常数逐渐增大,反应速度相应加快。
2.2.3 反应表观活化能的确定 Arrhenius反应速率公式反映温度对反应速率的影响:

式中,k为反应速率常数,单位min-1;Ea为反应活化能,J·mol-1;R为摩尔气体常数,R=8.315 J·mol-1·K-1;T为反应温度,单位K;k0为指前因子。Ea值越大,则反应速率随温度的变化显著。取表3数据做ln(k)~1/T关系图如图4所示。
由图4可见,ln(k)与1/T呈线性关系,相关系数为R2=0.9974。由直线斜率和截距求得反应表观活化能:Ea=61.39kJ·mol-1。
虽然还没有新枞酸氧化反应的文献,但在少数松香树脂酸氧化动力学的研究中粟子安等[23]以气相色谱法研究松香和枞酸初期氧化动力学模型,其氧化过程为一级反应过程,枞酸反应活化能为58.54kJ·gram molecule-1,松香为100.36kJ·gram molecule-1。秦荣秀等[20]采用紫外分光光度法研究了枞酸和松香热氧化反应,结果表明,枞酸氧化反应为表观一级反应,活化能为50.32kJ·mol-1,松香为83.2kJ·mol-1,文献两种不同方法测定的枞酸氧化动力学活化能比较接近。本方法采用了文献[20]的实验方法,从实验结果来看,新枞酸的氧化反应活化能(Ea=61.39kJ·mol-1)稍微大于枞酸的活化能(50.32kJ·mol-1)。
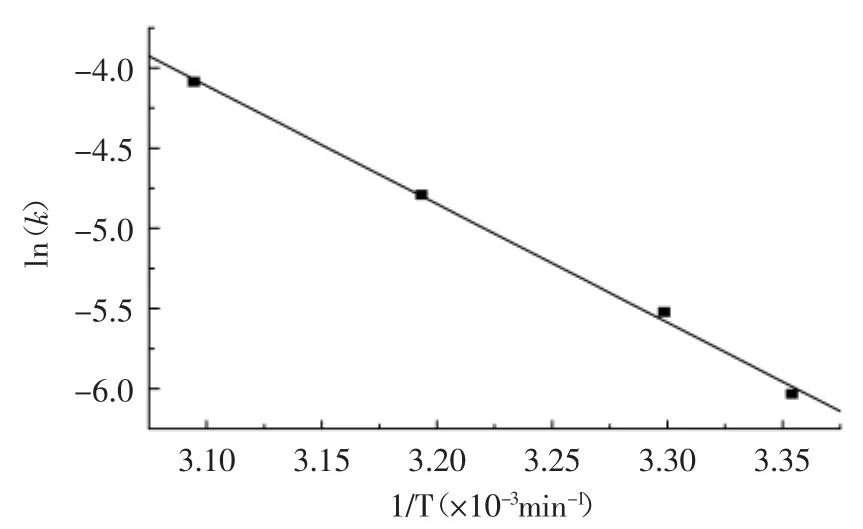
图4 ln(k)~1/T关系曲线Fig.4 Plots of the natural logarithm of kinetic data(ln(k))vs. the reciprocal of the reaction temperature(1/T)
3 结论
建立了紫外光谱法实时测定新枞酸物质的量新方法,测定了新枞酸催化氧化过程中物质的量变化,进而研究了新枞酸的氧化反应动力学,得出了如下结论:
3.1采用紫外分光光度计实时测定新枞酸物质的量新方法。新枞酸物质的量在0.6420×10-6≤n1≤3.854× 10-6mol内,线性方程为A1=0.7390×106n1+0.2403(R2=0.9995)。精密度和稳定性RSD范围分别为0.25%~0.55%和0.35%~0.65%。
3.2在不同温度下,测定了新枞酸紫外吸光度随氧化反应进程的变化,计算出新枞酸氧化反应为一级反应,该反应宏观动力学可表示为:rA=k′nA。
3.3在25、30、40、50℃下新枞酸的氧化速率常数为0.0024、0.0040、0.0083、0.0168min-1。反应的表观活化能Ea为61.39kJ·mol-1。
[1]贺近恪,李启基.林产化学工业全书[M].第二卷.北京:中国林业出版社,2001:1079-1083.
[2]Silvestre A J,Gandini A.Rosin:major sources,properties and applications[J].Monomers,Polymers and Composites from Renewable Resources,2008(6):67-88.
[3]Tanaka R,Tokuda H,Ezaki Y.Cancer chemopreventive activity of“rosin”constituents of Pinus spez.and their derivatives in two-stage mouse skin[J].Phytomedicine,2008,15(11):985-992.
[4]Wenkert E,Mahajan J R,Nussim M,et al.Conversion of neoabietic acid into manool[J].Canadian Journal of Chemistry,1966,44(21):2575-2579.
[5]Elliger C A,Zinkel D F,Chan B G,et al.Diterpene acids as larval growth inhibitors[J].Experientia,1976,32(11):1364-1366.
[6]粟子安,杨必胜,郭长泰.松香发红变质实验[J].林产化学与工业,1997(4):48-54.
[7]Malevskaya S S,Kazeeva E V.Auto-oxidation products of abietic acid[J].Russian Journal of Applied Chemistry,1952,25:1149-1154.
[8]Moore R N,Lawrence R V.Air oxidation of resin acids.I. photo-sensitized oxidation of levopimaric acid[J].Journal of the American Chemical Society,1958,80(6):1438-1440.
[9]Schuller W H,Moore R N,Lawrence R V.Air Oxidation of Resin Acids.II.The Structure of Palustric Acid and its Photosensitized Oxidation[J].Journal of the American Chemical Society,1960,82(7):1734-1738.
[10]Schuller W H,Lawrence R V.Air oxidation of resin acids. III.The ohotosensitized oxidation of neoabietic acid and the configurations of the pine gum resin acids[J].Journal of the American Chemical Society,1961,83(11):2563-2570.
[11]Schuller W H,Minor J C,Lawrence R V.Photosensitized oxidation of pine gum to yield peroxides[J].Industrial& Engineering Chemistry Product Research and Development,1964,3(2):97-100.
[12]Enoki A.Isomerization and autoxidation of resin acids[J]. Wood research:bulletin of the Wood Research Institute Kyoto University,1976,59:49-57.
[13]钟国华.松香的结构,氧化和脱色[J].广西林业科学,1997,26(2):77-78.
[14]吴宗华,陈少平.脂松香热氧化机理的研究[J].林产化学与工业,2000,20(3):13-16.
[15]吴宗华,陈少平.不同气体介质中脂松香的热氧化行为[J].福建师范大学学报:自然科学版,2000,16(1):64-67.
[16]杨学明,杨立英,金碧辉.化学动力学[J].中国基础科学,2005,7(3):24-25.
[17]刘珈伶,刘雄民,李伟光,等.松香,松脂中枞酸含量的紫外分析方法研究[J].食品工业科技,2011,32(9):427-430,463.
[18]Akiyama T,Hayashi A,Yamazaki T,et al.Identification methods of terpenoid gum bases using TLC and GC/MS[J]. Journal of the Food Hygienic Society of Japan,2010,51(5):264.
[19]秦荣秀,黄品鲜,刘雄民,等.松香和枞酸在聚乙烯膜上氧化反应动力学研究[J].高等学校化学学报,2009,30(5):954-958.
[20]刘雄民,秦荣秀,黄品鲜,等.枞酸和松香在紫外光辐照下的氧化反应动力学[J].物理化学学报,2010,26(8):2115-2120.
[21]Loeblich V M,Lawrence R V.An improved procedure for the isolation of Neoabietic acid from pine oleoresin and rosin[J]. The Journal of Organic Chemistry,1956,21(6):610-611.
[22]Jin Z,Pan Y,Liu J,et al.Separation of rosin acids by molecularrecognition:crystalstructure ofthe complex of neoabietic acid with 2-amino-6-methyl-pyridine[J].Journal of chemical crystallography,2000,30(3):195-198.
[23]粟子安,虞启庄,郭长泰,等.松香自动氧化与变色的研究[A].中国林化学会学术讨论会论文集[C].1986:40-55.
Study on the kinetics of oxidation of neoabietic acid using UV-VIS spectroscopy
LIU Jia-ling,LIU Xiong-min*,GUAN Wen-long,LAI Fang,LI Wei-guang
(School of Chemistry and Chemical Engineering,Guangxi University,Nanning 530004,China)
The method was applied to the analysis of the mole quantities of neoabietic acid by UV Spectrophotometry.The kinetics of oxidation of neoabietic acid was investigated using a continuous experiment apparatus.Results and conclusions drawn were as follows.Firstly,plot of absorption(A1)against the mole quantity(n1)was linear:A1=0.7390×106n1+0.2403,in the mole quantity range of 0.6420×10-6~3.854×10-6mol. Secondly,the oxidation reaction was first order at 25,30,40,50℃,respectively.The reaction rate constants were 0.0024,0.0040,0.0083,0.0168min-1,respectively.Finally,the reaction activation energy was 61.39kJ·mol-1.
neoabietic acid;oxidation;kinetics and mechanism;ultraviolet spectrophotometry
TQ651+2
A
1002-0306(2014)04-0140-04
2013-07-02 *通讯联系人
刘珈伶(1985-),女,大学本科,助教,研究方向:天然产物化工。
广西科学研究与技术开发计划项目(桂科攻12118008-2);广西研究生教育创新计划项目(105931003096);广西八桂学者团队项目;玉林市科技计划项目(201210505)。
