以吞咽困难为主要表现的弥漫性特发性骨质增生症一例报告
2014-02-13阳普山张超何文天用王德利吴剑宏阮狄克
阳普山 张超 何文天用 王德利 吴剑宏 阮狄克
. 病例报告 Case report .
以吞咽困难为主要表现的弥漫性特发性骨质增生症一例报告
临床资料
患者,男,70 岁,主诉吞咽不适感伴颈部酸痛2 年,加重1 个月入院。患者于2 年前自感吞咽硬食时咽部不适,于当地医院行胃食管镜检查,未见明显阳性结果。于同期出现颈部酸痛感,偶有双侧手指指端麻木感,无明显上肢放射痛及“踩棉花感”。患者于入院前1 个月吞咽不适感明显加重,进食时出现食物咽部“停留”感,仅能进软食或流食。遂就诊于我院门诊,行颈椎 X 线检查示 C2~6多节段融合,C2~6前方巨大骨赘形成。门诊以“食管型颈椎病”收入院。患者既往2 型糖尿病史 10 余年,应用胰岛素治疗;既往高血压病史4 年余,血压控制可。查体:患者颈部外观未见明显异常,嘱患者做吞咽动作,轻压甲状软骨可诱发明显咽部不适。颈椎无明显压痛,双上肢肌力及感觉正常,上肢腱反射正常,Hoffman征 (- )。余查体未见明显阳性体征。辅助检查:颈椎侧位X 线示 (图 1a ) :颈椎前方 C2~6“流注样”骨化影,诸椎间盘高度未见明显改变,关节突关节未见明显异常。CT示 (图 1b ): C2~6椎体前方连续但不规则高密度骨化影。骨化物在 C4椎体前方突出最明显,压迫前方软组织。颈椎 MRI 示 (图 1c ):颈椎前方-气管后缘 C2~T1异常信号;未见明显椎管狭窄及脊髓压迫。
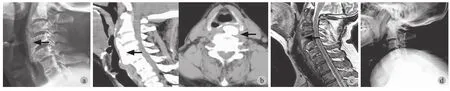
图1 a:术前颈椎 X 线片:颈椎前方 C2~6“流注样”骨化影,诸椎间盘高度未见明显改变;b:术前颈椎 CT:显示 C2~6多个椎体前方巨大骨桥形成,向前方突出,挤压椎体前方软组织结构;c:术前颈椎核磁:核磁 T2相显示 C2~6椎体前方骨质样高信号,未见明显椎管狭窄及脊髓压迫;d:术后颈椎 X 线片:术后患者颈椎侧位片显示颈椎前方增生的骨质完整切除Fig.1 a: The preoperative X-ray showed fowing ossifcation along the anterior aspect of the cervical vertebrae from C2to C6, without obvious changes in the hight of the vertebral discs; b: The preoperative CT showed continuous but irregular fowing hyperostosis alongside the anterior aspect of the whole cervical vertebrae as well as local ossifcation of the posterior longitudinal ligament from C2to C6; c: The preoperative T2-weighted image showed sclerotin-like high signals in the anterior aspect of the cervical vertebrae from C2to C6, without obvious spinal stenosis or spinal cord compression; d: The postoperative lateral X-ray showed the complete resection of hyperplasia in the anterior aspect of the cervical vertebrae
诊断:综上影像学特点,该患者符合 Resnick 等[1]提出的弥漫性特发性骨质增生症 (diffuse idiopathic skeletal hyperostosis,DISH ) 诊断标准。
治疗:患者颈椎前方骨化物巨大,压迫食管出现吞咽困难症状,常规保守治无法解除压迫。因此行颈椎前入路椎体前方骨化物切除手术。切除组织送组织学检测(图2):送检组织以骨组织为主,其内包含少量非特异性炎症细胞 (淋巴细胞、浆细胞及巨噬细胞 )。术后1 周,患者自觉仍存轻度吞咽困难 (考虑与术中食管受刺激相关 ) 但渐进性减轻,术后 X 线复查示 (图 1d ):颈椎椎体前方骨赘完整切除。术后第3 周患者已无明显吞咽困难出院。术后半年随访,患者吞咽正常,可正常进食,其颈部酸痛感较术前亦有明显改善。
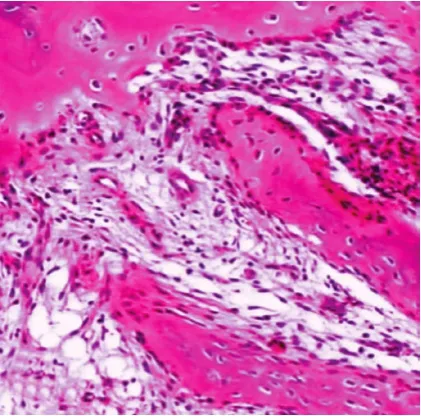
图2 以骨组织为主,其内包含少量非特异性炎症细胞 (淋巴细胞、浆细胞及巨噬细胞 ) (HE ×100 )Fig.2 The staining was performed mainly in resected bone tissues, in which some nonspecific inflammatory cells were involved, such as lymphocytes, plasma cells and macrophages (HE ×100 )
讨 论
DISH 是一种好发于中老年人,以广泛骨质增生,韧带及肌腱钙化或骨化为特征的疾病,以脊柱病变最为常见,亦可累及脊柱外四肢骨。该病在临床上并不罕见,但因大部分患者无严重的临床症状而被诊断为脊柱退行性疾病。古生物病理学研究发现,DISH 并非是在近代才出现的一种疾病。考古学家在古埃及法老 Ramesses II[2]发现 DISH 改变,也在公元 6 世纪的古意大利人[3]的骨骼残骸上就发现了 DISH 的病理改变。古人类学家发现生活在距今约 5000 年前的尼安得塔人的骨骼标本亦表现出 DISH样改变[4]。尽管该病由来已久,但该疾病一直未得到人们的广泛认知。由于对该病认识不一致,曾经命名较混乱,出现了如“念珠样骨肥厚”、“脊柱蜡油样骨病”等命名。直到 1950 年,Forestier 等[5]才对 DISH 进行了全面系统的描述,并将其命名为“老年性强直性骨肥大”,但在此后人们更习惯称该病为 Forestier’s 病。随着人们对该疾病的认识的深入,Resnick 等[6]于 20 世纪 70 年代提出以“DISH”命名该疾病,并提出了相应的影像学诊断标准,DISH 的命名逐步被人们接受并趋于统一。以下将对DISH 的临床特点及治疗等进行综述,以加深我们对该病的认识。
一、临床特点
1. 病因学:该疾病目前病因学尚未明确。代谢异常、内分泌异常[7]、遗传学及饮食因素[8]可能在其发生存在一定相关性。研究发现 DISH 患者常合并其它疾病,如高血压、2 型糖尿病[9]、肥胖、高尿酸血症[7]。因此推测上诉因素可能在 DISH 发生中起某些作用。也有文献报道椎体局部的血供改变可能是 DISH 发病的诱因[10]。国内有学者通过基因多态性分析发现多个信号通路 (MAPK 通路、Wnt 通路、TGF-β 通路等 ) 与 DISH 骨化有关[11]。国外亦有学者报道经典的 Wnt 通路在 DISH 的成骨作用中可能起重要作用。该通路中一个重要的阻断因子 DKK-1 低表达可导致明显新骨形成,而 DKK-1 高表达则导致明显骨溶解。测量外周循环中 DKK-1 的浓度发现 DISH 患者外周循环浓度发现比正常人群明显降低。提示该因子低表达可能在其广泛的新骨形成中起了重要作用[12]。综上所述,DISH 是一种目前病因不明,多种代谢异常疾病可能在其发病中起作用,而 DKK-1 因子的低表达可能是导致该病广泛新骨形成的原因之一。
2. 发病率:不同地区 DISH 的发病率差异巨大。一项来自芬兰的人口发病率调查显示男性发病率为 7%,而女性发病率仅为 3%[13]。而一项来自韩国的人口发病率显示该国人群发病率仅为 4% 左右[14]。Weinfeld 等[15]调查了美国两个大都市的发病率,发现美国发病率显著高于其它地方,男性发病率高达 25%,女性高达 15%。另一项针对匈牙利首都的大规模调查显示,男女发病率分别为 27.3% 和12.8%[16]。上述研究者均发现人群发病率随年龄增长而增长,且男性发病率均明显高于女性。国内目前尚缺乏大规模人群发病率调查研究,但一项来自江苏大学医学院的研究显示该病好发于 50 岁以上人群,发病率同样随年龄增长而升高[17]。以上数据可以得出,欧美人群发病率明显高于亚洲人群。发病率的地域差异可能与人群遗传学不同有关,同时与不同区域人群饮食及环境因素差异可能亦存在某些联系。
3. 临床表现:大部分 DISH 患者临床症状轻微,仅表现为颈部及腰背部酸痛感,无需特殊处理或治疗[18]。大部分患者仅于临床就诊摄 X 线片意外发现。很多学者认为DISH 患者腰背部疼痛发生率比正常人更高,但 Schlapbach等[19]的一项基于病例对照研究发现 DISH 组与正常人组腰背部疼痛发病率并无明显差异。尽管大部分 DISH 患者临床症状轻微,但亦不乏 DISH 导致严重临床症状的病例报道,其临床症状主要与患者骨赘形成的部位及大小相关。如新骨形成于颈椎导致压迫食管、气道[20]而出现相应的吞咽困难或呼吸困难需要手术治疗的病例。亦有作者报道骨赘形成于外周关节而导致严重疼痛需行手术切除的病例,如 Gregory 等[21]报道了骨赘发生于肘关节而导致严重肘关节疼痛的病例。更有学者报道 DISH 患者在轻度创伤下即发生脊柱骨折,并更容易伴发脊柱不稳而导致脊髓损伤导致截瘫[22]。由此可以看出,尽管大部分 DISH 患者临床症状轻微,无需特殊处理,但对于一些因骨赘部位特殊而产生严重临床症状的患者,需及时手术治疗。因此,DISH 患者不能简单应用“脊柱退行性改变”加以诊断而延误诊治。
二、诊断标准
目前 DISH 的诊断主要基于影像学。基于该病广泛的韧带、肌腱骨化的病理基础可以有相对特异的表现。Resnick 于 1976 年[1]首次提出该病的诊断标准:(1) 至少沿相邻4 个椎体的前外侧缘有连续性骨化,伴有或不伴有椎体与椎间盘交界处局部突出的骨赘;(2) 受累椎体的椎间隙宽度正常,无明显椎间盘退变表现;(3) 椎间小关及骶髂关节无明显关节面侵蚀、硬化或骨性强直。其中 2、3 条诊断标准为排除退行性变及强直性脊柱炎对该病诊断的干扰。学者 Arlet 等[23]认为,Resnick 诊断标准过于严格,可能导致部分早期 DISH 患者被漏诊,因此提出以 3个椎体前外侧缘骨化即可作为诊断标准。考虑到该病同时多存在脊柱外表现[6],Utsinger 等[24]建议将 X 线显示的外周骨赘形成也纳入诊断标准,提出2 个椎体前方骨赘形成并伴有对称性外周关节明显骨刺形成即可诊断 DISH。最近 Mader 等[25]希望征集不同专家意见以得到一个新的DISH 诊断标准,但却没有得到回应。上述诊断标准各有优缺点,但 Resnick 诊断标准目前为应用最为广泛的诊断标准。
三、治疗
1. 保守治疗:大部分 DISH 患者临床症状轻微,平时仅表现为颈部及腰背部酸痛感,无需特殊处理。有学者认为 DISH 患者温和的疼痛症状通常通过口服非甾体类抗炎药可以予以缓解[26]。Utsinger 等[27]证明低中强度的镇痛药结合局部热敷可以缓解 DISH 患者疼痛症状。另外有学者发现手法按摩及针灸亦可明显减轻患者临床症状[28-29]。亦有学者提出 DISH 患者可以通过运动治疗明显增加脊柱活动度,改善脊柱僵直及缓解腰背部疼痛症状[30]。上诉治疗均以缓解症状为目的,目前尚无药物能抑制或逆转该病的自然进程。
2. 手术治疗:对于部分因特殊部位骨赘形成产生严重的临床症状的患者,保守治疗通常无效,须行手术治疗。如 DISH 患者因颈椎巨大骨赘压迫前方食管、气管而产生吞咽或呼吸困难,该类患者须及时行骨赘切除以解除压迫症状[31]。另外,值得注意的是部分 DISH 患者在轻度创伤下即发生脊柱骨折并伴发脊柱不稳而导致脊髓损伤。对于该类患者,须及时行手术治疗,以恢复脊柱稳定性[32]。因此 DISH 需早期诊断,并对该类患者进行日常生活指导,并控制与其发病相关疾病,减缓疾病进程。对于一些严重脊柱改变的患者,更需告知其可能因微小创伤导致脊柱骨折的危险性,避免延误诊治。
[1]Resnick D, Niwayama G. Radiographic and pathologic features of spinal involvement in diffuse idiopathic skeletal hyperostosis (DISH). Radiology, 1976, 119(3):559-568.
[2]Chhem RK, Schmit P, Faure C. Did Ramesses II really have ankylosing spondylitis? A reappraisal. Can Assoc Radiol J, 2004, 55(4):211-217.
[3]Canci A, Marchi D, Caramella D, et al. Coexistence of melorheostosis and DISH in a female skeleton from Magna Graecia (Sixth Century BC). Am J Phys Anthropol, 2005, 126(3):305-310.
[4]Crubezy E, Trinkaus E. Shanidar 1: a case of hyperostotic disease (DISH) in the middle Paleolithic. Am J Phys Anthropol, 1992, 89(4):411-420.
[5]Forestier J, Rotes-Querol J. Senile ankylosing hyperostosis of the spine. Ann Rheum Dis, 1950, 9(4):321-330.
[6]Resnick D, Shaul SR, Robins JM. Diffuse idiopathic skeletal hyperostosis (DISH): Forestier’s disease with extraspinal manifestations. Radiology, 1975, 115(3):513-524.
[7]Kiss C, Szilagyi M, Paksy A, et al. Risk factors for diffuse idiopathic skeletal hyperostosis: a case-control study. Rheumatology (Oxford), 2002, 41(1):27-30.
[8]Verlaan JJ, Oner FC, Maat GJ. Diffuse idiopathic skeletal hyperostosis in ancient clergymen. Eur Spine J, 2007, 16(8):1129-1135.
[9]Mader R, Lavi I. Diabetes mellitus and hypertension as risk factors for early diffuse idiopathic skeletal hyperostosis (DISH). Osteoarthritis Cartilage, 2009, 17(6):825-828.
[10]El MY, Wassif G, El BM. Diffuse idiopathic skeletal hyperostosis (DISH): is it of vascular aetiology? Clin Exp Rheumatol, 2000, 18(2):193-200.
[11]赵华健. DISH黄韧带骨化细胞成骨相关miRNA的初步研究.天津医科大学, 2011.
[12]Senolt L, Hulejova H, Krystufkova O, et al. Low circulating Dickkopf-1 and its link with severity of spinal involvement in diffuse idiopathic skeletal hyperostosis. Ann Rheum Dis, 2012, 71(1):71-74.
[13]Julkunen H, Knekt P, Aromaa A. Spondylosis deformans and diffuse idiopathic skeletal hyperostosis (DISH) in Finland. Scand J Rheumatol, 1981, 10(3):193-203.
[14]Kim SK, Choi BR, Kim CG, et al. The prevalence of diffuse idiopathic skeletal hyperostosis in Korea. J Rheumatol, 2004, 31(10):2032-2035.
[15]Weinfeld RM, Olson PN, Maki DD, et al. The prevalence of diffuse idiopathic skeletal hyperostosis (DISH) in two large American Midwest metropolitan hospital populations. Skeletal Radiol, 1997, 26(4):222-225.
[16]Kiss C, O’Neill TW, Mituszova M, et al. The prevalence of diffuse idiopathic skeletal hyperostosis in a population-based study in Hungary. Scand J Rheumatol, 2002, 31(4):226-229.
[17]袁振州, 袁丹军, 李兰贵. 弥漫性特发性骨质增生症500例的影像学诊断分析. 现代医药卫生, 2011, (13):1929-1931.
[18]Bruges-Armas J, Couto AR, Timms A, et al. Ectopiccalcification among families in the Azores: clinical and radiologic manifestations in families with diffuse idiopathic skeletal hyperostosis and chondrocalcinosis. Arthritis Rheum, 2006, 54(4):1340-1349.
[19]Schlapbach P, Beyeler C, Gerber NJ, et al. Diffuse idiopathic skeletal hyperostosis (DISH) of the spine: a cause of back pain? A controlled study. Br J Rheumatol, 1989, 28(4):299-303.
[20]Carlson ML, Archibald DJ, Graner DE, et al. Surgical management of dysphagia and airway obstruction in patients with prominent ventral cervical osteophytes. Dysphagia, 2011, 26(1):34-40.
[21]Gregory J, Colmegna I. Diffuse idiopathic skeletal hyperostosis manifesting as recurrent elbow bursitis. Mayo Clin Proc, 2011, 86(7):702.
[22]Caron T, Bransford R, Nguyen Q, et al. Spine fractures in patients with ankylosing spinal disorders. Spine (Phila Pa 1976), 2010, 35(11):E458-E464.
[23]Arlet J, Mazières B. [Hyperostotic disease]. Rev Med Interne, 1985, 6(5):553-564.
[24]Utsinger PD. Diffuse idiopathic skeletal hyperostosis. Clin Rheum Dis, 1985, 11(2):325-351.
[25]Mader R, Buskila D, Verlaan JJ, et al. Developing new classification criteria for diffuse idiopathic skeletal hyperostosis: back to square one. Rheumatology (Oxford), 2013, 52(2):326-330.
[26]贾连顺. 弥漫性特发性骨肥厚症的概念与临床特征. 中国矫形外科杂志, 2007, (17):1319-1321.
[27]Utsinger PD, Resnick D, Shapiro R. Diffuse skeletal abnormalities in Forestier disease. Arch Intern Med, 1976, 136(7):763-768.
[28]Troyanovich SJ, Buettner M. A structural chiropractic approach to the management of diffuse idiopathic skeletal hyperostosis. J Manipulative Physiol Ther, 2003, 26(3):202-206.
[29]Mears T. Acupuncture for back pain in a patient with Forestier’s disease (diffuse idiopathic skeletal hyperostosis/DISH). Acupunct Med, 2002, 20(2-3):102-104.
[30]Al-Herz A, Snip JP, Clark B, et al. Exercise therapy for patients with diffuse idiopathic skeletal hyperostosis. Clin Rheumatol, 2008, 27(2):207-210.
[31]Verlaan JJ, Boswijk PF, de Ru JA, et al. Diffuse idiopathic skeletal hyperostosis of the cervical spine: an underestimated cause of dysphagia and airway obstruction. Spine J, 2011, 11(11):1058-1067.
[32]Hendrix RW, Melany M, Miller F, et al. Fracture of the spine in patients with ankylosis due to diffuse skeletal hyperostosis: clinical and imaging findings. AJR Am J Roentgenol, 1994, 162(4):899-904.
(本文编辑:马超 )
Diffuse idiopathic skeletal hyperostosis with dysphagia as the main manifestation:1 case report
YANG Pu-sha ZHANG Chao, HE Qing, WEN Tian-yong, WANG De-li, WU Jian-hong, RUAN Di-ke. Department of Orthopedics, Navy General Hospital of CPLA, Beijing, 100048, PRC
Diffuse idiopathic skeletal hyperostosis (DISH ), also called Forestier’s disease, is characterized by calcifcation and ossifcation of ligaments and soft tissues, and its pathology is still uncertain. Most of the patients with DISH do not have serious clinical symptoms. Dysphagia caused by calcifcation or ossifcation in the cervical spine is a rare occurrence. A patient with DISH who had severe dysphagia due to ossifcation in the cervical spine was treated recently, whose clinical data was reported as following.
Hyperostogeny; Deglutition disorders; Neck pain; Ossifcation heterotopic
10.3969/j.issn.2095-252X.2014.06.016
R681.5
100048 北京,中国人民解放军海军总医院骨科
阮狄克,Email: ruandikengh@163.com
2013-07-23 )
