培美曲塞联合顺铂治疗晚期非鳞型非小细胞肺癌的临床观察
2014-02-08周国仁叶劲军蒋鸣冯继锋陆建伟
周国仁 叶劲军 蒋鸣 冯继锋 陆建伟
肺癌是全球范围内癌症相关死亡占第一位的恶性肿瘤,其中非小细胞肺癌(non-small cell lung cancer NSCLC)约占肺癌的80%,临床确诊时约70%患者已处于晚期,丧失手术根治机会,含铂两药化疗目前是晚期NSCLC的标准治疗方案。近年来的研究证明培美曲塞(PMT)+顺铂(DDP)一线治疗非鳞型NSCLC的疗效肯定。本研究中采用PMT联合DDP方案作为观察组;采用多西他赛(DOC)联合DDP方案作为对照组,并将2组的疗效及不良反应进行比较,进一步探索晚期非鳞型NSCLC的优势方案。
1 资料与方法
1.1 一般资料选择我院2010年1月至2011年12月收治的92例晚期非鳞型NSCLC患者,将其分为观察组42例和对照组50例。所有患者中,ⅢB期患者55例,Ⅳ期患者37例。观察组男26例,女16例,年龄45~72岁,中位年龄56.7岁。对照组男24例,女26例,年龄40~76岁,中位年龄59.4岁。2组间性别、年龄、病程、疾病类型等差异无统计学意义(P>0.05),具有可比性。
1.2 化疗方案(1)观察组:PMT(豪森公司)500 mg/m2,静滴(>10 min),第1天静脉滴注;DDP25 mg/m2,静滴2 h,第1~3天;21 d为1个周期,至少2个周期。在首次PMT给药前1周内肌内注射维生素B121 mg,1次,以后每3个周期(9周)肌注1次,可以与PMT在同一天用药;每天口服叶酸400 μg,1次/d,连服到PMT用药结束后21 d。PMT用药前日、当日和次日连续口服地塞米松4 mg,2次/d。(2)对照组:DOC(恒瑞公司)75 mg/m2,静脉滴注,第1天;DDP 25 mg/m2,静滴2 h,第1~3天;21 d为1个周期,至少2个周期。DOC用药前日、当日和次日连续口服地塞米松4 mg,2次/d。
1.3 观察指标治疗2个周期后,按照2009年的RECIST 1.1版标准进行疗效评价。可测量病灶的评价:完全缓解(CR):所有靶病灶消失;病理性淋巴结短径<10 mm。部分缓解(PR):靶病灶长径总和缩小≥30%。进展(PD):靶病灶长径总和增加>20%,并且其绝对值增加>5 mm,出现新病变也视为PD。稳定(SD):靶病灶长径总和有缩小但未达PR或有增加但未达PD。
不可测量病灶的评价:CR:所有不可测量病灶消失;肿瘤标志物正常;所有的淋巴结短径<10 mm。非CR/非PD:持续存在的≥1个不可测量病灶和(或)肿瘤标志物异常增高。PD:不可测量病灶明显增大,新发≥1个病灶都视为PD。
有效率(response rate,RR)为CR和PR病例占所有病例的百分比。疾病控制率(disease control rate,DCR)为CR+PR+SD病例占所有病例的百分比。按NCI-CTC 3.0常见毒性分级标准评价不良反应。分成0~Ⅳ级。
1.4 统计学分析应用统计软件SPSS 13.0进行数据处理,疗效和不良反应率的比较采用等级资料的非参数检验和卡方检验。生存分析采用Kaplan-Meier分析方法。P<0.05为差异有统计学意义。
2 结果
2.1 近期疗效92例患者共化疗248.4个周期,平均化疗2.7个周期,均可评价疗效,结果见表1。观察组和对照组的疗效无统计学差异(Z=-1.715,P=0.086);观察组与对照组的RR、DCR率亦均无统计学差异(χ2=3.158,P=0.092;χ2=0.657,P=0.563)。观察组生存中位数为11月,对照生存中位数为12月,从生存曲线可见,2组生存无显著差异。见图1。

表1 2组患者近期疗效比较(n)
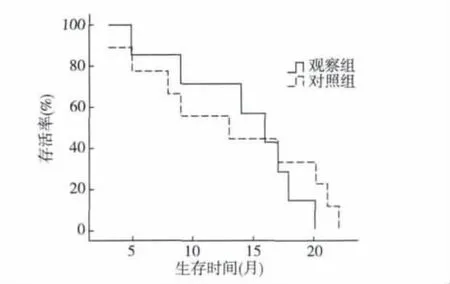
图1 2组患者的生存曲线
2.2 不良反应主要为骨髓抑制,其次为胃肠道反应、乏力和周围神经毒性,以1~2级为主,对照组偶见Ⅲ级不良反应。2组不良反应比较,详见表2。除乏力发生率相近外,观察组中性粒细胞减少、血红蛋白减少、血小板减少、恶心呕吐、脱发发生率显著低于对照组(P<0.05或P<0.01)。
3 讨论
PMT是一种新型的多靶点抗叶酸药物,2004年8月被美国FDA批准用于局部晚期或转移性NSCLC的二线治疗药物,它主要通过抑制胸苷酸合成酶、二氢叶酸还原酶和甘氨酰胺核苷甲酰基转移酶等多种酶的活性而发挥抗肿瘤作用,进一步影响肿瘤细胞合成,抑制细胞增殖[1]。体外实验结果显示,PMT对结肠癌、乳腺癌、白血病、胰腺癌、肺癌及胃癌等多种肿瘤具有抗瘤活性[2-3]。一项Ⅱ期临床研究表明,铂类联合PMT方案的疗效与常用的含铂两药方案相似,但不良反应的发生率则明显降低[4]。JMDB研究是一项PMT联合铂类一线治疗NSCLC的Ⅲ期研究[5],结果显示该方案的疗效不劣于其他第3代化疗药物联合铂类方案,且不良反应低,耐受性好。在治疗肺腺癌和大细胞癌中含PMT方案仍具有明显的治疗优势。鉴于此,美国FDA于2008年9月30日正式批准增加了叶酸酯类似物代谢抑制剂PMT的适应证,允许其与DDP联用作为伴有非鳞状组织学特性的局部晚期和远处转移的NSCLC的一线治疗方案[6]。
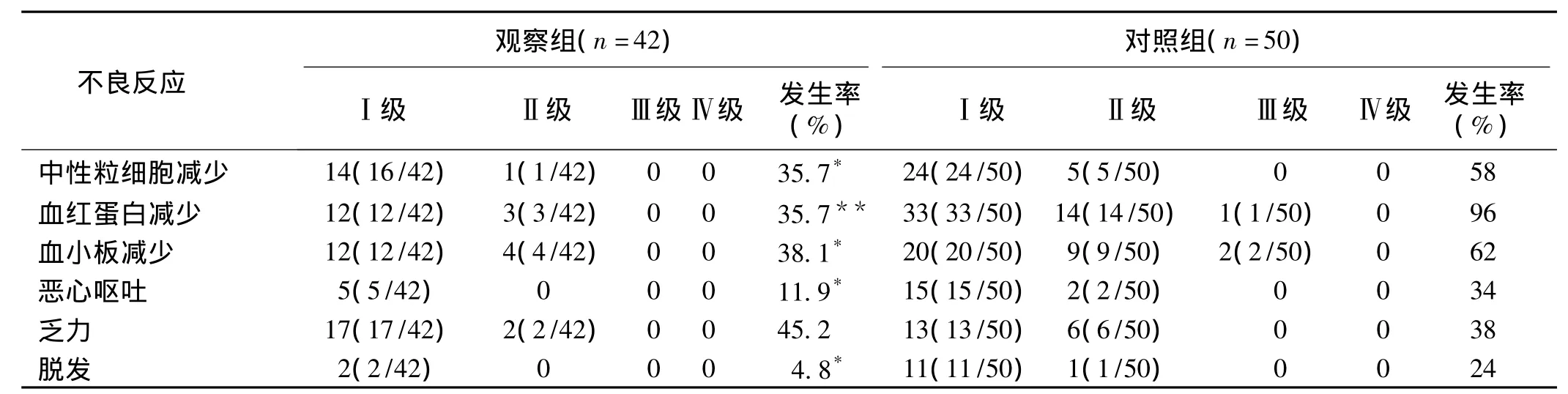
表2 2组患者化疗不良反应比较(n)
在晚期NSCLC的补救化疗中,DOC和PMT较常用,Hanna等[7]研究表明,PMT与泰素帝的总体有效率和中位生存期无明显差异,在不良反应方面,却以泰素帝组明显为高,这一研究奠定了PMT在NSCLC二线治疗中的地位。本研究中观察组RR为52.4%,DCR为88.1%;对照组RR为34%,DCR为82%。2组RR、DCR、中位生存期均无统计学差异,与目前文献报道结果相似。
2006年ASCO年会上再次报道了JMEN试验随访2年后的更新数据,进一步肯定了PMT对一线化疗失败的晚期NSCLC与DOC的疗效相当,但不良反应明显较DOC降低[8]。本组患者不良反应主要为骨髓抑制,其次为胃肠道反应、乏力和周围神经毒性,以Ⅰ~Ⅱ级为主,对照组偶见Ⅲ级不良反应。观察组不良反应显著低于对照组。
综上所述,PMT联合DDP方案和DOC联合DDP方案对晚期NSCLC的近期临床疗效相近,但PMT联合DDP方案组耐受性好,不良反应低于DOC联合DDP方案组,是较为理想的化疗方案,更适合于化疗耐受性较差的晚期NSCLC患者。
[1]Al-Saleh K,Quinton C,Ellis PM.Role of pemetrexed in advanced non-small-cell lung cancer:meta-analysis of randomized controlled trials,with histology subgroup analysis[J].Curr Oncol,2012,19(1):e9-e15.
[2]Treat J,Scagliotti GV,Peng G,et al.Comparison of pemetrexed plus cisplatin with other first-line doublets in advanced non-small cell lung cancer(nsclc):a combined analysis of three phase 3 trials[J].Lung Cancer,2012,76(2):222-227.
[3]Ito S,Ogawa Y,Harada H,et al.Long-term survival of patient with brain metastases from lung cancer treated by pemetrexed monotherapy[J].Gan To Kagaku Ryoho,2012,39(5):793-796.
[4]Scagliotti GV,Park K,Patil S,et al.Survival without toxicity for cisplatin plus pemetrexed versus cisplatin plus gemcitabine in chemonaive patients with advanced non-small cell lung cancer:a risk-benefit analysis of a large phaseⅢstudy[J].Eur J Cancer,2009,45(13):2298-2303.
[5]Scagliotti GV,Parikh P,von Pawel J,et al.PhaseⅢstudy comparing cisplatin plus gemcitabine with cisplatin plus pemetrexed in chemotherapy-naive patients with advancedstage non-small-cell lung cancer[J].J Clin Oncol,2008,26(21):3543-3551.
[6]Huang MS,Tsai JR,Shen MC,et al.Pemetrexed as a possible cause of severe rhabdomyolysis in the treatment of lung cancer[J].Lung Cancer,2012,76(3):491-492.
[7]Hanna N,Shepherd FA,Fossella FV,et al.Randomized phaseⅢtrial of pemetrexed versus docetaxel in patients with non-small-cell lung cancer previously treated with chemotherapy[J].J Clin Oncol,2004,22(9):1589-1597.
[8]Paz-Ares LG,Altug S,Vaury AT,et al.Treatment rationale and study design for a phaseⅢ,double-blind,placebo-controlled study of maintenance pemetrexed plus best supportive care versus best supportive care immediately following induction treatment with pemetrexed plus cisplatin for advanced nonsquamous non-small cell lung cancer[J].BMC Cancer,2010,10:85.
[9]赵富丽,郭人花.培养曲塞加顺铂治疗晚期非小细胞肺癌的效果[J].中国医药导报,2013,10(14):88-90.
