均匀设计优选干蟾中吲哚类生物碱的水提工艺※
2014-02-06王元清严建业
李 伟 王元清 严建业 罗 堃*
均匀设计优选干蟾中吲哚类生物碱的水提工艺※
李 伟1王元清2,3严建业2罗 堃2*
(1湖南省湘潭市中心医院,湘潭411100;2湖南中医药大学药学院中药现代化教育厅重点实验室,长沙410208;3中南林业科技大学生命科学与技术学院生物技术与工程实验室,长沙410004)
目的优选干蟾中吲哚类生物碱的最佳提取工艺。方法以吲哚类生物碱浸出量、浸膏得率为评价指标,对提取次数进行考察;选择浸泡时间、提取时间、溶媒用量等为影响因素,应用均匀设计优选其最佳提取工艺。结果最佳工艺条件为:水提3次,浸泡15min,加水量为14倍、12倍、12倍,提取时间为100min、80min、80min。结论该工艺稳定,可行,能为其工业化生产提供实验依据。
干蟾;均匀设计;提取工艺;吲哚类生物碱
干蟾收载于卫生部部颁标准,为蟾蜍科动物中华大蟾蜍Bufo bufo gargarizans Cantor或黑眶蟾蜍B.melanostictus Schneider的去除内脏的干燥全体[1-2],其提取物具有强心、抗肿瘤、抗病毒、止痛、促进骨髓增生等功效[3-4]。干蟾中有效活性成分主要分为水溶性成分和脂溶性成分,前者主要为吲哚类生物碱,后者主要有酯蟾毒配基等[5]。其中吲哚类生物碱具有较强的抗肿瘤、免疫调节、抗乙肝病毒等多种药理作用。干蟾中吲哚类生物碱的含量较低,有关其提取工艺研究尚未见报道,本文首次采用均匀设计法结合多指标综合评价来优选其水提工艺,为其进一步的制剂开发和工业化生产奠定基础。
1 仪器与材料
1.1仪器SP-756型紫外可见分光光度计(上海光谱仪器有限公司);DGF-4AB型立式电热鼓风干燥箱(天津市泰斯特仪器有限公司);DK-S22型电热恒温水浴锅(上海精宏实验设备有限公司);Shimadzu AY-120型电子分析天平(日本岛津公司)。
1.2材料5-羟色胺(批号:1130661-31205079,供含量测定用,由Sigma公司提供);干蟾(批号:20101206,湖南省医药销售有限公司提供),经湖南中医药大学药学院刘塔斯教授鉴定;对二甲氨基苯甲醛、盐酸等均为分析纯;水为蒸馏水。
2 方法与结果
2.1吲哚类生物碱的含量测定[6]
2.1.1对照品溶液的制备精密称取5-羟色胺对照品0.0062g,置于10mL量瓶中,加甲醇超声溶解,定容至刻度。精密移取0.5m L置于10mL量瓶中,加甲醇稀释至刻度,摇匀,即得(浓度为31μg/mL)。
2.1.2标准曲线的建立精密量取5-羟色胺对照品溶液0.5、1.5、2.5、3.5、5.0mL,分别置于10mL量瓶中,各加水至5mL,摇匀。加15%对二甲氨基苯甲醛盐酸溶液(2→3)至刻度,摇匀,放置30min,照分光光度法,以水做空白对照(5mL水加5mL15%对二甲氨基苯甲醛盐酸溶液,摇匀),在555nm的波长处测定吸光值。以5-羟色胺浓度(C)对吸光度(A)作标准曲线,得回归方程为:A =0.0031C+0.0855(r=0.9996),提示5-羟色胺浓度在1.55~15.5μg/mL范围内与吸收度线性关系良好。
2.1.3样品溶液中吲哚类生物碱的含量测定精密量取各样品溶液2mL,置于10mL量瓶中,依法显色,测定吸光度,并计算含量。
2.2浸膏得率的测定精密吸取样品液25mL,置于105℃已干燥至恒重(W1)的蒸发皿中,水浴蒸干,于105℃真空干燥3h,置干燥器中冷却30min,迅速称重(W2),按下列公式计算,即得。
浸膏得率%=[(W2-W1)×V提取液总)/(M干蟾×25)]×100%。其中:V提取液总表示提取液的总体积(mL),M干蟾表示每次投的干蟾的重量(mg)。
2.3提取工艺研究
2.3.1提取次数的考察称取干蟾10g,加水浸泡0.5小时,加热回流提取三次,加水量分别为10倍、8倍、8倍,提取时间分别为1.5h、1.0h、1.0h。分别收集各次提取液,定容,备用。取提取液,按前述方法分别测定吲哚类生物碱含量。结果表明,前两次提取量占三次提取总量的73%,提示两次提取不完全,因而需提取3次为宜。
2.3.2药材粒径的考察称取干蟾10g,共三份,分别为最粗粉、粗粉、中粉,加水浸泡0.5小时,加热回流提取三次,加水量分别为10倍、8倍、8倍,提取时间分别为1.5h、1.0h、1.0h。收集提取液,定容,备用。取提取液,按前述方法分别测定吲哚类生物碱含量。结果发现,最粗粉、粗粉、中粉的含量分别为1.128、1.322、1.319mg/g。可见,干蟾粉碎成粗粉时,吲哚类生物碱的浸出量较高,因而选择粉碎成粗粉为宜。
2.3.3浸泡时间的考察称取干蟾10g,粉碎成粗粉,共四份,各加水浸泡时间为0min、30min、60min、90min,加水倍量均为10倍、8倍、8倍,提取时间为1.5h、1.0h、1.0h,分别提取,收集提取液,按前述方法分别测定吲哚类生物碱含量。结果发现,加水浸泡0min、30min、60min、90 min时吲哚类生物碱含量分别为1.036、1.318、1.315、1.321mg/g。可见,干蟾药材浸泡30 min左右时,总生物碱的浸出量较高,因而选择浸泡30min为宜。
2.3.4U5*(53)均匀设计试验[7]优选提取工艺依据单因素试验考察结果,并考虑中药提取工艺的主要影响因素,选择提取时间、浸泡时间、加水倍量为考察因素,以吲哚类生物碱含量和浸膏得率为评价指标,用U5*(53)均匀设计表安排试验(见表1),依法进行测定、计算(见表2)。

表1 U5*(53)均匀设计因素水平表
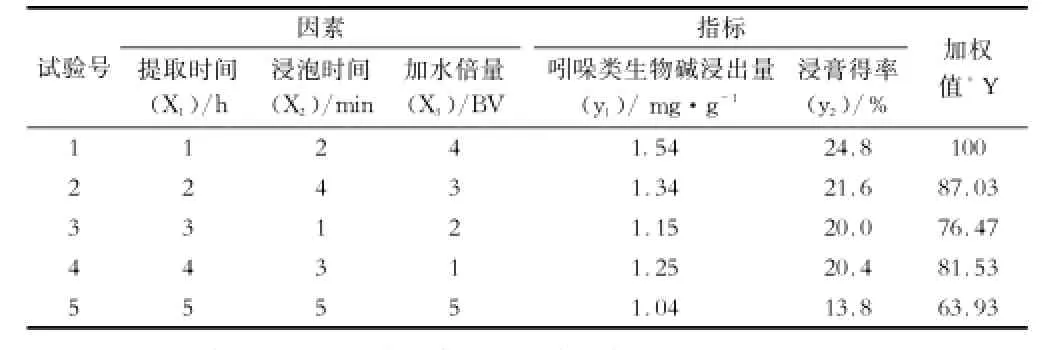
表2 U5*(53)均匀设计实验结果
采用spss15.0统计软件对上述均匀设计试验结果运用后退回归法进行回归分析。加权值Y与因素X1、X2、X3关系的分析:以Y对X1、X2、X3及其交叉项进行后退回归,得回归方程:Y=63.346+0.197 X1X3。其复相关系数P=0.924;调整决定系数Ra=0.854;F= 17.495,P=0.025<0.05。表明该方程具有统计学意义。方程中只保留了X1X3项,表明X1与X3存在一定的交互作用。X1X3的系数为正值,显示与加权值呈正相关。
最佳提取条件的确定:根据上述相关性的分析,因素X1X3项的系数为正值,X1与X3均大于或等于0,当它们增大时,Y也增大。因此因素X1可定为最大值4.75h,X3可定为最大值38倍,代入方程,得方程Y=63.346+ 0.197 X1X3,计算出y的理论预测值为98.90。X2对Y没有影响,为节约时间,提高效率,又使干蟾较充分润湿,可将浸泡时间定为15min。因此,干蟾中吲哚类生物碱的最佳水提工艺为:加水浸泡15min,加水量分别为14倍、12倍、12倍,提取时间分别为100min、80min、80min。
2.3.5验证试验取3批干蟾药材,每批100g,均按最佳水提工艺提取3次,分别测定吲哚类生物碱浸出量和浸膏得率(见表3)。结果表明,该工艺稳定、可行。
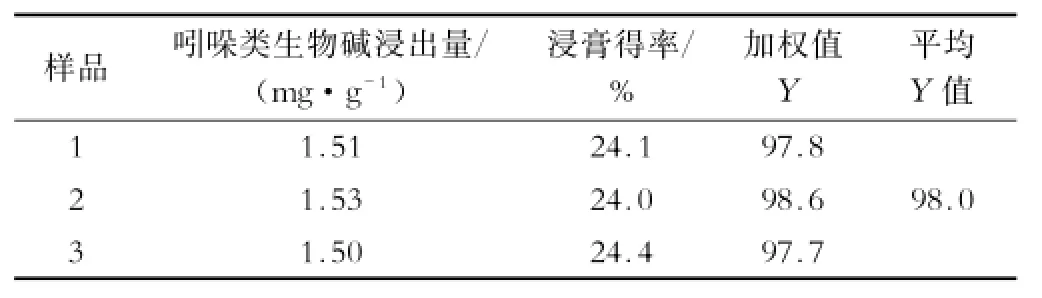
表3 验证试验结果
3讨论
有关蟾蜍的药用药材有干蟾、蟾皮、蟾酥、蟾衣等,其中干蟾和蟾皮在市场流通过程中有混用现象,其化学成分和临床应用研究报道较多,而有关其吲哚类生物碱的提取工艺研究较少。本试验优选出了干蟾中吲哚类生物碱的最佳提取工艺条件,验证试验结果表明该工艺稳定、可行,可为其进一步的制剂开发和工业化生产提供参考。
本试验中比色法测定的基本原理:吲哚类生物碱分子中的芳伯胺可与芳醛(如对二甲氨基苯甲醛)发生缩合反应,在酸性溶液中生成有色的希夫氏碱,此有色物质在某个波长处有明显的吸收峰。试验结果表明,此法专属性强,方法灵敏,重现性好,操作简便。在试验过程中,发现样品的最佳含量测定条件为:温度控制在20℃以上,加入显色剂后,样品在20~30min内测定,吸收值稳定。
[1]中华人民共和国卫生部药典委员会.中华人民共和国卫生部药品标准·中药材第一册[S].1992:4.
[2]卫生部药政管理局,中国药品生物制品检定所.中药材手册[M].1990:629.
[3]张绍杰,刘诚进.浅谈蟾蜍的药用价值[J].中华临床医学研究杂志,2007,13(10):1397-1398.
[4]逯华,陈日新.华蟾素抗恶性肿瘤的研究进展[J].右江民族医学报,2009,1(5):895-896.
[5]董岩,罗濛,姜同英,等.华蟾素注射乳剂的制备及制剂质量的研究[J].沈阳药科大学学报,2009,26(1):6-9.
[6]王元清,严建业,喻林华,等.华蟾素分散片溶出度的研究[J].中成药,2008,30(11):1667-1669.
[7]王元清,严建业,陈志文,等.均匀设计优选玉米须中总黄酮和多糖的水提工艺[J].食品与机械,2010,136(2):104-106.
Optimizing the water extracting conditions of Indole Alkaloids from Siccus Bufo by uniform design
LiWei1Wang Yuanqing2,3Yan Jianye2Luo Kun2✫
(1 Xiangtan Central Hospital,Hunan Xiangtan provicine,411100,China;2 Key Lab of Modernization of Chinese Medicine,collega of Pharmacy,Hunan University of Chinese M edicine,Changsha 410208,China;3 Lab of Biotechnology and Engineering,College of Life Science and Technology,Central South University of Forestry and Technology,Changsha 410004,China)
ObjectiveTo study the optimum extracting process for indole alkaloids from Siccus Bufo.MethodsThe extraction rate of extractum and extraction amount of indole alkaloids of Siccus Bufo were choosen as the assessment index,with solvent volume,macerating time and extracting time as examming factor,the optimum extraction progress was selected with the uniform design.ResultsThe optimum extraction progress conditions were as follows:macerated for 15 min in water,decocting for 3 times,with water of 14,12,12 times of the drug mixture respectively,105 min,80min,80min respectively.ConclusionThe extraction process of optimization can extract more indole alkaloids,and can provide the test foundation for production.
Siccus Bufo;uniform design;extraction process;indole alkaloids
10.3969/j.issn.1672-2779.2014.04.091
:1672-2779(2014)-04-0144-03
苏 玲 本文校对:林丽美
2013-11-06)
湖南中医药大学青年基金项目[No:99820001];湖南省高校科技创新团队资助项目[No:湘教通(2010)212号]
*通讯作者
