加标浓度直读法测定茶叶中不同溶解特性的铜
2014-01-18高向阳魏姜勉
高向阳,魏姜勉,张 娜
(1.郑州科技学院食品科学与工程学院,河南 郑州 450064;2.河南农业大学食品科学技术学院,河南 郑州 450002)
加标浓度直读法测定茶叶中不同溶解特性的铜
高向阳1,2,魏姜勉2,张 娜1
(1.郑州科技学院食品科学与工程学院,河南 郑州 450064;2.河南农业大学食品科学技术学院,河南 郑州 450002)
建立测定茶叶中不同溶解特性铜的一种新方法。茶叶样品依次经过水溶、醇溶和微波消解后,用铜离子选择性电极加标浓度直读法测定。结果表明:pH 4.00的总离子强度调节缓冲剂中,1.00 mol/L硝酸钾和1.00 mol/L氟化钠溶液的最佳用量均为5.00 mL。所用铜电极有良好的能斯特响应,转换系数大于93%。实验条件下,茶叶样品测定的相对标准偏差为2.4%(n=11)、加标回收率为94.38%~101.22%,铜离子的检出限为1.20×10-6mol/L,与国家标准方法进行对照,测定的结果令人满意。
加标浓度直读法;茶叶;铜;溶解特性
铜是人体30多种酶的活性成分,参于生长激素、脑垂体素等重要的生命活动,能促进铁在胃肠道中吸收,促进红细胞成熟,具有保持血管弹性、骨骼坚韧性、调节心搏的作用,是有机体必需的微量元素[1-2]。缺铜会导致精神发育停滞、运动障碍和全面营养不良。但摄入过多铜会危害机体,国家标准规定茶叶中铜含量不得高于60 mg/kg[3]。过量铜对机体的危害不仅取决于总量的多少,而且与其溶解特性有关。水溶态活性最强,醇溶态次之,残渣态活性最弱[4]。因此,测定茶中不同溶解形态中铜的含量,有利于了解铜的毒害机理,对保障食品安全有一定的现实意义。
目前,铜的检测方法主要有分光光度法[5-7]、硫胺素荧光光度法[8]、催化动力学分析法[9-10]、电位溶出法[11]、溶出伏安法[12]、原子吸收光谱法[13-18]、高效液相色谱法[19]和电感耦合等离子体发射光谱法[20-22]、电感耦合等离子体-质谱法[23-24]等。以上方法中,光度法与电位溶出法灵敏度较低,原子吸收法、高效液相色谱法和等离子发射光谱法仪器昂贵、操作繁琐、成本较高。加标浓度直读法具有操作简单、灵敏准确、成本低廉、设备携带方便,适用于现场检测,无需作图和进行复杂计算的显著优点,已在食品分析领域得到应用。但测定茶叶中不同溶解形态的铜未见文献报道,本实验采用铜离子选择性电极,以加标浓度直读法进行测定,建立一种快速测定茶叶中不同溶解特性铜的新方法,用于实际样品的分析,结果令人满意,有一定的推广应用价值。
1 材料与方法
1.1 材料与试剂
信阳毛尖、铁观音、竹叶青购自郑州市丹尼斯超市。所用水为二次去离子水,所用试剂均为分析纯。
1.2 仪器与设备
铜离子选择性电极、217型双盐桥饱和甘汞电极、PXSJ-216型离子分析仪、温度自动校正传感器 上海精密科学仪器有限公司;KQ-250E型超声清洗器 昆山市超声仪器有限公司;微波消解仪 上海新仪微波化学科技有限公司;TDL-5-A型离心机 上海安亭科学仪器厂;SYZ-B型石英亚沸高纯水蒸馏器 江苏省宜兴市勤华石英玻璃仪器厂;电热恒温干燥箱 上海新苗医疗器械制造有限公司;710ES型全谱直读电感耦合等离子体发射光谱仪 美国瓦里安公司。
1.3 方法
1.3.1 溶液的配制
10.00 mmol/L铜离子标准贮备液:准确称取三水合硝酸铜1.208 00 g,用重蒸水定容于500 mL容量瓶,混匀,用时逐级稀释。
总离子强度调节缓冲调节剂:1)1.00 mol/L硝酸钾溶液:准确称取经105 ℃烘至恒质量的硝酸钾50.500 0 g,用重蒸水定容于500 mL容量瓶,混匀。2)1.00 mol/L氟化钠溶液:准确称取经105 ℃烘至恒质量的氟化钠21.000 0 g于塑料杯中,用重蒸水定容于50 0 mL容量瓶,混匀后移至塑料瓶中备用。3)pH 4.00的HAc-NaAc缓冲液。
0.1 0 m m o l/L铜离子A标定液:用移液枪取10.00 mmol/L铜离子标准贮备液0.50 mL于塑料杯中,加入1.00 mol/L硝酸钾5.00 mL,用5.00 mol/L硝酸调pH 4.00,加pH 4.00的HAc-NaAc缓冲液5.00 mL,加入1.00 mol/L氟化钠5.00 mL,移至50 mL容量瓶,用调节pH 4.00的重蒸水定容,混匀,移至塑料杯中备用。
1.00 mmol/L铜离子B标定液:取10.00 mmol/L铜离子标准贮备液5.00 mL于塑料杯中,加1.00 mol/L硝酸钾5.00 mL,用5.00 mol/L硝酸调pH 4.00,加入pH 4.00的HAc-NaAc缓冲液5.00 mL,加入1.00 mol/L氟化钠5.00 mL,移至50 mL容量瓶,用调节pH 4.00的重蒸水定容,混匀后移至塑料杯中,备用。
铜离子空白溶液:取1.00 mol/L硝酸钾5.00 mL,用5.00 mol/L的硝酸调pH 4.00,加入pH 4.00的HAc-NaAc缓冲液5.00 mL,加入1.00 mol/L氟化钠5.00 mL,移至50 mL容量瓶,用调节pH 4.00的重蒸水定容,混匀后移至塑料杯中备用。
5.00 mmol/L铜离子标准溶液:吸取10.00 mmol/L铜离子标准贮备液25.00 mL于塑料杯中,加入1.00 mol/L硝酸钾5.00 mL,用5.00 mol/L的硝酸调pH 4.00,加入pH 4.00的HAc-NaAc缓冲液5.00 mL,加1.00 mol/L氟化钠5.00 mL,移至50 mL容量瓶,用调节pH值为4.00的重蒸水定容,混匀后移至塑料杯中备用。
1.3.2 样品的处理与测定
水溶态:用研钵将茶叶研磨至全部过60目尼龙筛,用四分法取样,称取样品5 g左右(准至0.000 1 g)于100 mL容量瓶中,用重蒸水定容,置于功率250 W频率40 kHz的超声清洗器中超声1 h,将样品水溶液倒入离心杯中,2 000 r/min离心3 min,取上清液10.00 mL置于小烧杯中,在电热板上蒸至约1 mL,移至消解罐中,用7.00 mL硝酸分数次洗涤烧杯并移至消解罐中,再加1.00 mL双氧水后密封。按表1程序消解,冷却后,排除酸雾。用少量重蒸水冲洗罐体,并移入烧杯中,加入1.00 mol/L硝酸钾5.00 mL,用1.00 mol/L氢氧化钠溶液调pH 4.00,加入pH 4.00 HAc-NaAc缓冲液5.00 mL,加入1.00 mol/L氟化钠5.00 mL,移至50 mL容量瓶,用调节pH 4.00的重蒸水定容,混匀后移至塑料杯中备用。
醇溶态:水溶后的残渣置于小烧杯中,于105 ℃烘箱中烘干,用80%乙醇溶液冲洗烧杯并定量移至100 mL容量瓶中定容,在超声清洗器中超声1 h,将样品醇溶液倒入离心杯中,2 000 r/min离心3 min,取上清液10.00 mL置于小烧杯中,在电热板上蒸至约1 mL,移至消解罐中,用7.00 mL硝酸分数次洗涤烧杯并移至消解罐中,再加1.00 mL双氧水后密封。按表1程序消解,冷却后,排除酸雾。以下操作同水溶态。
残渣态:将醇溶后的残渣置于小烧杯中,于105 ℃烘箱中烘干,分6份置于六联罐中。各加8.00 mL硝酸,30 min后补加2.00 mL硝酸和1.00 mL双氧水,密封好罐体,按表1程序消解,冷却后,排除酸雾。将6 个罐体中的液体合并至小烧杯,在电热板上蒸至约1 mL,用重蒸水冲洗罐体至小烧杯并转移到100 mL容量瓶中定容,混匀。取消解液10.00 mL于烧杯中,加1.00 mol/L硝酸钾5.00 mL。以下操作同水溶态。
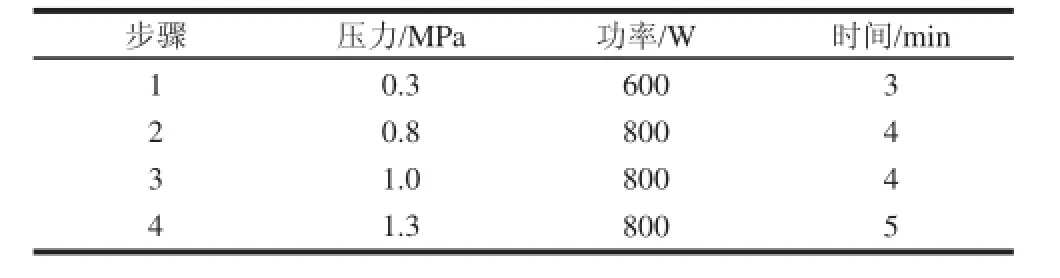
表1 微波压力消解参数的设定Table 1 Microwave digestion parameters
按仪器说明书安装和校正好仪器后,在仪器起始状态下,按“模式/4”键,进入“已知添加”功能,选择浓度单位“mmol/L”;输入添加标液的体积值0.50 mL,输入试液的体积值50.00 mL和标液的浓度值10.00 mmol/L,将处理好的电极对和温度传感器放入待测液中,仪器显示当前的电位值和温度值,稳定3 min,等显示稳定后,按“确认”键,仪器显示“添加标液”字样,添加10.00 mmol/L的铜离子标准液0.50 mL后,稳定3 min,等再次显示稳定,按“确认”键,仪器即直接显示试液中铜的浓度c。按下式计算茶叶干基样品中不同溶解特性铜的质量分数(ω)。
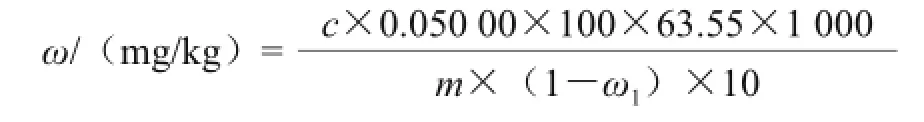
式中:c为试液中铜离子的浓度/(mmol/L);m为样品质量/g;ω1为样品含水的质量分数/%;0.050 00为测定时所用试液的体积/L。
2 结果与分析
2.1 样品水分测定
称取茶叶样品5 g左右(准至0.000 1 g),按国标[25]各进行3次平行测定,检验无可疑值后取平均值报告。结果表明:信阳毛尖、铁观音、竹叶青样品中水分的质量分数分别为2.26%、3.59%和4.32%。
2.2 铜选择性电极的转换系数
按照电极使用说明对所用铜电极进行斜率校准,用两点校准法测得铜电极的实际响应斜率为27.536,因理论斜率为29.580,由此计算出所用电极的转换系数为93.09%,表明该电极的能斯特响应良好。
2.3 总离子强度缓冲调节剂
2.3.1 硝酸钾添加量的影响
对浓度为5.00 mmol/L的铜离子标准溶液,分别加入1.00 mol/L硝酸钾溶液0.00、1.00、2.00、3.00、4.00、5.00、6.00、7.00 mL,按照实验方法各进行5次平行测定,取平均值。以硝酸钾溶液体积为横坐标,以铜离子浓度为纵坐标作图,结果见图1。
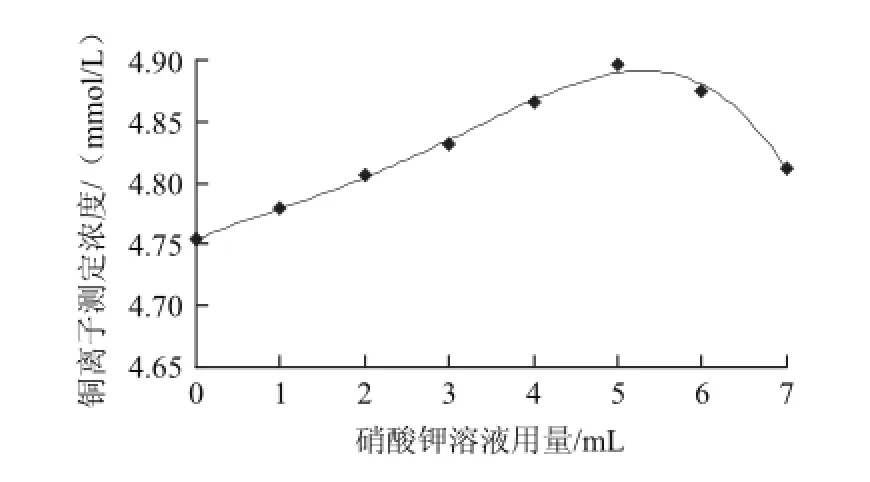
图1 硝酸钾用量对铜离子浓度测定的影响Fig.1 Effect of the amount of added potassium nitrate on the determination of copper ion concentration
由图1可知,1.00 mol/L硝酸钾溶液用量为5.00 mL时,测定体系有较大的测定信号。
2.3.2 氟化钠添加量的影响
对浓度为5.00 mmol/L的铜离子标准溶液,分别加入1.00 mol/L氟化钠溶液0.00、1.00、2.00、3.00、4.00、5.00、6.00、7.00 mL,按照实验方法各进行5次平行测定,取平均值。以氟化钠溶液用量为横坐标,以铜离子浓度为纵坐标作图,结果见图2。
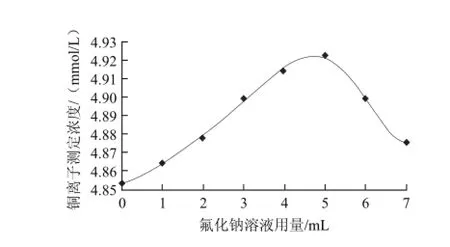
图2 氟化钠用量对铜离子浓度测定的影响Fig.2 Effect of the amount of added sodium fluoride on the determination of copper ion concentration
由图2可知,1.00 mol/L氟化钠溶液用量为5.00 mL时,测定体系有较大的测定信号。
2.3.3 pH值的影响
分别调节5.00 mmol/L铜离子标 准溶液的pH值为3.00、3.50、4.00、4.50、5.00、5.50,按照实验方法各进行5次平行测定,取平均值。以pH值为横坐标,以铜离子浓度为纵坐标作图,结果见图3。
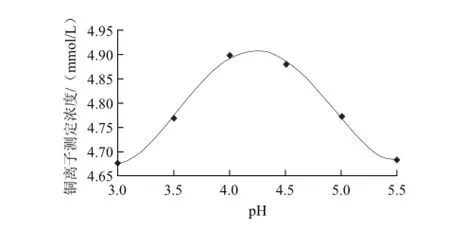
图3 pH值对铜离子浓度测定的影响Fig.3 Effect of pH of the copper standard solution on the determination of copper ion concentration
由图3可知,测定体系pH值为4.00时,铜离子有较大的测定信号。
2.4 温度的影响
溶液温度的影响可以通过仪器所带的温度传感器自动进行校正。
2.5 超声功率
所用超声波清洗器的额定功率为250 W,实验表明:在此功率和实验条件下对样品超声1 h,测定效果理想。
2.6 样品测定结果
按照实验方法,对茶叶样品中不同溶解特性的铜分别进行5次平行测定,检验无可疑值后取平均值报告,结果见表2。
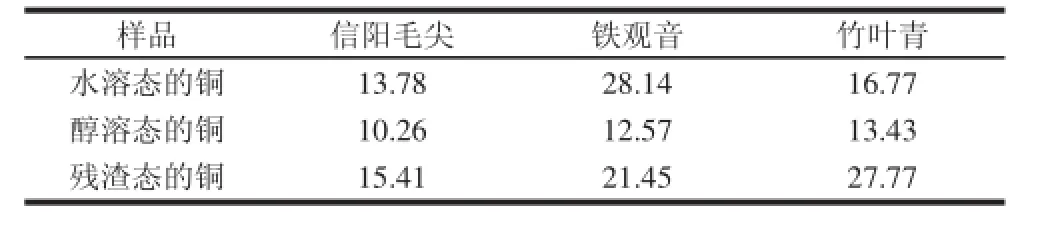
表2 样品测定结果Table 2 Determination results of real samples mg/kg 干基
由表2可知,所分析干基样品中,信阳毛尖、竹叶青残渣态铜含量高于水溶态和醇溶态铜,铁观音样品残渣态铜低于水溶态,3种茶叶的水溶态铜均高于醇溶态铜。水溶态铜的质量分数依次为铁观音>竹叶青>信阳毛尖。水溶态铜占总铜的溶出比为铁观音45.27%、信阳毛尖34.93%、竹叶青28.92%。
2.7 检出限和定量限
对1.00×10-5mol/L的硝酸铜溶液,在与样品相同条件下进行11次平行测定,按3倍信噪比计算的检出限为1.20×10-6mol/L,按10倍信噪比计算的定量限为4.00×10-6mol/L。
2.8 测定精密度
实验条件下,对竹叶青水溶态的铜进行11次平行测定,结果见表3。

表3 精密度的测定结果Table 3 Results obtained in the validation of the method for precision
由表3可知,样品1 1次平行测定的平均值为16.77 mg/kg,相对标准偏差为2.4%。
2.9 加标回收率
准确称取竹叶青样品各5.000 0 g,分别在水溶态、醇溶态、残渣态样液中加入10.00 mmol/L铜离子标准贮备液5.00 mL,按照实验方法进行3次加标回收率实验,检验无可疑值后,取平均值,结果如表4所示。由表4可知,加标平均回收率为94.38%~101.22%。
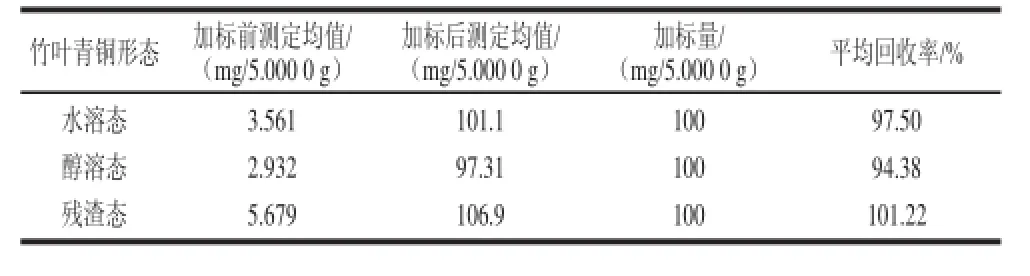
表4 回收率测定结果(n=3)TTaabbllee 44 SSppiikkee rreeccoovveerriieess ooff ddiiffffeerreenntt ccooppppeerr ssppeecciieess ((n = 3)
2.10 干扰实验
取1.00×10-5mol/L硝酸铜标准溶液10.00 mL于50 mL容量瓶,加入1.00 mol/L硝酸钾5.00 mL,用5.00 mol/L的硝酸调pH 4.00,加入pH 4.00的HAc-NaAc缓冲液5.00 mL,加入1.00 mol/L氟化钠5.00 mL。取浓度分别为0.100 0、0.010 0、0.001 0 mol/L的硝酸铅、氯化钠、三氯化铝、三氯化铁溶液10.00 mL于上述硝酸铜标准溶液中,定容至50 mL。通过离子分析仪的加标浓度直读功能读出铜离子的浓度。结果表明:1 000倍Cl-、Pb2+,100倍的Al3+、Fe3+离子对测定无干扰。
2.11 对照测定
按本法处理和微波消解水溶态、醇溶态和残渣态信阳毛尖样品,消解液按照国标法[26]和本法各进行5次平行测定,检验无可疑值后取平均值报告,经F检验和t检验表明:本法与国标法比较,测定结果不存在显著性差异,结论的置信度为95%。
3 结 论
将微波压力消解技术与加标浓度直读法结合,使两者的优点得到充分发挥。该法具有操作简单,快速方便,读数直观,无需作图和进行复杂计算,所用离子分析仪的质量仅为1 kg,小巧便携,适用于现场检测。在总离子强度缓冲调节剂pH 4.00,加1.00 mol/L硝酸钾溶液5.00 mL和1.00 mol/L氟化钠溶液5.00 mL时,该法测定茶叶中水溶态、醇溶态和残渣态铜结果满意。实验可知:铜选择性电极的转换系数为93.09%,表明所用电极有良好的能斯特响应,对竹叶青茶叶样品测定的相对标准偏差为2.4%(n=11)、加标回收率为94.38%~101.22%,铜离子的检出限为1.20×10-6mol/L,与国标法对照,测定结果不存在显著性差异。
[1] OUZOUNIDOU G. Changes of photosynthetic activities in leaves as a result of Cu-treatment: dose-response relations in Silene and Thlaspi[J]. Photosynthetica, 1993, 29: 455-462.
[2] REBOREDO F, HENRIQUES F. Some observations on the leaf ultrastructure of Halimione portulacaides(L.) Aellen grown in a medium containing copper[J]. Journal of Plant Physiology, 1991, 137: 453-467.
[3] 卫生部. GB 9679—1988 茶叶卫生标准[S]. 北京: 中国标准出版社, 1988.
[4] 杨居荣, 查燕, 刘虹, 等. 污染作物籽实中铜的分布、结合形态及其毒性[J]. 农业环境保护, 2001, 20(4): 199-201.
[5] 虞学俊, 李在均. 光度法测定食品中的微量铜[J]. 理化检验: 化学分册, 2005, 41(12): 937-938.
[6] 马晓贝, 张丽萍, 崔丽萍. 茶水中铜含量的分析方法研究[J]. 现代仪器, 2008, 14(4): 75-76.
[7] 刘璇, 冯志明. BCA法测定食品中的微量铜[J]. 食品科学, 2011, 32(14): 277-280.
[8] 兰昌云, 徐飞, 张莉, 等. 硫胺素荧光光度法测定食品中痕量铜[J].广东微量元素科学, 2012, 19(12): 13-16.
[9] 严小平. 催化动力学褪色分光光度法测定痕量铜(Ⅱ)及其在食品中的应用[J]. 光谱实验室, 2010, 27(6): 2167-2169.
[10] 朱庆仁, 耿明, 孙登明. 双波长双指示剂催化动力学光度法测定食品中的痕量铜[J]. 分析科学学报, 2010, 26(2): 240-242.
[11] 张丽. 电位溶出法同时测定茶叶中的铅、铜[J]. 食品研究与开发, 2006, 27(5): 120-121.
[12] 赖塔, 丘福保, 徐镇耿, 等. 微波消解-溶出伏安法对食品中铜、铅、镉的同时测定[J]. 分析测试学报, 2010, 29(2): 203-206.
[13] 李晶, 宋静. 火焰原子吸收光谱法测定茶叶中的铜[J]. 中国食物与营养, 2011, 17(4): 63-65.
[14] 张红艳, 肖英. 原子吸收光谱法测定大米粉中铜含量的不确定度[J].粮油食品科技, 2011, 19(2): 33-34.
[15] 赵西梅, 肖忠峰. FAAS测定3种菊花茶中8种金属元素的含量[J].食品研究与开发, 2008, 29(8): 123-124.
[16] 宋慧, 陈尚龙, 李超, 等. 火焰原子吸收光谱法测定牛奶中不同化学形态的钙[J]. 食品科学, 2012, 33(22): 278-281.
[17] 何奕波, 严静. 火焰原子吸收光谱法测定食用菌中铜、锰、铁、锌含量[J]. 理化检验: 化学分册, 2010, 46(3): 324-324; 326.
[18] 温圣平, 江秀明, 吕素敏, 等. 改性豆皮固相萃取-火焰原子吸收光谱法测定食品样品中痕量铜[J]. 分析化学, 2009, 37(A1): 16.
[19] 苏新国, 杨春燕. 高效液相色谱分析法测定几种煲汤药材金属元素含量[J]. 食品科学, 2007, 28(7): 403-405.
[20] 范维刚, 侯晓东. ICP-AES法测定某蔬菜地土壤中铜、锌、铅、镉[J].计量与测试技术, 2012, 39(6): 13-15.
[21] 王素燕, 黄志宏. ICP-AES测定茶叶及土壤中的铜和铅[J]. 安全与检测, 2010, 26(1): 64-66.
[22] 胡晓江. 微波消解-电感耦合等离子体发射光谱法测定葡萄酒中铁、铜含量[J]. 食品工程, 2010, 12(4): 55-57.
[23] 戴骐, 吴艳燕, 张伟, 等. 电感耦合等离子体质谱(ICP-MS)法测定动植物源食品中有害元素铅、砷、镉、汞、铜的含量[J]. 食品科技, 2009, 34(12): 315-317.
[24] 胡进, 陆锡锋, 张成, 等. 微波消解-电感耦合等离子体质谱测定海带中铅、镉、铬、铜和锌[J]. 食品科学, 2012, 33(20): 286-288.
[25] 卫生部. GB 5009.3—2010 食品中水分的测定[S]. 北京: 中国标准出版社, 2010.
[26] 国家质量监督检验检疫总局. SN/T 2056—2008 进出口茶叶中铅、砷、镉、铜、铁含量的测定[S]. 北京: 中国标准出版社, 2008.
Determination of Copper Ions with Different Dissolution Characteristics in Tea by Concentration Direct-Reading Method after Standard Solution Addition
GAO Xiang-yang1,2, WEI Jiang-mian2, ZHANG Na1
(1. School of Food Science and Engineering, University for Science and Technology Zhengzhou, Zhengzhou 450064, China; 2. College of Food Science and Technology, Henan Agricultural University, Zhengzhou 450002, China)
A new method to detect copper ions with different dissolution characteristics in tea was established. After sequential extraction of tea samples with water and alkali, the remaining residue was microwave-digested and detected with a copper-selective electrode by directly reading the concentrations of copper ions. Results showed that the optimal amounts of 1.00 mol/L potassium nitrate and 1.00 mol/L sodium fluoride added were both 5.00 mL in total ionic strength adjustment buffer (TISAB) at pH 4.00. The conversion factor of the copper ion selective electrode was more than 93%, indicating that the Nernst response of this electrode is quite good. Under these experimental conditions, the relative standard deviation for 11 repeated determinations of tea samples was 2.4%, the spike recoveries were in the range of 94.38%–101.22%, and the detection limit was 1.20 × 10-6mol/L. Satisfactory analytical results were obtained by using the method in comparison to the national standard method.
concentration direct-reading after standard solution addition; tea; copper; dissolution characteristics
TS207.3
A
1002-6630(2014)04-0146-05
10.7506/spkx1002-6630-201404030
2013-05-07
河南省重点学科建设基金项目(10466-X-082301)
高向阳(1949—),男,教授,本科,主要从事农产品质量与安全检测、食品快速分析技术、天然资源与开发研究。E-mail:ndgaoxy@163.com
