植物甾醇酯的化学合成及其分离研究进展
2014-01-09许青青金文彬苏宝根杨亦文任其龙
许青青 金文彬 苏宝根 杨亦文 任其龙
植物甾醇酯的化学合成及其分离研究进展
许青青1,2金文彬1苏宝根1杨亦文1任其龙1
(浙江大学生物质化工教育部重点实验室1,杭州 310027)
(衢州学院化学与材料工程学院2,衢州 324000)
植物甾醇具有降低血清胆固醇、独特的消炎、退热及抗肿瘤等功能,但其不溶于水,脂溶性也相当有限的缺点限制了其应用前景。酯化后的植物甾醇酯不仅大大改善了植物甾醇的脂溶性,而且抑制人体对胆固醇的吸收作用优于植物甾醇。植物甾醇酯的合成正成为世界各国竞相研究的热点。目前,已报道的制备方法主要有化学合成法、脂肪酶催化法和超临界生物酶法。后两者均采用酶做催化剂,由于酶的生产成本高,且酶法生产率低限制了其大规模工业化生产,因此化学合成法仍然是植物甾醇酯商业化生产的主要方法和研究重点。本文以此为重点,综述了近年来植物甾醇酯的化学合成及其分离纯化技术的研究概况和最新进展,并展望了未来的研究方向。
植物甾醇 植物甾醇酯 化学合成 分离纯化 研究进展
植物甾醇是一种天然活性物质,存在于多种水果、蔬菜、豆类、坚果、谷类及其它植物性食品中,除了众所周知的具有降低血清胆固醇外,还具有独特的消炎、退热、抗肿瘤、抗氧化、美容、抑制血小板凝聚及调节动物生长等功能,广泛应用在食品、保健、医药以及化工等领域。植物甾醇种类繁多,至今发现已有100多种,常见的为β-谷甾醇(β-Sitosterol)、豆甾醇(Stigmasterol)、菜油甾醇(Campesterol)和菜籽甾醇(Brassicasterol)等4种4-无甲基甾醇,其分子的基本骨架由3个六元环和一个五元环组成,C-3位连有一个羟基,C-17位连有一个由8~10个碳原子构成的脂肪族侧链,C-5位上为双键。植物甾醇的基本结构及常见的4-无甲基甾醇的分子结构如图1所示。
从图1可以看到,植物甾醇的分子结构中甾体的多元环及C-17位上连有8~10个碳原子组成的烃链导致其在水中的溶解度极小,C-3位羟基使其在油相中的溶解度相当有限,而且其熔点较高,从而限制了其实际应用范围。植物甾醇的C-3位羟基是重要的活性基团,可与脂肪酸化合形成植物甾醇酯。酯化后的甾醇酯大大改善了植物甾醇的脂溶性,且熔点也更低;甾醇酯可通过胰胆固醇脂酶水解成为游离甾醇被人体吸收,降胆固醇效果优于甾醇[1-2];甾醇酯还保护了甾醇中活泼的C-3位羟基,增强了稳定性。
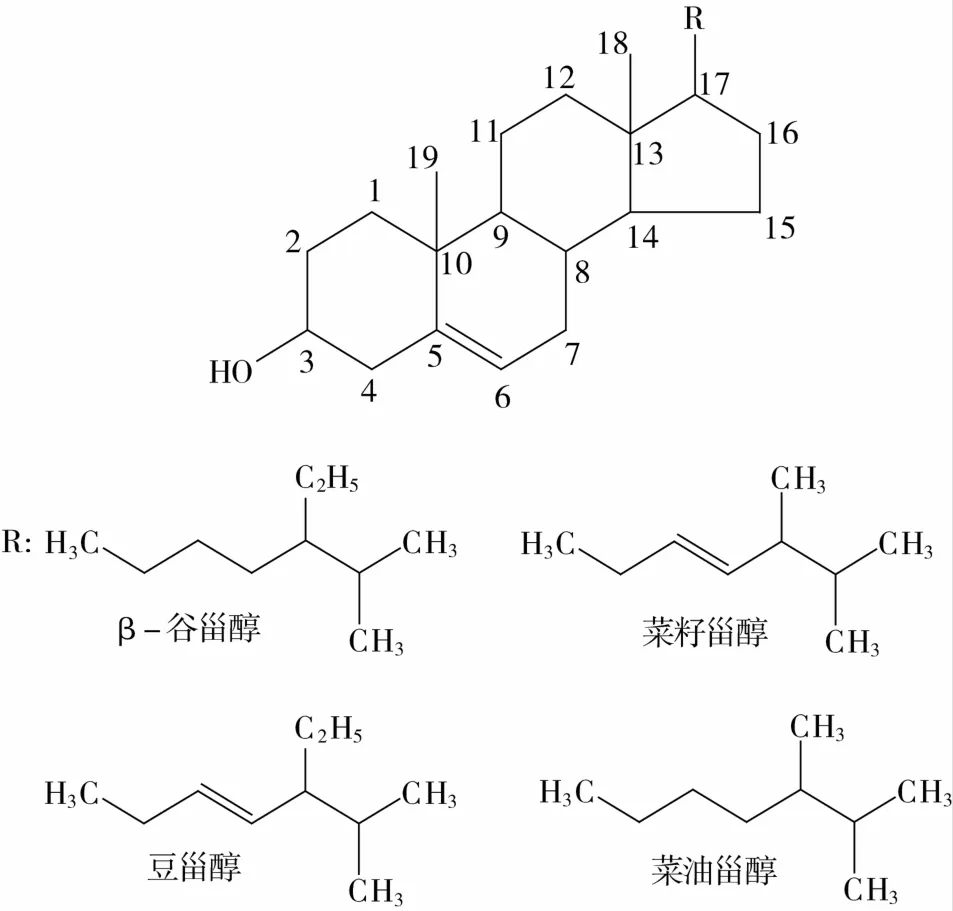
图1 植物甾醇的基本结构及常见的植物甾醇的分子结构
国外自90年代初就开始研究植物甾醇酯制备工艺,并将其添加到油脂和食品中。甾醇酯的安全性已经得到了世界多个国家的认可。1999年,美国食品与医药管理局(FDA)批准添加了植物甾醇酯的食品可以使用“有益健康”的标签。2004年,欧盟委员会批准植物甾醇酯在黄油涂酱、牛奶类产品及优酪乳类等食品中使用。2007年,英国食品标准局给予植物甾醇酯健康成分的审批。目前国外市场已经成功开发出添加植物甾醇酯的人造奶油、黄油、食用油等保健食品,在医药和化妆品方面也得到了广泛应用[2-9]。2010年,我国允许植物甾醇酯作为新资源食品在食品中添加(中华人民共和国卫生部食品安全综合协调与卫生监督局,2010年第3号新资源食品公告),其产品质量指标见表1。

表1 植物甾醇酯的质量指标
目前,已报道的植物甾醇酯制备方法主要有化学合成法[6-12]、脂肪酶催化法[13-17]和超临界生物酶法[18-19]。后两者均采用酶做催化剂,虽然具有反应条件温和、高效专一、副产物少、易于分离纯化等明显优势,但酶的生产成本高,且酶法生产率低等限制了其在工业化生产中的应用。到目前为止,化学合成法仍然是植物甾醇酯商业化生产的主要方法,是国内外研究的重点。我国目前对植物甾醇的提取和分离纯化技术研究较多,但对植物甾醇酯的开发研究还处于起步和探索阶段,研究水平仍大大落后于国外,难以达到产品质量指标。因此,探索和开发操作简便、条件温和、绿色、高效的植物甾醇酯化学合成与分离纯化技术具有十分重要的实际应用价值。本文将对近年来植物甾醇酯化学合成与分离纯化技术的研究概况和最新进展进行总结,并展望今后植物甾醇酯合成的研究重点和方向。
1 植物甾醇酯的制备
植物甾醇酯主要是以酯化或酯交换的方法来制备,酯化一般有以下3种途径:1)植物甾醇与脂肪酸直接酯化;2)植物甾醇与脂肪酸酸酐反应;3)植物甾醇同脂肪酸卤化物反应。酯交换一般是植物甾醇同脂肪酸甲酯(乙酯)进行酯交换。用于合成的植物甾醇原料主要为β-谷甾醇、豆甾醇、菜油甾醇和菜籽甾醇,或者是它们的混合物。用于合成的脂肪酸原料包括饱和脂肪酸,如硬脂酸、软脂酸、月桂酸,不饱和脂肪酸如油酸、亚油酸、共轭亚油酸(CLA)、亚麻酸、二十碳五烯酸(EPA)和二十二碳六烯酸(DHA),以及各种脂肪酸不同比例的混合物和葵花籽油等食用油脂。在合成中可采用不同的原料、不同的合成原理、不同的催化剂,在不同的工艺条件下进行。
1.1 植物甾醇与脂肪酸直接酯化
植物甾醇与脂肪酸直接酯化,又叫羧酸酯化,所用的原料均容易获得,适合大部分甾醇酯的合成,是化学合成中最重要的方法。羧酸酯化是可逆反应,产物水存在于反应体系中对整个酯化过程是不利的。有些学者考虑在反应体系中加入一定量的甲苯或二甲苯,既作为反应溶剂又作为带水剂。如陈茂彬等[20]以二甲苯为带水剂,硫酸氢钠为催化剂,植物甾醇与油酸为原料直接酯化合成甾醇酯。在油酸与甾醇的物质的量比为1.3∶1,催化剂用量为甾醇物质的量的2%,反应温度135℃,反应时间8 h的最佳反应条件下,酯化率为84.3%。由于甲苯或二甲苯有毒,产品可能存在安全性问题,有些学者采用不加带水剂,以过量脂肪酸充当反应溶剂,在一定的真空度下去除反应生成的水。如Higgins[6]在真空条件下,以过量熔融脂肪酸作溶剂,硫酸氢钠作催化剂,脂肪酸与甾醇物质的量比1.2∶1,反应温度100~200℃,直接酯化合成甾醇酯,酯化率高达98%。之后,Higgins[7]又以熔融脂肪酸作溶剂,植物甾醇、棕榈油、油酸、硬脂酸、二十二碳六烯酸(DHA)、共轭亚油酸(CLA)为原料,硫酸氢钠作催化剂,在反应温度100~200℃,反应时间12~15 h,真空下合成高纯度食品级植物甾醇酯。
植物甾醇属于仲醇,其主体甾核为环戊烷多氢菲核,空间位阻较大,酯化较困难。同时,随着脂肪酸碳链的加长,直接酯化难度也逐渐增大。为了促进反应的进行,反应温度一般都控制在100℃以上,并延长反应时间。为了防止高温副反应,有些学者考虑与一些新型技术相结合,如陈舒[21]结合微波技术合成甾醇酯,在硬脂酸与甾醇的物质的量比1.2∶1,反应温度135℃,反应时间10 min的最优工艺条件下,酯化率为90.6%。结合微波技术,大大缩短了反应时间。
由于羧酸中羰基的活性较低,酯化速率较慢,促使许多学者开展羧酸酯化催化剂的探索性研究。文献报道羧酸酯化催化剂可选择无机酸、有机磺酸和酸式盐等。经过试验对比,综合考虑催化剂的腐蚀性、催化效果、价格及后处理等因素,认为有机磺酸和酸式盐比浓硫酸、磷酸等无机酸催化剂腐蚀性小,后处理方便,催化效果好。陈茂彬[22]分别对对甲苯磺酸、硫酸氢钠和磷酸二氢钠催化剂进行了对比试验。结果表明,对甲苯磺酸催化效率较高,但副反应多,得到的产品颜色较深且不易脱色。磷酸二氢钠作催化剂得到的产品颜色较浅,但酯化率不高;硫酸氢钠催化剂易溶于水,在反应后容易除去,所得产品色泽较浅,但反应时间相对要长。Deng等[23]以硫酸氢钠作催化剂,不含有机溶剂下直接酯化生产多不饱和脂肪酸甾醇酯。在多不饱和脂肪酸与甾醇的质量比为4∶1,催化剂用量为原料重量的3%,反应温度130℃,反应时间8 h的条件下,酯化率高达96%。董涛等[24]采用十二烷基硫酸钠作催化剂,以甾醇和月桂酸为原料直接酯化合成甾醇月桂酸酯。在酸醇物质的量比1.4∶1,反应温度120℃,催化剂用量为甾醇量的1.5%,反应时间4 h的最佳反应条件下,酯化率为87.9%。在月桂酸与甾醇物质的量比1.3∶1,反应温度120℃,催化剂十二烷基硫酸铜用量为甾醇量的1.0%,反应时间4 h的合成条件下,酯化率为 92.1%[25]。
文献报道羧酸酯化催化剂也可选择氧化锌、氧化钙、氧化铝、分子筛、硅胶、杂多酸和强酸性离子交换树脂等。Roden等[9]以ZnO2或碱水等作催化剂,采用硬脂酸、棕榈酸、DHA、二十碳五烯酸(EPA)、油酸、亚油酸、亚麻酸为原料,以羧酸、多不饱脂肪酸、饱和酸以及不饱和酸为溶剂,在反应温度100~220℃,真空下与甾醇直接酯化合成甾醇酯,酯化率达98%。郭涛等[26]以氧化钙为催化剂,甾醇与脂肪酸直接酯化合成甾醇酯,并且与其他催化剂(氧化铝、氧化锌、硅胶、4A型分子筛)的催化效果进行比较。结果表明:以氧化铝为催化剂,在氧化铝用量0.8%,酸醇物质的量比1.4∶1,反应温度190℃下反应10 h,酯化率最高,可达99.5%;氧化钙、分子筛和硅胶也有较好的催化性能。Meng等[10]在催化剂 ZnO/Al2O3用量10 g/kg(以 ZnO质量计算),油酸与甾醇物质的量比2∶1,反应温度170℃下反应10 h,酯化率为90%以上。在催化剂硅钨酸用量0.2%,酸醇物质的量比1.5∶1,反应温度150℃,反应时间5 h下合成脂肪酸甾醇酯,酯化率可达90%以上[27]。王勇等[28]以硅胶为催化剂,用甾醇与脂肪酸直接酯化合成甾醇酯。在酸醇物质的量比1.5∶1,反应温度190℃,反应时间10 h的条件下,酯化率达94.3%。何则强等[29]用氧化锡固载磷钨杂多酸(PW12/SnO2)催化合成α-亚麻酸甾醇酯。在植物甾醇与α-亚麻酸物质的量比为1∶3,催化剂用量为(占总反应物料的质量分数)0.6%,温度50℃,反应时间5 h条件下,酯化率为85.92%。陈静等[30]以强酸性离子交换树脂为催化剂直接酯化合成甾醇酯。在植物甾醇与脂肪酸的物质的量比1.4∶1,反应温度135℃,催化剂质量分数11%,反应时间13 h的合成条件下,酯化率为40%~60%。
使用离子液体作为催化剂合成甾醇酯的相关研究也有报道。与以上传统催化剂相比,离子液体催化酯化反应有许多优点,如良好的催化活性,成本低,易于制备、分离和回收[31-33]。杨谦等[34]以烟酸和植物甾醇为原料,甲基咪唑或吡咯烷酮酸性离子液体作催化剂,制备了甾醇烟酸酯。在酸醇物质的量比1.2∶1,反应温度120℃,反应时间1 h时,酯化收率达82.5%,离子液体可重复使用3次以上,催化活性不受影响。杨叶波等[35]以离子液体 ChCl·2SnCl2为催化剂直接酯化合成亚油酸甾醇酯。在酸醇物质的量比2∶1,ChCl·2SnCl2用量为植物甾醇质量的8%,反应温度160℃,反应时间4 h的最佳反应条件下,酯化率为89.73%。离子液体在重复使用5次后仍有较高催化活性。在月桂酸与植物甾醇物质的量比3∶1,反应温度150℃,7%的离子液体ChCl·2SnCl2作为催化剂,反应时间4 h的合成条件下,酯化率达92%[12]。寻找一种高效绿色的催化剂一直是羧酸酯化合成领域的热点,不同催化剂对羧酸酯化的影响见表2。
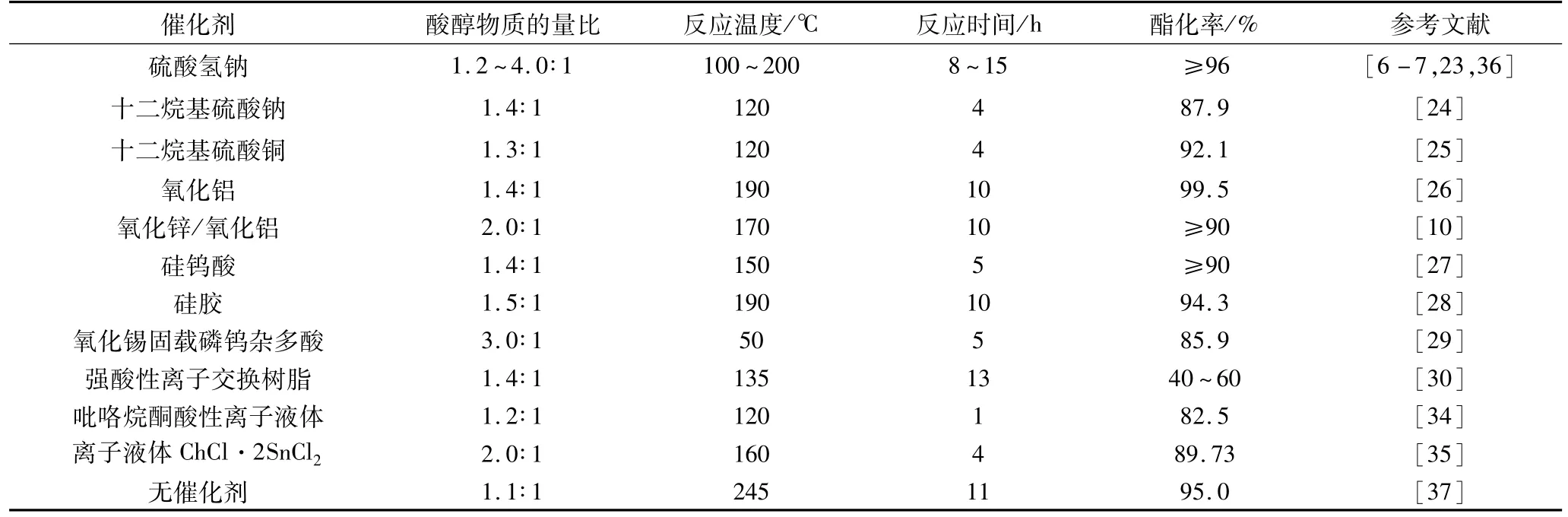
表2 不同催化剂对直接酯化的影响
截至目前,羧酸酯化法基本上都是在无溶剂状态下合成,整个过程不使用有毒有害物质。如张品等[36]在真空度为 0.03~0.04 MPa,α-亚麻酸与甾醇的质量比4∶1,硫酸氢钠催化剂量2.5%(底物的质量),反应时间8 h,反应温度140℃的条件下无溶剂直接酯化合成 α-亚麻酸甾醇酯,酯化率为98.9%,是一种绿色、安全、高效的合成工艺。另外,羧酸酯化也可不用催化剂,如美国专利报道了以卡诺拉油脂肪酸、亚油酸、油酸为原料,在反应温度150~260℃下与甾醇直接酯化合成甾醇酯,酯化率大于95%[37]。整个过程无溶剂和无催化剂,产品达到食品级,并可用于大规模生产。
1.2 植物甾醇与脂肪酸酸酐反应
植物甾醇与脂肪酸酸酐反应生成甾醇酯,称为酸酐酯化。羧酸酐是比羧酸更强的酰化剂,适用于空间阻碍较大、较难反应的植物甾醇的酯化。植物甾醇与酸酐的物质的量比一般为1∶8~10左右,羧酸酐过量可提高反应速率,缩短反应时间。常加入少量吡啶作为催化剂来加速反应,反应温度一般控制在80~90℃,反应时间为3~4 h。如陈茂彬等[38]采用植物甾醇与乙酸酐酯化的方法合成甾醇乙酸酯。在原料配比 n(甾醇)∶n(乙酸酐)∶n(吡啶)=1∶9∶5,反应温度85℃;反应时间2 h的最优工艺条件下,酯化率达98%。
1.3 植物甾醇同脂肪酸卤化物反应
植物甾醇同脂肪酸卤化物反应,叫羧酸酰氯酯化。先把羧酸制成酰氯,再与甾醇反应生成甾醇酯,虽然经过2步,结果却比直接酯化好。因为酰氯的反应活性比相应的羧酸和酸酐都强,酰氯的酯化反应极易进行,是一个不可逆反应。对于不宜采用羧酸直接酯化法来合成甾醇酯的长碳链脂肪酸、支链脂肪酸、芳香族羧酸和其它存在空间阻碍的羧酸,酰氯酯化法是一个普遍适用的方法。如烟酸与植物甾醇直接酯化很困难,故而采用酰氯酯化法[39]。
1.4 酯交换反应
1996年,美国专利介绍了一种酯交换方法:植物甾醇与过量的脂肪酸甲酯混合,加入乙醇钠催化剂在90~120℃,666.6~1 999.8 Pa真空度下反应2 h;最后经分离、真空干燥,即得所需的甾醇酯产品。酯交换是一个可逆反应,反应转化率和产品选择性与原料配比、反应温度、反应时间、催化剂种类和催化剂的用量等有关[40]。为促使反应向正方向进行,可采用把生成的低沸点甲醇或乙醇从反应体系中移除的方法。另外,可通过选用合适的催化剂,提高反应温度,延长反应时间等手段来提高产品收率。为了防止高温副反应,反应体系也可在充氮、真空或加压条件下进行。如美国专利报道了在反应体系充氮气,流速80 mL/min,油酸甲酯与植物甾醇物质的量比1∶1,催化剂氧化镧5%,机械搅拌速度500 r/min,反应温度240℃下反应7 h合成油酸甾醇酯的方法[41]。
碱性催化剂是目前酯交换反应使用最广泛的催化剂,尤其是烷氧基碱金属化合物,如甲醇钠、乙醇钠是最常用的催化剂。van Amerongen等[42]提供了一种植物甾醇与葵花籽油脂肪酸甲酯为原料,以甲醇钠作催化剂,进行酯交换制备脂肪酸甾醇酯的生产工艺。在温度110~125℃,微压,无溶剂条件下进行,酯化率为40%~85%,产品达到食品级。之后,Flickinger等[43]采用脂肪酸甘油酯(卡诺拉油、玉米、葵花籽、棉籽、橄榄和亚麻油脂肪酸甘油酯)与游离甾醇在甲醇钠或乙醇钠作用下发生酯交换合成甾醇酯,条件:n(脂肪酸甘油酯)∶n(甾醇)=(0.8~10)∶1,催化剂用量0.01%~0.5%,反应时间0.5~0.6 h,反应温度120~260℃,真空度1.333~133.322 Pa。Burdiek等[44]采用植物甾醇(β-谷甾醇,豆甾醇,菜油甾醇及混合物)与EPA(二十碳五烯酸)、DHA(二十二碳六烯酸)等n-3系列不饱和脂肪酸(n-3 PUFA)甲酯或乙酯为原料,以C1~C4醇的烷氧基钠作催化剂,在反应温度80~140℃,压力133~665 Pa下合成多不饱和脂肪酸甾醇酯。李春荣等[45]以甲醇钠作催化剂,通过植物甾醇与共轭亚油酸甲酯发生酯交换反应来制备甾醇共轭亚油酸酯,在反应温度100℃,反应时间2 h,真空度1 333.22~2 666.44 Pa下,产率94%,纯度96%。姜媛媛等[46]以甲醇钠作催化剂,采用植物甾醇与高油酸葵花籽油甲酯酯交换的方法合成了甾醇高油酸葵花籽油酯。在甲酯与甾醇物质的量比2∶1,催化剂为甾醇质量的3%,反应温度132℃,反应时间5 h的最优工艺条件下,酯化率达62.1%。夏辉等[47]以甲醇钠为催化剂,植物甾醇、油酸甲酯为原料,研究了甾醇酯的合成工艺。确定了反应的最优条件为:油酸甲酯与甾醇物质的量比4∶1,催化剂用量1.2%,反应温度125℃,反应时间4 h,真空度0.095 MPa,甾醇酯纯度为92.28%。
氢氧化钠相对于甲醇钠的价格要便宜些。Lin Linsen[8]采用甾醇(包括40%β-谷甾醇,20%~30%菜油甾醇,10%~30%的菜籽甾醇)与共轭亚油酸甲酯(共轭亚油酸包括41%顺9、反11-CLA;44%反10、顺12-CLA,10% 顺 10、顺 12-CLA)为原料,以甲醇钠、氢氧化钠作酯交换催化剂,在110℃,真空度2 666.44 Pa下进行2~20 h合成共轭亚油酸甾醇酯。甲醇钠在用于制备甾醇酯的碱催化剂中表现出较高的催化活性。另外,CaO、Ca(OH)2、Mg(OH)2等固体碱具有成本低,碱性强的优点,也表现出较好的催化活性。Milsten等[48]以菜籽油、棕榈仁油、椰子油、猪油、玉米油、棕榈油、橄榄油、芝麻油、十二烷双酸、壬二酸、十三烷双酸为原料,以 CaO、Ca(OH)2、Ca(COO)2、Mg(OH)2或组合物作酯交换催化剂同植物甾醇反应合成甾醇酯。其反应条件为:催化剂用量0.01%~0.2%,酯交换温度190~210℃,反应压力 <3 000 Pa。
酯交换反应使用碱性催化剂的优点是反应条件温和、反应速度快,易于工业化。但酯化率不高,碱性催化剂对设备的强腐蚀性以及副产物甲醇都是合成食品级甾醇酯所不期望的,且在制备过程易生成皂化物,给产物的分离带来困难。另外,由于产物色泽深,还需要脱色等后处理步骤,易造成环境污染等问题。因此,寻找一种新型高效催化剂,使其具有催化效果好、价格便宜、易于工业化、环保等特点,是酯交换反应合成领域的一个重要课题。
通过上述分析,结合实际研究中各种合成方法的特点,可把其优缺点归纳如表3所示。

表3 不同合成方法的比较
2 植物甾醇酯的分离纯化
合成的植物甾醇酯粗产品中除了甾醇酯,还混有少量的植物甾醇和脂肪酸,这些非目标产物的存在,使合成的甾醇酯往往不能满足食品、药品等领域的苛刻要求,需进一步分离纯化。目前关于甾醇酯分离纯化的报道不多,主要有以下几种:
2.1 溶剂萃取法
甾醇酯在烷烃溶剂中有较大的溶解度,且随着温度升高溶解度显著提高,而在醇类、酯类中的溶解度很小,且即使升温溶解度也变化不大。甾醇在醇类(特别是正丁醇)中的溶解度随温度变化很大,而在烷烃中溶解度较小,且随温度变化也不如在醇类中显著。姜媛媛等[46]利用高油酸葵花籽油甲酯、植物甾醇和甾醇酯在有机溶剂中的溶解性差异,用甲醇和正己烷对甾醇酯粗产品进行萃取。试验表明:先用正己烷溶解产品,再用甲醇提取残留的甲酯,即使提取次数增加,也不能达到产品质量要求;将甲醇与正己烷的添加顺序颠倒,则提纯后产品颜色很白,符合产品质量要求。董涛[25]利用月桂酸酯和植物甾醇在正庚烷中的溶解度差异实现甾醇与甾醇酯的分离。先用正庚烷溶解甾醇酯,将部分甾醇与甾醇酯分离,再用1 mol/L NaHCO3溶液去除体系中的游离脂肪酸。分离月桂酸酯收率为71.5%,纯度为92.5%。同理,使用正己烷分离共轭亚油酸酯收率为62.4%,纯度为87.2%。
单纯以正己烷为溶剂,脂肪酸皂化后整个溶液为一混浊体系,使醇酯较难分离。张娟聪等[49]选择正己烷/无水酒精体系则有效地解决了这个问题。以50 mL正己烷无水酒精(1∶1)溶液溶解5 g甾醇油酸酯粗品后,加入过量的NaHCO3以皂化过量的游离脂肪酸,除去皂化物,上层甾醇酯溶液中加入5 g高岭土脱色2 h,抽滤除去脱色剂后滤液旋转蒸发得到纯化的甾醇酯,收率为95.85%。
杨叶波等[50]以正己烷/无水乙醇/NaHCO3水溶液形成的萃取剂对粗产物一步分离提纯。处理工艺为:在正己烷/无水乙醇的复合溶剂中完全溶解粗产物形成澄清溶液,滴加NaHCO3中和,溶液分为2层,上层为溶解了甾醇酯的正己烷相,收集并经旋转蒸发即得到纯化产品。将萃余相加热去除乙醇后可收集植物甾醇,再进行盐析可回收脂肪酸盐。最佳分离工艺参数为∶正己烷∶无水乙醇为1∶1、正己烷/粗产物液质比(mL/g)为 7.5,纯度达 99.2%,收率达95.4%。
2.2 硅胶柱层析法
董涛[25]采用硅胶柱层析法分离甾醇月桂酸酯。将反应粗品投入无水乙醇中(料醇比=1∶5),加热到60℃,加2滴酚酞,用0.1 mol/L的KOH乙醇溶液滴至溶液变红,振摇30 s不变色。取下层油状物真空干燥。将上述干燥的混合物加环己烷溶解,然后用硅胶柱层析分离。硅胶柱规格:1 000 mm×12 mm i.d.,100~200目硅胶。硅胶柱色谱条件:流动相为环己烷/无水乙醚(19∶1),流速 25 mL/h,按 1管/15 min收集洗脱液,并用TLC检测产物,收集甾醇酯。当甾醇酯全部洗脱出来之后洗脱液换成环己烷/无水乙醚/乙醇(19∶1∶10),流速25 mL/h,按 l管/15 min收集洗脱液,并用TLC检测将吸附在硅胶上的甾醇洗脱下来回收利用。采用硅胶柱层析分离可以得到较为纯净的甾醇酯,且分离简单,易行,经HPLC测定,纯度高达99%[50]。但硅胶柱层析分离耗时且效率低,不适用于工业化生产。
2.3 重结晶法
陈茂彬等[39]将甾醇烟酸酯在有机介质中加入36%盐酸,25~30℃搅拌反应3~4 h,对产品进行重结晶精制,得到盐酸甾醇烟酸酯。采用丙酮和正己烷做溶剂对甾醇酯粗产品进行重结晶。试验表明:用丙酮重结晶后产品仍为粉末状,且颜色不是很白;用正己烷重结晶出的产品为白色片状晶体,总产率78.1%,纯度 95.95%[22]。
2.4 洗涤法
甾醇油酸酯粗产品中还含有少量未反应完的游离植物甾醇和过量油酸,应设法除去。陈茂彬等[20]将提纯工艺分为2步,首先以一定量的2%碳酸氢钠溶液进行洗涤,使油酸变成水溶性的油酸钠。粗产品经过2次洗涤后,去掉了大部分油酸。第二步采用少量乙醇进行洗涤,边搅拌边加热到45℃左右。用乙醇洗涤3次后,再经真空干燥,即得甾醇油酸酯产品。经检测,产品的酸值为2.3 mgKOH/g,游离植物甾醇的质量分数为3.3%,产品纯度为90.2%。
2.5 分子蒸馏法
在用植物甾醇与脂肪酸直接酯化合成的甾醇酯样品中加入3%活性白土脱色后进入分子蒸馏设备。蒸馏温度170~200℃,压力0.1 Pa,收集重相即为甾醇酯产品[26]。当分子蒸馏选择在200℃时,甾醇酯质量分数可达到98.4%[28]。
通过上述分析,目前适于工业化生产的分离纯化方法见表4。

表4 分离纯化方法比较
由表4可知,选择正己烷/无水乙醇/碳酸氢钠水溶液形成的萃取体系进行溶剂萃取是目前较为理想的分离提纯方法,与其它方法相比,该工艺采用一步法将甾醇酯从脂肪酸-甾醇-甾醇酯三元体系中提取出来,简单、经济。但由于脂肪酸的化学结构不同,所形成的甾醇酯的生理活性和物理化学性质有较大的差别,对甾醇酯产物进行分离纯化时,仍必须根据各种甾醇酯在有机溶剂中的溶解度的不同,各种合成方法带来的产物中杂质种类和含量的不同,对产物纯度和色泽度要求的不同,采取相应的萃取、柱层析、重结晶、洗涤、脱色、分子蒸馏等分离纯化方法进行处理。
3 结论与展望
植物甾醇酯的制备采用化学合成法具有工艺简单、成本低、产量高、易于控制和实现工业化生产等优点,近年来国内外不断有新的成果出现,人们可以结合实际需要选择不同方法来实现自己的合成目标。由于直接酯化法酯化率高,在成本上也更经济,适合于生产食品级产品及大规模工业生产,在工业上基本都采用该法。但直接酯化仍存在一些问题,如需要在较高温度下,长时间反应,这样容易发生副反应,且随着脂肪酸碳链的加长,反应难度加大等。因此,选择一种合适的催化剂以及在合成过程中如何采用有效、便捷、适宜于工业化应用的保护措施,以避免副产物的生成仍是直接酯化中一个有待解决的关键技术。
我国对植物甾醇酯的开发研究近年来虽有所发展,但与国际水平相比差距甚远。这无疑是对我国研究工作者的一大挑战,也是我们面临的艰巨任务。由于植物甾醇和脂肪酸的种类很多,植物甾醇与脂肪酸酯化得到甾醇酯产品的种类也很多,反应后的体系中酯、酸、醇并存,且它们在有机溶剂中均有相当的溶解度,难以分离完全。目前的分离纯化方法中仍存在高纯度和高回收率不能兼得的缺陷,要得到高质量的产品是目前制备植物甾醇酯的一个技术难点。因此,探讨高效的植物甾醇酯分离纯化技术,以提高产品质量,降低生产成本,适应各种应用的需求也是植物甾醇酯制备中的挑战性课题。
展望未来,寻找一种廉价、高效、绿色的催化剂进行合成,选择一个合适的溶剂体系和处理工艺进行分离纯化,以达到简化工艺、节省能源、降低生产成本、高安全无污染的目的,将是我国未来植物甾醇酯制备研究的重要发展方向。
[1]博迪克 D C,莫伊尼 G,雷德斯多夫 D,等.植物甾醇和植物甾烷醇衍生物[P].CN:1256277A,2000-06-14
[2]Berry C J,Bierenbaum M L.Anticholesterolemic edible oil:[P]US:6277431.2001-08-21
[3]Wester I.Fat composition for use in food:US,6162483[P].2000-12-19
[4]Stewart D J,Milanova R,Zawistowski J,et al.Phytosterol compositions and use thereof in foods,beverages,pharmaceuticals,nutraceuticals and the like:US,6087353[P].2000-07-11
[5]Nashed B,Yeganeh B,Hayglass K T,et al.Antiatherogenic effects of dietary plant sterols are associated with inhibition of proinflammatory cytokine production in apo E-KO mice[J].Journal of Nutrition,2005,135(10):2438-2444
[6]Higgins III JD.Preparation of sterol and stanol-esters:US,5892068[P].1999-04-06
[7]Higgins III JD.Preparation of sterol and stanol-esters:US,6147236[P].2000-11-14
[8]Liu linsen.Sterol esters of conjugated linoleic acids and process for their production:US,6413571[P].2002-07-02
[9]Roden A,Williams J L,Bruce R,et al.Preparation of sterol and stanol-esters:US,6184397[P].2001-02-06
[10]Meng X,Pan Q,Yang T.Synthesis ofphytosteryl esters by using alumina-supported zinc oxide(ZnO/Al2O3)from esterification production of phytosterol with fatty acid[J].Journal of the American Oil Chemists Society,2011,88(1):143-149
[11]Robles-Manuel S,Barrault J,Valange S.Selective synthesis of phytosterol esters from natural sterols and fatty methyl esters over Mg-containing solid catalysts[J].Comptes Rendus Chimie,2011,14(7-8):656-662
[12]Yang Y B,He W S,Jia C S,et al.Efficient synthesis of phytosteryl esters using the Lewis acidic ionic liquid[J].Journal of Molecular Catalysis A:Chemical,2012,357:39-43
[13]ShimadaY,HirotaY,Baba T,et al.Enzymatic synthesis of steryl esters of polyunsaturated fatty acids[J].Journal of the American Oil Chemists'Society,1999,76(6):713-716
[14]Vu PL,Shin JA,Lim CH,et al.Lipase-catalyzed production of phytosteryl esters and their crystallization behavior in corn oil[J].Food Research International,2004,37(2):175-180
[15]Villeneuve P,Turon F,Caro Y,et al.Lipase-catalyzed synthesis of canola phytosterols oleate esters as cholesterol lowering agents[J].Enzyme and Microbial Technology,2005,37(1):150-155
[16]Kim B H,Akoh C C.Modeling and optimization of lipasecatalyzed synthesis of phytosteryl esters of oleic acid by response surface methodology[J].Food Chemistry,2007,102(1):336-342
[17]Zheng M M,Dong L,Lu Y,et al.Immobilization of candida rugosa lipase on magnetic poly(allyl glycidyl ether-coethylene glycol dimethacrylate)polymer microsphere for synthesis of phytosterol esters of unsaturated fatty acid[J].Journal of Molecular Catalysis B:Enzymatic,2012,74(1-2):16-23
[18]King JW,Snyder JM,Frykman H,et al.Sterol ester production using lipase-catalyzed reaction in supercritical carbon dioxide[J].European Food Research and Technology,2001,212(5):566-569
[19]王腾宇,胡立志,孙博,等.超临界CO2状态下生物酶法催化合成植物甾醇酯[J].食品科学,2010,31(22):293-296
[20]陈茂彬,黄琴,吴谋成.植物甾醇油酸酯产品的合成工艺研究[J].中国油脂,2005,30(6):63-65
[21]陈舒.植物甾醇酯微波加热合成的研究[D].西安:西安理工大学,2007
[22]陈茂彬.植物甾醇酯的制备、生物活性及应用研究[D].武汉:华中农业大学,2005
[23]Deng Q C,Zhang P,Huang Q D,et al.Chemical synthesis of phytosterol esters of polyunsaturated fatty acids with ideal oxidative stability[J].European Journal of Lipid Science and Technology,2011,113(4):441-449
[24]董涛,贾承胜,张晓鸣.SDS催化合成植物甾醇月桂酸酯的研究[J].食品与机械,2008,24(3):44-47.
[25]董涛.植物甾醇酯的化学合成及其抗氧化性研究[D].无锡:江南大学,2008
[26]郭涛,姜元荣,王勇,等.植物甾醇酯制备方法的研究[J].中国油脂,2011,36(1):53-56
[27]Meng X H,Sun PL,Pan Q Y,et al.Synthesis of plant sterol esters catalyzed by heteropolyacid in a solvent-free system[J].European Journal of Lipid Science and Technology,2006,108(1):13-18
[28]王勇,姜元荣,郭涛,等.甾醇酯化反应中催化剂的研究[J].粮油加工,2011(7):30-32
[29]何则强,熊利芝,梁凯.PW12/SnO2催化合成 α-亚麻酸植物甾醇酯[J].中国油脂,2010,35(2):33-36
[30]陈静,屈凌波,李亚平,等.植物甾醇酯的合成[J].应用化学2011,28(10增刊):168-169
[31]Xu ZJ,Wan H,Miao J.et al.Reusable and efficient polystyrene-supported acidic ionic liquid catalyst for esterifications[J].Journal of Molecular Catalysis A:Chemical,2010,332(1-2):152-157
[32]Zhang L,Xian M,He Y,et al.A bronsted acidic ionic liquid as an efficient and environmentally benign catalyst for biodiesel synthesis from free fatty acids and alcohols[J].Bioresource Technology,2009,100(19):4368-4373
[33]Joseph T,Sahoo S,Halligudi SB.Brönsted acidic ionic liquids:a green,efficient and reusable catalyst system and reaction medium for Fischer esterification[J].Journal of Molecular Catalysis A:Chemical,2005,234(1-2):107-110
[34]杨谦,余晓姣,姚秉华.吡咯烷酮酸性离子液体催化制备甾醇烟酸酯[J].西北农业学报,2010,19(3):109-113
[35]杨叶波,何文森,贾承胜,等.离子液体催化合成亚油酸植物甾醇酯[J].中国油脂,2011,36(12):28-32
[36]张品,邓乾春,黄庆德,等.无溶剂直接酯化法合成α-亚麻酸植物甾醇酯工艺研究[J].中国粮油学报,2010,25(1):55-59
[37]Roden A,Williams J L,Bruce R,et al.Preparation of sterol and stanol-esters:US,6410758[P].2002-06-25
[38]陈茂彬,李万芬,吴谋成.植物甾醇乙酸酯的合成研究[J].化学与生物工程,2003(5):33-34
[39]陈茂彬,黄琴.植物甾醇烟酸酯研究与开发[J].粮食与油脂,2004(12):7-9
[40]Tatu M,Hannu V,Ingmar W.Use of a stanol fatty acid ester for reducing serum cholesterol level:US,5502045[P],1996
[41]Barrault J,Boisseau M,Pouilloux Y,et al.Method for preparing a fatty substance ester and use thereof in pharmaceutics,cosmetics or food industry:US,6828451[P].2004-12-07
[42]van Amerongen M P,Lievense L C.Process for the production of stanol esters,and use thereof:US,6106886[P].2000-08-22
[43]Flickinger B D,Grabiel R,Poppe G.Methods for producing ester-rich composition:US:20020107232,[P].2002-08-08
[44]Burdiek D C,Mone G,Raederstorff D.Phytosterol and/or phytostanol derivatives:US,20020055493[P].2002-05-09
[45]李春荣,王三永,谢志桥.植物甾醇共轭亚油酸的制备及其血脂调节作用的研究[J].中国食品添加剂,2007(3):69-72
[46]姜媛媛,董晓丽,吴文忠.植物甾醇酯的制取与分析[J].大连工业大学学报,2010,29(1):8-10
[47]夏辉,史宣明,鲁海龙,醇酯交换法合成甾醇酯工艺研究[J].粮油食品科技,2011,19(1):26-28
[48]Milstein N,Biermann M,Leidl P.Processes for preparing sterol esters:US:6713466[P].2004-03-30
[49]张娟聪.植物甾醇的改性研究[D].杭州:浙江工业大学,2008
[50]杨叶波.离子液体催化合成植物甾醇酯及其分离工艺研究[D].无锡:江南大学,2012.
Progress in the Chemical Synthesis,Separation and Purification of Phytosterol Esters
Xu Qingqing1,2Jin Wenbin1Su Baogen1Yang Yiwen1Ren Qilong1
(Key Laboratory of Biomass Chemical Engineering of Ministry of Education,Zhejiang University1,Hangzhou 310027)
(College of Chemical and Material Engineering,Quzhou University2,Quzhou 324000)
Phytosterols have a ability of reducing serum cholesterol with unique anti-inflammatory,antipyretic and anticancer activities,etc.However,they have some drawbacks such as insoluble in water,which has pretty limited the fat-soluble.Phytosterol esters can greatly improve the fat-soluble and inhibiting cholesterol absorption properties.As a result,synthesis of phytosterol esters is becoming a research hotspot by mass of countries.At present,the preparation of phytosterol esters has been reported mainly in aspects as chemical synthesis,catalysis of lipase,and biological enzyme catalysis in supercritical fluid.The latter two methods both use the enzymes as catalysts;their industrial application is limited because of the high production cost and low productivity of enzymes.Chemical synthesis is still the main method to conduct large-scale commercial production and research focus of phytosterol esters.The progress of chemical synthesis,separation and purification of phytosterol esters in recent years is reviewed in the article.
phytosterols,phytosterol esters,chemical synthesis,separation and purification,progress
O621.25+6.4;O6-332
A
1003-0174(2014)03-0120-09
国家自然科学基金(20936005),“十二五”国家科技支撑计划(2011BAD23B03)
2013-05-16
许青青,女,1969年出生,副教授,化学合成与分离
杨亦文,男,1963年出生,教授,天然产物提取分离与结构修饰
