“医改”深化和药房自动化实践下的药学监护
2014-01-08张石革北京大学第四临床医学院北京积水潭医院北京100035
张石革 (北京大学第四临床医学院,北京积水潭医院,北京 100035)
当前,“医改”逐步深入,围绕“低收入看不起病,社区医疗看不了病,三甲医院看不上病”的三大社会难题,探索实现“管办分开,医药分开”,借以促进临床合理用药,节约医药资源,合理分配医保支出,体现药师在保障安全用药中的作用。纵观“医改”中各项措施,“药改”占据“医改”权重的半数,多数政策与药品有关,包括批零零差价、医药收支两条线、使用国家基本药物等;同时临床药物治疗进展十分迅猛,“医药护治疗”团队作用更加突显,用药安全成为全社会关注的“热点”,药房(药店)的服务功能更加凸显,成为医院“第一窗口”。简单的人工药品调配、发放已不能满足患者用药安全及临床药物治疗需求。医师更期盼用药风险的防范措施;患者更加关心药品用法及相关合理用药知识,主动寻求药师帮助。药房自动化以快捷、自动化手段,“以患者为中心”,代替药师手工发药,使药师有充裕的时间更好地进行药学服务和用药指导,促进药师职责和技术的发挥,使药房功能更加完美地转型。
1 有关药房自动化
伴随着社会经济、医药科技、医药信息和自动化技术的飞速发展,药房自动化成为医药发展的必然趋势,是医药科技、信息化和自动化技术相互结合的成果。自动化药房作为国际上药学运营领域的一项技术,早在20 世纪80 年代中期,已成熟应用,在全球发达国家中较为普遍的应用。2006 年,上海市第一药店率先在国内运营;目前,解放军第302 医院、安徽医科大学第一附属医院、中国医科院北京协和医院、浙江省人民医院、福建省人民医院、首都医科大学附属北京友谊医院等200 余家医院已经实施(约占三级甲等医院总数的1/5)。2010 年12 月,卫生部出台《二、三级综合医院药学部门基本标准(试行)》,要求三级综合医院药学部要逐步配备全自动分包装系统、自动化调剂配方系统和药品管理信息系统。
1.1 药房自动化的优势
实现药房自动化系统,能提高处方准确率和发药效率,促进临床合理用药,同时把药师从繁杂的人工配药劳动中解脱出来,有充裕的时间进行专业性的药学服务工作。其优势如下:(1)简化工作流程,加快调配处方和发药速度,减少患者的等待时间;(2)提高工作效率和药房科学管理水平;(3)有效控制和减少配药差错;(4)降低药品损耗,减少污染;(5)促使药房布局合理、环境舒适、功能完善;(6)降低管理成本,提高医院经济效益;(7)降低药师工作强度,促使药师更好地发挥专业知识,为患者提供用药指导、用药咨询和用药监护,体现药学工作由单纯供应保障向药学知识技术服务转型;(8)打破传统窗口封闭式的服务方式,实现药师与患者零距离的交流,体现对患者深层次的关怀,促进临床药学的开展,提高合理用药的水平。
1.2 药房自动化的缺陷
(1)药品异型包装,限制上机;(2)国内医院门诊量大,一般三级甲等医院门、急诊患者就诊量为3 000~8 000 人次,与单机存储数量(品种与数量)相差数倍;(3)系统故障(维护);(4)费用/效益;(5)应提高软件的易用性和亲和力。
2 药房自动化后的药师工作模式转型
降低药师工作强度,拓宽开展药学服务的充裕时间,药学工作由单纯供应保障向药学技术服务转型后“药师应当干些什么、药学服务核心应转向哪里”成为每位药师面临抉择的课题,即工作中心应转向患者、核心应转向合理用药的精髓,即“安全、有效、经济、适宜。将事物型工作转向学术型和技术型,增强对用药安全、有效性的监护:(1)安全性:增强用药安全管理,包括用药风险的评估、不良反应的鉴别与救治、不良事件的规避与警戒。(2)有效性:增强处方审核,对重要的药物治疗方案进行遴选与调整(联合用药、剂量、疗程)、开展用药咨询、药学监护。(3)经济性:开展药物经济学评价,进行成本/效益分析与系统评价。(4)适宜性:以适宜的药物给予适宜的患者,包括给药途径、剂量、时间、疗程和目标。其理论基础是循证医学,药师应关注各种“指南”、系统评价和临床研究结论。“指南”体现相关医学领域的最佳研究现状,是临床医、药师最为强大的理论依据,也是最为方便的法门,借以真正寻觅到医药契合的切入点,掌握合理用药真绨,造益于广大人群。
2.1 增强对用药风险的防范,加强对处方安全性的审核
2.1.1 应用第4 代氟喹诺酮类抗菌药物莫西沙星引起的心电图O-T 间期延长:莫西沙星所引起Q-T 间期延长的发生机制与折返有关[1],带来心脏复极化相关变化[2],因心肌细胞传导缓慢、心室复极不一致所引起。常反复发作,易致昏厥,可发展为心室颤动而致死。病因为各种原因所致的Q-T 间期延长综合征、严重的心肌缺血或其他心肌病变、应用延长心肌复极药物(奎尼丁等)、电解质紊乱(低血钾、低血镁)等和服用抗过敏药(阿司咪唑、特非那丁、氯雷他定)、促胃肠动力药(西沙必利)和氟喹诺酮类抗菌药物(环丙沙星、氧氟沙星、左氧氟沙星、加替沙星、莫西沙星)。在用药期间宜注意监护:(1)老年和女性患者可有更长的Q-T 间期,对引发Q-T 间期延长的药品更为敏感,应格外注意;(2)Q-T 间期延长的程度与药物血浆浓度(≥1 000 ng/ml)密切相关,应监护剂量[3];(3)监护血钾水平,提前纠正低钾血症;(4)告之驾驶和操作机械者用药期间禁止驾车、操作机械或高空作业;(5)规避不良联合用药,应用尤其是肝酶CYP3A4 抑制剂;(6)对心动过缓者在提高基础心率(>110 次/min)基础上静脉滴注异丙肾上腺素。
2.1.2 警惕肝素所致的血小板减少症-血栓:血小板减少症(haparin induction thrombocytopennia,HIT)是由肝素免疫介导的严重不良反应[4],表现为血小板计数降至150 万×109/L 以下或用药前最高值下降50%以上者,20%~50%患者出现血栓并发症,发生率为未分组肝素>低分子肝素>戊糖酸钠。典型的HIT 约在应用肝素后5~10 d 内抗体产生,7~14 d 达到血小板减少症的阈值[5]。HIT 通过肝素-血小板-抗体复合物以损伤内皮细胞,肝素与血小板结合,使血小板α 颗粒释放具有高正电荷的四聚体蛋白PF4,其通过葡萄糖胺聚糖与血小板结合,同时与肝素结合,当与PF4 与肝素结合后,使其分子结构象改变,产生抗原性[6]。同时产生相关抗体IgA、IgM 和IgG,尤其发挥病理作用的为IgA。HIT 可形成大量的动、静脉血栓,应对措施有:(1)抗凝血治疗期间应监测血小板,一旦发现,及时补充血小板成分输注;(2)怀疑肝素诱发血小板减少症、血小板计数中度减少时,及时停用包括用于冲洗静脉通路的肝素;(3)替代治疗:应用直接凝血酶抑制剂来匹卢定、阿加曲班或达比加群酯[7]。
2.1.3 利奈唑胺导致的相关性血小板减少症:欧美报道其发生率为2.4%,老年人发生率为20.9%,多出现在用药后(9.33 ±3.28)d[8]。与氯霉素可逆性抑制骨髓机制相似,抑制线粒体呼吸作用诱导,或由免疫因素所致。对用药超过1 周尤其肾功能不全(内生肌酐清除率≤60 ml/min)、骨髓抑制者、血浆药物浓度过高(≥7.5 μg/ml)者[9],应进行全血细胞计数检查,必要时输注血小板。
2.1.4 万古霉素所致的肾毒性和非免疫性反应:万古霉素、去甲万古霉素于使用前、后应监测患者肾毒性(蛋白尿、管型尿、血尿、尿素氮、血肌酐)和肾衰竭;并控制药液浓度和滴速,滴速过快可致由组胺引起的非免疫性与剂量相关反应(红人综合征)[10],突击性大量注射不当,可致严重低血压。滴速控制宜慢,每1 g 至少加入200 ml(5 mg/ml)液体,滴注时间控制在2 h 以上(危险因素包括年龄、人种、剂量、浓度、滴速等)。同时注意注射液体的温度(大容积输液的温度在冬季不宜过冷,必须加热至室温),对心肌梗死或心脏骤停后者尤应注意[11]。2.1.5 应用环磷酰胺应监护膀胱毒性(bladder toxicity):环磷酰胺为氮芥类双功能烷化剂,属于细胞周期非特异性药物,在体内经肝脏微粒体功能氧化酶的作用转化为磷酰胺氮芥及丙烯醛,后者具有强烈毒性,通过增加氧化应激损伤膀胱尿路上皮、炎症和一氧化氮(NO)水平[12],引起肾出血、膀胱出血、膀胱纤维化、肾盂积水和尿道泛流等。为预防肾、膀胱毒性,药师应注意:(1)鼓励患者多饮水,大剂量应用时应水化、补液利尿,以保障足量的液体和尿量;(2)同时给予尿路保护剂美司钠;(3)为预防白血病及淋巴瘤患者出现尿酸性肾病,可大量补液、碱化尿液和给予别嘌醇抑酸。
2.2 规避和处置药品不良反应
药品是把双刃剑,疗效与不良反应并存,药品除治疗作用外,尚有药品不良反应(advers drug reaction,ADR),即指合格药品,在正常用法与用量下,出现的与用药目的无关的或意外的有害反应。但药师应当事前提前防范,把风险提示和告之;事后及时果断的救治,并对因果关系进行判断。
2.2.1 急性胰腺炎(acute pancreatitis):胰腺炎多由胰腺管梗阻,以致管内压力增高,胰液外溢,其胰腺消化酶对胰腺自身消化引起的化学性炎症,分为水肿型和出血坏死型,其中后者病情危险,是猝死病因之一。胰腺炎病因甚多,如胆道感染、胆石症、胆道蛔虫等胆道疾病;其次,酗酒、暴饮暴食、十二指肠憩室炎、流行性腮腺炎、伤寒、病毒性肝炎、腹部手术及外伤、内窥镜逆行胆囊胰腺造形术检查时注射造影剂压力过高等均为病因。但用药时也可诱发胰腺炎[13],引发胰腺炎的相关药品有:(1)调节血脂药:他汀类(洛伐他汀、辛伐他汀、普伐他汀、氟伐他汀、瑞舒伐他汀)与考来烯胺、吉非贝齐、氯贝丁酯、依折麦布等可引起胰腺炎,尤其见于用药最初3 个月内。(2)抗糖尿病药:二肽基肽酶-4(DPP-4)抑制剂西格列汀、沙格列汀、利格列汀、阿格列汀、维格列汀可使胰腺炎和胰腺导管化发生率增加及胰腺导管细胞更新加快,临床也收到关于其他DPP-4 抑制剂(西格列汀、沙格列汀、利格列汀)诱发胰腺炎的临床报告和上市后报告[14-15]。此外,已证明2 型糖尿病患者的急性胰腺炎风险高于未患2 型糖尿病的个体,如利拉利汀组336 例患者中较多报告发生胰腺炎(1 例/538 人年,而对照组则为0 例/433 人年)[16]。(3)生长素释放抑制激素类似物:奥曲肽、兰瑞肽偶见引起急性胰腺炎,通常在用药初始数小时或数日内,但停药后逐渐消失;长期服用且发生胆结石者也可能出现胰腺炎。(4)利尿剂:呋塞米、布美他尼、依他尼酸、氢氯噻嗪等,尤其长期过量应用利尿剂如呋塞米、氢氯噻嗪和抗高血压药甲基多巴及糖皮质激素等,可于用药数周后引起急性胰腺炎。(5)抑酸剂:西咪替丁偶致胰腺炎。(6)免疫抑制剂:环孢素、硫唑嘌呤。
胰腺炎的处置措施:(1)立即停用致病药物。(2)抑制胰腺分泌:①对重型急性胰腺炎,应用奥曲肽;②急性轻型(水肿型)胰腺炎或急性出血坏死性胰腺炎选用加贝酯;③对出血、坏死型胰脉炎可用抑肽酶,缓慢静脉注射。(3)镇痛、解痉。(4)选用甲硝唑、氟喹诺酮类抗菌药物,严重时可用亚胺培南/西司他丁等抗菌药物控制感染。此外,应密切监护新药(免疫抑制剂、靶向抗肿瘤药、抗人类免疫缺陷病毒药)的胰腺毒性。2.2.2 光敏反应(photosensitivity reaction):光敏反应属于一种光毒作用,系由药物汇集于皮内所致,表现为日晒斑加重,早期以手足、口鼻的刺麻等感觉异常为主,继之在裸漏的皮肤部位出现红斑、色素沉着,偶见大疱,数日或数周后可消失,少数病例出现丘疹性皮疹和荨麻疹,约25%发生光敏反应者出现指(趾)甲松动。导致光敏反应的药品有:(1)抗菌药物:氟喹诺酮类药吸收后能使紫外线能量大部分在皮肤中释放,由光激发而致皮肤细胞的损伤。其中以司帕沙星、氟罗沙星、依诺沙星、西他沙星和克林沙星所致的反应为最重[17],产生光毒性的原因与阳光照射和自身敏感性有关,药物氧化生成活性氧,激活皮肤的成纤维细胞中蛋白激酶C 和酪氨酸激酶,2 种酶又激活环氧酶,促使前列腺素合成,引起皮肤的炎症。氯霉素服后少见有日光性皮炎、剥脱性皮炎、皮疹、血管神经性水肿。四环素类中的多西环素、米诺环素、美他环素、地美环素服用后也易发生光敏反应。(2)磺胺类药:药热多发生在服药后5~10 d;皮疹多发生在7~9 d,常伴有发热。皮疹有麻疹样疹、瘀斑、猩红热样疹、荨麻疹或巨疱型皮炎;也可发生剥脱性皮炎、光敏性皮炎。(3)肝胆疾病辅助用药:原卟啉钠在夏季服药时,可出现色素沉着或日光性皮炎。(4)皮肤科用药:甲氧沙林为植物中提取的色素形成剂,具有强烈的光敏活性,易被波长为320~400 nm 的紫外线激活而产生光毒作用,促使表皮细胞DNA 合成及有丝分裂受到抑制,减缓表皮细胞更新速度,再经照射紫外线,在皮肤上可产生红斑反应,加速黑色素形成。但光敏反应可使黑素细胞中酪氨酸酶活力增加,促使黑色素细胞形成并向表皮移动,出现色素沉着,在治疗前24 h 和治疗后12 h 应避免阳光直射,以免发生光变应性接触性皮炎[18]。(5)抗肿瘤药:柔红霉素用药后易出现光敏性皮炎。
一旦出现光敏反应,及时查找并停用光敏药物,并采用下列处置措施:(1)对敏感体质者服后注意采取遮光措施(避免强光照射、防护服、防护膏)或变换给药时间(睡前服药);(2)加服核黄素、维生素C;(3)对症应用抗过敏药;(4)对有红斑、水肿伴明显和瘙痒者,选用炉甘石洗剂或2.5%吲哚美辛溶液外搽;(5)对有渗出、糜烂、结痂者,应用3%硼酸溶液或5%醋酸铝溶液湿敷,1 次15 min,1 日3~4 次;(6)口服泼尼松1 次10 mg,1 日3 次,服用3 d 后停药。
3 加强对重点药物治疗的监护
自20 世纪以来,国内外无数次惨痛的药品不良事件(adverse drug event,ADE)包括“反应停”、“磺胺酏”、“欣弗”、“亮菌甲素”、“甲氨蝶呤”等的教训,使人们清醒的认识到:仅仅依靠新药审批,只管好事后监测是远远不够的!所有的ADE 都是以血和生命代价为起始,同时以巨大经济损失而告终。因此,对待ADE 要彻底转变观念,做到以预防为主,通过各种警戒措施,尽可能消灭在萌芽状态,将ADE 的防控作前略性前移,而完成此项使命的核心力量是药师,包括质量设计、遴选药物、用药、疗效跟踪、用药方案调整、不良反应防治等全程。
3.1 抗凝血药的监护
血栓(thrombus)是血液在血管流动中发生凝聚后所形成的特殊结构,其形成是一个十分复杂的由量变到质变循序渐进的过程。其中静脉血栓多与血液瘀滞有关,形成的血栓主要以交织的纤维蛋白和红细胞为主,对血小板依赖性低,若伴随血流阻塞血管可形成下肢静脉、心、肺或术后栓塞。血栓的防治以抗凝为主,常用药物有肝素和低分子肝素、华法林、直接凝血酶抑制剂或凝血Ⅹa 因子抑制剂。华法林作为维生素K 拮抗剂,可竞争性抑制维生素K 环氧化物还原酶,阻止其还原成氢醌型维生素K,妨碍维生素K 的循环再利用而产生抗凝作用,其作用持久、疗效稳定、价格便宜,用于外周动脉血栓栓塞、缺血性冠状事件一级预防、瓣膜病和非瓣膜病性心房颤动,成为一线首选药[19]。但其安全指数小,易致出血,药物与药物和食物间相互作用较多,应用中注意监护:
3.1.1 注意在华法林起效滞后的时间段须联合应用肝素:华法林服用后抗凝作用出现较慢,主要缘于2 个方面:(1)华法林抑制羧基化酶,但对已活化的凝血因子Ⅱ、Ⅶ、Ⅸ、Ⅹ无影响,必须等上述因子在体内相对耗竭后,才能发挥抗凝效应。(2)华法林在体内开始起效必须依赖于体内已合成的凝血酶原因子Ⅱ明显下降,而凝血酶原因子Ⅱ的半衰期为72 h,所以,口服华法林真正起到抗凝作用至少需要3 d,抗凝血的最大效应时间为72~96 h,抗血栓形成的最大效应时间为6 d。鉴于华法林起效缓慢,如需快速抗凝时(深静脉栓塞),应先用肝素或低分子肝素治疗,华法林和肝素同步治疗延续肝素最少5~7 d 直至国际标准化比值(INR)控制在目标范围内2 d 以上,才可停用肝素,继以华法林维持治疗[20],借以保证充分抗凝。
3.1.2 应用华法林期间须监护所致的出血和INR:应用华法林过量易致出血,尤其当监测INR,治疗初期应每日监测INR,稳定至少2 d 后可每周2~3 次监测至第4 周,INR >1.5 时起效,INR 为2.0~3.0 时为最佳治疗窗,INR >4 时出血危险性增加,INR >5 时危险性急剧增加,且应注意个体化包括人种、性别、年龄、身高、体质量、基因、肝酶CYP2C9 多态性、饮食、维生素K 环氧化物还原酶亚基1(VKORC1)、肝肾功能、精神疾病等因素而调节剂量[21]。如出现抗凝过度、INR 超标,高危出血倾向,将华法林减量或停服,监测INR 降至目标范围再从小剂量开始应用。如患者有高危出血倾向,需将INR 在24 h 内降至正常,可给予维生素K1口服1~2.5 mg。紧急纠正应缓慢静脉注射维生素K15~10 mg(>30 min,静脉注射后恢复凝血功能需4 h)。当有严重出血或INR >20 时,可应用维生素K110 mg、新鲜血浆和凝血酶原复合物缓慢静脉注射。高剂量维生素K1能引起华法林抵抗,重新使用华法林时应同时给予肝素,直至患者恢复对华法林敏感性。
3.1.3 提示不宜服用华法林的人群:(1)严重肝肾功能不全、未控制的高血压、凝血功能障碍(血友病、血小板减少性紫癜、真红细胞增多症、白血病)、近期颅内出血、泌尿道出血、活动性溃疡、感染性心内膜炎、心包炎或心包积液者。(2)于近日择期手术和术后3 d 及行脑、脊柱和眼科手术者。(3)华法林具低分子量极易通过胎盘屏障而致畸,导致流产和死胎率高达16%,妊娠早期服用可致“胎儿华法林综合征”,妊娠晚期服用可引起母体和胎儿出血、死胎。对先兆流产、妊娠期妇女禁用;而肝素不通过胎盘屏障,可替代华法林作为妊娠期妇女的选择[22]。(4)严重过敏者。(5)开放性创伤者。
3.1.4 规避可缩短华法林作用时间的药物:许多药物可与华法林发生相互作用,发生拮抗而影响华法林疗效,在治疗期间应予规避或酌增剂量[23]。包括:(1)抗菌药物:双氯西林、萘夫西林、灰黄霉素、利福平、磺胺;(2)抗癫痫与镇静药:扑米酮、卡马西平、苯妥英钠、苯巴比妥、戊巴比妥、异戊巴比妥;(3)抗肿瘤药:环磷酰胺、硫唑嘌呤、巯嘌呤;(4)催眠药:水合氯醛、氯氮卓、地西泮;(5)糖皮质激素:泼尼松;(6)利尿剂:氯噻酮、螺内酯;(7)非甾体抗炎药:阿司匹林、吲哚美辛;(8)抗甲状腺药:丙硫氧嘧啶、甲巯咪唑;(9)抑酸与胃黏膜保护药:西咪替丁、雷尼替丁、硫糖铝;(10)其他:别嘌醇、莫雷西嗪、奎尼丁、氯贝丁酯、维生素K、雌激素、口服避孕药、氟哌利多、维生素C、曲唑酮等。
大环内酯类抗菌药物、氯霉素、胺碘酮、别嘌醇、甲硝唑、咪康唑等抑制肝微粒体酶,使华法林的代谢降低,血浆药物浓度升高、血浆半衰期延长;苯巴比妥、格鲁米特、卡马西平、镇静催眠药、利福平、灰黄霉素等诱导肝脏细胞色素氧化酶系统,使华法林的代谢增加,从而使其抗凝作用减弱[24]。
3.1.5 服用期间应规避富含维生素K 的果蔬:鉴于华法林为维生素K 拮抗剂,在华法林治疗期间进食富含维K 的食物应尽量稳定,以免拮抗华法林的药理作用。富含维K 来源为绿色蔬菜叶,如葡萄柚、芒果、鳄梨、曼越桔、大蒜、生姜、洋葱、海藻、海带、豆奶、豆腐、寿司、菠菜、芹菜、花菜、甘蓝、卷心菜、菜花、芦笋、莴苣、绿萝卜、胡萝卜、蛋黄、猪肝、绿茶、椰菜、芽菜、包心菜、油菜籽油、合掌瓜、芫荽籽、黄瓜皮、苣荬菜、芥兰叶、奇异果、莴苣叶、薄荷叶、绿芥菜、柑榄油、荷兰芹、开心果、紫熏衣草、黄豆、黄豆油,长期服用可诱发华法林的并发症。
3.1.6 应用部分中药饮片宜谨慎:对联合应用部分具有活血化瘀功能的饮片,有增加大出血的风险。用药期间不宜服用益母草、月见草、甘草、钩果草、猫爪草、葫芦巴、大蒜、生姜、茴香、丹参、甘菊、蒲公英、银杏叶、当归、阿魏、黄芩、芹菜、紫云英、丁香油、山金车、小白菊、辣椒素、番木瓜、绣线菊、睡菜、金鸡钠等。而西洋参、人参、枸杞等可以减弱华法林的抗凝作用。
3.2 酸相关性疾病的药物治疗监护
体内胃酸分泌呈昼夜变化,入睡后几小时达峰,清晨醒前最低。胃液中的胃酸有助于杀灭食物里细菌,同时增加胃蛋白酶活性,对消化食物起着重要的作用。但胃液分泌过多,会出现吞酸、反胃等现象,与其相关性疾病包括:消化性溃疡(PUD)、胃食管反流病(GERD)、功能性消化不良(FD)、幽门螺杆菌感染(Hp)和出血等。其中影响酸相关性疾病因素有:(1)胃酸抑制程度;(2)每日胃酸抑制持续时间;(3)胃酸抑制疗程。在药物治疗中因注意监护:
3.2.1 保持抑酸剂最佳酸环境持续时间:一般抗酸药的抗酸持续时间仅为2 h,H2受体阻断剂(H2RA)为6 h,质子泵抑制剂(PPI)为18 h。延长抗酸达标的持续时间十分重要,而单纯控制pH≥3.0~4.0 并非能提高溃疡愈合率,使pH 达标的控制时间则为关键。如抑酸剂连续服用4 d,每日使pH≥3.0 维持16~18 h 能加速十二指肠溃疡的愈合;如pH≥4.0 维持17~18 h,预期愈合率达到100%;如胃液pH≥3.0 的时间少于每日的25%,则溃疡愈合效果不佳。再如反流性食管炎连续用药8 周,每日使pH≥3.0 维持18~20 h 的疗效最明显;十二指肠溃疡连续用药4 周,每日使pH≥3.0 维持18~20 h 的疗效最明显。常见消化性溃疡抑酸的最佳水平见表1。

表1 常见消化性溃疡抑酸的最佳水平
3.2.2 关注PPI 的用药安全性:(1)PPI 对妊娠期妇女、儿童的安全性尚未确立,对妊娠及哺乳期妇女、儿童禁用;对有过敏史及高龄者慎用。(2)PPI 可能掩盖胃癌症状,对疑有恶性肿瘤伴发胃溃疡者,须排除恶性病变后再用。(3)对溃疡治愈后需继续应用非甾体抗炎药治疗者,PPI 不能减量,以防无症状性溃疡的发生或加重。(4)PPI 很少发生耐药现象,但停药后引起的基础胃酸和最大胃酸分泌反弹持续时间则较长,可达2 个月。(5)肝、肾功能不全者慎用;严重肝损害者应减量并定期测定肝酶谱变化。
3.2.3 选择最佳服药时辰:(1)PPI:餐前30~60 min 即服。若与抗酸药联合应用,可降低其生物利用度,缘于抗酸药增加胃内酸度,防碍PPI 的溶解如需合用应至少间隔30 min。若与抗菌药物联合用于杀灭Hp,应在早餐前30 min 服用。其中奥美拉唑有“夜间酸突破”现象,睡前顿服可克服[25]。(2)H2RA:餐后口服比餐前效果为佳,此是因为餐后胃排空延迟,有更多缓冲作用;或每日下午或临睡前1 次服药疗效最佳。西咪替丁抑酸分泌作用出现早,与食物中和胃酸相重合,改用全日量睡前。(3)胃泌素受体阻断剂:丙谷胺于餐前15 min 给药。(4)胆碱受体抑制剂:哌仓西平早、晚餐前90 min 服用。(6)复方氢氧化铝:抗酸药应于餐后60 min 服用,以利于中和餐后的高胃酸;睡前加服1 次,效果更好。(7)胃黏膜保护剂:需在酸性条件下,与胃黏膜表面的黏蛋白络合形成保护膜,与抑酸药联合应用时宜间隔60 min。(8)硫糖铝:须空腹或餐前30~60 min 服用,不宜与牛奶、抗酸药同服,连续用药不宜超过8 周。(9)果胶铋:应在餐前30~60 min 服用或睡前服用,以达最佳疗效,服后粪便色泽可变黑,停药后1~2 d 内粪便色泽可转为正常。
3.2.4 提高PPI 的稳定性:PPI 具有相同的硫酸酰基苯并咪唑结构,其稳定性受到酸、光、金属离子、温度等多种因素影响,其中亚磺酰基为弱酸性化合物,pKa 约为4.0,其水溶液不稳定,易溶于碱,微溶于水,在酸性溶液中可持续发挥抑酸作用,但不稳定而极快分解[26],结构发生变化而出现聚合、变色,分解产物为砜化合物、硫醚化合物。为此,PPI 须制成肠溶制剂(片或胶囊、微囊),至小肠内溶解再吸收,以规避酸性的破坏作用,在临床应用须注意,服用时应以整片(粒)吞服,不得咀嚼和压碎,并至少在餐前1 h 服用。其注射剂仅用氯化钠注射液或专用溶剂溶解,不宜应用酸性较强的溶剂,且须在溶解后4 h 用毕。
3.2.5 对车辆驾驶员等特殊工作者应规避服用抑酸剂:抑酸药中组胺H2受体阻断剂雷尼替丁、西咪替丁、法莫替丁可能引起幻觉、定向力障碍;PPI 的奥美拉唑、兰索拉唑、泮托拉唑服后偶见有疲乏、嗜睡、视物模糊、意识模糊的反应。因此,对车辆驾驶员、高空作业、精密仪器操作者慎用,或提示在服用后休息6 h 后再从事工作。
3.3 围术期预防性应用抗菌药物的监护
预防性应用抗菌药物是在感染尚未发生之前开始用药,主要因为患者具有感染高危因素(手术、创伤、分娩、殖入、侵袭性操作)的经历,要有明确的时间性和目标性。围术期预防所致的感染,应强调在手术操作时人体组织中的抗菌药物浓度保持在有效杀菌水平,含概细菌侵入的危险时间段,术后则应尽快停用。应注意监护预防性用药的起始、持续时间,总预防用药时间不超过24 h,单剂给药与多剂给药相比预防手术感染效果并无明显差异[27]!
3.3.1 依据切口类型选择适宜的抗菌药物(活性与抗菌谱):应选择相对广谱、有效杀菌剂,并注意入侵细菌与抗菌药物的活性与抗菌谱相互匹配。头孢菌素较理想,列为首选。抑菌剂作用弱;氨基糖苷类具有严重耳、肾毒性;氟喹诺酮类抗菌谱不够平衡,细菌耐药率高,原则上不选。下列部位的切口应依据卫生部文件要求选择:(1)心脏、心血管、头颈、胸腹、四肢:金黄色葡萄球菌、凝固酶阴性葡萄球菌——头孢唑林、头孢拉定。(2)腹腔、盆腔、空腔脏器:大肠杆菌、肠杆菌(产气杆菌、阴沟杆菌)、肺炎克雷白杆菌——头孢呋辛。(3)食管、下消化道(胆、阑尾、结直肠):厌氧菌(脆弱类杆菌、梭状芽孢)、革兰阴性菌——头孢呋辛、头孢噻肟+硝基咪唑类。(4)泌尿道:革兰阴性菌——头孢唑林、头孢呋辛。(5)妇产生殖:革兰阴性菌、肠球菌、B 族链球菌、厌氧菌——头孢呋辛、头孢曲松、头孢噻肟+硝基咪唑类。(6)乳房、剖宫产:葡萄球菌——头孢唑林。(7)使用人工植入物骨科手术:金黄色葡萄球菌,凝固酶阴性葡萄球菌,革兰阴性杆菌——头孢唑林、头孢呋辛、头孢曲松。
对青霉素和头孢菌素过敏者,针对革兰阳性球菌可选克林霉素,针对杆菌可用氨曲南,或两者联合使用。
3.3.2 警惕术中可致严重出血反应的抗菌药物:头孢菌素中的头孢孟多、头孢唑林、头孢孟多酯、特仑匹酯、泊肟匹酯、头孢曲松、头孢哌酮、头孢甲肟、头孢布烯、头孢唑肟、头孢克肟、头孢美唑、头孢米诺、拉氧头孢、美罗培南等均可发生。上述抗菌药物在分子中有一甲硫四氮唑结构,与谷氨酸分子结构相似[28],在肝脏微粒体中,与维生素K 竞争性结合谷氨酸-γ 羟化酶,抑制肠道正常菌群,减少维生素K 合成,导致维K 依赖性凝血因子合成障碍而减少,并减弱凝血功能(低凝血酶原血症)而致出血。其发生凝血障碍与用量、疗程密切相关!
3.3.3 警惕术中可致凝血机制异常的抗菌药物:大剂量青霉素类(青霉素、羧苄西林、美洛西林、哌拉西林、阿洛西林、替卡西林、磺苄西林等)应用时偶可出现凝血机制异常;头孢菌素中头孢孟多、头孢哌酮、头孢噻肟、拉氧头孢、头孢匹胺、氨曲南等引起的凝血机能障碍与自发性出血反应已引起重视;头孢替坦、头孢米诺、替卡西林/克拉维酸钾、氨曲南、亚胺培南/西司他丁、厄他培南可使凝血酶原时间延长,引起出血和术中出血!3.3.4 警惕高胆红素血症儿童不能应用头孢菌素:头孢曲松钠可将胆红素从血清白蛋白上置换下来,患高胆红素血症的新生儿(尤其早产儿)可能发展成核黄疸或致死,应避免用于高胆红素血症的新生儿。其他头孢菌素也可从血清白蛋白中置换胆红素,发生胆红素脑病,新生儿禁用。
另新生儿酶系统不成熟,口服氯霉素后由于缺乏葡萄糖醛酸转移酶,不能与葡萄糖醛酸结合为无活性代谢物,致游离氯霉素增多,新生儿皮肤呈灰色,引起“灰婴综合征”;磺胺药、硝基呋喃类也使葡萄糖醛酸转移酶缺乏的儿童溶血。对黄疸不退儿童应用酶促剂苯巴比妥或人白蛋白,可促使胆红素排出。
3.4 给药时间适宜性监护
人体的器官功能和分泌状态伴随时间的推移所呈现规律性变化,包括近日节律(昼夜节律,circadian rhythm)和近年节律(circannual rhythm)。各种生物的生命活动均具有时间的规律性,包括体温、血糖、血压、血脂、基础代谢率等与昼夜、季节变化都有一定的关系。药物疗效和不良反应同样与给药时间密切相关。因此,药师依据时辰药理学,指导患者选择适宜服药时间,可达到以下效果:(1)顺应人体生物节律变化,充分调动人体积极的免疫和抗病因素;(2)增强药物疗效,提高药物的生物利用度和血浆峰浓度;(3)减少ADR 和减小剂量;(4)促进合理用药,节约医药资源;(5)提高患者的用药的依从性。
3.4.1 溶栓药的治疗时间窗:目前,基因重组组织型纤溶酶原激活剂(阿替普酶)对血栓开通率提高,但血浆半衰期短,须连续静脉给药;第3 代溶栓药瑞替普酶,与第2 代溶栓酶相比,其血浆半衰期长,栓塞开通率高,给药方便。但上述溶栓酶治疗时间窗为发病后3~4.5 h 内,对时间窗及适应证的要求应严格[29],否则易引起颅内出血。
急性脑卒中发作后,闭塞动脉供血区中心部分缺血严重,梗死将在60 min 内形成。梗死周边部分缺血组织可通过侧支循环得到部分血流,使之维持在泵衰竭水平之上、电活动需要量以下,即缺血半暗带。急性脑组织梗死后,梗死周边组织会按照组织血流量[单位:ml/(100 g·min)]分为正常组织[50 ml/(100 g·min)]、血流异常组织[40 ml/(100 g·min)]、电衰竭[20 ml/(100 g·min)]、膜衰竭[8~10 ml/(100 g·min)]和死亡组织[0 ml/(100 g·min)],其中电衰竭和膜衰竭之间的脑组织为缺血半暗带,位于最严重的缺血区和血正常灌注区之间的中间区,其可向正常和死亡组织双向移动,即及时溶栓恢复供血可促使脑组织(缺血半暗带)复活,实验表明,如这种不稳定的血流3~4 h 后仍不改善,则可能出现代谢衰竭乃至死亡。尽早用药的目的是:(1)超早期治疗的关键是抢救缺血半暗带(早期恢复供血、缩小梗死面积),采取脑保护措施减轻再灌注损伤[30]。超过6 h 的缺血性脑卒中者可给予尿激酶100~150 万IU,静脉滴注30 min。(2)血栓富含水分,易于溶解。
3.4.2 抗心绞痛药的治疗时间窗:抗心绞痛药的疗效也有节律性,钙通道阻滞剂、β 受体阻断剂、硝酸酯类药于上午服用,可明显扩张冠状动脉、改善心肌缺血,下午服用的作用强度不如前者[31]。硝苯地平对心绞痛发作的疗效存在一定的昼夜节律差别,日均剂量80 mg 对心电图心肌缺血有明显的改善作用,几乎可完全取消通常于上午6:00~12:00 发生的心肌缺血高峰,对下午21:00~24:00 的心肌缺血虽有一定作用,但强度明显不如前者,强度约为1/4。同时心绞痛发作的昼夜节律(稳定或不稳定型心绞痛),其发作均具有相似的昼夜节律。对1 002 例慢性稳定型心绞痛患者的总计33 999 次发作进行分析,发现每日0:00~6:00 发作次数最少,6:00 后增多,上午10:00~12:00 为发作达峰,这一节律在劳力型心绞痛者尤其显著。钙通道阻滞剂尤其是硝苯地平适宜于清晨用药。
4 开展药物系统评价和药物经济学研究
4.1 靶向治疗药的药物经济学思考
靶向抗肿瘤药疗效较为显著,毒副作用相对较小,但价格昂贵,在很大程度上限制了其在临床的应用。有关靶向治疗药药物经济学评价,需关注2 个层面:(1)首先需严格控制靶向药适应证(基因检测),尤其是病理分子分型。如曲妥珠单抗在使用时应确定是否人表皮生长因子受体-2(HER-2)阳性,只有阳性者才有使用指征,其为人HER-2 胞外区的人源化单克隆抗体,仅阳性患者都可从曲妥珠单抗治疗中获益[32-33]。同时也应积极预测靶向药物疗效的分子标记物,如应用西妥昔单抗治疗直、结肠癌时,疗效与癌蛋白(KRAS)基因第12 或第13位密码子的突变状态有关,仅对KRAS 野生型患者可延长无进展生存时间,对没有发生突变的野生型(约60%患者)有效,突变型不仅无效(约40%患者),且增加副反应,浪费经费,因为KRAS 基因突变后会自发激活RAS-Raf 传导通路,而不再受EGFR 调控[34]。把真正能够从靶向药治疗中获益人群筛选出来,避免过度使用。(2)其次是靶向抗肿瘤药的药物经济学分析。与传统放化疗的比较,靶向药物单价较高,但与化疗比具有不良反应少、不需要住院的优点,在住院费用以及毒副作用处理方面可以节约费用。同时,靶向药物多数可以取得较好的临床反应率,但经验告诉我们,临床试验中客观反应率或中位肿瘤无进展时间不等同于生存时间的优势。在患者中位生存时间、中位肿瘤无进展时间、患者生活质量、安全性指标上有无显著差异,成本/效益比值等药物经济学问题仍需继续考验。
4.2 抗菌药物的应用评价
头霉素类(头孢西丁、头孢米诺)从药学效及药动学讲都是较差的药物,尤其不适合呼吸道感染,呼吸道感染的常见病原菌,如肺炎链球菌药效较差,但却在国内大量使用。很多老年人就是因为早期选用的抗菌药物疗效差,延误有效治疗,成为重症或频死[35]。总体而言,头霉素类抗菌作用均较头孢菌素微弱,对厌氧菌较果较好。在国外通常用于腹部及妇科手术的预防性用药。第2 代头孢菌素中头孢孟多酯钠、头孢替坦,可干扰维生素在肝脏的代谢,造成低凝血因子Ⅱ血症,对凝血功能的干扰较大,导致出血倾向或出血时间延长,不宜作为围术期预防性用药[36]。第3 代头孢菌素:一种属于平衡广谱、非抗铜绿假单胞菌的第3 代头孢菌素,用于革兰阴性和革兰阳性菌感染,但不抗铜绿假单胞菌,代表药为头孢曲松;另一种为抗铜绿假单胞菌的第3 代头孢菌素,仅用于革兰阴性杆菌感染,对革兰阳性菌感染无效,代表药为头孢他定。
4.3 给药剂型的应用评价
出于“用药幼稚和误区”,同时追求丰厚经济利益,临床中滥用注射剂现象司空见惯,使我国输液剂年总产量超过百亿瓶,人年均8 瓶,远超世界水平(2.5~3.3 瓶),成为不合理用药的重灾区。其所带来的感染、创伤、炎症、血栓、异物、血栓、微粒、热源和热源样反应、过敏反应乃至死亡事件和医疗费用的浪费十分震惊,在2013 年全国严重不良反应/事件报告中,占据总量的七成,排序居第1 位。
氯化钠注射液、葡萄糖注射液在2010 年、2011 年全国销售金额分别连续占据国内全部用药金额排序(2010 年化学药品品种数为2 174 种,总金额为1 142.6 亿元;2011 年化学药品品种数为2 203 种,总金额为1 328.92 亿元)的第1、12 位,销售总金额方面,氯化钠注射液为20.6 和24.13 亿元,葡萄糖注射液为9.49 和10.68 亿元。2 年排序分别居第6、4 位的为人血白蛋白,其销售总金额分别为11.11、16.07 亿元。另外,包括二磷酸果糖、转化糖、转化糖电解质注射液等临床疗效有待验证的药品也排序较前(分别居第180、123、144 位)。静脉输液剂的生产量、临床用量已经远远超过病患者实际需求量,也远远超过世界发达国家的用药量。药师应遴选不合理用药指征的标的药品,尤其应重点监测:(1)有口服给药剂型,且2 种给药途径(口服、静脉滴注)的生物等效性(吸收率、生物利用度、血浆浓度达峰时间)相近,但治疗成本(价格)相差数倍或十数倍的药品,如氟喹诺酮类抗菌药物,见表2。(2)口服吸收良好,血浆半衰期长,且连续治疗时间(疗程)较长,没有必须注射给药指征的药品,如阿奇霉素服后较易吸收,生物利用度为37%~40%,血浆半衰期长达48~72 h,1 日1 次给药,疗程一般为5~7 d。(3)有口服给药剂型,且静脉滴注更易发生严重毒性或不良反应的药品,如抗病毒药阿昔洛韦静脉注射所致的严重肾毒性;血浆代用品羟乙基淀粉注射液所致的肝、肾毒性。(4)临床应用不近合理,有超常用药现象的药品,如人血白蛋白。
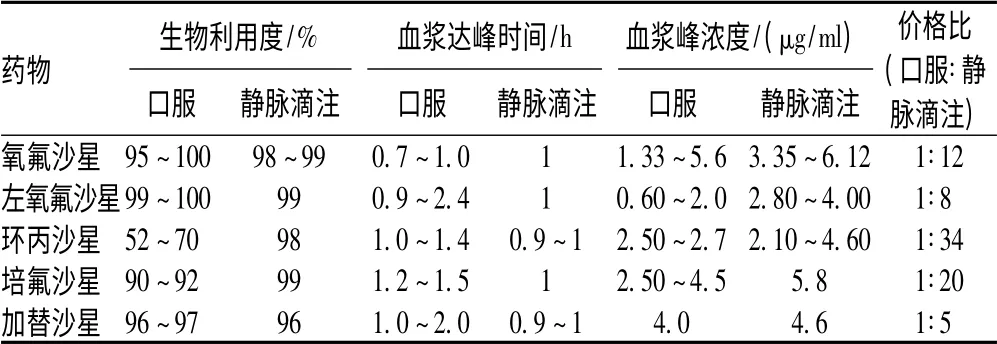
表2 生物等效性近似的氟喹诺酮类抗菌药物
4.4 处方点评与处方分析
4.4.1 处方点评:依据《药品管理法》、《处方管理办法》和《医院处方点评管理规范》等有关法律、法规与规章,开展处方点评。每月定期、定量、随机抽查门、急诊处方和病房医嘱(n=100 张),对处方书写的规范性及药物临床使用的适宜性(药品适应证、药物选择、给药途径、用法用量、药物相互作用、配伍禁忌等)进行评价。对不合理用药的处方(超适应证、无适应证、超剂量、超疗程、有禁忌证、不良药物相互作用、有配伍禁忌)本着公平、公正的原则和科学、严谨的学风,进行学术性和理论性分析,结合药学和行政干预手段,促进合理用药水平。
4.4.2 处方分析:为科学、真实地反映医院临床、药店合理用药状况,评价上市后药品(药品亚类、次亚类、小类或通用名称药品)的临床疗效(主要观察终点、次要观察终点、毒性、不良反应、副作用)或一种疾病的药物治疗方案的治疗效果、成本/效益分析或Meta 分析。(1)门诊处方(医嘱)或医院信息系统(HIS)数据分析:处方数据应有连续3 年跨度的时段,最好是省市、地区乃至全国样本采购药品数据,或门诊处方量5 000 张以上,进行用药频度(DDDs)、药物利用指数(DUI)、限定日费用(DDC)、金额/DDDs 排序比(B/A)分析、临床诊断与用药适宜性分析、联合用药分析。主要考察药品的利用度、用药趋势与因果关系、用药频度、用药金额、用药金额与用药人数的同步性、处方合理性。(2)病例分析:确定1 种适应证的不少于2 000 例临床病例,或1 种通用名称药品的治疗病例,求出用药的主要疗效(临床诊断与用药适宜性分析、有效率、临床症状、主要终点事件、次要终点事件、中位无疾病进展时间、中位生存期、细菌学清除率、联合用药等)和副作用(不良反应、不良事件)、剂量、疗程、性别、周期等差异参数,进行统计学处理。主要考察药品的利用度、疗效、不良反应及合理性。(3)药品疗效的文献Meta 分析:选择1 种药品20 个随机对照试验(RCT)以上、300 个RCT 以下的Meta 分析,求出各组(治疗组、阳性药物对照组、空白对照组)的主要疗效(有效率、临床症状、主要终点事件、次要终点事件、中位无疾病进展时间、中位生存期、生活质量等)和副作用(不良反应、不良事件)等参数,进行统计学处理。主要考察药品(联合用药方案)的利用度、疗效、设定的主要观察终点(亚组)、不良反应及用药合理性,并做出森林图和漏斗分布图。
5 关注循证医学和学习指南
5.1 循证医学内容
循证医学(evidence-based medicine,EBM)又称有据医学或实证医学,即遵循证据的医学,其核心思想是医务人员应该谨慎、正确、明智地运用在临床研究中得到的最新的、最有力的科学研究信息来诊治患者。循证医学是研究证据与医师的临床实践及患者价值三者之间的最佳结合,为患者的诊治做出最佳决策和方案。这是医师、药师必须掌握的条件与素质。
5.2 循证医学信息
循证药物信息(EBDI)以多中心、随机、双盲、对照的临床试验为主体,以计算机/数据库技术实现高效、准确数据作统计,对药物疗效做出客观评估,得到充足证据的药物信息。美国药典信息开发部对药物适应证或禁忌证信息开始注明证据等级,共分5 类3 级:A 类:有良好证据支持;B 类:有较好证据支持;C 类:缺乏证据支持;D 类:有较充实的证据反对;E 类:有充分证据反对。证据1 级来自至少1 个适当的RCT;证据2 级来自至少1 个未随机化但设计完善的试验;证据3 级来自权威的临床经验为基础的意见、描述性研究或专家委员会的报告。例如抑肽酶用于减少外科手术出血,在常位肝移植术的等级为C-1,在全髋关节置换术的等级为C-1,在心脏外科急性心肌梗死使用重组组织型纤溶酶原激活剂、尿激酶或链激酶的出血控制的等级为C-3。
5.3 循证医学的证据分类
目前,临床应用的英国牛津大学循证医学中心(Oxford Centre for Evidence-based Medicine)在2001 年制定的证据等级标准(证据级别分类为5 级;推荐建议分为A、B、C、D 4 级)以及在2004 年推出的将各个分级标准综合而形成的GRADE 标准(分为高、中、低、极低4 个等级;推荐建议只分为强、弱2 级)。
循证医学中的证据主要指临床人体研究的证据,包括病因、诊断、预防、治疗和预后等方面的研究。依据按质量和可靠程度分为5 级:(1)一级(A 级):按照特定病种的特定疗法收集所有质量可靠的随机、对照试验后所作的系统评述(SR),包括Meta分析(汇总、荟萃),是国际公认的最有效、最安全、最可靠的依据(金标准)。(2)二级(B 级):单个样本量足够的RCT 结果(建议采用)。(3)三级(C 级):设有对照组但未用随机方法分组的研究(可以采用)。(4)四级(D 级):无对照的系列病例观察(可供参考)。(5)五级(E 级):病例报告、根据专家个人多年临床经验提出的诊治方案、经验和观点(仅供参考)。
5.4 关注“指南”
“临床诊疗指南”(简称“指南”)是在浩如烟海的全球年逾200 万篇生物医学文献中检索和荟萃,经严格检验的事实、最佳研究成果、循证医学证据(多项设计良好RCT),并经一批流行病学、医学、临床药学、药物经济学、卫生统计学、社会医学和信息学等专家共同协作,分析和评价,达成共识意见并形成的。“指南”基本体现相关医学领域(治疗系统)最佳研究现状和结论,是临床医、药师最为强大理论和实践依据(包括用药方案、药品应用、安全与有效性评价、经济学评价等)。一个好的“指南”可以改变临床实践的结果和患者的预后。因此,临床药师必须关注各种新版“指南”的进展,掌握其中精髓,以真正寻觅到医药契合的切入点,掌握合理用药的真谛。
5.4.1“ 指南”的特点:(1)广泛性:多种学科的疾病均有“指南”。以心血管内科为例,临床“指南”涵盖绝大部分心血管系统的常见病和多发病,如原发性高血压、血脂异常(高脂血症)、心力衰竭、心房颤动、心肌梗死、心律失常等,甚至具体到某一种疾病的处置或某一类药物的应用均可制定相应的“指南”。此外,广泛性还包据针对各种相关临床工作者的“指南”,诸如医师、药师、护士等。(2)权威性:“指南”在总结大量系统评价与循证医学证据的基础上,由专家共同商讨制定,是临床研究精华的荟萃。(3)时效性:所有“指南”均非固定不变的,有一定的使用周期,需要随时依据新证据进行修改。以心力衰竭的治疗原则为例,传统的“强心、利尿、扩张血管”已转化为当前的“拮抗神经内分泌过度激活、改善血流动力学、延缓心肌重构”,这对心力衰竭的临床药物治疗具有重大指导意义,其结果就是传统的强心苷类的地高辛等已退居次席,血管紧张素转换酶抑制剂、血管紧张素Ⅱ受体阻断剂和β 受体阻断剂(改善左室功能、降低心脏猝死)、利尿剂(控制液体潴留)等已成为首选的药物治疗选择。(4)地域性:“指南”是由各医学专门权威机构制定的,这些机构分布于全球各地,根据本国、本地区的流行病学、疾病谱以及基因组学特点制定的“指南”,多数是对特定对象研究后得出的结果,故同一疾病可能存在多个“指南”。比如“高血压病临床指南”就包括欧洲心脏学会、美国心脏学会/美国心血管学会和中华医学会心血管病学分会等不同版本,正确参考不同版本的临床“指南”可以避免认识上的混乱。
5.4.2“ 指南”在循证医学上的等级:依据循证医学等级原则(A-E),各医药学专业组织(学会)制定的“指南”在2004 年中国循证医学中心制定的证据分5 级的标准中被定为B 级,“专家共识”定为E 级。“指南”是非强制性的,它即非行政部门指令,更不是政策法规,仅是一个业务领域的指导性文件,是不断提高医疗水平、合理用药水平、改善患者预后的建议。因此,在临床实际应用中必须密切结合实际实施个体化治疗,绝不能生搬硬套。选择“指南”的原则有:(1)优先选用国内各种“指南”;(2)参考和应用美国、英国、法国、加拿大、欧盟等发达国家的相关“指南”;(3)应用最新版本,保持学术的前沿性;(4)不同“指南”意见相互矛盾和有争议时,应结合我国临床实践,公正评价和遴选;(5)注意前因后果,切忌断章取义,应全面、客观、如实摘要;(6)注意人种、性别、基因组、个体化的差异。
如建议在经皮冠状动脉介入治疗(PCI 术)前使用高剂量他汀类药以降低围术期急性心肌梗死(AMI)风险是合理的[《美国经皮冠脉介入术指南》(2012),A/B 级证据,Ⅱa 推荐][37];建议对所有急性冠脉综合征(ACS)者,一旦入院治疗,勿论其血脂水平如何,均即给予高剂量(负荷量)他汀类药,并应用维持量稳定一定时期(一般用4~6 周后再予以评估是否继续给药),即可大大降低主要心血管事件(MACE)[《欧洲心血管疾病防治指南》(2012),A 级证据,Ⅰ级推荐][38]。他汀类药可减少心血管内皮过氧化,稳定或缩小动脉粥样硬化脂质斑块,其调节血脂外的多效性,已使其从调节血脂药转为一类新抗动脉粥样硬化药[39]。
阿司匹林用于预防心脑血管不良事件的业绩昭著,已被多项循证医学研究结果所确立。其可使任何心脑血管事件发生率下降1/4、致死性心肌梗死下降1/3、心脑血管病死亡下降1/6、心绞痛发作下降1/20。目前已有6 个RCT(BMD、HOT、PPP、PHS、TPT 和WHS)总计98 000 例心血管高危因素者的研究,对阿司匹林在无冠心病病史患者中的作用进行评价,结果显示,阿司匹林能使血管事件的总发生率下降15%,使心肌梗死和冠心病死亡的危险性总体降低23%[40]。美国心脏病学会(ACC)建议阿司匹林用于10 年心血管事件危险≥10%的健康者;英国高血压协会建议对50 岁以上、患高血压但血压控制满意(<150/90 mmHg)、同时具靶器官损害、糖尿病或有高血压病史10 年发生心力衰竭的危险性≥5%者服用。阿司匹林在心脑血管疾病一级预防的作用予以充分的肯定与全面推荐[41][美国糖尿病协会(ADA)糖尿病指南(2011)、美国心脏病协会(AHA)和美国脑卒中协会(ASA)脑卒中一级预防指南(2010)、《中国心血管疾病一级预防指南》(2011)、《中国高血压防治指南》(2010),A 级证据,Ⅰ级推荐]。
心房颤动(atrial fibrillation)是临床十分常见的心律失常,心房颤动并发体循环栓塞具有极高的风险性,我国每年新增200 万例脑卒中患者,其中15%~20%是由心房颤动所致,其治疗策略包括心律控制、心室率控制和抗栓治疗3 个方面。2010年欧洲心脏病学会(ESC)发布的《欧洲心房颤动诊疗指南》指出:“抗凝治疗是降低心房颤动相关卒中死亡率的关键”!中国首个《心房颤动抗凝血治疗中国专家共识》(2013 年)明确指出,若无禁忌证,CHADS2(充血性心力衰竭、高血压病、年龄≥75岁、糖尿病、卒中或短暂性脑缺血发作病史)评分≥1 分的心房颤动者,诱发脑卒中风险较高,应积极进行抗凝治疗[42]。
综上所述,药品是把双刃剑,疗效与不良反应并存,利弊相依。疗效是患者、医生和执业药师所期盼的理想结果,而不良反应(包括毒性、副作用、后遗作用、有害的相互作用、三致反应)是在与疾病搏击中所必然要付出的代价,是潜在的、正常的和不可预知的,但可规避和减少!药师应追求药物治疗的最大获益(使药物的作用发挥的淋漓尽致),而规避不良反应直至最小(使潜在风险分化得风吹草尽),达到药物治疗的理想境界,即是药师的本责和风范。“位卑未敢忘国”,“学而不厌,诙人不倦。”
[1] Taubel J,Ferber G,Lorch U,et al.Thorough QT study of the effect of oral moxifloxacin on QTc interval in the fed and fasted state in healthy Japanese and Caucasian subjects[J].Br J Clin Pharmacol,2013,75(5):1328-1335.
[2] Komatsu R,Honda M,Holzgrefe HH,et al.Sensitivity of common marmosets to detect drug-induced QT interval prolongation:moxifloxacin case study[J].J Pharmacol Toxicol Methods,2010,61(3):271-276.
[3] Bloomfield DM,Kost JT,Ghosh K,et al.The effect of moxifloxacin on QTc and implications for the design of thorough QT studies[J].Clin Pharmacol Ther,2008,84(4):475-480.
[4] Hsieh J,Kuzmanovic I,Vargas MI,et al.Cerebral venous thrombosis due to cryptogenic organising pneumopathy with antiphospholipid syndrome worsened by heparininduced thrombocytopenia[M].BMJ Case Rep,2013.
[5] Alsaleh KA,Al Nasser SM,Bates SM,et al.Delayed-onset HIT caused by low-molecular-weight heparin manifesting during fondaparinux prophylaxis[J].Am J Hematol,2008,83(11):876-879.
[6] Dasararaju R,Singh N,Mehta A.Heparin induced thrombocytopenia:review[J].Expert Rev Hematol,2013,6(4):419-428.
[7] Hassell K.Heparin-induced thrombocytopenia:diagnosis and management[J].Thromb Res,2008,123(Suppl 1):S16-S22.
[8] Pascoalinho D,Vilas MJ,Coelho L,et al.Linezolid-related immuune-mediated severe thrombocytopenia[J].Int J Antimicrob Agent,2011,37(1):88-89.
[9] Nukui Y,Hatakeyama S,Okamoto K,et al.High plasma linezolid concentration and impaired renal function affect development of linezolid-induced thrombocytopenia[J].J Antimicrob Chemother,2103,68(9):2128-2133.
[10] Angela L,Andrea Gaedigk,Laura P,et al.Defining Risk Factors for Red Man Syndrome in Childrenand Adults[J].Pediatr Infect Dis J,2012,31(5):464-468.
[11] de Waard MC,Bierman H,Brinckman SL,et al.Autometed peritoneal larage:an extremely rapid and safe way to induce hypothermia in post-resuscitatuon patients[J].Crit Cure,2013,17(1):R31-R35.
[12] Tasdemir S,Tasdemir C,Vardi N,et al.Effects of ozone therapy on cyclophosphamide-induced urinary bladder toxicity in rats[J].Clin Invest Med,2013,36(1):E9-E17.
[13] Badalow N,Baradarian R,Iswara K,et al.Drug-induced acute pancreatitis:an evidence-based review[J].Clin Gastroenterol Hepatol,2007,5(6):648-661.
[14] Kunjathaya P,Ramaswami PK,Krishnamurthy AN,et al.Acute nacrotizing pancreatitis associated with vildagliptin[J].JOP,2013,14(1):81-84.
[15] Sue M,Yoshihara A,Kuboki K,et al.A case of severe acute necrotizing pancreatitis after administration of sitagliptin[J].Clin Med Insights Case Rep,2013(6):23-29.
[16] Exenatide and sitagliptin:pancreatitis and pancreatic cancer.Harms on the rise[J].Prescrire Int,2011,20(121):267.
[17] Dawe RS,Ibbotson SH,Sanderson JB,et al.A randomized controlled trial(volunteer study)of sitafloxacin,enoxacin,levofloxacin and sparfloxacin phototoxicity[J].Br J Dermatol,2003,149(6):1232-1241.
[18] Bonamonte D,Foti C,Lionetti N,et al.Photoallergic contact dermatitis to 8-methoxypsoralen in Ficus carica[J].Contact Dermatitis,2010,62(6):343-348.
[19] Kozlowski D,Budrejko S,Raczak G,et al.Anticoagulant prevention in patients with atrial fibrillation:alternatives to vitamin K antagonists[J].Curr Pharm Des,2013,19(21):3816-3826.
[20] Ghanbari H,Phard WS,Al-Ameri H,et al.Meta-analysis of safety and efficacy of uninterrupted warfarin compared to heparin-based bridging therapy during implantation of cardiac rhythm devices[J].Am J Cardiol,2012,110(10):1482-1488.
[21] Hylek EM.Vitamin K antagonists and time in the therapeutic range:implications,challenges,and strategies for improvement[J].J Throm Thrombolysis,2013,35(3):333-335.
[22] Toyoda K.Antithrombotic therapy for pregnant women[J].Neurol Med Chir,2013,53(8):526-530.
[23] Martins MA,Reis AM,Sales MF,et al.Rifampicinwarfarin interaction leading to macroscopic hematuria:a case report and review of the literature[J].BMC Pharmacol Toxicol,2013(14):27-29.
[24] Carlquist JF,Horne BD,Muhlestein JB,et al.Genotypes of the eytochrome P450 isoform,CYP2C9,and the vitamin K epoxide reductase complex subunit 1 conjointly determine stable dose:a prospective study[J].Thromb Thrombolysis,2006,22(3):191-197.
[25] Janiak P,Thumshirn M,Menne D,et al.Clinical trial:the effects of adding ranitidine at night to twice daily omeprazole therapy on nocturnal acid breakthrough and acid reflux in patients with systemic sclerosis-a randomized controlled,cross-over trial[J].Aliment Pharmacol Ther,2007,26(9):1259-1265.
[26] Higuchi Y,Takesue Y,Yamada Y,et al.A single-dose regimen for antimicrobial prophylaxis to prevent perioperative infection in urological clean and clean-contaminated surgery[J].J Infect Chemother,2011,17(2):219-223.
[27] Missaghi S,Young C,Fegely K,et al.Delayed release film coating applications on oral solid dosage forms of proton pump inhibitors:case studies[J].Drug Dev Ind Pharm,2010,36(2):180-189.
[28] Ozen IO,Moraliogˇlu S,Karabulut R,et al.Cefoperazone induced gastro-intestinal haemorrhage.A case report[J].Acta Chir Belg,2008,108(6):777-778.
[29] Fisher M,Albers GW.Advanced imaging to extend the therapeutic time window of acute ischemic stroke[J].Ann Neurol,2013,73(1):4-9.
[30] Minematsu K,Toyoda K,Hirano T,et al.Guidelines for the intravenous application of recombinant tissue-type plasminogen activator (alteplase),the second edition,October 2012:a guideline from the Japan Stroke Society[J].J Strock Cerebrovasc Dis,2013,22(5):571-600.
[31] Kardas P.Compliance,clinical outcome,and quality of life of patients with stable angina pectoris receiving once-daily betaxolol versus twice daily metoprolol:a randomized controlled trial[J].Vasc Health Risk Manag,2007,3(2):235-242.
[32] Romond EH,Perez EA,Bryant J,et al.Trastuzumab plus adjuvant chemotherapy for operable HER2-positive breast cancer[J].N Engl J Med,2005,353(16):1673-1684.
[33] Chung C,Lam MS.Pertuzumab for the treatment of human epidermal growth factor receptor type2-positive metastatic breast cancer[J].Am J Health Syst Pharm,2013,70(18):1579-1587.
[34] Bokemeyer C ,Bondarenko I ,Hartmann JT ,et al .Biomarkers predictive for outcome in patients with metastatic colorectal cancer (mCRC)treated with first-line FOLFOX4 plus or minus cetuximab:Updated data from the OPUS study[C].Orlando,USA:Proceedings of American Society of Clinical Oncology(ASCO)Gastrointestinal Cancer Symposium,2010:428-430.
[35] Dale W.Bratzler,Peter M.Antimicrobial prophylaxis for surgery:an advisory statement from the national surgical infection prevention project [J].Clinical Infectious Diseases,2004,38(12):1706-1715.
[36] Kaiser CW,McAuliffe JD,Barth RJ,et al.Hypoprothrombinemia and hemorrhage in a surgical patient treated with cefotetan[J].http://www.ncbi.nlm.nih.gov/pubmed?term = McAuliffe% 20JD% 5B Author% 5D&cauthor = true&cauthor_uid = 1901205Arch Surg,1991,126(4):524-525.
[37] Lyseng-Williamson KA.Prasugrel:a guide to its use in patients with acute coronary syndromes undergoing percutaneous coronary intervention in the US[J].Am J Cardiovasc Drugs,2012,12(3):207-216.
[38] Perk J,De Backer G,Gohlke H,et al.European guidelines on cardiovascular disease prevention in clinical practice(version2012):the fifth joint task force of the European society of cardiology and other societies on cardiovascular disease prevention in clinical practice (constituted by representatives of nine societies and by invited experts)[J].Int J Behav Med,2012,19(4):403-488.
[39] Perk J,De Backer G,Gohlke H,et al.European Guidelines on cardiovascular disease prevention in clinical practice (version 2012).The Fifth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice(constituted by representatives of nine societies and by invited experts)[J].Eur Heart J,2012,33(13):1635-1701.
[40] Antithrombotic Trialists’(ATT)Collaboration,Baigent C,Blackwell L,et al.Aspirin in the primary and secondary prevention of vascular disease:collaborative meta-analysis of individual participant data from randomized trials[J].Lancet,2009,373(9678):1849-1860.
[41] Goldstein LB,Bushnell CD,Adams RJ,et al.Guidelines for the primary prevention of stroke:a guideline for healthcare professionals from the American Heart Association/American Stroke Association[J].Strock,2011,42(2):517-584.
[42] Ahmad Y,Lip GY.Dabigatran etexilate for the prevention of stroke and systemic embolism in atrial fibrillation:NICE guidance[J].Heart,2012,98(19):1404-1406.
