呋喃酰腙及其镍、锰配合物的合成与晶体结构及抑菌活性
2014-01-02杨滋渊徐守卫郑长征
杨滋渊 宋 斌 徐守卫 郑长征*,
(1陕西省人民医院,西安 710068)
(2西安工程大学,环境与化学工程学院,西安 710048)
Schiff碱类化合物主要以O、N为配位原子,作为配体具有较强的配位能力和多样的配位方式[1-3],形成的金属配合物在分析化学、催化化学、功能材料、生物及药物活性等方面有广泛的应用[4-9]。呋喃环化合物作为五元杂环化合物的典型代表,广泛存在于自然界,大多具有抑菌、消毒、杀虫等生物活性[10-13]。从生物化学方面看,呋喃环中的氧原子可参与生物体中氢键的形成,增加授受间分子亲和性,将呋喃环导入Schiff碱类化合物后得到的化合物拥有更好的抑菌活性[14]。因此研究呋喃酰腙及其配合物的抑菌活性具有重要意义。本文用2-呋喃甲醛与4-甲氧基苯甲酰肼缩合出一个未见报道的新型呋喃酰腙化合物2-呋喃甲醛缩对甲氧基苯甲酰腙,用溶剂挥发法获得配体及其与Ni、Mn的两个配合物单晶,通过X-射线单晶衍射确定了晶体结构,用琼脂扩散法测定了抑菌活性。
1 实验部分
1.1 试剂与仪器
4-甲氧基苯甲酸乙酯、2-呋喃甲醛(使用前经蒸馏)、水合肼(80%)以及其它试剂均为市售分析纯。
Varian-400型核磁共振仪(美国),FTIR-8400 型红外光谱仪(KBr压片)(日本),Vario ELⅢ型元素分析仪(德国),Bruker Smart-APEXII CCD 单晶衍射仪(德国)。
1.2 配合物的合成
1.2.1 配体2-呋喃甲醛缩对甲氧基苯甲酰腙(HL)的合成
4-甲氧基苯甲酰肼参考文献方法[15]制备,产率83%。
搅拌下,用恒压滴液漏斗向溶有8.30 g(0.05 mol)4-甲氧基苯甲酰肼的50 mL乙醇溶液中缓慢滴入新蒸馏的4.80 g(0.05 mol)2-呋喃甲醛,TLC跟踪,反应完成后冷却至室温析出浅黄色固体,抽滤,少量冰无水乙醇洗涤得粗品。粗品用无水乙醇重结晶,真空干燥得淡黄色固体,产率78%。称取0.122 g(0.5 mmol)配体HL搅拌溶解在30 mL乙醇和DMF(体积比为14∶1)的混合溶剂中,过滤,滤液室温静置挥发14 d,得到适合X-射线单晶衍射测试的无色单晶。合成路线图见图1。

图1 合成路线图Fig.1 Synthetic route
1H NMR(DMSO)δ:7.05~7.89(4H,Ar-H),7.82(s,H,-CH=N),6.63~7.4(3H,Furan ring-H),6.90(s,H,-NH-),3.84(s,3H,-OCH3)。 FT-IR(KBr) ν/cm-1:3 451(m),1 642(s),1 574(s),1 511(w),1 258(m),1 177(w)。Anal.Calc.for C13H12N2O3(%):C,63.75;H,4.86;N,11.51;Found(%):C,63.93;H,4.95;N,11.47。
1.2.2 配合物NiL2的合成
称取0.244 g(1 mmol)配体HL溶解在30 mL乙醇和丙酮(体积比为2∶1)的混合溶剂中,搅拌下用恒压滴液漏斗缓慢滴入溶有0.290 8 g(1 mmol)Ni(NO3)2·6H2O的乙醇溶液10 mL,室温反应2h后过滤,得黄绿色滤液,室温静置挥发20 d,获得适合X-射线单晶衍射测试的红色长条状单晶。FTIR(KBr) ν/cm-1:1 606(s),1 495(s),1 466(w),1 374(s),1343(w),1250(s),1169(m),1020(w),564(s),510(m)。
1.2.3 配合物Mn(HL)2Cl2的合成
称取0.244 g(1 mmol)配体HL溶解在30 mL乙醇和丙酮(体积比为2∶1)的混合溶剂中,搅拌下用恒压滴液漏斗缓慢滴入溶有0.197 9 g(1 mmol)MnCl2·4H2O的乙醇溶液10 mL,室温反应2 h后过滤,得浅棕黄色滤液,室温静置挥发18 d,出现适合X-射线单晶衍射测试的淡黄色方块状单晶。FTIR(KBr)ν/cm-1:3 150(m),1 610(s),1 562(m),1 508(s),1 352(w),1 296(w),1 255(s),1 183(w),1 021(w),631(s),552(m)。
1.3 晶体结构测定
选取尺寸分别为0.26 mm×0.19 mm×0.14 mm的配体HL单晶、0.32 mm×0.27 mm×0.19 mm的配合物NiL2单晶和0.34 mm×0.26 mm×0.17 mm的配合物Mn(HL)2Cl2单晶置于Bruker Smart-APEXⅡCCD单晶衍射仪上,用经石墨单色器单色化的Mo Kα 射线(λ=0.071 073 nm),在 296(2)K 下以 φ-ω扫描方式分别在 1.63°≤θ≤25.09°、2.38°≤θ≤25.10°和 2.01°≤θ≤25.10°范围内收集单晶衍射数据,对全部衍射强度数据进行经验吸收校正、Lp校正后用直接法解得晶体结构,对全部非氢原子坐标及其各向异性热参数进行全矩阵最小二乘法修正,氢原子为理论加氢。所有计算用SHELX-97程序完成[16](有关晶体学数据见表1)。

表1 配体和配合物的晶体学数据Table 1 Crystal data and structure refinement for the ligand and complexes
CCDC:926194,HL;926193,NiL2;926195,Mn(HL)2Cl2。
2 结果与讨论
2.1 晶体结构
2.1.1 配体HL的晶体结构
配体HL的分子结构如图2,主要键长和键角见表3。HL中呋喃环与苯环的二面角为27.868°,表明HL的结构略有扭曲。HL的单个晶胞含有18个配体分子,配体分子间存在三中心氢键(氢键参数见表 2),3个非氢原子 N1、O2和 N2#1(对称操作码:#1-y+4/3,x-y+2/3,z-1/3)共享 1 个 H2A#1,其中 N1 与N2#1的距离为 0.309 77(35)nm,O2与N2#1的距离为0.299 24(35)nm。不同分子通过这种氢键作用不仅在分子间形成一个五元环结构 (五元环由N1、N1、C6、O2、H2A#1构成), 而且使配合物分子相互交错排布呈现出链式结构。配体分子间氢键作用力见图3。

图2 配体HL的椭球图Fig.2 Ellipsoid(50%)structure of HL

表2 配体HL和配合物MnL2Cl2的氢键参数Table 2 Hydrogen bond lengths and angles

图3 配体HL的分子间氢键Fig.3 Hydrogen bonds of HL
2.2.2 配合物的晶体结构
配合物NiL2的分子结构图如图4,主要键长和键角见表3。NiL2的单个晶胞含有2个配合物分子,每个配合物分子由1个配位中心Ni(Ⅱ)和2个配体分子构成,Ni(Ⅱ)采用四配位形式,分别与2个羰基O和2个亚胺基N配位,形成2个闭合的五元环,构成平面四方构型。Ni(Ⅱ)周围4个键键长范围为0.1828(2)~0.1851(2)nm,键角在 83.68(8)°~96.32(8)°之间。相邻分子的呋喃环和苯环之间存在边对面π…π作用力,呋喃环与苯环π平面的二面角为65.630(101)°,呋喃环上C2到苯环质心Cg#1(对称操作码:#1-x+1,-y+2,-z+2)(C7、C8、C9、C10、C11、C12)的距离为0.388 93(35)nm。分子间边对面π…π作用力使配合物分子构成两个方向上的层状结构。分子间边对面π…π作用力见图5。
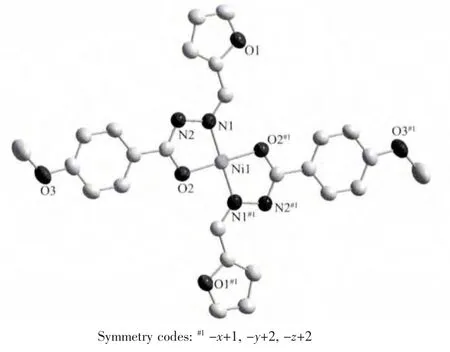
图4 配合物NiL2的椭球图Fig.4 Ellipsoid(50%)structure of NiL2
配合物Mn(HL)2Cl2的分子结构图如图6,主要键长和键角见表3。Mn(HL)2Cl2的单个晶胞含有2个配合物分子,每个配合物分子由1个配位中心Mn(Ⅱ)、2个配体分子和2个Cl构成,Mn(Ⅱ)采用六配位形式,分别与来自配体的2个羰基O、2个亚胺基N形成2个闭合的五元环结构,继而与2个Cl配位形成四角双锥构型,2个Cl分别位于锥顶和锥底。Mn(Ⅱ)周围键角范围在 70.4(2)°~109.6(2)°,6 个键键长在0.215 9(5)~0.247 4(2)nm之间。N2上的H2与相邻分子的 Cl1#2(对称操作码:#2-x+2,-y,-z+2)存在典型的分子间氢键N2-H2…Cl1#2(氢键参数见表2),Cl1#2原子与N2的距离为0.322 14(70)nm。配合物分子中苯环与相邻呋喃环还存在面对面π…π作用力,苯环与呋喃环π平面的二面角为6.882(269)°,苯环质心 Cg2(C7、C8、C9、C10、C11、C12)与呋喃 环 质 心 Cg1#2(O1#2、C1#2、C2#2、C3#2、C4#2) 距 离 为0.383 09(11)nm。分子间氢键和面对面π…π作用力使配合物分子构成2D链式层状结构。分子间氢键和面对面π…π作用力见图7。

图6 配合物Mn(HL)2Cl2的椭球图Fig.6 Ellipsoid(50%)structure of Mn(HL)2Cl2
2.2 红外光谱分析
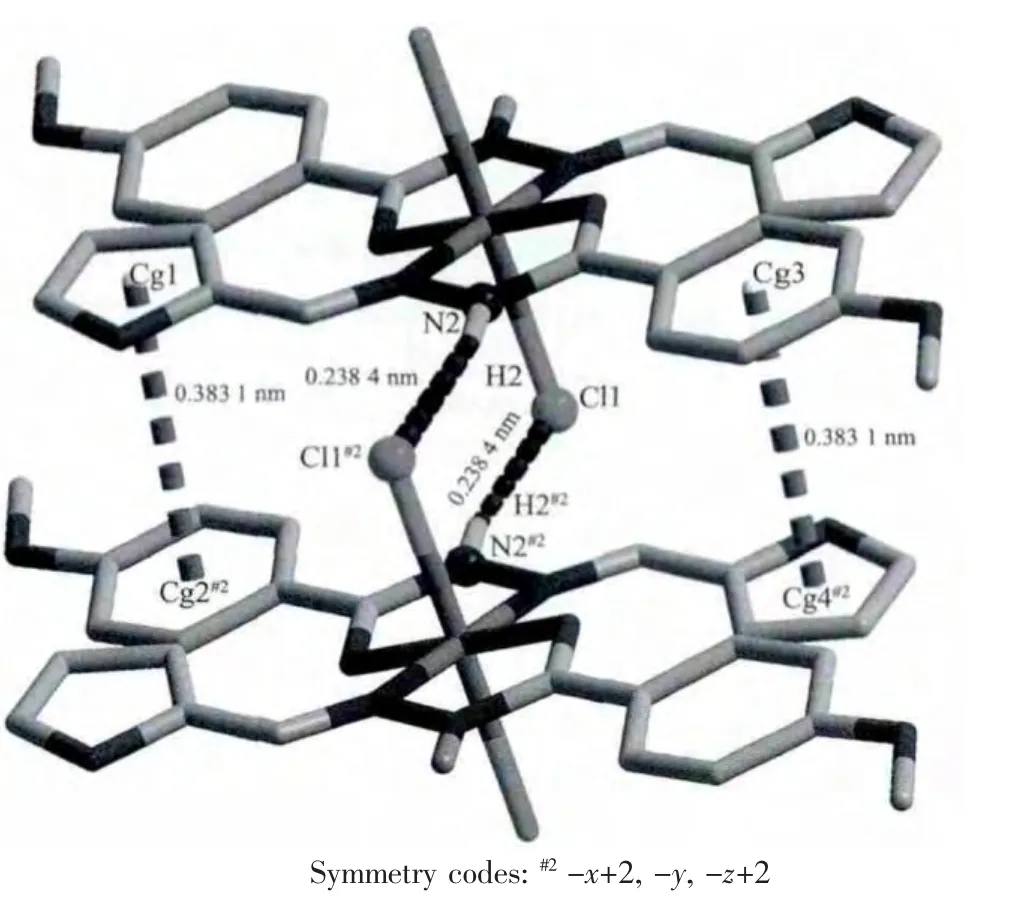
图7 配合物Mn(HL)2Cl2的氢键和π…π作用力Fig.7 H-bonds and π…π interactions of Mn(HL)2Cl2
用KBr压片法测定了配体HL及其Ni、Mn配合物在400~4 000 cm-1的红外光谱,各吸收峰参照文献[17]指认。HL在3 451 cm-1出现肼基(-NH-N=)中等强度而宽的νN-H吸收峰,在1 642 cm-1出现强而尖锐的νC=O吸收峰。在配合物NiL2中,这些峰均消失,在1 606 cm-1处出现强而尖锐的νC=N-N=C吸收峰,在1 250 cm-1处出现尖锐的烯醇νC-O吸收峰,表明在NiL2中配体HL的肼基H经烯醇化重排后失去。在配合物Mn(HL)2Cl2中,强而尖锐的νC=O吸收峰相对于配体向低波数方向移动了32 cm-1,出现在1 610 cm-1,表明配体HL中的羰基O与金属锰配位。HL中1 574 cm-1的νC=N吸收峰在形成配合物NiL2后向低波数方向移动79 cm-1,出现在1 495 cm-1,而在形成配合物Mn(HL)2Cl2后向低波数方向移动12 cm-1,出现在1 562 cm-1,表明配体HL中C=N上的N与金属形成反馈配键。NiL2中νNi-N和νNi-O吸收峰分别出现在563 cm-1和510 cm-1处,Mn(HL)2Cl2中νMn-N和νMn-O吸收峰分别出现在630 cm-1和552 cm-1处[18-19]。红外光谱分析与晶体结构分析结果一致。
1.3 抑菌活性
采用琼脂扩散法[20]测试配体HL及其Ni、Mn配合物对细菌菌株(由陕西省人民医院提供)大肠杆菌(ATCC25922)、金黄色葡萄球菌(ATCC25923)和绿脓杆菌(ATCC27853)的抑制活性,供试菌经接种活化3次后配成浓度为 5×105~5×106cfu·mL-1菌悬液备用。称取配体和配合物各5 mg,超声振荡溶解在25 mL DMF中备用。将已灭菌的直径6 mm滤纸片(新华一号)浸入上述各溶液2 h,取出放置在已涂布菌悬液的营养琼脂培养基上,与溶剂空白对照组一起置入37℃温箱中培育16~18 h后,测量抑菌环直径来比较抑菌活性。测试结果列于表4。

表4 配体和配合物的抑菌活性Table 4 Antibacterial activities of the ligand and complexes
配体HL、配合物NiL2和配合物 Mn(HL)2Cl2对大肠杆菌、金色葡萄球菌和绿脓杆菌均有不同程度的抑制活性,配合物的抑菌活性都比配体的强,配合物NiL2比配合物Mn(HL)2Cl2强。配体HL、配合物NiL2和配合物Mn(HL)2Cl2对大肠杆菌和绿脓杆菌的抑制活性相当,对金色葡萄球菌均有更强的抑制活性,表明配体和配合物的抑菌活性具有选择性。配合物NiL2对金色葡萄球菌有高达14 mm的抑菌环,表明其对金色葡萄球菌有显著的抑制活性,可以用来作为潜在的抑菌材料。
[1]Monfort M,Resino J,Ribas J,et al.Inorg.Chem.,2000,3(9):2572-2576
[2]YANG Rui(杨锐),HE Shui-Yang(何水样),WU Wang-Ting(武望婷),et al.Acta Chimica Sinica(化学学报),2004,62(20):2040-2044
[3]Daniet M E,Seema C,Melvyn R C,et al.Inorg.Chem.,2001,40(7):1591-1596
[4]REN Hai-Xian(任海仙),TANG Jing(唐静),WEI Tai-Bao(魏太保),et al.Chinese J.Inorg.Chem.(无机化学学报),2007,23(11):1907-1911
[5]Schuetz S A,Silvernail C M,Incarvito C D.Inorg.Chem.,2004,4(3):6203-6207
[6]Adsule S,Barve V,Ahmed F,et al.J.Med.Chem.,2006,49(24):7242-7246
[7]ZHU Shan-Shan(朱姗姗),LU Jun-Rui(卢俊瑞),XIN Chun-Wei(辛春伟),et al.Chinese J.Org.Chem.(有机化学),2010,30(12):1914-1920
[8]CHEN Qiong(陈琼),LONG De-Qing(龙德清),CHENG Jing(程靖),et al.Chem.J.Chinese Universities(高等学校化学学报),2006,27(3):454-459
[9]LIU Jing-Gang(刘劲刚),JI Liang-Nian(计亮年).Chinese J.Inorg.Chem.(无机化学学报),2000,16(2):195-203
[10]Abbas A,Hassan K,Farzad K,et al.J.Chem.Eng.Data,2010,55(11):4725-4731
[11]Punam B,Sujeetkumar J,Imran A.J.Agric.Food Chem.,2009,57(20):9780-9786
[12]HE Shui-Yang(何水样),CHEN Jun-Li(陈军利),YANG Rui(杨锐),et al.Chinese J.Org.Chem.(有机化学),2003,23(12):1387-1392
[13]Jose R P,Cristina S,Suely L,et al.J.Med.Chem.,2001,44(22):3673-3681
[14]CHENG Wei-Hua(程卫华),SI Zong-Xing(司宗兴).Chinese J.Applied Chem.(应用化学),2000,17(4):444-446
[15]CHEN Xiao-Hua(陈小华),LIU Shi-Xiong(刘世雄).Chinese J.Inorg.Chem.(无机化学学报),2004,20(6):683-687
[16]Sheldrick G M.SHELX-97,University of Göttingen,Germany,1997.
[17]Nakamoto K,Translated by HUANG De-Ru(黄德如),WANG Ren-Qing(汪仁庆).Infrared and Raman Spectra of Inorganic and Coordination Compounds.3rd Ed.(无机和配位化合物的红外和拉曼光谱.3版).Beijing:Chemical Industrial Press,1986.
[18]YANG Ying-Qun(杨颖群),LI Chang-Hong(李昶红),LI Wei(李薇),et al.Chinese J.Chem.(结构化学),2008,27(2):149-152
[19]LU Wen-Guan(卢文贯),PENG Cui-Hong(彭翠红),LIU Hong-Wen(刘宏文),et al.Chinese J.Inorg.Chem.(无机化学学报),2003,19(11):1222-1226
[20]ZHAO Sheng-Ming(赵胜民),ZHENG Lai-Jiu(郑来久),DU Bing(杜冰).Science&Technology Review(科技导报),2009,27(7):37-40
