十二烷基二甲基苄基氯化铵从碱性氰化液中固相萃取金的研究
2014-01-02解润芳杨项军韩云山李树华
解润芳 杨项军 韩云山 李树华
(1昆明医科大学法医学院,昆明 650500)
(2云南大学化学科学与工程学院,昆明 650091)
(3云南铜业股份有限公司检验中心,昆明 650102)
氰化法提金是国内外黄金提取方法中占主导地位的方法。从氰化浸出液富集金的处理工艺,传统的金属还原法存在生产周期长、环境污染大、成本较高的缺点;此外,用液-液萃取法处理堆浸或槽浸获得的氰化液中金,也存在富集倍数低、有机溶剂使用量大、容易出现第三相、相分离速度较慢等缺点。
陈景等[1-8]提出用十六烷基三甲基溴化铵(CTMAB)络合金,并用含30%(体积分数)TBP的磺化煤油溶液萃取处理的方法,获得较好效果,但仍难完全克服前述困难,因此国内外在生产实践中至今未见有成功的报道。
固相萃取技术(Solid Phase Extraction,SPE)是从20世纪80年代中期开始快速发展起来的一种富集和分离技术。SPE技术在许多方面存在优点,特别是反相键合硅胶材料的固相萃取柱,其疏水缔合的保留特性适合于从水溶液中富集痕量物质。国内外对反相键合硅胶材料固相萃取的研究主要限于有机物,而用于萃取无机物的报道较少。本文在文献[9-17]基础上,创新性地把固相萃取与表面活性剂十二烷基二甲基苄基氯化铵溶液(BDMDAC)萃取金两种技术结合进行研究,取得了满意的结果。
1 实验部分
1.1 主要仪器和试剂
固相萃取柱,图1所示为Sep-PakRCartridge(购买于美国Waters公司),每只小柱填料重约为0.33 g,填料为反相键合硅胶,填料粒度为30 μg,使用pH值为1~12,小柱使用前用一定量的乙醇活化,再用蒸馏水洗去残留的乙醇,即可用于样品萃取富集。
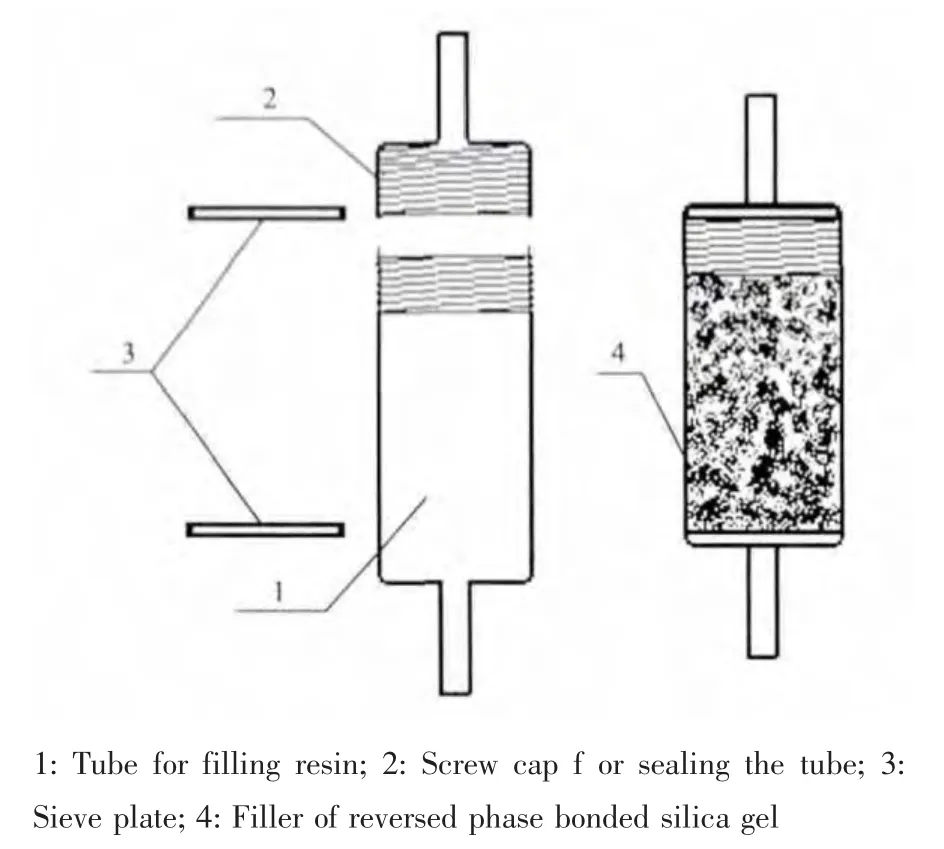
图1 反向键合硅胶固相萃取柱示意图Fig.1 Schematic diagram of SPE column with reversed phase bonded silica gel
UV-2401紫外分光光度计(日本岛津公司)。
BeckmanQ-200型酸度计(美国Beckman公司)。
8302型恒温水浴锅 (河南省巩义市予华仪器厂)。
金标准液:用分析纯KAu(CN)2配成含金2 g·L-1(cAu=0.010 15 mol·L-1)的储备液(用 pH 约为 10.5的NaOH的溶液配制),用上述金储备液配制含金50 μg·mL-1(cAu=0.253 8 mmol·L-1)的溶液(用 pH 值约为10.5的NaOH的溶液稀释);以后供实验用的各溶液均由上述溶液配制并用pH值约为10.5的NaOH的溶液稀释。
十二烷基二甲基苄基氯化铵(BDMDAC)溶液:0.010 15 mol·L-1(用pH约为10.5的NaOH的溶液配制),0.253 8 mmol·L-1(用上述溶液配制并且用 pH约为10.5的NaOH的溶液稀释)。
其余所用试剂均不低于分析纯级,水为一次蒸馏水。
所用固相小柱为C18固相小柱(特别指明除外)。
实验条件为BDMDAC溶液与KAu(CN)2溶液物质的量比为1.5∶1,其中混合溶液中金的浓度为20 μg·mL-1(特殊指明者除外)。
1.2 实验方法
准确移取20 mL KAu(CN)2溶液(金的浓度为50 μg·mL-1)于100 mL锥形瓶中,再准确加入30 mL浓度为 0.253 8 mmol·L-1的 BDMDAC 溶液(nBDMDAC∶nAu=1.5∶1),因此可得出该混合溶液中金的浓度为20 μg·mL-1,然后充分混匀该混合溶液,放置5 min后,让该混合溶液以15 mL·min-1的流速通过活化好的小柱,再以5.0 mL·min-1的流速用6.0 mL乙醇洗脱。准确取出1 mL流出液,用硫酸和硝酸分解氰根后,用孔雀绿分光光度法测定流出液中金的量,根据加入金的量与流出液中金的量的差值计算出小柱对金的萃取率(如果流出液中未检出金,被认为金完全被小柱萃取);洗脱液中金,经蒸干乙醇(注意一定要蒸干乙醇否则会发生爆炸),用硫酸和硝酸分解氰根后,用孔雀绿分光光度法测定金的量,根据测定的金的量与加入金的量的比值算出金的萃取率(两种计算萃取率的方法可以达到相互验证的目的)。
2 结果与讨论
2.1 BDMDAC与Au的物质的量比对金回收率的影响
实验了 nBDMDAC∶nAu比为 0∶1;0.25∶1;0.5∶1;0.75∶1;1∶1;1.25∶1;1.5∶1;2∶1;2.5:1;3∶1 条件。 从图 2 的结果可看出,按上述比列加入BDMDAC后金的回收率有一定的提高,nBDMDAC∶nAu比超过 1.25∶1 后金的回收率不再增加,并且金的回收率仅达到60%左右,但如果萃取前萃取小柱先用一定量浓度为0.010 15 mol·L-1的BDMDAC过柱后,金的回收率都达到98%以上。实验选择被萃液中nBDMDAC∶nAu比为1.5∶1并且小柱必须先用一定量 10.15 mmol·L-1的BDMDAC过柱。

图2 BDMDAC/Au物质的量比对金回收率的影响Fig.2 Effect of BDMDAC/Au mole ratio on the recovery rate of gold
2.2 萃取酸度的影响
由于Au(CN)2-在pH>9.4的条件下才能稳定存在,而本实验所用的固相萃取柱的使用pH范围为1~12,因此实验了pH值在9.5~12范围内变化对金回收率的影响,结果见图3。从图3可看出当pH值在9.5~12范围内变化时,金的萃取回收率均在98%以上,而且pH值改变对金的回收率无影响,实验选择萃取pH为10.5。

图3 pH值对金回收率的影响Fig.3 Effect of pH value on the recovery rate of gold

表1 不同填料固相萃取柱的萃取容量Table 1 Extraction capacity of solid phase extraction column with different filler
2.3 过柱流速的影响
实验了过柱流速对金回收率的影响,结果表明当过柱流速小于25 mL·min-1时,金的回收率都高达98%以上,但流速大于25 mL·min-1后金的回收率开始下降,这可能是流速过快会导致金的离子缔合物和固定相还未完全作用就流出,影响了金在固相柱上的吸附。过柱流速还和压力密切相关,过柱压力随流速的增加而增加,流速过快会导致过柱压力过大而使萃取操作难度增加。综合回收率、分析时间和可操作性考虑,实验选用过柱流速为15 mL·min-1。
2.4 不同填料固相萃取柱容量的测定
2.4.1 C18固相萃取柱容量的测定
准确移取金浓度为 50 μg·mL-1的 KAu(CN)2溶液 20 mL与 30 mL浓度为 0.253 8 mmol·L-1的BDMDAC溶液混合,并且配制很多个上述混合溶液,每个混合溶液都以15 mL·min-1的流速过柱,当混合溶液过柱体积超过850 mL时,金开始穿漏,被认为小柱对金的萃取达到饱和。可得出小柱对金的最大萃取容量为17 mg;实验推荐C18小柱的萃取容量控制在14 mg内。
2.4.2 C8、C4、C2固相萃取柱容量的测定
操作方法同 2.4.1,实验了 C8、C4、C2各种填料固相萃取柱的萃取容量。
4种填料对金的萃取容量结果见表1,从表1可看出,4种填料对金的萃取容量依次递减。从购买和经济的角度考虑本文推荐选用C18固相萃取小柱。
2.5 洗脱剂的选择与用量及洗脱流速
实验了不同洗脱剂洗脱小柱上富集的离子缔合物,发现富集量在17 mg左右时,用甲醇、乙醇、乙腈、丙酮、四氢呋喃等极性有机物均能把小柱上富集的离子缔合物完全洗脱下来,洗脱剂用量可控制在较小体积(4.0 mL以内)。由于乙醇无毒,挥发性弱且价格便宜,本实验选用乙醇洗脱。
洗脱剂用量和小柱上富集的离子缔合物量有关,富集的离子缔合物越多,所需洗脱剂量越大。对于洗脱相同量的离子缔合物,洗脱剂用量还与洗脱流速有关,洗脱流速越大,所需的洗脱剂量越大。当金的富集量为17 mg,乙醇为洗脱剂时,综合考虑富集倍数和洗脱时间,本实验选用洗脱流速为5 mL·min-1。
2.6 反相固相萃取、富集金的机理研究
2.6.1 反相固相萃取过程机理
反相固相萃取是基于溶质、极性流动相和非极性固定相表面间的疏水效应建立起来的一种液-固萃取模式,萃取过程是一个包括液相和固相的物理萃取过程,在萃取过程中,固相对样品溶液中溶质的吸附力大于溶剂,当样品通过固相萃取柱时,带有一定疏水性基团的溶质能保留在萃取柱上,溶质所带疏水性基团的疏水性越强,保留值越高。
实验中,金氰络阴离子不具有疏水性,不能直接被反相固定相萃取,有BDMDAC加入时,BDMDAC+阳离子与Au(CN)2-络阴离子生成具有一定疏水性的离子缔合物[18-21],存在水溶液中的带有疏水性基团的离子缔合物通过反相固相萃取柱时,固定相对离子缔合物的吸附力大于水,离子缔合物通过极性作用吸附在反相固定相上。
2.6.2 洗脱过程机理
用洗脱剂洗脱时,固定相对离子缔合物的吸附力小于洗脱剂与离子缔合物的作用力,富集的离子缔合物被洗脱下来[22-25]。用纯有机溶剂洗脱时,洗脱能力随溶剂极性的减少而增强 (顺序为:甲醇<乙醇<乙腈<丙酮<四氢呋喃)。当用能与水混溶的极性有机溶剂洗脱时,有机溶剂占的比列越高,洗脱能力越强。
2.7 不同初始金浓度的萃取回收率
参照实际矿山料液中金的浓度,实验了不同金浓度的回收率,结果见表2。从表2可看出,在浓度2~50 μg·mL-1范围内 (此浓度指 nBDMDAC∶nAu=1.5∶1 混合溶液中金的浓度),金浓度的变化对萃取回收率无影响,金的回收率均在98%以上。小柱的萃取容量有限,对金的最大萃取容量不能超过小柱的萃取容量(实验把C18小柱的萃取容量控制在14 mg),表2也表明固相萃取对低浓度的金的富集倍数高,优势更明显。

表2 不同初始金浓度的萃取回收率Table 2 Extraction recovery rate of different initial concentration with gold
2.8 共存离子的影响
对于金含量为 5 μg·mL-1溶液,下列量 Mn+(mg·mL-1) 离子不干扰, 能有效分离,Na+,Mg2+,K+,Ca2+,NH4+(25);V(Ⅴ),Ni2+,PO43-,SO42-,Al3+(7);Fe3+,Co2+,Mo(Ⅵ),Mn2+,SiO32-(4);Cr3+,W(Ⅵ),Ti(Ⅳ)(0.8);Sn(Ⅵ),Cd2+,As(Ⅴ), Zn2+(0.2);Hg2+,Cu2+(0.1);Ag+,Pb2+(0.04);Pt(Ⅳ)(0.008);Pd2+(0.005)。
3 样品分析及结果
用本方法测定6个低、中、高浓度的氰化浸出液,并用原子吸收光谱法作对照,结果见表3。从表3可看出,本法测得值与AAS法对比相对误差小于10%,RSD小于5%,加标回收率大于98%,说明本实验方法可靠,重现性好。

表3 样品分析结果(n=5)Table 3 Analytical results of samples(n=5)
4 结 论
本文把一直应用于萃取有机物的固相萃取技术用于萃取无机物金,并与表面活性剂萃取金技术结合,探索出了表面活性剂十二烷基二甲基苄基氯化铵固相萃取金的最佳萃取条件,过柱流速,pH值、洗脱条件等,建立了一种高选择性固相萃取金的样品前处理新方法,解决了一直困扰分析工作者的难题(样品含量越来越低,对样品的前处理提出了更高的要求),一次萃取率可超过98%,用乙醇洗脱后富集倍数非常高。此外,本文建立的新方法,也可用于贵金属的富集和分离提纯工艺中,将展现出潜在的应用前景,对促进我国黄金生产及西部大开发也具有重要意义。两种技术结合后,在理论研究上将因液-液萃取和固相萃取的交叉,发现一些新的亮点,可以丰富萃取化学的知识。
[1]XIE Qi-Ying(谢琦莹),CHEN Jing(陈景),YANG Xiang-Jun(杨项军),et al.Chinese J.Inorg.Chem.(无机化学学报),2007,23(1):57-62
[2]XIE Qi-Ying(谢琦莹),CHEN Jing(陈景),YANG Xiang-Jun(杨项军),et al.Chinese J.Inorg.Chem.(无机化学学报),2008,24(6):897-901
[3]ZOU Lin-Hua(邹林华),CHEN Jing(陈景).Chin.J.Precious Metals(贵金属),1995,16(4):61-67
[4]HUANG Kun(黄昆),CHEN Jing(陈景),WU Jin-Guang(吴瑾光),et al.Chin.J.Nonferr.Metals(中国有色金属学报),2001,11(2):307-311
[5]HUANG Kun(黄 昆),CHEN Jing(陈 景),CUI Ning(崔 宁),et al.Chin.J.Nonferr.Metals(中国有色金属学报),2001,11(3):518-521
[6]YANG Xiang-Jun(杨项军),CHEN Jing(陈 景),XIE Qi-Ying(谢琦莹),et al.Chin.J.Prog.Chem.(化学进展),2009,21(7/8):1583-1591
[7]YAN Wen-Fei(闫文飞),MA Gang(马刚),YAN Chun-Hua(严纯华),et al.Chin.J.Spectrosc.Spectr.Anal.(光谱学与光谱分析),1999,19(6):806-810
[8]LIU Yue-Ying(刘月英),CHEN Jing(陈景),XIE Qi-Ying(谢琦莹).Chin.J.Nonferr.Metals(中国有色金属学报),2009,19(7):1316-1321
[9]XIE Run-Fang(解润芳),HUANG Feng(黄锋),WEI Qun-Yan(韦群艳),et al.Chin.J.Phys.Testing Chem.Anal.Part B(理化检验-化学分册),2008,44(5):444-446
[10]Hu Q F,Chen X B,Yang X J,et al.Anal.Sci.,2006,22:627-630
[11]Amin A S,Saber A L,Mohammed T Y.Spectrochim.Acta Part A,2009,73:195-200
[12]Rajesh N,Gurulakshmanan G.Spectrochim.Acta Part A,2008,69:391-395
[13]LIN Hong(林洪),ZHU Li-Ya(朱利亚),LI Hai-Tao(李海涛),et al.Chin.J.Precious Metals(贵金属),2005,26(3):51-54
[14]Yang G Y,Hu Q F,Yang J H,et al.Anal.Sci.,2003,19:299-302
[15]Qi D J,Kang X J,Chen L Q,et al.Anal.Bioanal.Chem.,2008,390:929-938
[16]CHAI Yao-Dong(柴跃东),LI Ming(李明),YANG Yan(杨艳),et al.Chin.J.Gold(黄金),2005,26(4):42-44
[17]PAN Xue-Jun(潘学军),CHEN Jing(陈景).Chin.J.Rare Metals(稀有金属),2000,24(2):90-95
[18]Kocúrová L,Balogh I S, Škrlíková J,et al.Talanta,2010,82:1958-1964
[19]Badiei Y M,Jiang Y B,Widger L R,et al.Inorg.Chem.,2012,382:19-26
[20]Sandlin R D,Whelan C J,Samuel B M,et al.Inorg.Chem.,2012,391:135-140
[21]PAN Xue-Jin(潘学军),CHEN Jing(陈景).Chin.J.Rare Metals(稀有金属),1999,18(2):88-96
[22]ZHANG Hai-Xia(张海霞),ZHU Peng-Ling(朱彭龄).Chin.J.Rev.Prog.Chem.Anal.(分析化学评述与进展),2000,28(9):1172-1180
[23]Xie F,Dreisinger D.J.Hazard.Mater.,2009,169:333-338
[24]Li X Y,Leopold K.Analy.Chem.,2012,84:4340-4349
[25]WU Fang-Hua(吴芳华).Chin.J.Anal.Testing Techno.Instru.(分析测试技术与仪器),2012,18(2):114-120
[26]Ghiladi R A,Rheingold A L,Siegler M A,et al.Inorg.Chem.,2012,389:131-137
