羟丙基豌豆淀粉制备工艺及性质研究
2013-12-23战晓凤邬应龙
战晓凤,邬应龙*
(四川农业大学食品学院,四川 雅安 625014)
豌豆是世界各地广泛种植的主要食用豆之一,其产量在豆科类农作物中排名第四,仅低于黄豆、花生和干大豆,产量超过1000万t[1]。傅翠珍等[2]对我国西部地区豌豆成分进行分析发现,其籽粒中总淀粉含量为28.70%~58.69%,平均为49.17%,而蛋白质和粗纤维含量分别高达25%和5%左右。豌豆淀粉主要作为制取豌豆浓缩蛋白的副产物,产量巨大[3]。在豌豆淀粉糊化溶液中,由于较多的直链淀粉相互作用,致使淀粉更易老化,出现溶液浑浊和水分析出等现象,尤其经反复多次冻融,其稳定性更差。豌豆淀粉的这类性质限制了其在食品工业的广泛应用[4]。据报道在淀粉分子上引进了一定数量的羟丙基团可有效地改善淀粉糊的性质,增强淀粉糊的亲水性和保水性能,使淀粉糊的透明度和稳定性增高,不易沉淀[5]。羟丙基改性在马铃薯淀粉[6]、甘薯淀粉[7]、木薯淀粉[8]等薯类淀粉,小麦淀粉[9]、指状小米淀粉[10]、大米淀粉[11]等谷类淀粉被报道并具有良好的效果,但在更加易老化的豆类淀粉的研究中却鲜见报道。本研究为制备羟丙基豌豆淀粉对制备工艺中的各主要影响因素进行优化,并对其性质进行研究,以期为羟丙基豌豆淀粉进一步开发利用提供理论参考。
1 材料与方法
1.1 材料与试剂
豌豆淀粉 市售;环氧丙烷、1,2-丙二醇等试剂均为分析纯。
1.2 仪器与设备
HS80恒温水浴摇床 中国科学院武汉科学仪器厂;7200分光光度计 尤尼柯(上海)仪器有限公司;HG-9245A型电热恒温鼓风干燥箱 上海精宏实验设备有限公司;Super3型快速黏度测试仪 澳大利亚New Port公司;PHS-3C型数显酸度计 上海绿宇精密仪器制造有限公司。
1.3 方法
1.3.1 羟丙基豌豆的制备
称取一定量的豌豆淀粉,配成40%(m/m)的淀粉乳,缓慢加入20%(m/m)硫酸钠,于摇床上混匀30min。之后用1mol/L NaOH溶液调至一定pH值,并将一定量的环氧丙烷加入淀粉乳中,密闭容器(用氮气作为保护)。反应搅拌一定时间,待反应结束后,用0.5mol/L硫酸调pH值至5.5。抽滤,蒸馏水洗涤3次,烘干,粉碎,得羟丙基豌豆淀粉。
1.3.2 羟丙基淀粉取代度的测定
以羟丙基改性淀粉中羟丙基含量表示改性淀粉的取代度。羟丙基含量的测定采用分光光度法,淀粉样品(100mg)加入100mL的容量瓶中,再加入(25mL 0.5mol/L)的硫酸。混合物在沸水浴锅中消化直至获得澄清的溶液,冷却后蒸馏水定容至100mL。移液管移取溶液(1mL)到25mL刻度测试管中,插入冷水中,逐滴加入管中8mL浓硫酸。充分混匀后,试管放入沸水中水浴20min。之后将其放入冰水浴中直至溶液冷却。将茚三酮试剂(0.15g茚三酮溶于10mL 12.5% NaHSO3,0.6mL)加入具塞管中,混匀后放入25℃水浴100min。溶液用浓硫酸定容到25mL,混合充分。然后转移到1cm比色皿中,10min后,595nm处测定吸光度,淀粉空白作为对照[12-13]。羟丙基淀粉的摩尔取代度(MS) 按下式计算:

式中:H为羟丙基的含量/%;F为试样或空白样稀释倍数;M样为在标准工作曲线上对应的丙二醇质量/g;M原为在标准工作曲线上查得的原淀粉空白样中丙二醇质量/g;W样为试样质量/g;W原为原淀粉质量/g;0.7763为丙二醇含量转换成羟丙基含量的转换系数;2.79为羟丙基含量转换成取代度的转换数。
1.3.3 单因素试验
豌豆淀粉乳40%(m/m),无水硫酸钠20%。分别考察环氧丙烷添加量(2%、6%、10%、14%、18%、22%),pH值(9.5、10.1、10.7、11.3、11.9),反应温度(30、34、38、42、46℃),反应时间(4、8、12、16、20、24h)。考察单一因素时,其余条件固定为:环氧丙烷添加量10%、pH11.3、温度40℃、时间12h。
1.3.4 响应面试验
根据单因素试验结果,以环氧丙烷的添加量、反应pH值、反应温度和反应时间为影响因素,羟丙基的取代度为响应值,利用Design Expert 8.0软件对4个因素设计四因素三水平的响应面试验法。因素水平见表1。

表 1 Box-Behnken试验设计Table 1 Factors and their coded levels for Box-Behnken design
1.3.5 体外消化性的测定
取原淀粉、高取代度(HS)、中等取代度(MS)、低取代度(LS),考察化学改性对豌豆淀粉体外消化性的影响。
参考Englyst等[14]方法略有改动。分别取100mg淀粉(干基)装在两个100mL三角瓶中,加入10mL蒸馏水,混匀后沸水浴15min,冷却后加入醋酸缓冲液10mL和直径为10mm的玻璃珠7个混匀,将三角瓶放在37℃摇床中10min后,加入5mL酶液Ⅲ,以此刻为零时,在37℃摇床中以190r/min的转速摇动,20min后,取其中一个三角瓶煮沸灭活后全部转移,测定还原糖值,得到G20。再过100min后,再取另外一个三角瓶煮沸灭活全部转移,测定G120。
快速消化淀粉(RDS)含量/%=(G20-游离葡萄糖)× 0.9/m×100
慢消化淀粉(SDS)含量/%=(G120-G20)×0.9/m×100
抗性淀粉(RS)含量/%=(总葡萄糖-G120)×0.9/m×100
式中:m为样品质量/mg;G20为反应20min时测得的还原糖含量;G120为反应120min时测得的还原糖含量。
1.3.6 快速黏度仪(rapid visco-analyser,RVA)的测定
称2.5g不同取代度的羟丙基淀粉(绝干)用移液管加入25mL蒸馏水,于RVA容器中混匀。采用RVA Super3 Standardl标准的程序升温-降温循环:在50℃保持1min,后经3.5min加热到95℃,再在95℃保持3min,然后,在3.5min内降低到50℃,然后在50℃保持2min。每个样品测定3次。
1.3.7 溶胀度的测定
精确称取淀粉0.25g,转移到离心管中(离心管称质量w1),在离心管中加入50mL蒸馏水,用可变漩涡混匀器混匀30s,在水浴中选择34~90℃,保温1h,之后将悬浮液快速冷却到室温,5000×g离心15min。获得沉淀物,将上清液倒掉后,称取残渣质量(w2)。
淀粉溶胀度/%=[(w2-w1)/m-1]×100
式中:m为称取的淀粉样品干质量。
2 结果与分析
2.1 反应条件对取代度的影响
从图1可以看出,羟丙基豌豆淀粉的取代度随环氧丙烷添加量升高而逐渐增大。当环氧丙烷用量少于14%时,产品的取代度提高较快;当其用量超过14%后,取代度的提高程度逐渐趋于缓慢;其他条件一定时,取代度随pH值的增加,淀粉的分子取代度提高较快,当其pH值超过11.3,羟丙基淀粉分子取代度的提高速度很缓慢;升高温度可提高淀粉与环氧丙烷的有效碰撞机率,故使羟丙基反应效率提高,取代度增大。当反应温度低于42℃时,产品的分子取代度和反应效率随温度升高而明显增大,当温度超过42℃,产品取代度的提高趋于缓慢,当反应温度达到50℃以后,淀粉大量糊化;淀粉的取代度随反应时间延长呈上升趋势,当反应时间达到20h后趋于稳定。

图 1 反应条件对取代度的影响Fig.1 Effect of reaction condition on substituent degree
2.2 响应面法优化羟丙基豌豆淀粉的制备条件
2.2.1 响应面法的试验设计与结果
在单因素试验的基础上,利用响应面法优化羟丙基豌豆淀粉制备工艺,根据Box-Behnken试验设计原理,以羟丙基取代度为响应值,试验设计和结果见表2。

表 2 Box-Behnken试验设计方案及响应值结果Table 2 Box-Behnken experimental design and corresponding results
2.2.2 模型回归方程方差分析
利用Design Expert 8.0软件对响应面试验结果进行多元回归拟合,对表2的数据进行回归分析后得到模型为二次多项回归方程,取代度(MS)对反应pH值、环氧丙烷添加量、反应温度、反应时间的方程为:MS=0.10+0.063A+0.046B+0.058C+0.026D+0.028AB+0.037AC+0.018AD+0.015BC+1.068×10-3BD+8.926×10-3CD-6.090×10-3A2-0.023B2+5.728×10-3C2-5.145×10-3D2。
对模型进行方差分析结果(表3)可知,用上面所得的方程描述因子回归得P<0.0001,方程回归极显著,A、B、C、D、AB、AC、AD、B2也极其显著,说明用上述回归方程描述各因素与响应值之间的关系时,其因变量和全体自变量之间的线性关系显著,即这种试验方法是可靠的。从回归方程各项方差的进一步检验也可知,A、B、C、D都是影响羟丙基取代度的关键因子。回归模型预测的最佳羟丙基豌豆淀粉制备工艺条件为环氧丙烷添加量12%、反应温度40℃、反应pH值为11.3、反应时间18h,此条件下,值得同等高取代度改性淀粉,各因素量值最低。

表 3 二次回归模型的方差分析结果Table 3 Analysis of variance for the fitted regression equation
利用Design Expert软件对表2数据进行二次多元回归拟合得到二次回归方程的响应面及其等高线主要见图2,并对二因素交互作用影响羟丙基取代度进行分析。图2a为反应时间(18h)和pH值(11.3)不变,环氧丙烷添加量和反应温度对产物取代度的交互作用。固定环氧丙烷的添加量,随着反应温度的升高,在40℃以下区间,产物取代度的变化随温度的升高而增加;高于40℃,反应温度升高对于产物取代度影响不明显;在环氧丙烷添加量水平较低时,温度的升高,产物取代度反而有所降低。图2b表明,当环氧丙烷的添加量一定时,pH11.3以下,产物取代度的随温度的升高而变大;pH11.3以上,反应pH值变化对于产物取代度影响较弱。图2c为环氧丙烷添加量和反应时间对产物取代度的交互作用。环氧丙烷的添加量一定时,随着反应时间的延长,反应时间18h以内时,产物取代度随温度升高明显变大;反应时间超过18h,再延长反应时间对于产物取代度影响不明显。其中,最高取代度不到0.2。图2d表明,反应时间18h、反应温度40℃条件下,产物取代度的随两者变化而增加较大;18h、40℃以上时,反应温度及反应时间对于产物取代度影响不大。其中,最高取代度为0.14。


图 2 各因素交互作用的的响应面及等高线分析Fig.2 Analysis of response surface and contour of any two factors
2.3 体外消化性的测定

表 4 化学改性豌豆淀粉消化性Table 4 Digestibility of chemically modified pea starch
由表4可知,未改性的豌豆淀粉几乎全部被消化(78.5%RDS,20.3%SDS,1.20%RS)。用环氧丙烷醚化之后,RS从1.20%增加到32.7%、25.8%和16.1%;总消化性从98.8%降低到67.3%、74.2%和83.9%;SDS均有不同程度降低。可以推测,羟丙基化可以增加完全糊化后豌豆淀粉抗酶解能力,这是由于引入的羟丙基团起到了空间阻碍作用,使淀粉酶不易与淀粉分子结合成活性复合物。HS的消化性与MS、LS相比,其中RDS降低2.0%和15.0%,RS增加7.1%和16.6%,TDS降低6.9%和16.6%。羟丙基取代度增加其消化性呈现逐渐降低的趋势,这与Leegwater等[16]的结果相一致。HS的SDS较LS由17.6%降低到12.7%,而RS由25.8%增加到32.7%,可能是通过改性,SDS部分转化成为RS[15]。
2.4 RVA的测定

图 3 淀粉的RVA糊化性质Fig.3 Pasting profiles of starches measured by RVA

表 5 不同取代度羟丙基豌豆淀粉RVA特性值Table 5 The RVA value of different substitution degree hydroxypropyl pea starch
如图3所示,豌豆原淀粉及羟丙基豌豆淀粉糊化曲线,在开始加热到95℃保温区间里,取代度分别为0.05、0.10、0.15的实验组的糊化曲线相似,具有相近的黏度峰值。冷却阶段,原淀粉比变性淀粉具有较大的黏度回升值。如表5所示,羟丙基化显著改变了豌豆淀粉的糊化性质,其糊化性质取决于取代度水平。羟丙基化后峰值黏度和崩解值增加,与此同时糊化温度和回生值降低。类似的现象在玉米淀粉中有所报道[17]。与原淀粉相比,豌豆所有的羟丙基淀粉糊化温度下降了11~18℃,而峰值黏度增加了74%~109%,降低的糊化温度和增加的峰值黏度反映了豌豆淀粉颗粒内部相关黏结力强度下降,可能是羟丙基基团促进了渗透,加速了水分子进入淀粉颗粒,改性颗粒的无定形区域塑化作用的初始速率增加[18],羟丙基化使低取代度变性淀粉糊峰值黏度提高;当取代度超过0.1,随取代度增加,峰值黏度会有所降低,主要是淀粉颗粒内聚力变弱。有报道表明低摩尔取代度的羟丙基淀粉(MS≤0.2)具有较低的糊化温度,如芭蕉芋淀粉降低了8℃[19],马铃薯淀粉6~14℃[20],羟丙基淀粉的回生值比原淀粉低约16%~59%。变性淀粉上的大量羟丙基基团具有较强空间效应,阻碍了淀粉链的靠拢、结晶。
2.5 溶胀度的测定
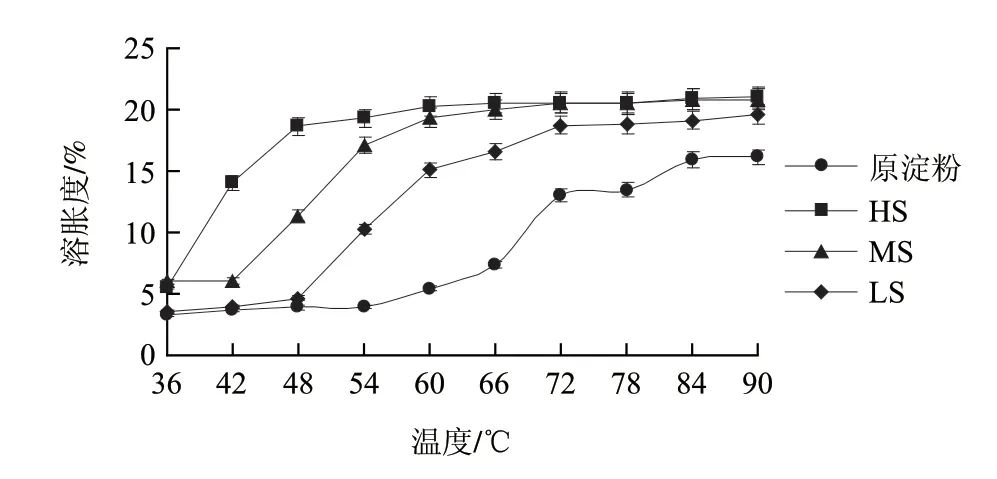
图 4 温度对豌豆原淀粉及其羟丙基淀粉溶胀度的影响Fig.4 Effect of temperature on free swelling capacities of native and hydroxypropyl pea starch
如图4所示,各淀粉溶胀度随着温度升高呈上升趋势。在36~90℃范围内,羟丙基豌豆淀粉溶胀度均高于原淀粉。同一测定温度下,溶胀度随羟丙基豌豆淀粉取代度增加而升高。一定温度条件下,引入的羟丙基基团利于淀粉非晶区对水分子的吸收,增强了吸水性[21]。与原淀粉相比,各取代度的羟丙基豌豆淀粉达到溶胀度最大值的温度均有提前。且羟丙基取代度越高,溶胀度越大。可能因为羟丙基的引入削弱淀粉链间的结合力,使水合作用加快,增加淀粉颗粒亲水性。说明豌豆淀粉经羟丙基化可增加其溶胀度。
3 结 论
3.1 在单因素试验的基础上,利用响应面法对进行了优化,并对4个关键因素的最佳水平及其交互作用进行了研究,得出制备羟丙基豌豆淀粉最佳工艺参数为:环氧丙烷添加量12%、反应pH11.3、反应温度40℃、反应时间18h。
3.2 豌豆淀粉经羟丙基化后,其性质有很大改观,表现出良好的体外抗消化性,且抗消化性取决于取代度的高低;淀粉的起始糊化温度、峰值温度和峰值时间明显提前;淀粉溶胀度最大值温度提前,溶胀度增大。
[1] 李兆丰, 顾正彪, 洪雁. 豌豆淀粉的研究进展[J]. 食品与发酵工业,2003, 29(10): 70-74.
[2] 傅翠真, 胡谟彪, 曹永生, 等. 西部地区食用豆类营养特点及其利用[J]. 西南农业学报, 1997, 10(2): 62-66.
[3] HOOVER R, SOSULSKI F. Composition, structure, functionality, and chemical modification of legume starches: a review[J]. Canadian Journal of Physiology and Pharmacology, 1991, 69(1): 79-92.
[4] HOOVER R, SOSULSKI F. Effect of cross linking on functional properties of starch[J]. Starch-Stärke, 1986, 38(5): 149-155.
[5] 温其标, 卢声宇. 羟丙基淀粉消化性能的研究[J]. 华南理工大学学报: 自然科学版, 2002, 30(11): 134-137.
[6] KAUR L, SINGH N, SINGH J. Factors influencing the properties of hydroxypropylated potato starches[J]. Carbohydrate Polymers, 2004, 55(2): 211-223.
[7] LEE H, YOO B. Effect of hydroxypropylation on physical and rheological properties of sweet potato starch[J]. LWT-Food Science and Technology, 2011, 44(3): 765-770.
[8] TAKAHSSHI S, MANINGAT C, SEIR P, et al. Acetylated and hydroxypropylated wheat starch: paste and gel properties compared with modified maize and tapioca starched[J]. Cereal Chemistry, 1989, 66(6): 499-506.
[9] van HUNG P, MORITA N. Physicochemical properties of hydroxypropylated and cross-linked starches from A-type and B-type wheat starch granules[J]. Carbohydrate Polymers, 2005, 59(2): 239-246.
[10] LAWAL O S. Starch hydroxyalkylation: physicochemical properties and enzymatic digestibility of native and hydroxypropylated finger millet (Eleusine coracana) starch[J]. Food Hydrocolloids, 2009, 23(2): 415-425.
[11] CHOI H, KOO H. Physicochemical properties of hydroxypropylated rice starches[J]. Korean Journal of Food Science and Technology, 2005, 37(1): 44-49.
[12] JECFA. Compendium of food additive specifications. Hydroxypropyl starch, FAO Food and Nutrition Paper 52 (Add. 9)[S]. Geneva: 2001.
[13] 李学红, 杨京, 徐贵华. 羟丙基淀粉取代度测定方法初探[J]. 粮食与油脂, 2000(8): 36-37.
[14] ENGLYST K, ENGLYST H N. Rapidly available glucose in foods: an in vitro measurement that reflects the glycemic response[J]. American Journal of Clinical Nutrition, 1999, 69(3): 448-454.
[15] CHUNG H J, SHIN D H, LIM S T. In vitro starch digestibility and estimated glycemic index of chemically modified corn starches[J]. Food Research International, 2008, 41(6): 579-585.
[16] LEEGWATER D C, CAND L C. A study on the in vitro digestibility of hydroxypropyl starches by pancreatin[J]. Starch-Stärke, 1971, 23(12): 430-432.
[17] SHI X, BEMILLER J N. Effect of sulfate and citrate salts on derivatization of amylose and amylopectin during hydroxypropylation of corn starch[J]. Carbohydrate Polymers, 2000, 43(4): 333-336.
[18] SEOW C, THEYAMALA K. Internal plasticization of granular rice starch by hydroxypropylation: effects on phase transitions associated with gelatinization[J]. Starch-Stärke, 1993, 45(3): 85-88.
[19] CHUENKAMOL B, PUTTANLEK C, RUNGSARDTHONG V, et al. Characterization of low-substituted hydroxypropylated canna starch[J]. Food Hydrocolloids, 2007, 21(7): 1123-1132.
[20] KIM H R, HERMANSSON A M, ERIKSSON C E. Structural characteristics of hydroxypropyl potato starch granules depending on their molar substitution [J]. Starch-Stärke, 1992, 44(3): 111-116.
