脂微球前列地尔治疗急性脑梗死合并2型糖尿病的效果观察
2013-12-23田发发
李 莉 田发发
中南大学湘雅医院神经内科,湖南长沙 410008
目前脑梗死的病因大部分为动脉粥样硬化性血栓,其中部分与合并有2 型糖尿病血管高危因素有关。 在临床治疗和观察中,2 型糖尿病患者发生急性脑梗死后治疗效果较无2 型糖尿病的患者治疗效果差。 目前脑梗死的治疗多采用抗血小板聚集、稳定斑块、抗自由基、改善脑缺血、保护神经细胞等综合治疗方法[1]。 脂微球前列地尔不仅具有抑制血小板凝聚、保护血管内皮细胞药理作用,还对末梢循环障碍有较好的治疗效果[2]。 本研究给予60 例脑梗死合并2 型糖尿病患者脂微球前列地尔注射液(该药系前列地尔脂微球载体靶向制剂)治疗,现将结果报道如下:
1 资料与方法
1.1 一般资料
选择中南大学湘雅医院神经内科2011 年8 月~2012年7 月收治的脑梗死合并2 型糖尿病的患者60 例,均符合全国第四届脑血管会议制订的诊断标准[3],发病至治疗时间均在72 h 之内,并满足下列条件:①经头颅CT 或MRI 确诊;②颈部血管彩超提示有颈部动脉硬化斑块形成;③无全身严重并发症(尤其是心肝、肾功能不全)。2 型糖尿病患者均符合WHO 糖尿病专家委员会提出诊断标准(1999年),经口服降糖药或者胰岛素,使血糖控制在空腹小于8.0mmol/L,餐后2 h 小于10.0 mmol/L,病程大于2 年。 排除标准:①起病在6 h 内,予以溶栓治疗的患者;②合并房颤,风湿性心脏病的患者; ③美国国立卫生研究院神经功能缺损评分(NIHSS) 小于4 分或大于15 分和由于其他原因如股骨头坏死、关节融合等影响NIHSS 真实评分的病例。将60 例患者随机分为脂微球前列地尔联合常规药物组(治疗组)30例和常规药物组(对照组)30 例。治疗组中男20 例,女10 例,平均年龄(54.7±5.3)岁;对照组中男18 例,女12 例,平均年龄(53.2±3.9)岁。 本研究取得所有患者知情同意,且通过医院伦理委员会审批。
1.2 治疗方法
两组均给予糖尿病基础治疗。 治疗组用脂微球前列地尔注射液(商品名为曼新妥,10 μg/支,批号201001024,哈药集团生物工程有限公司)10 μg(2 mL)加入0.9%生理氯化钠溶液250 mL,静滴,1 次/d,连用14 d 为1 个疗程。 同时进行常规抗栓治疗, 即服用拜阿司匹林片 (批号BJ04827)100 mg,口服,每晚1 次;阿托伐他汀片(批号1137043)20 mg,口服,每晚1 次;尼莫同片(批号BJ04657)30 mg,口服,每天3 次;依达拉奉(批号80-110301)30 mg,静滴,2 次/d; 金输(银杏叶制剂)(批号110913)20 mL,静滴,1 次/d。 对照组只进行常规抗栓治疗,方案同上。
1.3 观察指标及评定标准
入院后检测两组患者各项基础生理指标,并于次日清晨空腹抽静脉血10 mL, 同日早餐后2 h 抽静脉血5 mL,分别检测总胆固醇(TC)、三酰甘油(TG)、尿素氮(BUN)、肌酐(Cr)、空腹及餐后2 h 血胰岛素、C 肽,分析两组各项指标结果。
依据NIHSS 评分标准和Barthel 指数(BI)评分标准,由神经内科经过培训的专业医师在患者入院时及治疗后7、14 d 时各评分1 次并记录,用于观察患者神经功能缺损情况。 观察患者入院时机治疗后14 d 时血液流变学指标,即全血比黏度、血浆比黏度、红细胞压积、纤维蛋白原、红细胞聚集指数等变化,并对两组进行疗效比较。 同时,根据全国第4 届脑血管病学术会议制定的《脑卒中患者临床神经功能缺损评分标准》及《临床疗效判断标准》[3-4],分别于治疗前和治疗后14 d 对两组进行疗效评定,评定标准为:①基本痊愈:评分减少90%~100%,病残程度0 级;②显著进步:评分减少45%~<90%,病残程度1~3 级;③进步:评分减少18%~<45%;④无变化:评分减少或增加<18%;⑤恶化:评分增加≥18%。 同时观察患者的不良反应。 总有效率=(基本痊愈+显著进步+进步)/总例数×100%。
1.4 统计学方法
应用SPSS 18.0 软件进行统计学处理, 计量资料以均数±标准差(s)表示,重复测量的计量资料采用方差分析,两独立样本比较采用t 检验,组内比较采用两配对样本t 检验,计数资料比较采用χ2检验,以P <0.05 为差异有统计学意义。
2 结果
2.1 两组临床特征比较
治疗前两组在病程、体重指数(BMI)、收缩压、舒张压、TC、TG、Cr、BUN、 空腹及餐后2 h 胰岛素、C 肽值方面比较,差异均无统计学意义(P >0.05)。 见表1。
2.2 两组治疗前后NIHSS 及BI 评分比较
治疗前, 两组NIHSS 评分和BI 评分的差异均无统计学意义(P >0.05)。 治疗组患者用药后7、14 d 的NIHSS 评分降低,BI 评分升高, 与治疗前相比差异均有高度统计学意义(均P <0.01)。对照组患者用药后7、14 d 的NIHSS 评分降低,BI 评分升高,与治疗前相比,差异均有高度统计学意义(均P <0.01)。用药后7、14 d 时,治疗组与同期对照组NIHSS 评分和BI 评分相比,差异有统计学意义(P <0.05)。见表2。
2.3 两组血液流变学指标比较
与治疗前比较,治疗组治疗后14 d 全血比黏度、血浆比黏度、红细胞压积、纤维蛋白原、红细胞聚集指数明显降低,差异有高度统计学意义(P <0.01);对照组治疗后较治疗前无明显变化(P >0.05),治疗组治疗后效果显著优于对照组(P <0.05)。 见表3。
2.4 两组临床疗效比较
治疗组总有效率为93.3%,高于对照组(76.6%),两者比较差异有统计学意义(P <0.05)。 见表4。
2.5 不良反应
治疗组有1 例在用药注射后第3 天注射部位出现红肿反应,应用硫酸镁湿敷后好转,未影响治疗,对照组无一例发生不良反应,两组比较差异无统计学意义(P >0.05)。
3 讨论
2 型糖尿病患者发生脑梗死后致残率及致死率均较非糖尿病患者高。 糖尿病患者主要病理改变是合并微血管病变和动脉血管壁的硬化, 糖尿病存在血液流变学的异常,包括红细胞和血小板聚集性增加, 红细胞变形性下降,纤维蛋白原增加,发生脑梗死概率大。 发生脑梗死时缺血区内受损的血管内皮细胞合成PGI2明显减少,则血小板功能亢进, 血小板黏附及聚集进一步加强, 多种促裂素释放,TXA2相对增多,纤维蛋白原增加,血凝机制亢进,进一步加剧缺血半暗带发展致脑梗死[5-6]。
前列地尔的药理作用有以下几个方面:①可升高血管平滑肌内的环磷酸腺苷(CAMP),抑制血管交感神经,使血管平滑肌扩张,改善梗死区的血液供应,而不发生脑缺血现象;②通过激活腺昔酸环化酶,使血小板内的含量升高,同时抑制血栓素的释放,从而达到抑制血小板聚集、防止血栓形成的目的;③增加红细胞的变形能力,降低血液黏滞度,改善微循环;④减少自由基的生成,阻止自由基引发的脂质过氧化反应,进而防止动脉硬化的形成[7-8]。 因此,脂微球前列地尔在治疗脑梗死合并2 型糖尿病的患者中可以防止缺血和进一步血栓形成,使得神经功能最大限度得到保存,同时也可改善微循环,对合并糖尿病周围血管病变也有一定疗效。
表1 两组临床特征比较(s)
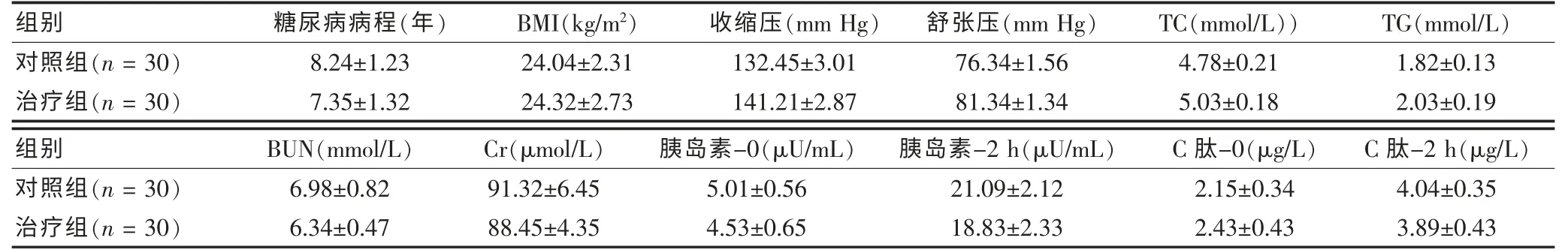
表1 两组临床特征比较(s)
注:BMI:体重指数;TC:总胆固醇;TG:三酰甘油;BUN:尿素氮;Cr:肌酐;1 mm Hg = 0.133 kPa
对照组(n = 30)治疗组(n = 30)8.24±1.23 7.35±1.32 24.04±2.31 24.32±2.73 132.45±3.01 141.21±2.87 76.34±1.56 81.34±1.34 4.78±0.21 5.03±0.18 1.82±0.13 2.03±0.19组别 BUN(mmol/L) Cr(μmol/L) 胰岛素-0(μU/mL) 胰岛素-2 h(μU/mL) C 肽-0(μg/L) C 肽-2 h(μg/L)对照组(n = 30)治疗组(n = 30)6.98±0.82 6.34±0.47 91.32±6.45 88.45±4.35 5.01±0.56 4.53±0.65 21.09±2.12 18.83±2.33 2.15±0.34 2.43±0.43 4.04±0.35 3.89±0.43
表2 两组治疗前后NIHSS 及BI 评分比较(分,s)

表2 两组治疗前后NIHSS 及BI 评分比较(分,s)
注: 与本组治疗前比较,△P <0.01; 与对照组同期比较,#P <0.05;NIHSS:神经功能缺损评分;BI:Bathel 指数
治疗组(n = 30)治疗前治疗后7 d治疗后14 d对照组(n = 30)治疗前治疗后7 d治疗后14 d 6.89±3.76 4.50±3.11△#3.18±2.29△#48.56±19.25 59.78±19.68△#70.16±20.12△#6.75±6.05 5.01±5.56△4.42±5.18△49.78±32.14 55.89±31.16△62.40±31.86△
表3 两组患者血液流变学指标比较(s)

表3 两组患者血液流变学指标比较(s)
注:与本组治疗前比较,△P <0.01;与对照组同期比较,#P <0.05
血浆比黏度(mPa·s)红细胞压积(L/L)纤维蛋白原(g/L)红细胞聚集指数治疗组(n = 30)治疗前治疗后14 d对照组(n = 30)治疗前治疗后14 d 6.0±0.7 4.6±0.4△#1.91±0.32 1.56±0.51△#0.53±0.03 0.47±0.08△#5.3±2.0 3.7±2.6△#2.1±0.5 1.3±0.6△#6.1±0.9 6.2±1.1 1.83±0.46 1.77±0.52 0.52±0.02 0.49±0.05 5.2±1.8 5.3±1.3 2.0±0.7 1.9±0.3

表4 两组临床疗效比较(n)
然而,虽然前列地尔有很好的治疗作用,但由于它首次经过肺循环时在氧化酶的作用下即被代谢,从而大大降低其生物活性,且用药剂量过大会出现发热、皮疹、注射部位疼痛和血管刺激症状等不良反应,极大地限制了其临床应用。 本研究中治疗组患者所用药物是将前列地尔封入直径仅0.2 μm 的脂微球中,避免其在肺内失活,减少药物对血管的刺激,从而使其在体内的活性时间延长,最终具有高效、低不良反应、高选择性及靶向性等优点[9]。
本研究结果显示,在常规治疗的基础上加用脂微球前列地尔注射液治疗脑梗死合并2 型糖尿病患者后,患者的NIHSS 评分较治疗前显著降低(P <0.05),且低于对照组,差异有统计学意义 (P <0.05),BI 评分在使用脂微球前列地尔治疗后显著升高,且治疗组升高幅度高于对照组(P <0.05), 表明脂微球前列地尔能有效改善急性脑梗死合并2型糖尿病患者的神经功能缺损情况。 同时治疗组患者在血液流变学指标,即全血比黏度、血浆比黏度、纤维蛋白原、红细胞聚集指数等结果的数值显著低于对照组(P <0.05),说明脂微球前列地尔有降低血液黏度的功效,同时,加用此药后临床的治疗效果得到了显著的提高(P <0.05),且无明显不良反应。
综上所述,脂微球前列地尔能有效改善急性脑梗死合并2 型糖尿病的神经功能缺损,具有良好的安全性、可靠性,值得临床推广应用。
[1] 宋一峰.152 例脑梗死合并糖尿病临床分析[J]. 海南医学院学报,2009,15(4):344.
[2] Toyota T.Lipo-PGE1,a new lipid-encapsulated preparation of prostagl andin E1:Placebo and prostaglandin E1 controlled multicenter trials in patients with diabetic neuropathy and legulcers [J]. Prostaglandin,1993,46(5):453.
[3] 中华神经科学会,中华神经外科学会.脑卒中患者临床神经功能缺损程度评分标准(1995)[J].中华神经外科杂志,1996,29:381-383.
[4] 孙传兴.临床疾病诊断依据治愈好转标准[M].2 版.北京:人民军医出版社,2002:410.
[5] 潘家祜,张磊.脑梗死的药物治疗[J].中国新药与临床杂志,1999,18(4):233-235.
[6] 吴孝田.前列地尔治疗老年椎动脉性眩晕的效果观察[J].中国老年学杂志,2005,25(8):916-917.
[7] Korosue K,Kondoh T,Ishikawa A,et al. Clinical and hemodynamic effects of lipo PGE1 in cerebral infarction[J].No Shinkei Geka,1988,16:819-826.
[8] Komaba Y,Kitamura S,Terashi A. Effect of prostaglandin E1 on cerebral blood flow in patients with chronic cerebral infarction [J]. Intern Med,1998,37:841-846.
[9] 赵中.脂微前列腺素E1 对脑梗死患者血清VEGF,NO 水平调节的临床研究[J].中风与神经疾病杂志,2004,21:74.
