均匀设计试验筛选阿替洛尔分散片的处方
2013-12-03董晓晨赵文明辽宁医学院辽宁锦州121001
董晓晨,赵文明(辽宁医学院,辽宁锦州121001)
分散片又称水分散片,是指在水中能迅速崩解并均匀分散的片剂[1]。这一剂型具有吸收快、生物利用度高、不良反应少、制备工艺简单等性能,且可直接吞服、咀嚼或投入水中分散后服用,特别适用于儿童、老年人及吞服困难的患者,因此得到广泛关注。
阿替洛尔(Atenolol)是β1受体阻滞药,通过减慢心率、降低心输出量而发挥降血压作用,能有效降低心脏收缩期和舒张期的血压[2],主要用于治疗高血压、心绞痛及心律失常、青光眼的眼压控制等。阿替洛尔疗效准确、临床应用广泛,但为难溶性药物、生物利用度低[3],故影响其疗效。目前国内仅有普通片上市。为提高阿替洛尔的溶出度和生物利用度,笔者将阿替洛尔与适宜的辅料制备成分散片,并采用均匀设计试验,以溶出度为指标,考察了填充剂、崩解剂、润滑剂、黏合剂的用量,对阿替洛尔分散片进行处方筛选。
1 材料
1.1 仪器
L-2000Elite型高效液相色谱仪(日立高新技术集团,配二极管阵列检测器);UV-2550岛津紫外分光光度计(日本Shimadzu公司);RC-6溶出度测试仪(天津市新天光分析仪器技术有限公司);BJ-2A智能崩解仪(天津创兴电子设备制造有限公司);TDP-1.5型单冲压片机(上海旺群制药机械有限公司);硬度仪(上海黄海药检仪器);FA1004N电子天平(上海精密科学仪器有限公司)。
1.2 药品与试剂
阿替洛尔对照品(中国食品药品检定研究院,批号:100117-200504,纯度:99.8%);阿替洛尔片(江苏方强制药厂有限责任公司,批号:20120516,规格:25 mg/片);阿替洛尔原料药(武汉大华伟业医药化工有限公司,批号:20120620,纯度:99.0%);阿替洛尔分散片样品(自制,批号:130512、130513、130514,规格:25 mg/片);微晶纤微素(MCC)、羧甲基淀粉钠(CMS-Na)、预胶化淀粉、硬脂酸镁均来自安徽山河药用辅料股份有限公司,无水乙醇为分析纯。
2 方法与结果
2.1 制备工艺
将原料过200目筛,辅料过100目筛,按处方筛选中各处方配比量称取原、辅料。将阿替洛尔与MCC、预胶化淀粉、CMS-Na(内加部分)混合均匀,以50%乙醇溶液为黏合剂制软材,过24目筛制湿粒,烘干,整粒。加入CMS-Na(外加部分)、硬脂酸镁,混合均匀,压片。
2.2 填充剂的筛选
根据分散片常规处方工艺,采用MCC和预胶化淀粉作为分散片的填充剂,其余组分投料量不变,片剂硬度控制在4~5 kg,崩解剂加入方法为内加法。以分散片外观光洁度和30 min体外累积溶出度为指标进行考察,分别考察MCC、预胶化淀粉两者分别单独使用及以质量比为1∶1、1∶2、2∶1混合作为填充剂时对片剂质量的影响。填充剂种类筛选试验结果见表1。

表1 填充剂筛选结果Tab 1 Results of filler selection
表1结果表明,将MCC和预胶化淀粉两种填充剂混合使用,制得的片剂表面光洁,溶出度较二者单独使用时高。由于MCC具有多孔性,会吸附主药,导致溶出度偏低,并且具有吸水性,能迅速吸水,因此与预胶化淀粉混合使用能使片剂迅速崩解[4]。故选用以MCC和预胶化淀粉质量比为1∶1作为填充剂。
2.3 崩解剂的筛选
在处方3的基础上,以MCC和预胶化淀粉为填充剂,控制片剂硬度在4~5 kg,崩解剂加入方法为内加法。以分散片外观光洁度和崩解时限为指标进行考察,对CMS-Na、低取代羟丙基纤维素(L-HPC)、干淀粉3种崩解剂进行筛选,筛选结果见表2。

表2 崩解剂筛选结果Tab 2 Results of disintegrating agent selection
表2结果表明,片剂外观以CMS-Na制得片剂最优;3种崩解剂制得片剂崩解时限顺序为CMS-Na<L-HPC<干淀粉,故选用CMS-Na为崩解剂。
2.4 崩解剂加入方法的选择
在处方3的基础上,崩解剂加入方法分别采用内加法、外加法、内外加法,其余组分投料量不变,分别压片。对所得分散片以外观光洁度、硬度、崩解时限、30 min体外累积溶出度为指标进行考察,结果见表3。
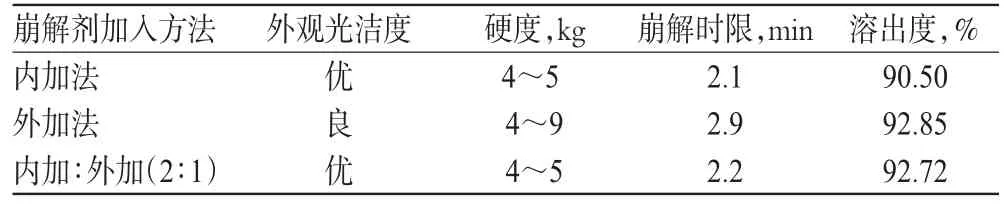
表3 不同崩解剂加入方法对分散片质量的影响Tab 3 Effects of different adding methods with disintegrating agent on dispersible tablets
表3结果表明,外加法溶出效果最好,但外观不佳,细粉较多,并且片子硬度不易控制;内加法崩解最快,但溶出较慢;内外加法既有利于片剂的崩解,也有利于片剂的溶出,故崩解剂加入方法选择内外加法。
2.5 黏合剂的筛选
由于阿替洛尔与聚乙烯吡咯烷酮有配伍反应[5],并且遇水黏性较大,故拟选用纯水、50%乙醇、3%淀粉浆为黏合剂,在确定的填充剂种类、崩解剂种类及其加入方法的基础上,按“2.1”项下方法制备,观察所得颗粒形态并以分散片外观光洁度、硬度、崩解时限为指标对黏合剂进行筛选,结果见表4。

表4 黏合剂筛选结果Tab 4 Results of adhesive selection
表4结果表明,用50%乙醇作黏合剂制得颗粒大小均匀,片剂外观最佳,硬度容易控制并且崩解时限合适,故选用50%乙醇作为黏合剂。
2.6 分散片处方优化
由以上单因素试验结果可知,对阿替洛尔分散片制备工艺影响较大的因素为填充剂中MCC的用量、崩解剂CMS-Na的用量、乙醇的质量分数。通过相关文献[6-7]可知,近几年来大多采用微粉硅胶作润滑剂,但微粉硅胶与阿替洛尔有配伍反应[5],故选用硬脂酸镁作润滑剂。压片时,硬脂酸镁的用量可直接影响片剂的弹性形变[8],因此,硬脂酸镁的用量对阿替洛尔分散片制备工艺影响较大。
2.6.1 均匀设计优化处方。4个考察因素及其基本范围[4,8]分别为:MCC用量(A)25%~45%;CMS-Na用量(B)4%~7%;硬脂酸镁用量(C)0.46%~1.06%;乙醇的质量分数(D)10%~60%。用预胶化淀粉调节片重。
选择U11(1110)表[9]中1,2,5,7列,并以30 min的体外累积溶出度为指标对各因素进行筛选,结果见表5(括号内为水平编号)。
2.6.2 计算结果。利用均匀设计软件,通过逐步回归法得回归方程:溶出度(y)=43.80+1.873×B+6.35×10-3×AB+1.063×10-2×AC-9.317×10-3×B2(r=0.9957);检验值F=172.7,F>F(0.05,4,6)=4.534,F验证通过(α=0.05)。
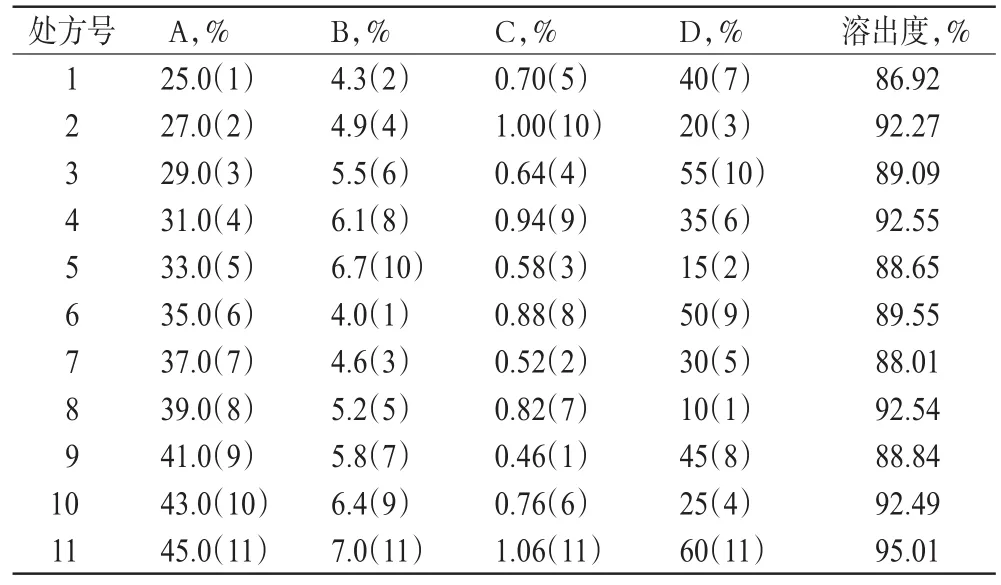
表5 均匀设计试验方案与结果(n=6)Tab 5Uniform design experiment program and result(n=6)
2.6.3 优选处方的选定。均匀设计计算结果表明,各因素影响溶出度的主次顺序为:A和B的交互作用>B>A和C的交互作用,D因素和溶出度关系不大。经均匀设计软件自动优化可知,当取A 45.0%、B 7.0%、C 1.00%时可使y值最大,溶出度最大。综合考虑制粒过程中黏合剂随乙醇质量分数增加,颗粒细粉随之增加,黏性降低,故D取40%。最终确定优选处方为A11B11C10D7,即A45.0%、B 7.0%、C 1.00%、D 40%。
2.7 验证试验
按最优处方制备3批阿替洛尔分散片,检查质量,验证处方的合理性。
2.7.1 分散均匀度。依据2010年版《中国药典》(二部)相关要求,取供试品6片,置于250 ml烧杯中,加15~25℃的水100 ml,振摇3 min,应全部崩解并通过二号筛,结果详见表6。

表6 3批阿替洛尔分散片验证试验结果Tab 6 Results of validation test of 3 batches of Atenolol dispersible tablets
2.7.2 混悬液稳定性[10]。取3批阿替洛尔分散片各1片,分别加入(20±1)℃水50 ml,充分搅拌,立即于700 nm波长处测其透光率,并记录0、5、10、15、20、25、30 min时的透光率(T0和Tt)。各批次样品分别测定6次,取算数平均值后计算(Tt-T0)/T0,以(Tt-T0)/T0对时间作图,经线性回归,计算斜率k。k值越小,表明混悬液沉降越慢,越稳定。结果详见表6。
表6结果表明,该制备工艺条件下制成的阿替洛尔分散片均符合2010年版《中国药典》中片剂的相关规定,该处方合理,制备工艺稳定可行。
2.8 溶出度
2.8.1 方法学考察。标准曲线的绘制:精密称取阿替洛尔对照品0.025 g,置于500 ml量瓶中,用盐酸溶液(9→1000)溶解并稀释至刻度,精密移取上述溶液10、15、20、25、30、35、40 ml至100 ml量瓶中,用盐酸溶液定容,摇匀;在224 nm波长处测得吸光度,以质量浓度(c)对吸光度(A)进行线性回归;得标准曲线方程A=0.0357c+0.0093(r=0.9999),表明阿替洛尔线性范围为5~20 μg/ml。精密度试验RSD=0.87%(n=6),符合精密度试验要求。平均回收率为99.8%,RSD=1.08%(n=3)。
2.8.2 与普通片剂溶出度比较。取样品(批号:130512)和市售普通片各6片,溶出度试验采用桨法[1],以盐酸溶液(9→1000)1000 ml为溶出介质,转速50 r/min,依法操作,分别于5、10、15、20、30、45 min时取溶液测定并计算其体外累积溶出度。分散片样品及普通片的溶出度见表7,溶出曲线见图1。
表7 2种片剂的体外累积溶出度比较(%%,±s,n=6)Tab 7 Comparison of accumulative dissolution rate between 2 kinds of tablet(s%%,±s,n=6)

表7 2种片剂的体外累积溶出度比较(%%,±s,n=6)Tab 7 Comparison of accumulative dissolution rate between 2 kinds of tablet(s%%,±s,n=6)
剂型普通片分散片时间,min 513.5±1.544.3±2.71032.1±1.777.2±4.51547.7±1.990.3±1.22060.2±3.391.3±0.93077.7±3.492.3±0.94589.0±1.293.4±0.9
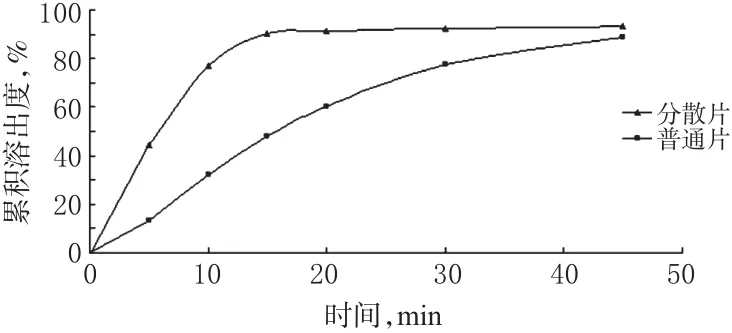
图1 两种片剂的溶出曲线Fig 1 Dissolution curves of 2 kinds of tablets
由图1可知,分散片溶出速率明显高于普通片,达到溶出平台期时间较短,最终溶出度高。对两种剂型参数进行方差分析,结果差异有统计学意义(P<0.01)。分析表明,分散片的溶出速率比普通片快,且各参数间差异具有显著性。
3 讨论
本处方中阿替洛尔的用量是依据2010年版《中国药典》(二部)中阿替洛尔标准制订的。
在填充剂筛选试验中,由于MCC在片剂中的用量通常为15%~45%,并且阿替洛尔用量较小,所以笔者考虑用部分预胶化淀粉代替MCC作为填充剂。此外,MCC除可作为填充剂以外,亦有崩解剂作用[11-12],并与CMS-Na相容性较好。通过对崩解剂加入方法的进一步研究,使分散片的崩解性能和溶出速率大大提高。试验表明,黏合剂乙醇对分散片的溶出度影响不大。
分散均匀度要求片剂3 min内完全崩解并通过二号筛,且主药溶出度与颗粒大小成反比,故选择24目筛制粒。片剂的硬度会对片剂的崩解、主药的溶出度、片剂的生产、运输和贮存带来直接影响。经综合考虑,本试验分散片硬度采用4~5 kg。试验证明,制得的阿替洛尔分散片崩解时限短、溶出速率快、制备工艺简单可行。因此,阿替洛尔分散片的研制具有良好的应用前景。
[1]国家药典委员会.中华人民共和国药典:二部[S].2010年版.北京:中国医药科技出版社,2010:附录ⅠA、附录74.
[2]Kmap O,Sieswedra GT,Visser CA.Comparison of effects on systolic and diastolic left ventricular function of nebivolol versus atenolol in patients with uncomplicated essential hypertension[J].Am J Cardiol,2003,92(3):344.
[3]胡国钧.阿替洛尔的药理[J].新药与临床,1989,8(3):176.
[4]罗明生,高天惠.药剂辅料大全[M].成都:四川科学技术出版社,2003:742-744.
[5]梁荣财,范本杰,孙考祥.阿替洛尔与片剂辅料相容性的热分析考察[J].中国药业,2009,18(10):19.
[6]姚梦竹,洪怡.分散片研究进展[J].数理医药学杂志,2012,25(6):717.
[7]唐建涛,黄占周,张志刚.分散片研究进展[J].临床合理用药,2011,4(12A):180.
[8]郭仁庭,覃忠富,傅长明.硬脂酸镁的性质、应用及市场前景综述[J].企业科技与发展,2011(7):15.
[9]张春华,严云良.医药数理学统计[M].北京:科技出版社,2001:270-271.
[10]韩丽梅,王卓,邓英杰.用透光率评价分散片混悬性的方法[J].药物分析杂志,1996,16(6):396.
[11]姚敦武,何清林,肖德华.加替沙星分散片处方及制备工艺研究[J].中国药房,2006,17(9):659.
[12]彭礼明.分散片处方、工艺特点及其进展[J].药品评价,2005,2(3):230.
